Похожие презентации:
Химические свойства солей в свете теории электролитической диссоциации
1.
2.
Ранее изученные темы:1. «Химические свойства …. в свете
теории электролитической диссоциации».
2. «Химические свойства …. в свете
теории электролитической диссоциации».
3. «…… их классификация и химические
свойства».
3. Тема урока: «Химические свойства солей в свете теории электролитической диссоциации».
4. «…наибольшее удовольствие в жизни не может существовать без «соли». Это вещество так необходимо человеческому роду, что даже
Эпиграф«…наибольшее удовольствие в жизни не
может существовать без «соли». Это
вещество так необходимо человеческому
роду, что даже духовные удовольствия не
могут быть лучше выражены, чем словом
«соль».
Все наслаждения жизни, вся острота и
радость, свобода и красота
существования не могут найти слова в
нашем языке, которое характеризовало
бы их лучше, чем это слово».
Плиний-Старший
5.
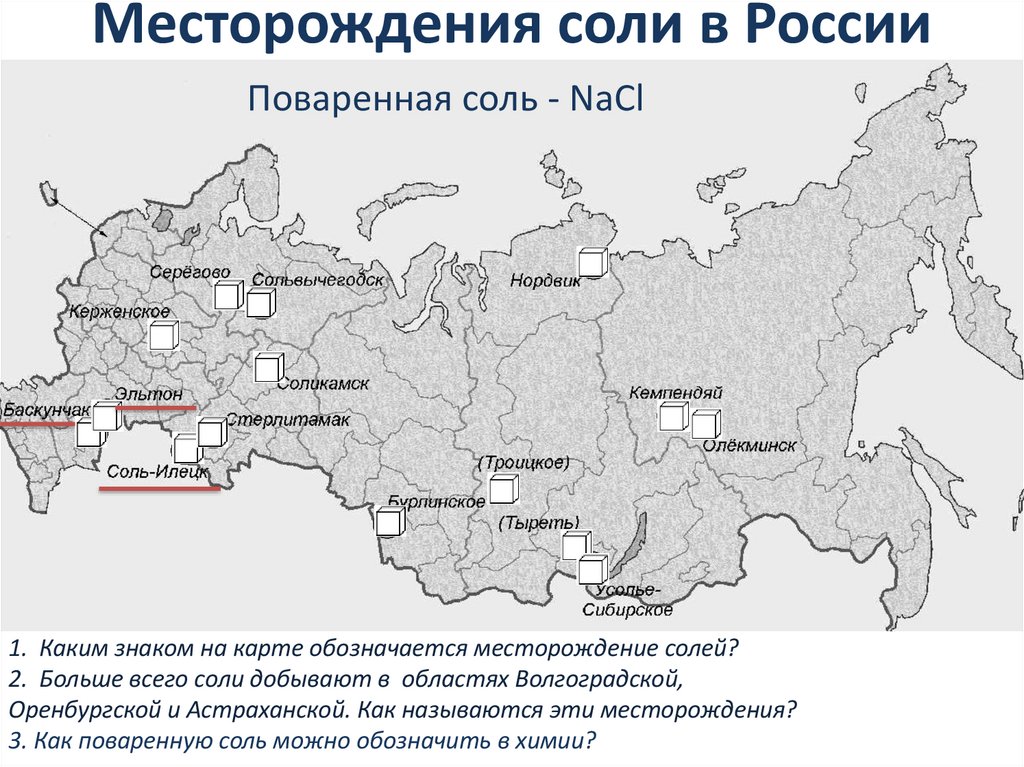
Месторождения соли в РоссииПоваренная соль - NaCl
1. Каким знаком на карте обозначается месторождение солей?
2. Больше всего соли добывают в областях Волгоградской,
Оренбургской и Астраханской. Как называются эти месторождения?
3. Как поваренную соль можно обозначить в химии?
6.
7. ОПРЕДЕЛЕНИЕ «СОЛИ»
1-это сложные вещества, состоящие
из металла и кислотного остатка
2-
это
сильные
электролиты
существующие в водных растворах
в виде катионов металлов (или
NH4+)
и
анионов
кислотных
остатков, где иногда встречаются
ионы H+ и OH-
8.
9. СРЕДНИЕ СОЛИ
Средние соли – это продуктыполного замещения атомов водорода
в кислоте на металл.
Na2CO3 – карбонат натрия
Эти соли диссоциируют на катионы
металла и анионы кислотного остатка.
Na2CO3 = 2Na+ + CO32-
10. КИСЛЫЕ СОЛИ
Кислые соли – это продукты неполногозамещения атомов водорода в кислоте на
металл.
К кислым солям относится такая соль как
NaHСO3. Название её складывается из
названия средней соли с прибавлением
слова «гидро».
NaHСO3 – гидрокарбонат натрия
Эта соль диссоциирует ступенчато. На
первой ступени образуется катион металла и
анион кислотного остатка, содержащий ион
водорода, а на второй ступени отщепляется
ион водорода и кислотный остаток.
NaHСO3 = Na+ + HСO3HСO3- ↔ H+ + СO32-
11. ОСНОВНЫЕ СОЛИ
Основные соли – это продуктынеполного замещения гидроксогрупп в
основании на кислотный остаток.
К таким солям относится малахит,
формула которого:
(CuOH)2CO3 – гидроксокарбонат меди (II).
ЗАДАНИЕ
12.
13. Типичные реакции средних солей
1.2.
3.
4.
14.
15.
Задание.Дописать уравнение реакции.
ЭТАЛОН
1. СаCO3 + 2HCl = СaCl2 + CO2↑ + H2O.
2. FeSO4 + 2NaOH = Fe(OH)2↓ + Na2SO4.
16.
17. Домашнее задание
§42Творческое задание:
1. Сделайте заголовок – название воды.
2. Найдите химический состав, в тетради запишите
отдельно катионы и анионы.
3. Составьте из ионов формулы солей, например:
2Na+ + SO42- = Na2SO4.
4. Подчеркните формулы кислых солей, назовите
их.
5. Подсчитайте общее число получившихся формул
солей.
6. Где расположен источник?
7. С какой глубины происходит подъем воды?
8. К какому типу минеральных вод она относится?
9. Какая еще информация есть на этикетке?
10.Личное отношение к минеральным водам.

















 Химия
Химия








