Похожие презентации:
Термодинамика и теплопередача. Идеальные газы
1. Термодинамика и теплопередача
Идеальные газы2.
Уравнение Клапейрона:Pv RT
Объединенный закон Бойля-Мариотта и
Гей-Люссака:
p1V1 p 2V2
T1
T2
Для произвольного количества газа
массой m уравнение состояния:
PV mRT
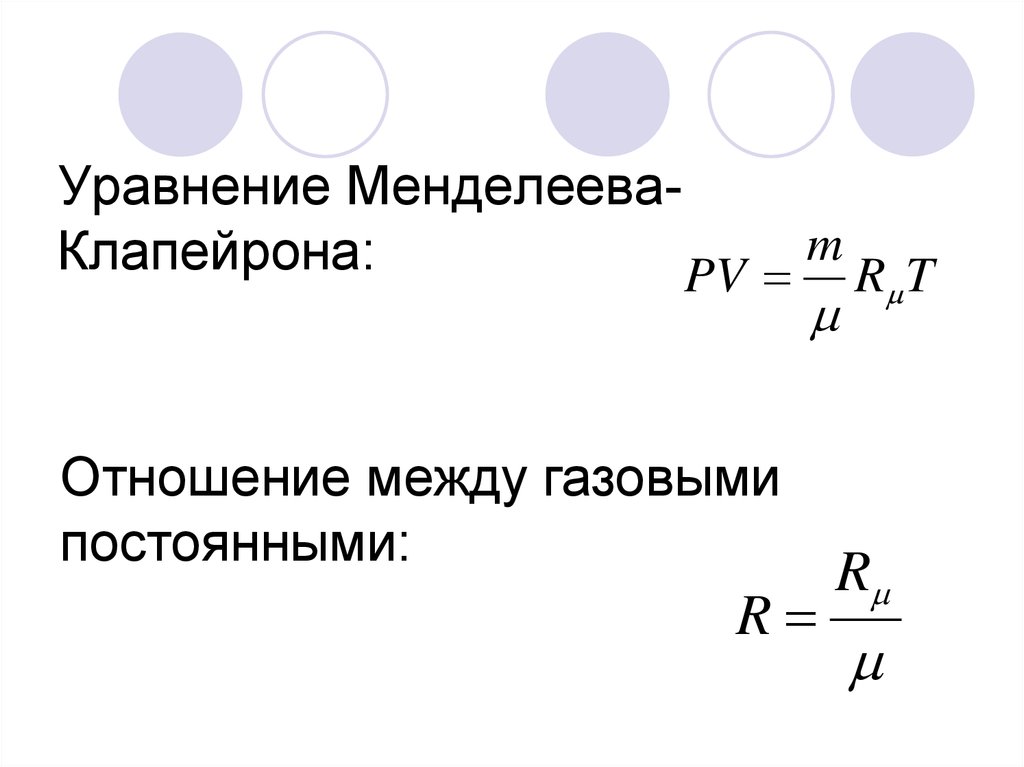
3. Уравнение Менделеева-Клапейрона:
Уравнение МенделееваmКлапейрона:
PV R T
Отношение между газовыми
постоянными:
R
R
4. Смесь идеальных газов
Общее давление смеси газов:Р Р1 Р2 Р3 ...Рп Рi
Объемные доли:
r1
V1
Vсм
Массовые доли:
m1
M1
M см
Мольные доли:
r /1
v1
vсм
V
r2 2
Vсм
m2
r/2
M2
M см
v2
vсм
rп
Vп
Vсм
mn
Mn
M см
r/n
vn
vсм
5.
V1 V2 ... Vn VCMМ 1 М 2 ... М n М CM
r1 r2 ... rn 1
т1 т2 .... тn 1
Связь между объемными и массовыми
долями:
т1 r1 1 / cм
тn rn n / cм
6. Молекулярная масса смеси:
cм 1r1 2 r2 ... n rnГазовая постоянная смеси:
т т
т
Rсм т1 R1 т2 R2 ... тn Rn R 1 2 ... n
Rn
1 2
1
r1 r2 ... rn
R R
Rn
2
1
7. Удельная массовая теплоемкость смеси:
ссм т1c1 т2 c2 ... тn cnУдельная объемная теплоемкость
смеси:
ссм r1c1 r2 c2 ... rn cn
Удельная мольная теплоемкость
смеси:
ссм r 1c1 r 2 c2 ... r n cn
/
/
/






 Физика
Физика








