Похожие презентации:
Презентация _Кислоты_ (8 класс)(1)
1.
2.
Что нас объединяет?3.
4. Кислый вкус лимону придает лимонная кислота, яблоку — яблочная кислота, скисшему молоку — молочная кислота. У щавеля кислый
вкус благодаря наличию вего листьях щавелевой кислоты
5. Кислоты
L/O/G/OЭлектронное пособие для 8-го класса (по учебнику Рудзитис)
6. Определение
Кислоты – это сложные вещества, в составкоторых входят атомы водорода и
кислотный остаток
Общая формула:
НхА
7.
СО2
КОН, CuО,Н
Н
,
Nа
РО
SО
Н2СО
2СО
3
3
4
,
2
3
3
Прослушайте аудиозапись определения кислот
еще раз.
Ответьте на вопросы:
1.В данном ряду найдите формулу кислоты.
Поясните.
2.Как называется вторая часть формулы?
7
8.
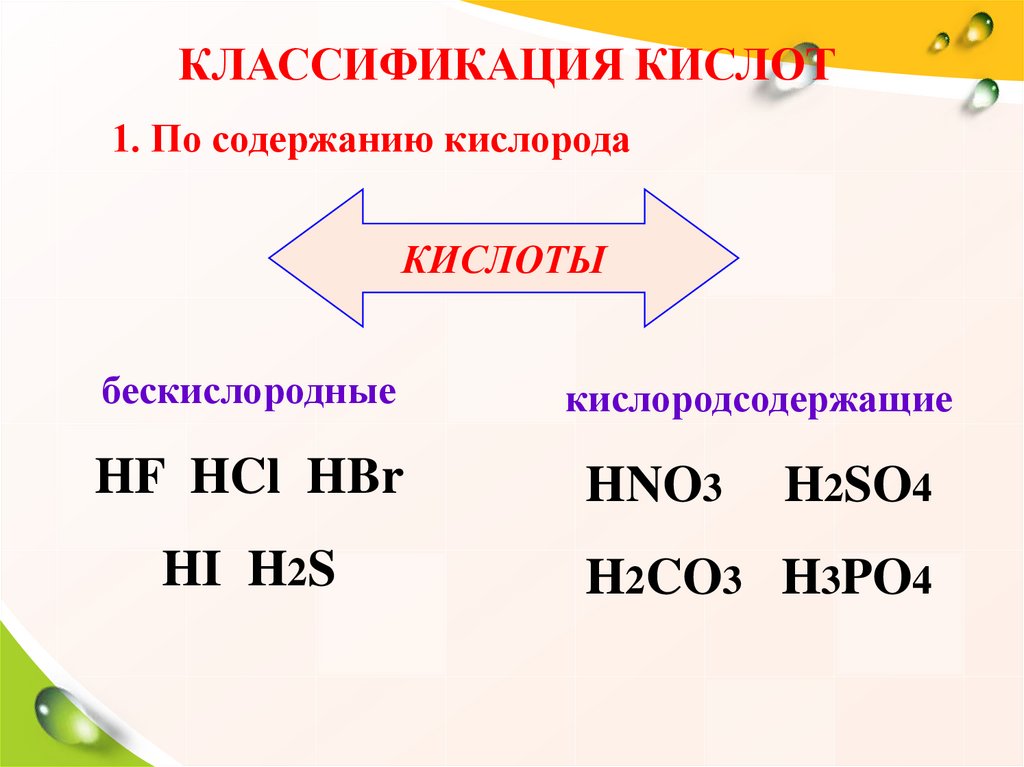
КЛАССИФИКАЦИЯ КИСЛОТ1. По содержанию кислорода
КИСЛОТЫ
бескислородные
кислородсодержащие
HF HCl HBr
HNO3
HI H2S
H2SO4
H2CO3 H3PO4
9.
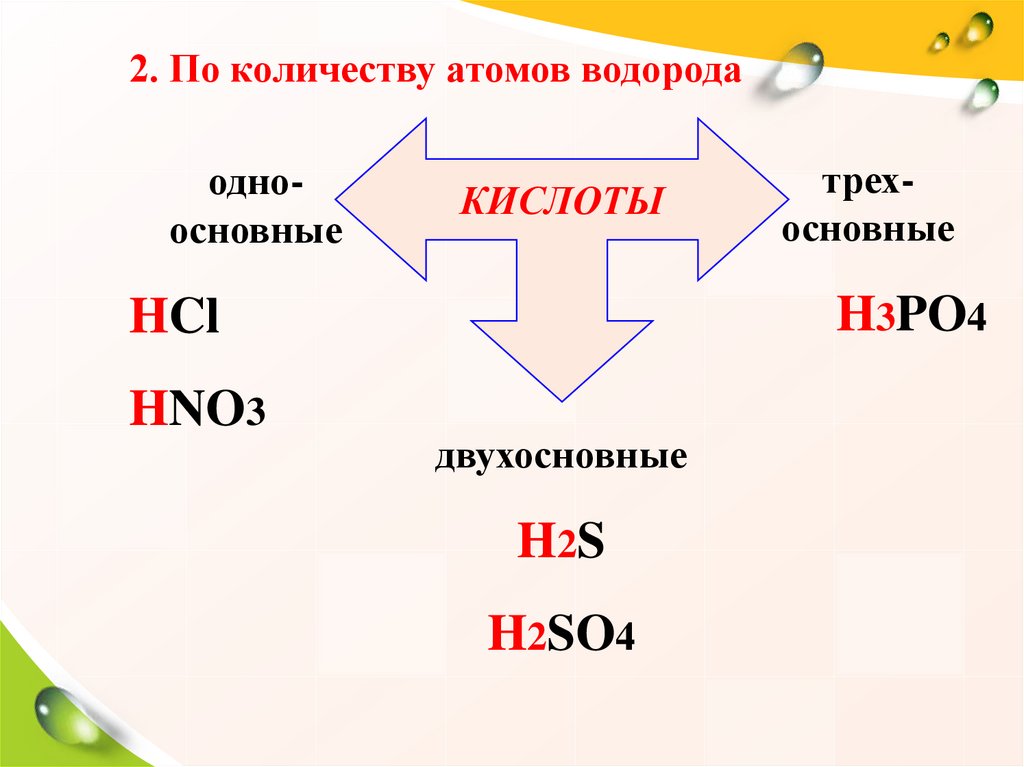
2. По количеству атомов водородаодноосновные
КИСЛОТЫ
H3PO4
HCl
HNO3
трехосновные
двухосновные
H2S
H2SO4
10. Кислотный оксид - кислота
Каждой кислоте соответствует свой кислотный оксид. Приэтом валентность центрального атома в оксиде и в кислоте
совпадают. Например в оксиде серы:
IV
IV
SO2 в соответствующей кислоте Н2SO3
V
V
Р2О5 и Н3РО4
Валентность кислотного остатка
определяется по количеству атомов
водорода в кислоте!
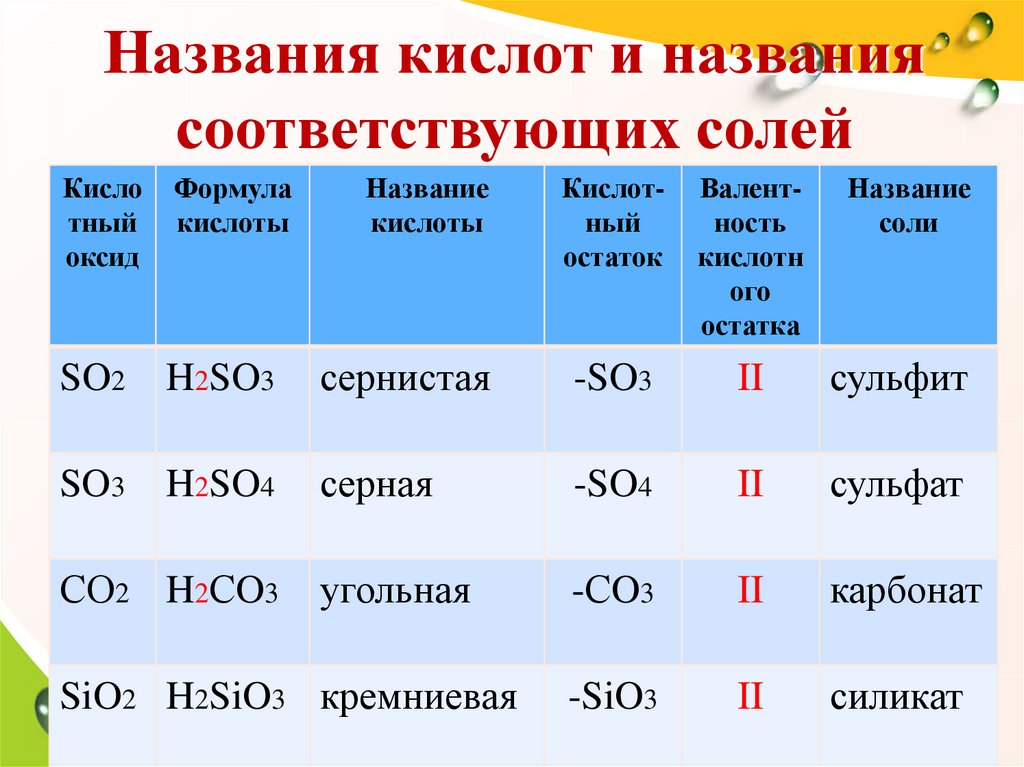
11. Названия кислот и названия соответствующих солей
Кислотный
оксид
Формула
кислоты
Название
кислоты
Кислотный
остаток
Валентность
кислотн
ого
остатка
Название
соли
SO2
H2SO3
сернистая
-SO3
II
сульфит
SO3
H2SO4
серная
-SO4
II
сульфат
угольная
-СO3
II
карбонат
-SiO3
II
силикат
СО2 H2СO3
SiO2 H2SiO3 кремниевая
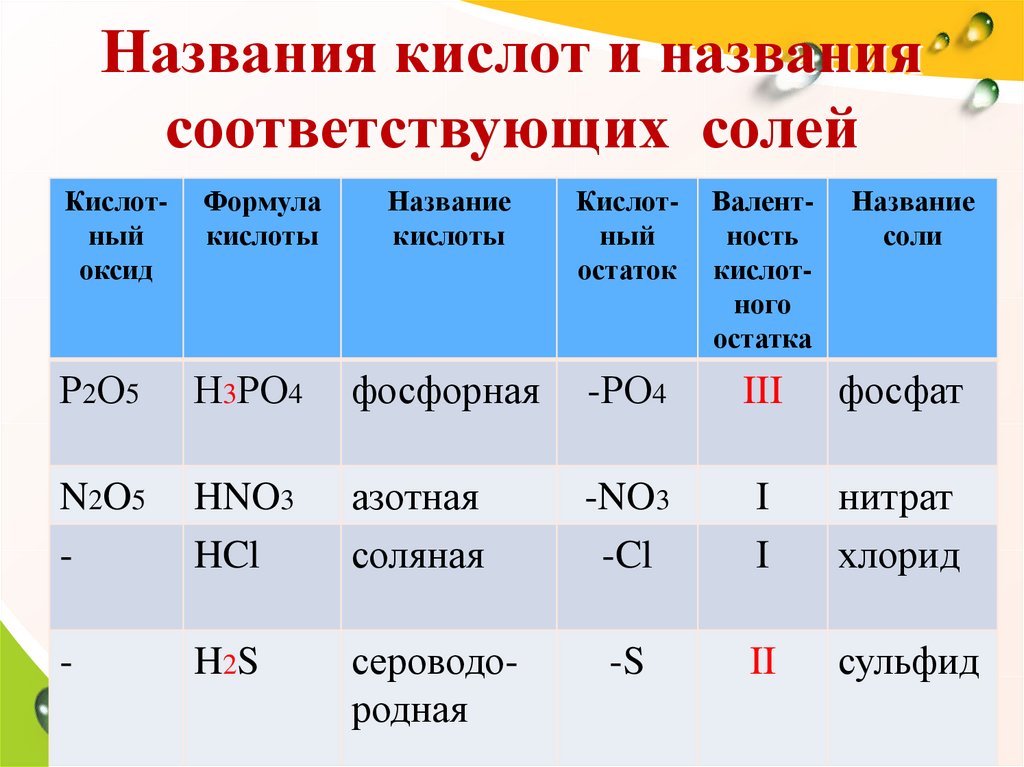
12. Названия кислот и названия соответствующих солей
Кислотныйоксид
Формула
кислоты
Название
кислоты
Кислотный
остаток
Валентность
кислотного
остатка
Название
соли
Р2О5
Н3РО4
фосфорная
-РО4
III
фосфат
N2O5
-
HNO3
HCl
азотная
соляная
-NO3
-Cl
I
I
нитрат
хлорид
-
H2S
сероводородная
-S
II
сульфид
13. Физические свойства кислот
• При обычных условиях кислоты могут бытьтвердыми и жидкими.
• Кислоты –едкие жидкости (кроме кремниевой), с
кислым вкусом, без запаха, разъедают многие
вещества.
• Слабые кислоты (угольная и сернистая) при
обычных условиях тут же разлагаются на
кислотный оксид и воду:
Н2SO3 = SO2 ↑ + H2O
H2CO3 = CO2 ↑+ H2O
14.
Формулы каких веществ «лишние» ипочему?
1) HCI 2) CO2 3) NaOH 4) H2SO4
5) NaCI 6) H3PO4 7) HNO3
8) H2S
9) СаО 10) H2CO3 11) Н2О 12) Н2SiO3
15.
ФормулыНазвания
H2СО3
СОЛЯНАЯ
HСl
УГОЛЬНАЯ
H2SO4
ФОСФОРНАЯ
HNO3
СЕРНАЯ
H3PO4
АЗОТНАЯ
15
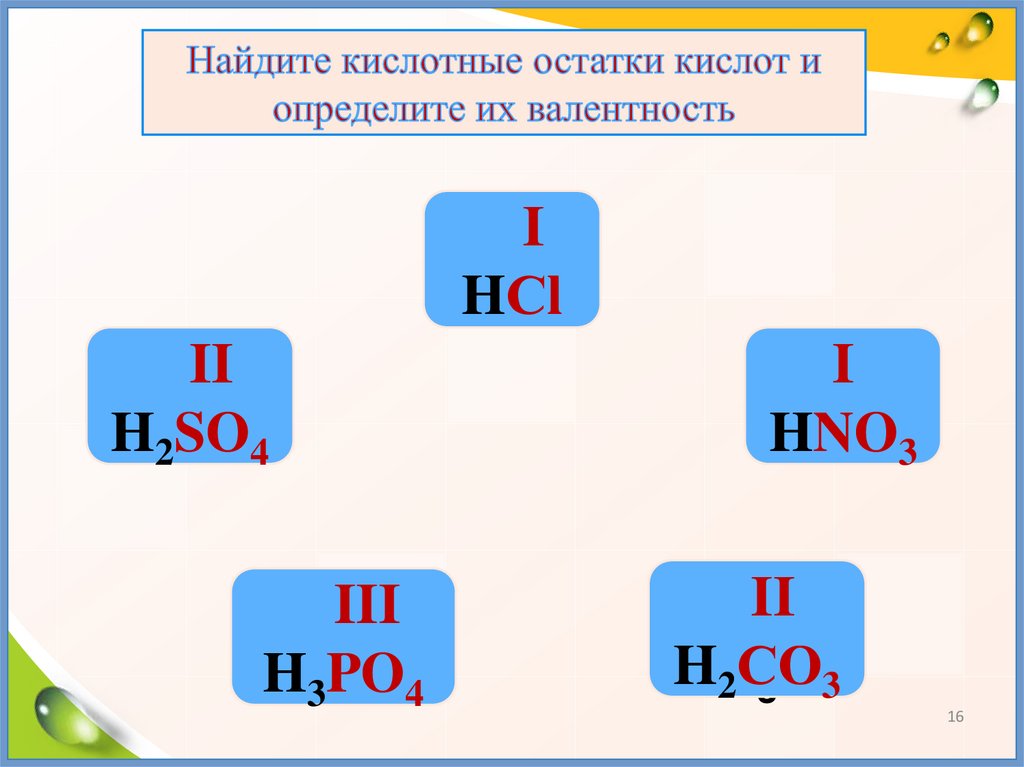
16.
IHСl
HСl
II
H2SO
H24SO4
III
H3PO
H34PO4
I
HNO
HNO
3 3
H2II
С
HО
2СО
3 3
16
17. По какому признаку кислоты разделены на группы?
ents 1По какому признаку
кислоты разделены на группы?
HCl
HNO3
HF
H2SO4
HBr
H2CO3
H2S
H2SiO3
HI
H3PO4
18. По какому признаку кислоты разделены на группы?
??
?
HF
HCl
HBr
HI
HNO3
HClO4
H2S
H2SO4
H2SO3
H2CO3
H3PO4
H3BO3
H2SiO3
19.
ПРАВИЛА БЕЗОПАСНОСТИЕдкое вещество—кислота!
Разрушает и раздражает
кожу, слизистые оболочки.
Попавшие на кожу капли раствора
кислоты немедленно смойте
сильной струей холодной воды, а
затем обработайте поврежденную
поверхность 2%-м раствором
питьевой соды.
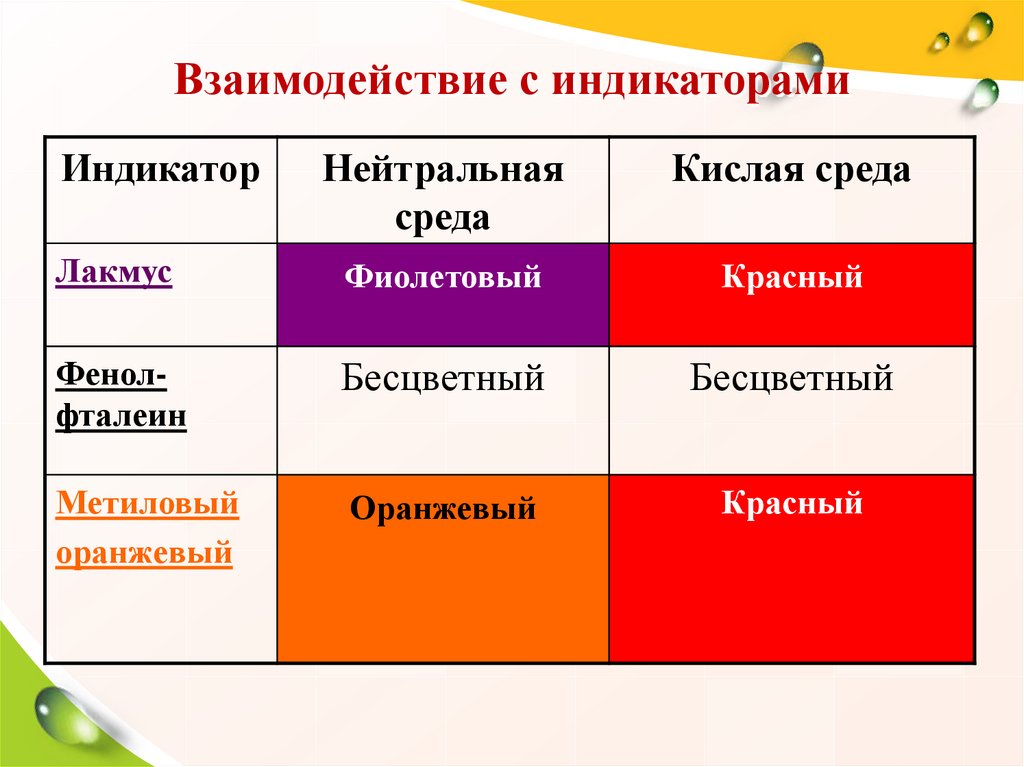
20. Взаимодействие с индикаторами
ИндикаторНейтральная
среда
Кислая среда
Лакмус
Фиолетовый
Красный
Фенолфталеин
Бесцветный
Бесцветный
Метиловый
оранжевый
Оранжевый
Красный














 Химия
Химия








