Похожие презентации:
предельные одноатомные спирты_
1.
Раздел: Кислородсодержащие соединенияТема: Предельные одноатомные спирты
2.
Цели урока:1. Учебная.
Рассмотреть строение молекул, основы международной
номенклатуры, гомологический ряд и изомерию предельных
одноатомных спиртов, строение гидроксильной
группы и спрогнозировать химические свойства спиртов.
2. Развивающая: развивать познавательный интерес учащихся,
умение анализа, обобщения и систематизации учебной
информации, критическое мышление, умение анализировать,
выделять главное, развивать рефлексивную культуру учащихся;
формировать навыки наблюдения
3. Воспитывающая: Показать вредное воздействие спиртов на
живые организмы, воспитывать самостоятельность, активность,
доброжелательность.
3.
1. Состав, строение молекулыH
H
H
C
C
H
OH
H
C2 H5 OH
C2 H6
2. Определение
Предельные одноатомные спирты –
производные предельных углеводородов,
в молекулах которых один атом водорода
замещён на гидроксильную группу.
Запомните! Атомность спиртов определяется числом групп – ОН
4.
Гидроксильная группаявляется функциональной группой спиртов!
Функциональная группа – группа атомов,
которая обусловливает характерные
химические свойства вещества
5.
4. Гомологический ряд спиртовОбщая формула ряда: СnH2n+1OH или СnH2n+2O ,
R – OH, где R- это УВ радикал, ОН- функциональная
группа CH OH метанол
3
C2H5OH
этанол
C3H7OH
пропанол
C4H9OH
бутанол
C5H11OH
пентанол
6.
3. НоменклатураНазвания спиртов образуют от соответствующих алканов
добавлением суффикса – ол.
Например: метан – метанол, пропан - пропанол
Нумерацию атомов углерода начинают с того конца
молекулы, где ближе функциональная группа, в конце
цифрой указывают положение функциональной
группы
3
2
1
СН3 – СН – СН2 ОН
СН3
2-метил пропанол -1
7.
Назвать вещества:СН3
1. СН3 – СН2 – СН – СН – СН – СН3
ОН СН3
СН3
2. СН3 – СН – СН2 – СН – СН – СН3
ОН
С2Н5
8.
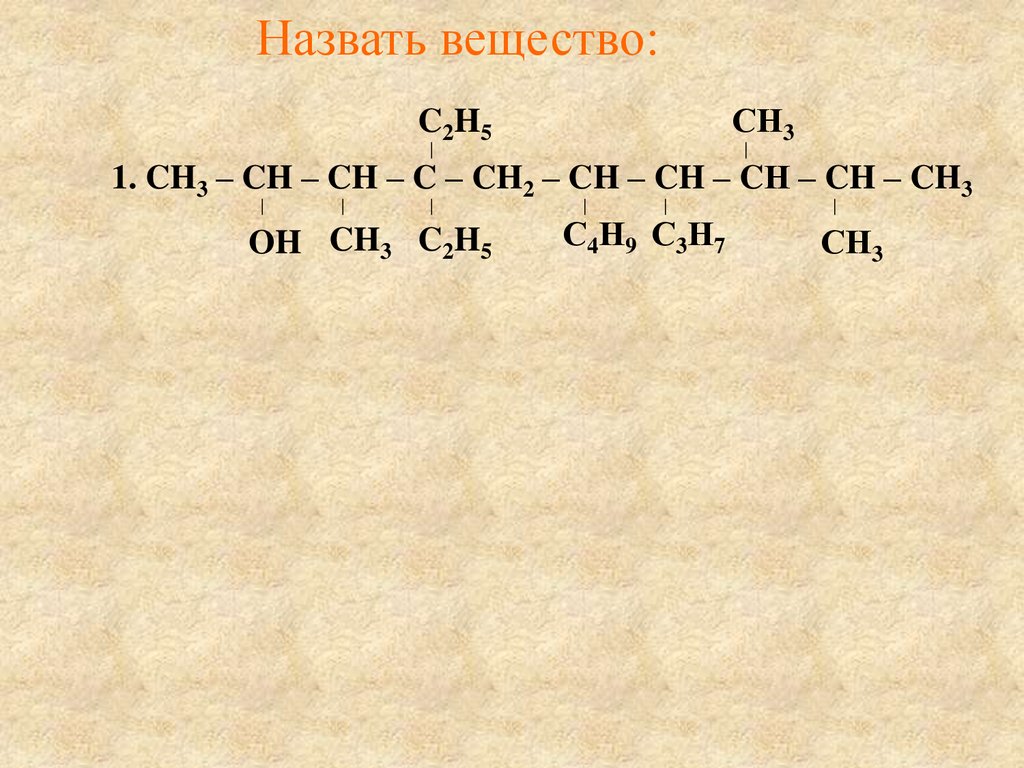
Назвать вещество:СН3
C2H5
1. CH3 – CH – CH – C – CH2 – CH – CH – CН – CH – CH3
OH CH3 C2H5
С4Н9 С3Н7
СН3
9.
Составить формулу:2-метил-3-этилпентанола-2
СН3
1
2
С Н3– С –
ОН
3
4
5
СН – СН2– СН3
С2Н5
Составить формулу:
1). 2,4-диметил-3-этилгексанола-2
2). 2, 2-диметил-3-этилбутанола-1
10.
5. ИзомерияДля спиртов характерна структурная изомерия:
1. изомерия положения ОН-группы (начиная с С3);
1
1.
2
3
1
2
3
СН2 – СН2 – СН3
ОН
2. СН3 – СН – СН3
пропанол - 1
пропанол-2
ОН
11.
2. Изомерия углеродной цепи (начиная с С4)1
2
3
4
СН3 – СН – СН2 – СН3
ОН
бутанол - 2
СН3
1
2
3
СН3 – СН – СН3
ОН
2-метилпропанол-2
12.
Составить 3 изомера гексанола-213.
6. Физические свойстваС1 –С11 – при обычных условиях жидкости,
с резким запахом, хорошо растворимы в
воде,
С12 – твёрдые вещества, без запаха, не
растворимы в воде.
Среди спиртов нет газообразных веществ,
благодаря наличию между их молекулами
водородных связей
14.
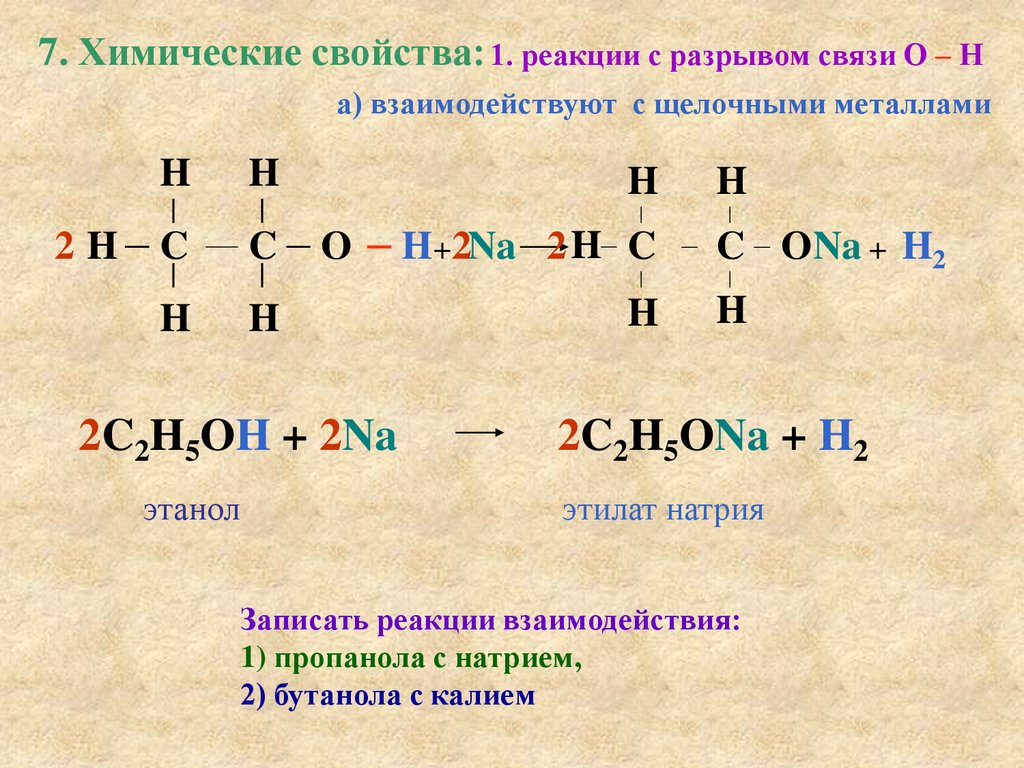
7. Химические свойства: 1. реакции с разрывом связи О – На) взаимодействуют с щелочными металлами
2H
H
H
C
C
H
H
H
O
2C2H5OH + 2Na
этанол
H+2Na 2 H C
H
H
C ONa + H2
H
2C2H5ONa + H2
этилат натрия
Записать реакции взаимодействия:
1) пропанола с натрием,
2) бутанола с калием
15.
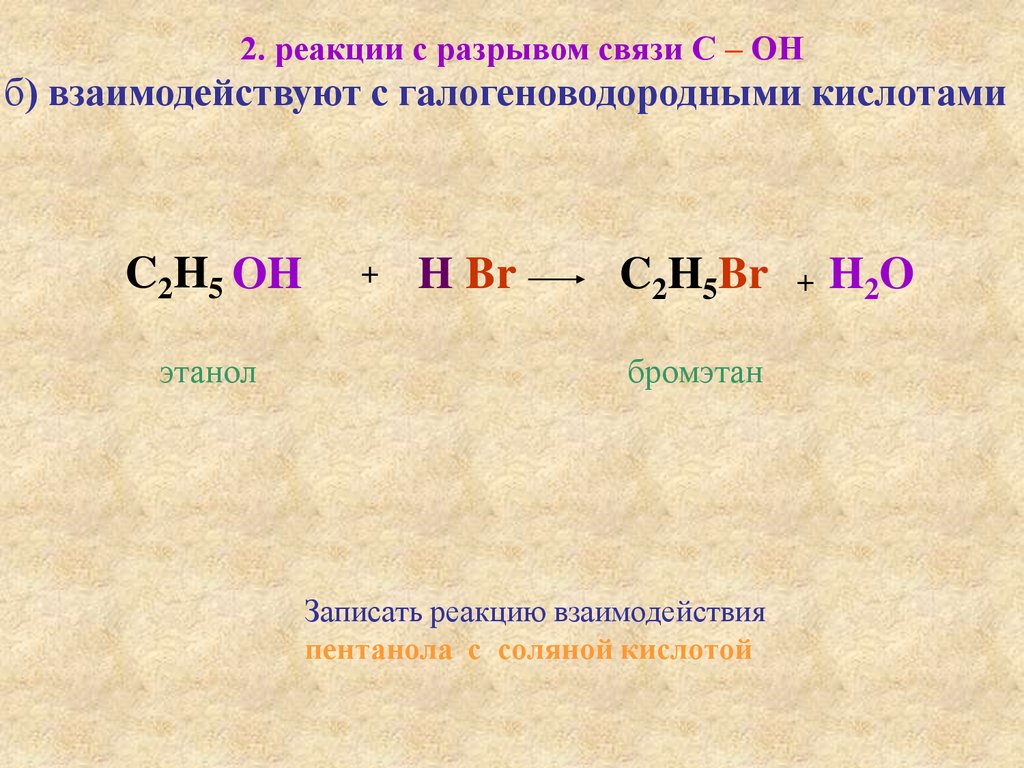
2. реакции с разрывом связи С – ОНб) взаимодействуют с галогеноводородными кислотами
C2H5 OH
этанол
+
H Br
C2H5Br + H2O
бромэтан
Записать реакцию взаимодействия
пентанола с соляной кислотой
16.
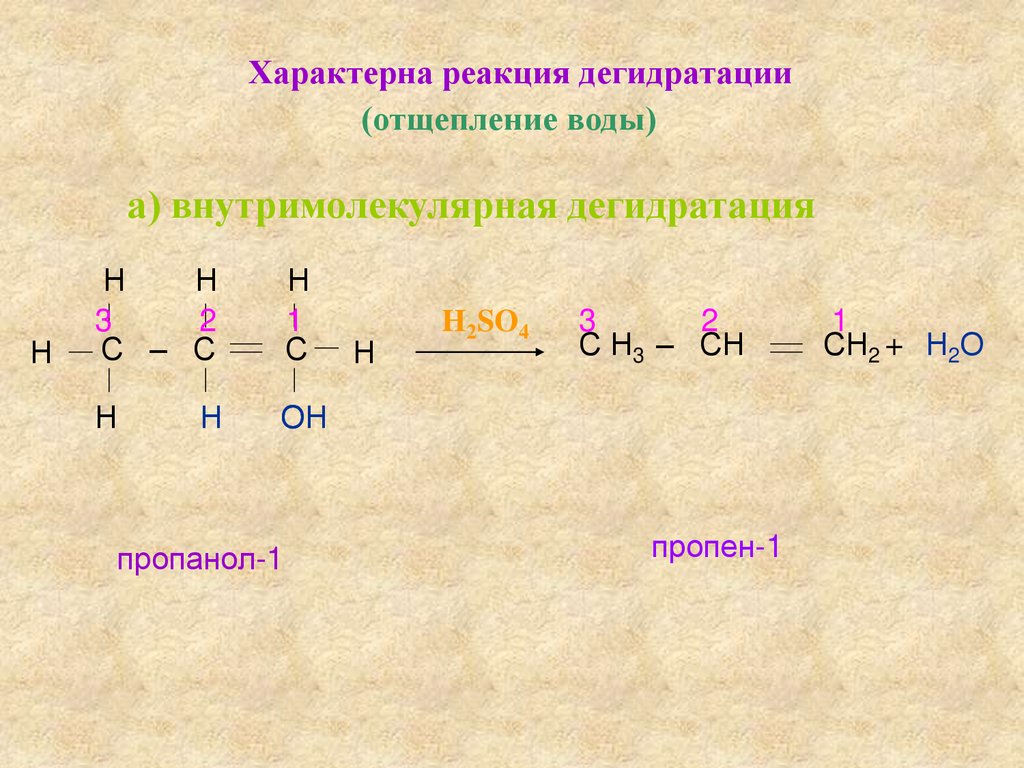
Характерна реакция дегидратации(отщепление воды)
а) внутримолекулярная дегидратация
Н
Н
Н
3
2
С – С
Н
1
С
Н
ОН
Н
пропанол-1
Н
H2SO4
3
2
С Н3 – СН
пропен-1
1
СН2 + Н2О
17.
б) межмолекулярная дегидратацияС2Н5О Н
этанол
+
О
С2Н5 + Н2О
НОС2Н5
С2Н5
этанол
диэтиловый эфир
18.
Характерна реакция окисления (горения)С2Н5ОН + 3О2 = 2СО2 + 3Н2О + 1374кДж
19.
Получение спиртов1. Гидратацией алкенов:
СН2 = СН2 + Н2О
СН3 – СН2 – ОН
2. В результате брожения сахаристых веществ
С6Н12О6
С2Н5ОН
20.
8. Применение стр.120Метанол (метиловый спирт) CH3OH
В производстве формальдегида, муравьиной кислоты;
как растворитель.
Этанол (этиловый спирт) С2Н5ОН
В производстве ацетальдегида, уксусной кислоты,
бутадиена, простых и сложных эфиров;
как растворитель для красителей, лекарственных и
парфюмерных средств;
в производстве ликеро-водочных изделий;
как дезинфицирующее средство в медицине;
горючее для двигателей, добавка к моторным топливам
21.
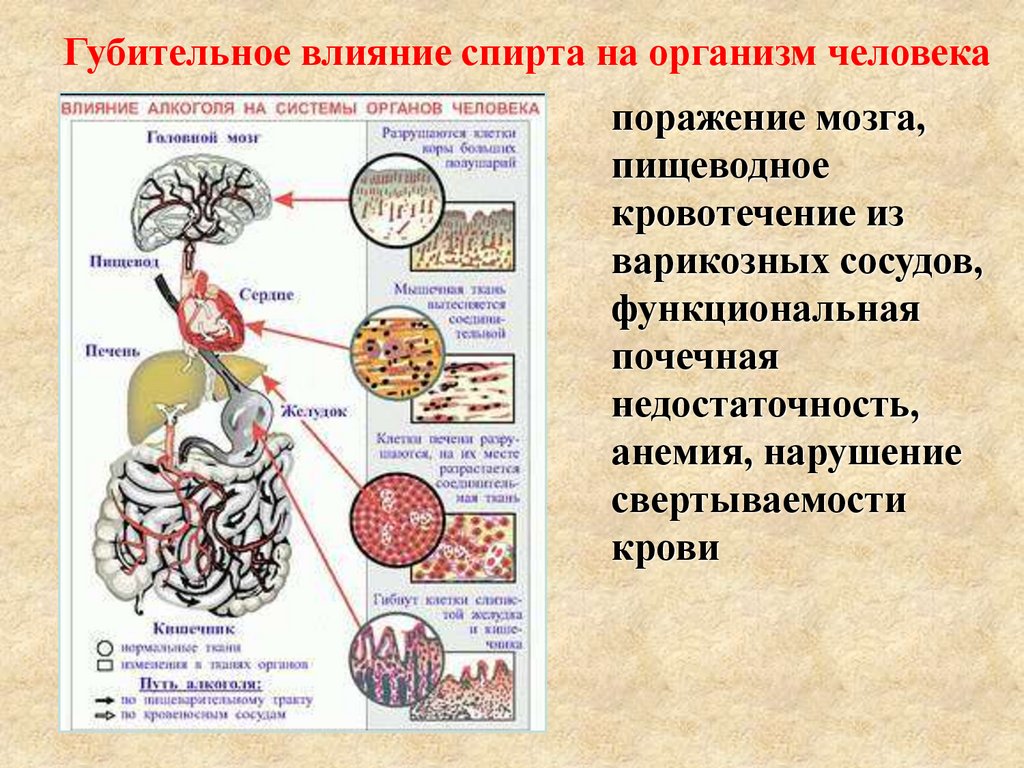
Губительное влияние спирта на организм человекапоражение мозга,
пищеводное
кровотечение из
варикозных сосудов,
функциональная
почечная
недостаточность,
анемия, нарушение
свертываемости
крови
22.
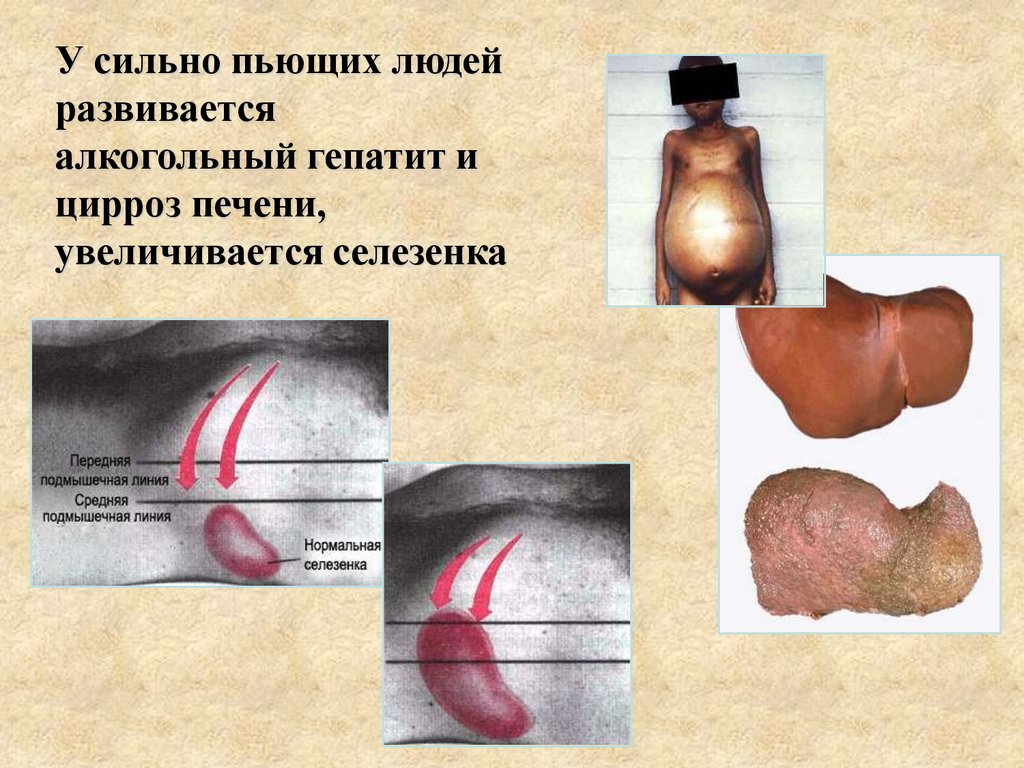
У сильно пьющих людейразвивается
алкогольный гепатит и
цирроз печени,
увеличивается селезенка
23.
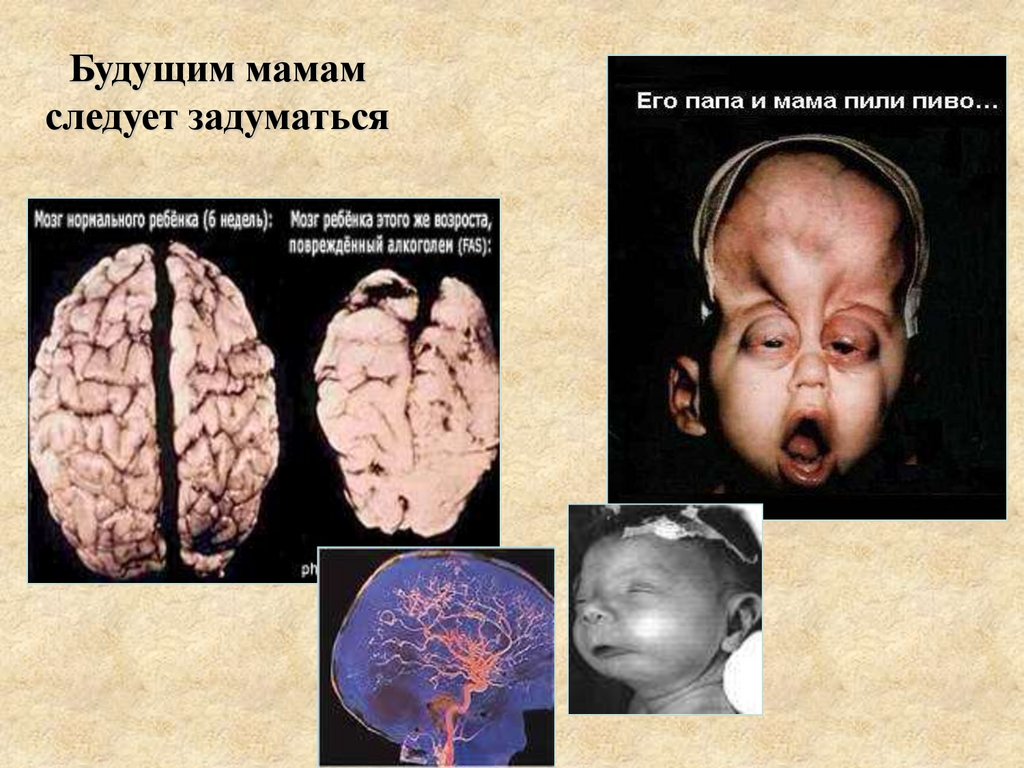
Будущим мамамследует задуматься
24.
Подростковыйалкоголизм возникает
и при чрезмерном
употреблении пива
25.
Феодосий Печерский.Бесноватый страдает по
неволе и может удостоится
жизни вечной, а пьяный
страдает по собственной воле
и предан на вечную муку
К. Ушинский. Пьяному на
светлой улице темно
И. Ефимов. Нет крепких вин,
есть слабые головы
Н. Семашко. Можно сказать,
что сколько мужья выпили
водки, столько их жены и дети
пролили слез

















 Химия
Химия








