Похожие презентации:
Теория химического строения Бутлерова. Предмет органической химии. Первое положение теории Бутлерова
1. ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ ЦЕНТР ДОВУЗОВСКОЙ ПОДГОТОВКИ И ПРОФОРИЕНТАЦИИ КАФЕДРА ХИМИИ
Теория химического строенияА. М. Бутлерова. Часть I
1.Предмет органической химии.
2. Первое положение теории
А. М. Бутлерова.
Составитель: доктор биологических наук, профессор,
зав. кафедрой химии
Степанова Ирина Петровна
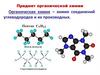
2. Предмет органической химии
Органическая химия – химия соединенийуглеводородов и их производных.
3.
Предмет органической химииОсобенности органических веществ:
1. Многообразие в природе: около 27 млн
(неорганических веществ – около 100 тысяч).
2. Образуются небольшим количеством
атомов-неметаллов, которые получили
названия органогены: С, Н, О, N (реже S, Р,
галогены).
4.
Основные положения теорииА. М. Бутлерова
А. М. Бутлеров
5.
Основные положения теории А. М. БутлероваАтомы в составе молекулы соединены
между собой в определенном порядке, в
соответствии с их валентностью.
Атом углерода четырехвалентен:
С
Химическая связь
(общая электронная
пара) изображается
черточкой.
6.
Предмет органической химииПорядок соединения атомов называется
химическим строением молекулы и
отображается с помощью структурных
формул.
Четырехвалентность атома углерода:
H
H
H
метан
H C
C C
H C H
O
H
H
этилен
H
C H
C
H
ацетилен
H
формальдегид
7.
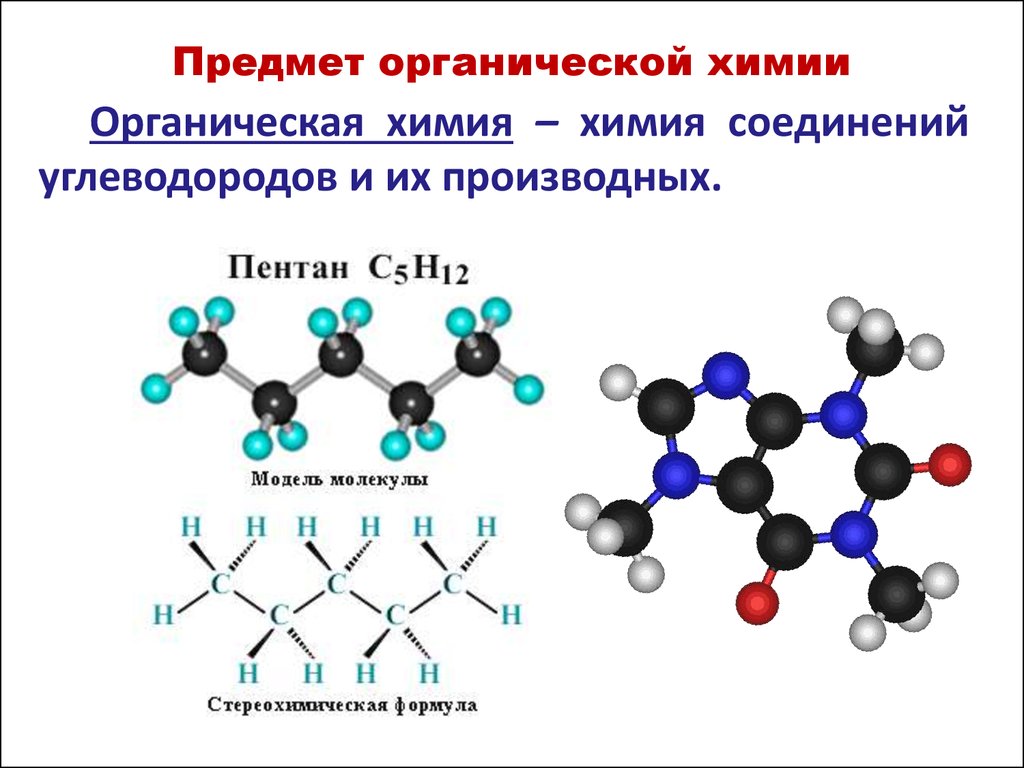
Предмет органической химииФормулы:
молекулярная
C6H6 ,
,
полная структурная
сокращенная структурная
.
8.
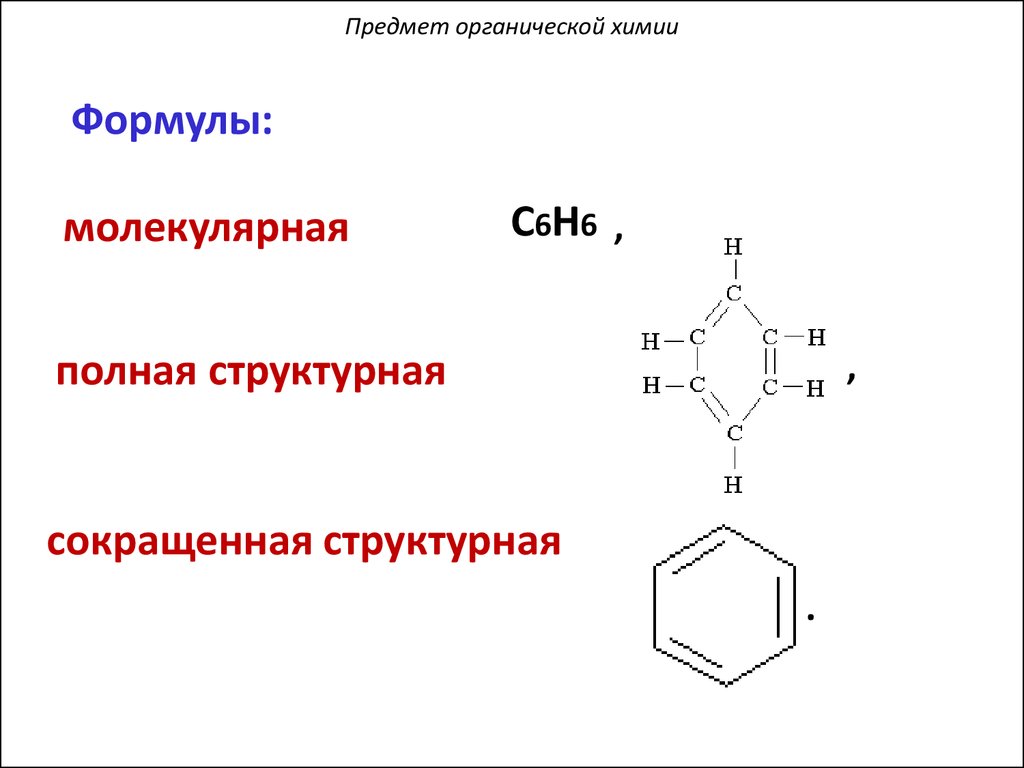
Предмет органической химииРазличают первичные, вторичные, третичные,
четвертичные атомы углерода.
Тип звена определяется числом соседних
атомов углерода, связанных с данным
углеродным атомом.
9.
Предмет органической химииСтепень окисления атома углерода лежит в
интервале значений от -4 до +4.
Например:
-4
-8/3
0
+2
CH4, C3H8, HCHO, HCOOH,
+4
CCl4
10.
Предмет органической химииОсновные связи – ковалентные:
Химическая связь
Ковалентная
Dc < 1,7
Ковалентная
полярная
0 < Dc < 1,7
Ковалентная
неполярная
Dc = 0
Ионная
Dc > 1,7
11.
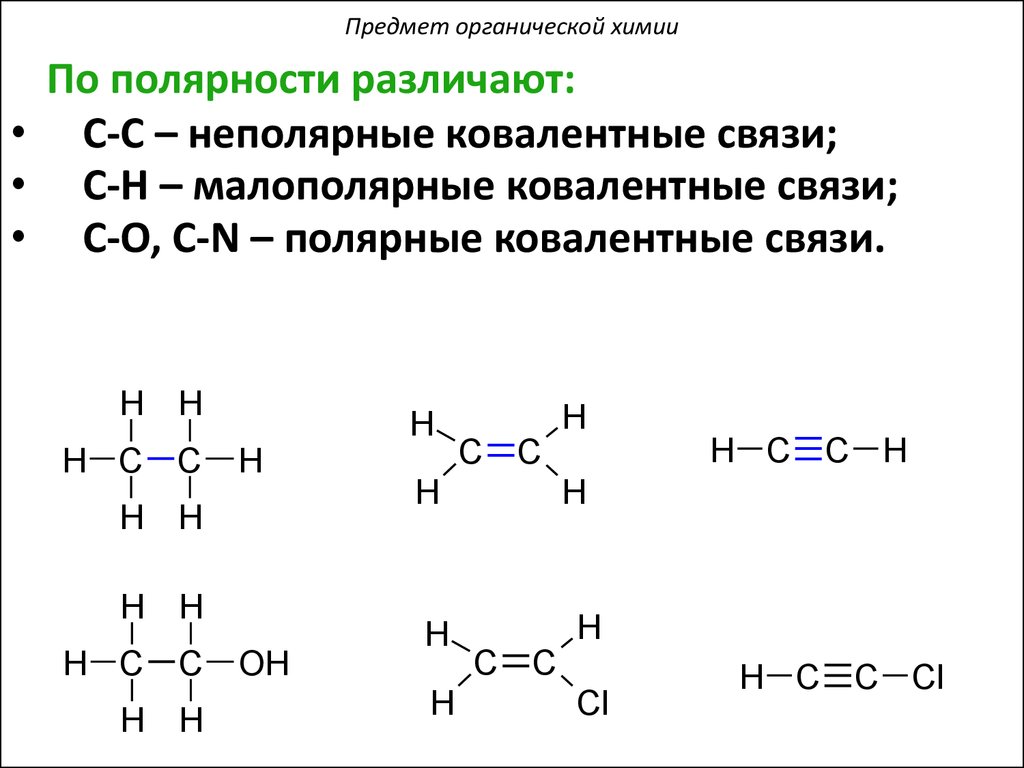
Предмет органической химииПо полярности различают:
• С-С – неполярные ковалентные связи;
• С-Н – малополярные ковалентные связи;
• С-О, С-N – полярные ковалентные связи.
H H
H C C
H
H
H H
H H
H C C
H H
OH
H
H
H
H
H C C H
C C
H
H
C C
Cl
H C C Cl
12.
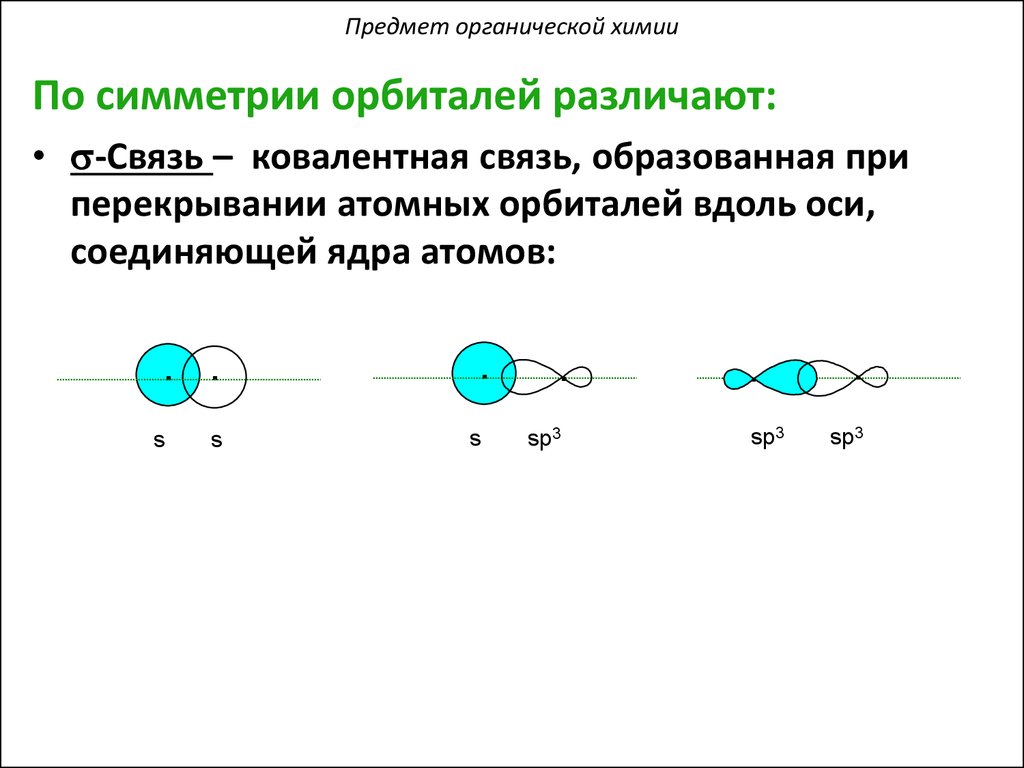
Предмет органической химииПо симметрии орбиталей различают:
• s-Cвязь – ковалентная связь, образованная при
перекрывании атомных орбиталей вдоль оси,
соединяющей ядра атомов:
. .
s
s
.
s
.
sp3
.
sp3
.
sp3
13.
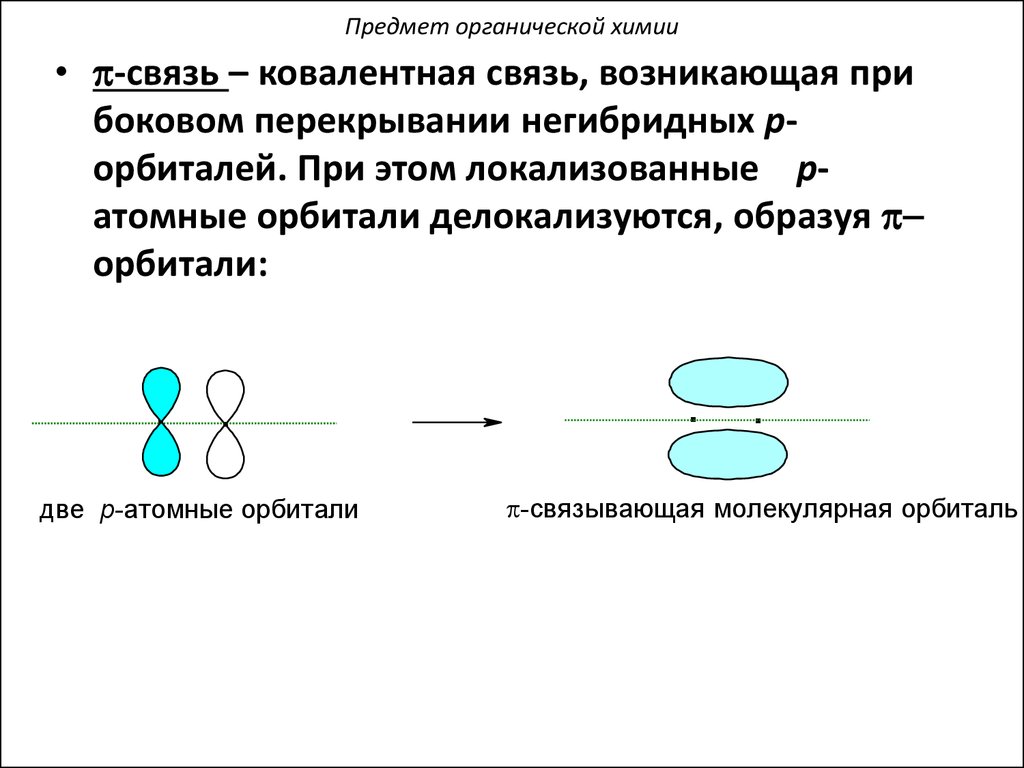
Предмет органической химии• p-связь – ковалентная связь, возникающая при
боковом перекрывании негибридных pорбиталей. При этом локализованные pатомные орбитали делокализуются, образуя pорбитали:
. .
двe p-атомныe орбитали
. .
p-связывающая молeкулярная орбиталь
14.
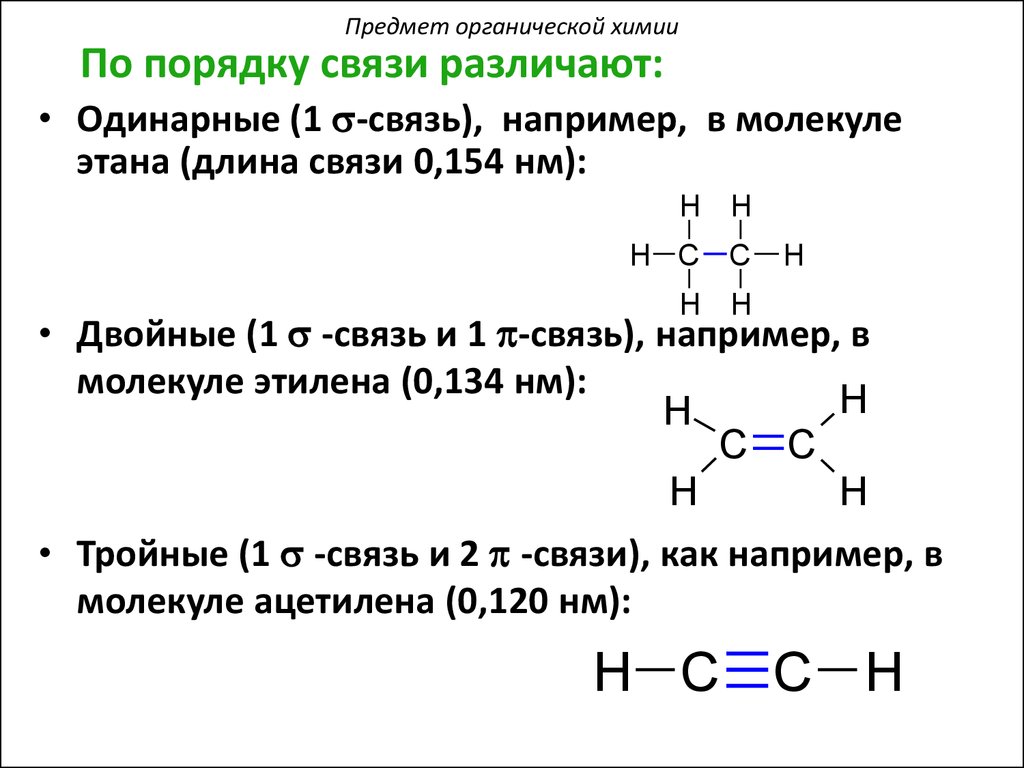
Предмет органической химииПо порядку связи различают:
• Одинарные (1 s-связь), например, в молекуле
этана (длина связи 0,154 нм):
H H
H C C
H
H H
• Двойные (1 s -связь и 1 p-связь), например, в
молекуле этилена (0,134 нм):
H
H
C C
H
H
• Тройные (1 s -связь и 2 p -связи), как например, в
молекуле ацетилена (0,120 нм):
H C C H
15. Только σ-связи имеются в молекулах:
ТестыТолько σ-связи имеются в молекулах:
1) этилена
3) этанола
2) бензола
4) ацетилена
16. Соединение с максимальным числом -связей в молекуле
ТестыСоединение с максимальным числом
p-связей в молекуле
1) ацетилен
3)этилен
2) формальдегид
4)винилацетилен
17.
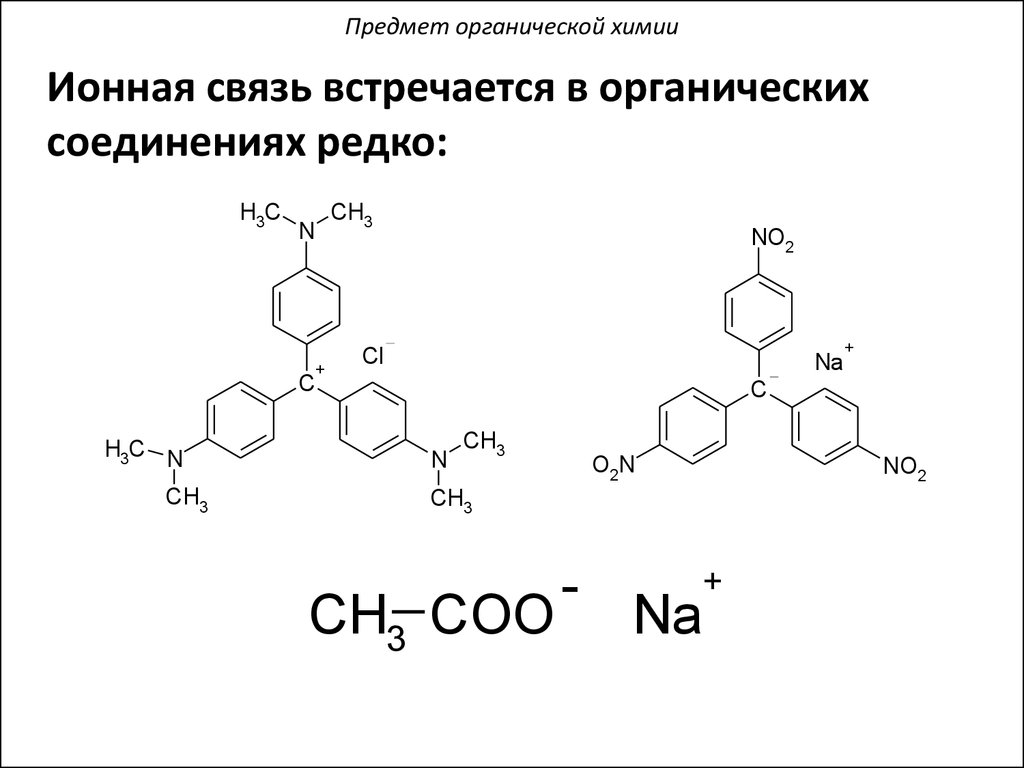
Предмет органической химииИонная связь встречается в органических
соединениях редко:
H3C
C
H3C N
CH3
CH3
N
+
NO2
Cl
Na
+
C
N
CH3
O2N
NO2
CH3
CH3 COO
-
Na
+
18.
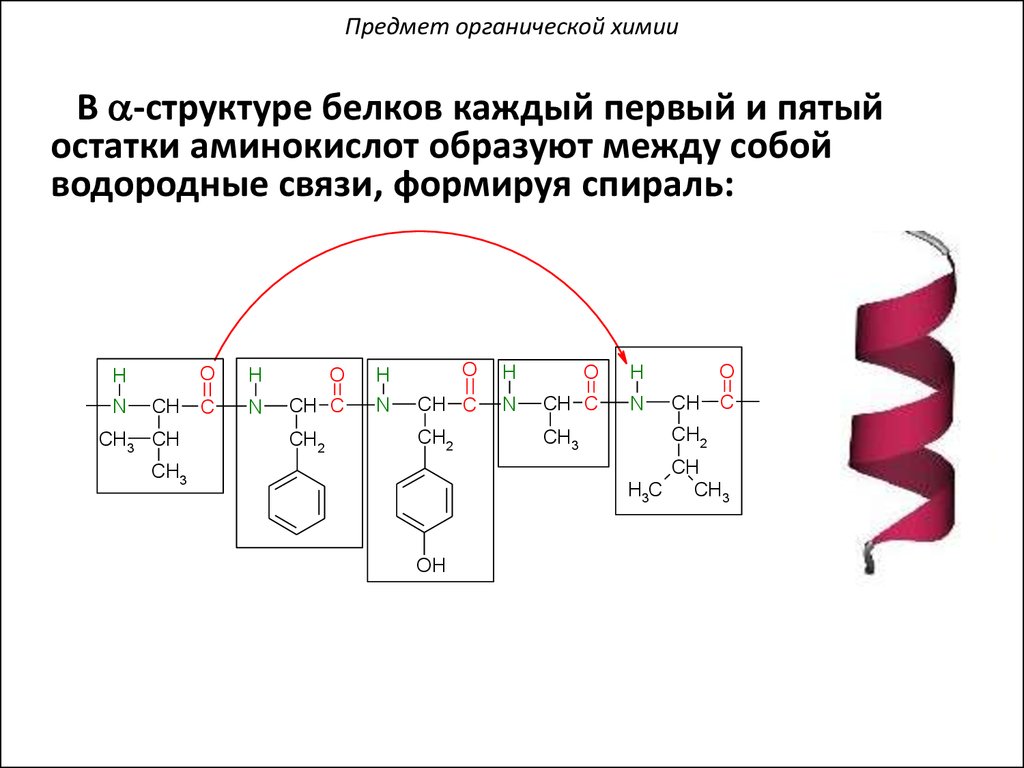
Предмет органической химииВ a-структуре белков каждый первый и пятый
остатки аминокислот образуют между собой
водородные связи, формируя спираль:
H
N
CH
CH3 CH
O
H
O
H
O
H
O
H
C
N
CH C
N
CH C
N
CH C
N
CH2
CH2
CH3
O
CH
C
CH2
CH
H3C
CH3
CH3
OH
19.
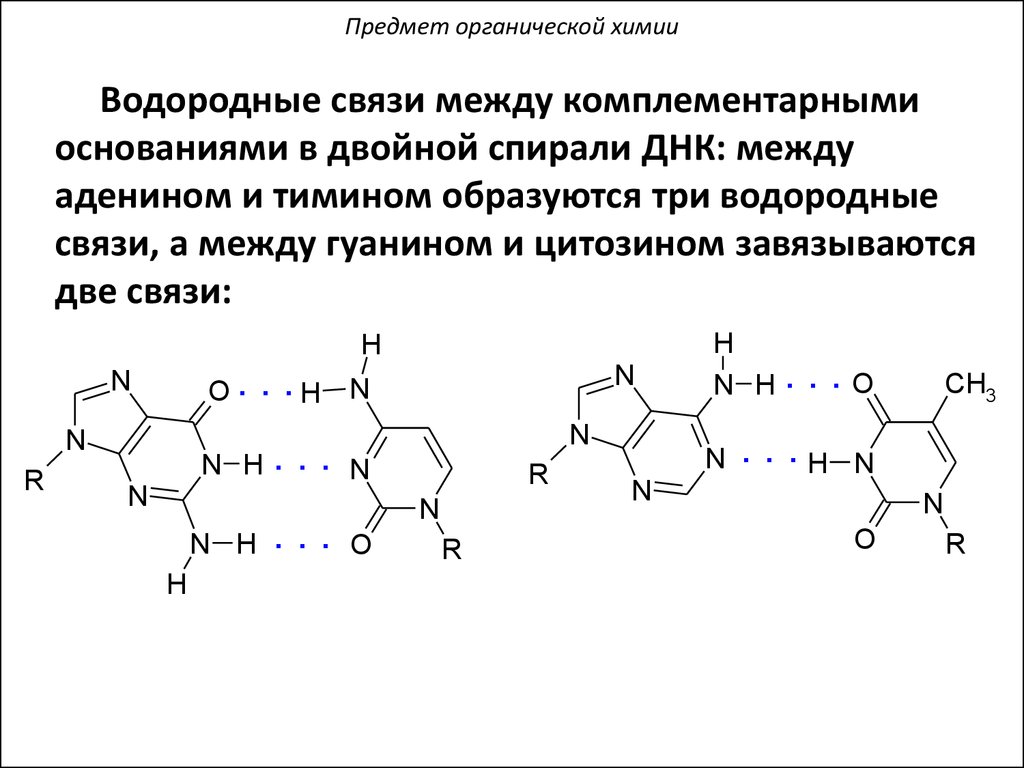
Предмет органической химииВодородные связи между комплементарными
основаниями в двойной спирали ДНК: между
аденином и тимином образуются три водородные
связи, а между гуанином и цитозином завязываются
две связи:
H
O.
N
N
R
. .H
N H
...
N
N
N
N H
H
...
N
N
R
N
O
R
H
N H.
N
..O
. . .H
CH3
N
N
N
O
R
20.
Предмет органической химииВ основном органические вещества
имеют молекулярное строение.
Для них характерна низкая температура
плавления, соединения не прочны.
21.
Предмет органической химииАтом углерода образует связи в
состоянии:
sp3-гибридизации (характерна
для алканов): С-С;
sp2-гибридизации (характерна
для алкенов): С=С;
sp-гибридизации (характерна для
алкинов): С≡С.
22.
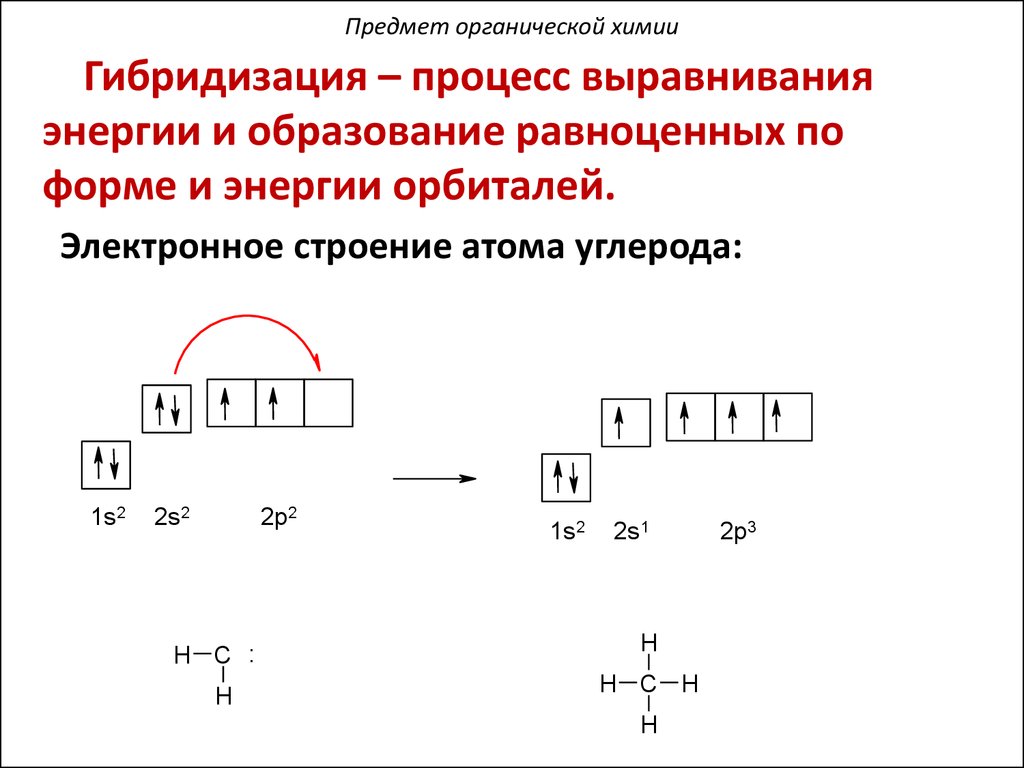
Предмет органической химииГибридизация – процесс выравнивания
энергии и образование равноценных по
форме и энергии орбиталей.
Электронное строение атома углерода:
1s2
2s2
2p2
H C :
H
1s2
2s1
H
H C H
H
2p3
23.
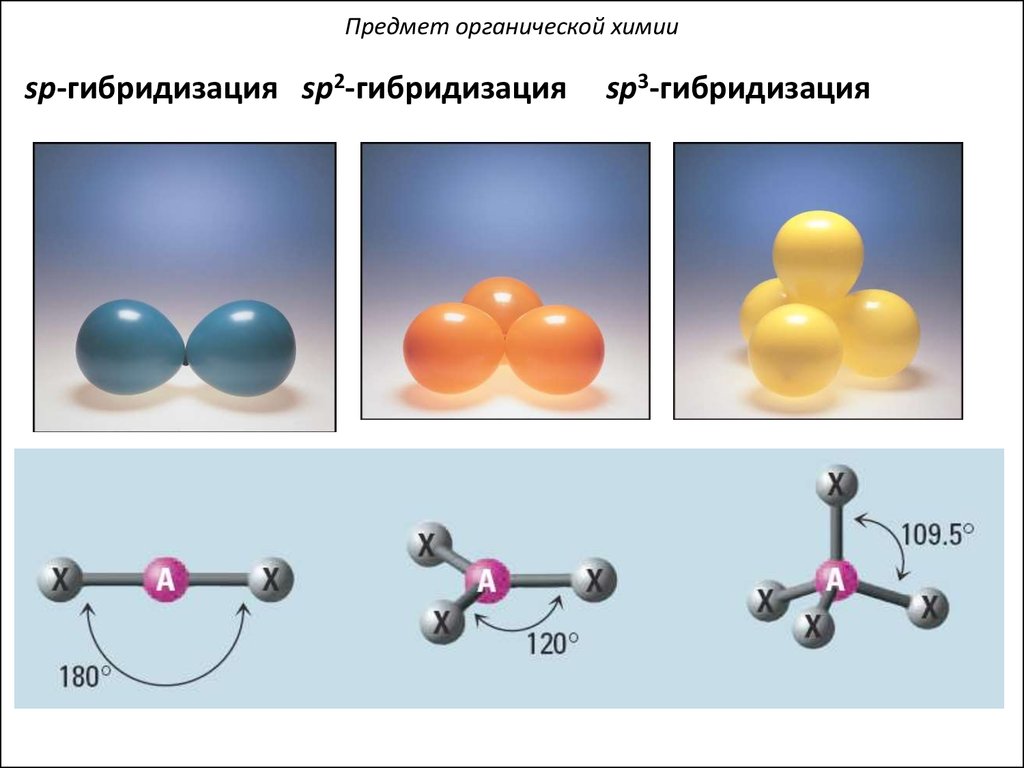
Предмет органической химииsp-гибридизация sp2-гибридизация
sp3-гибридизация
24.
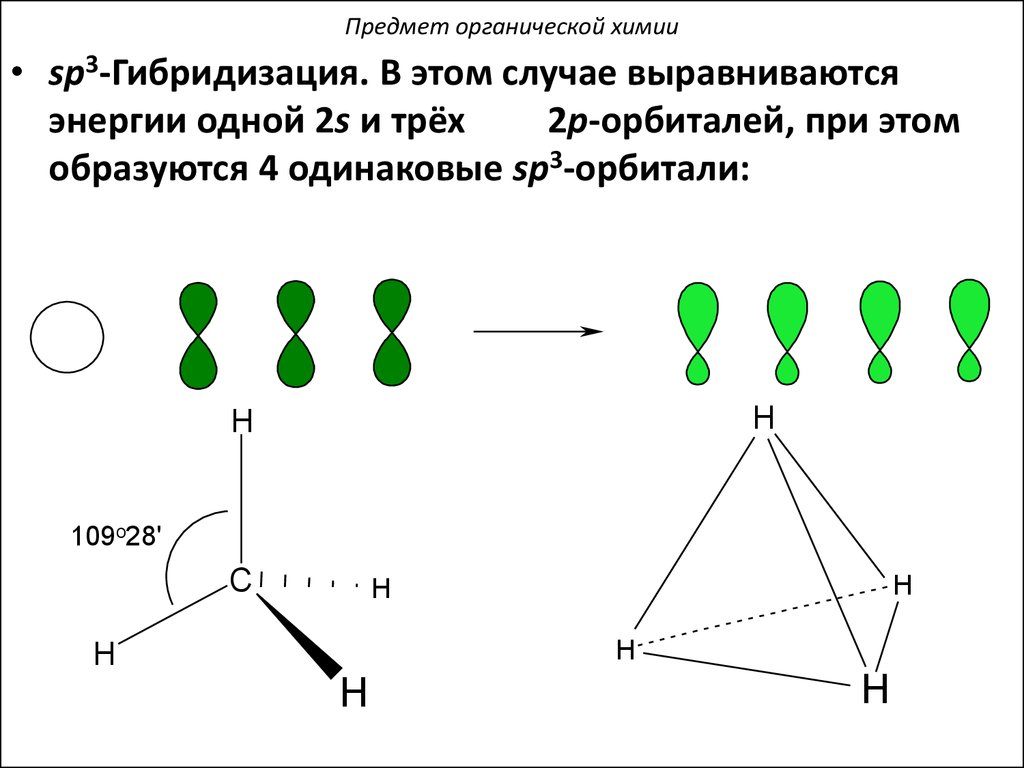
Предмет органической химии• sp3-Гибридизация. В этом случае выравниваются
энергии одной 2s и трёх
2p-орбиталей, при этом
образуются 4 одинаковые sp3-орбитали:
H
H
109o28'
C
C
H
H
H
H
H
H
25.
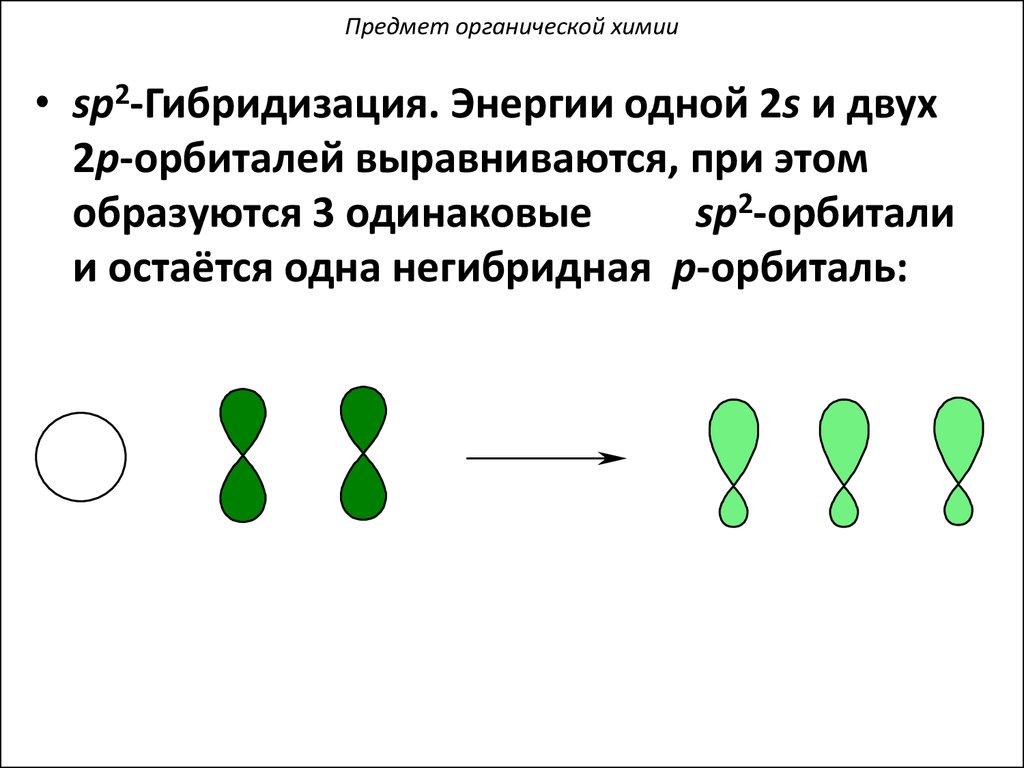
Предмет органической химии• sp2-Гибридизация. Энергии одной 2s и двух
2p-орбиталей выравниваются, при этом
образуются 3 одинаковые
sp2-орбитали
и остаётся одна негибридная p-орбиталь:
26.
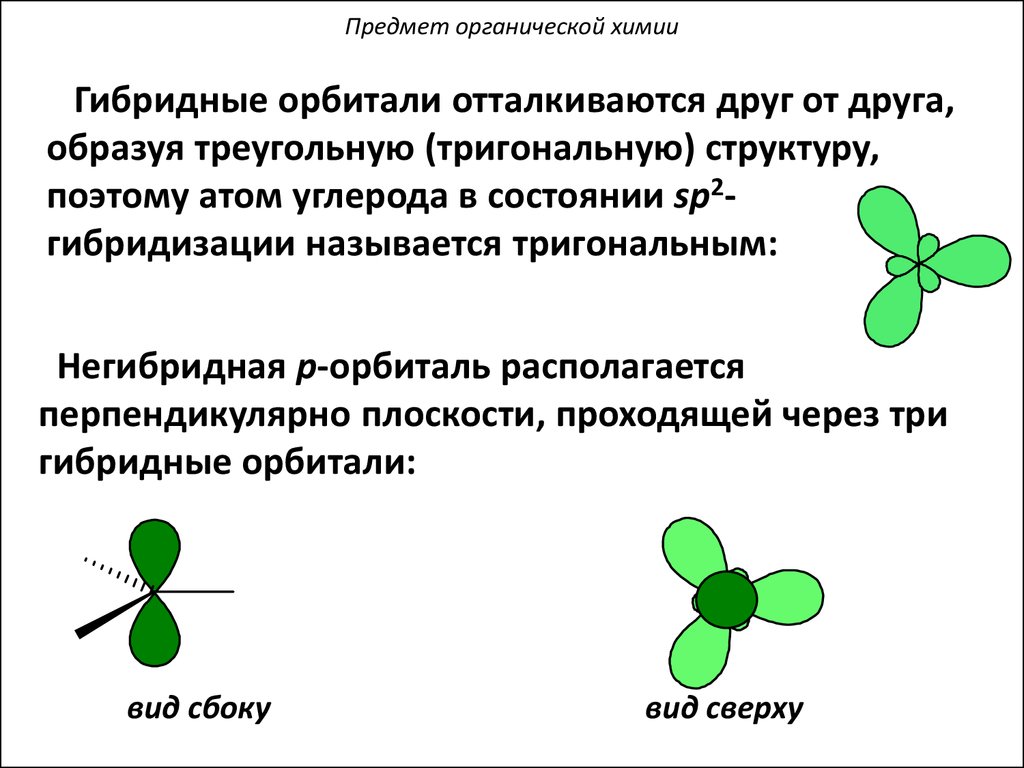
Предмет органической химииГибридные орбитали отталкиваются друг от друга,
образуя треугольную (тригональную) структуру,
поэтому атом углерода в состоянии sp2гибридизации называется тригональным:
Негибридная p-орбиталь располагается
перпендикулярно плоскости, проходящей через три
гибридные орбитали:
вид сбоку
вид сверху
27.
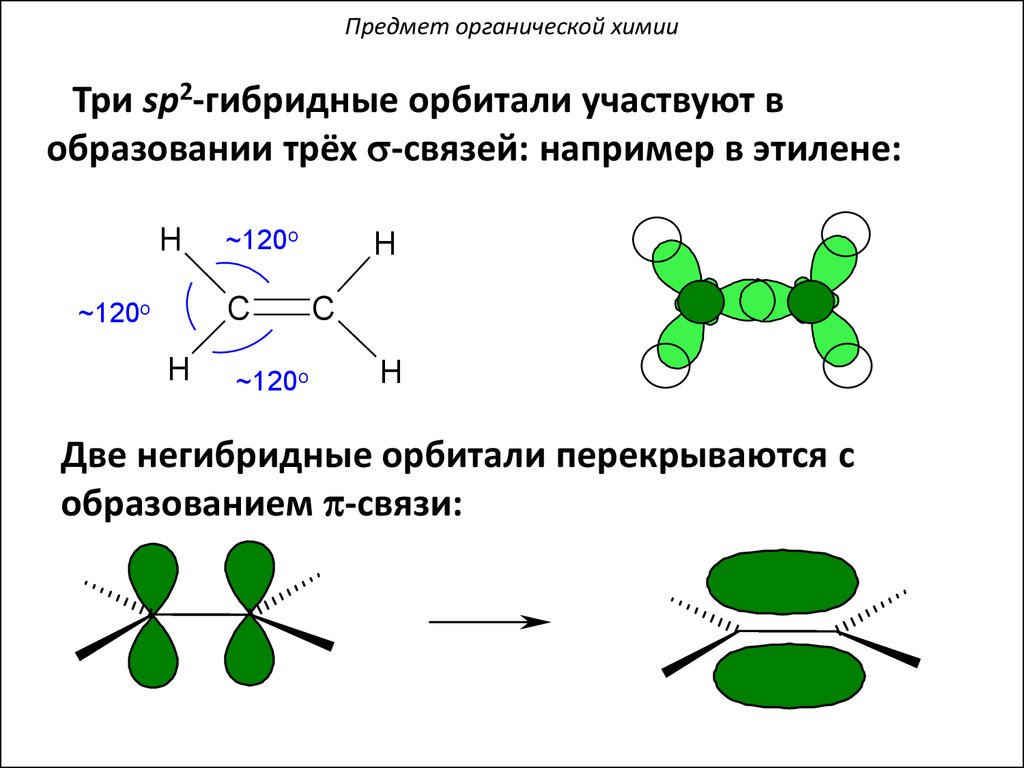
Предмет органической химииТри sp2-гибридные орбитали участвуют в
образовании трёх s-связей: например в этилене:
H
~120o
C
~120o
H
~120o
H
C
H
Две негибридные орбитали перекрываются с
образованием p-связи:
28.
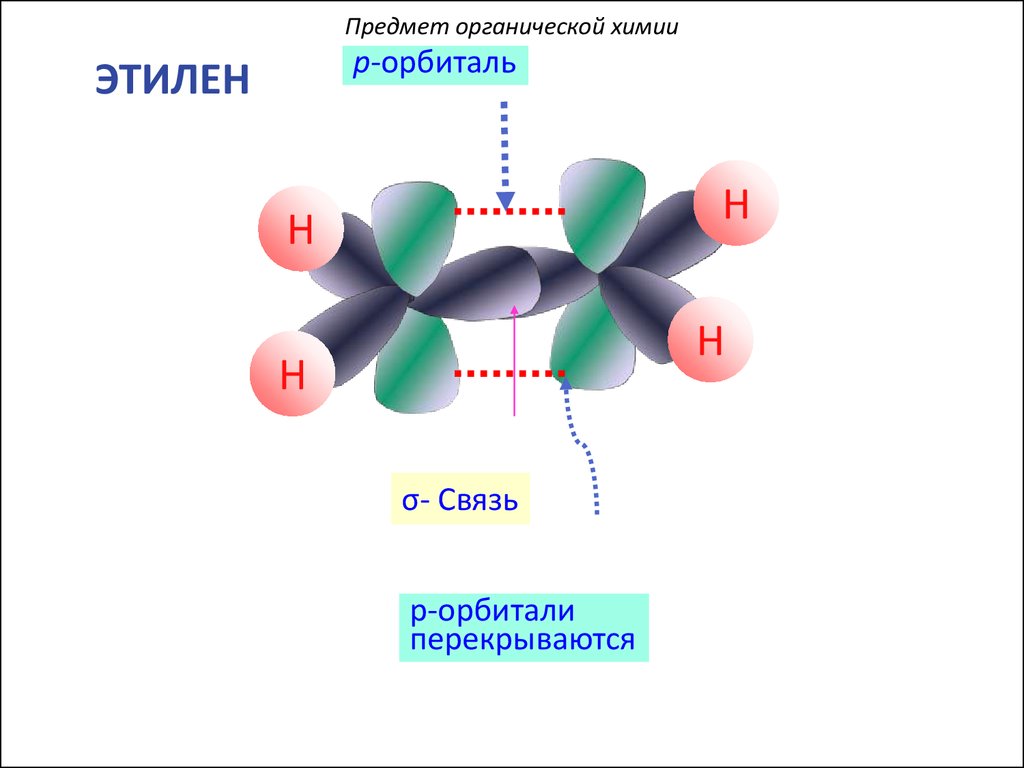
Предмет органической химииp-орбиталь
ЭТИЛЕН
H
H
H
H
σ- Связь
p-орбитали
перекрываются
29.
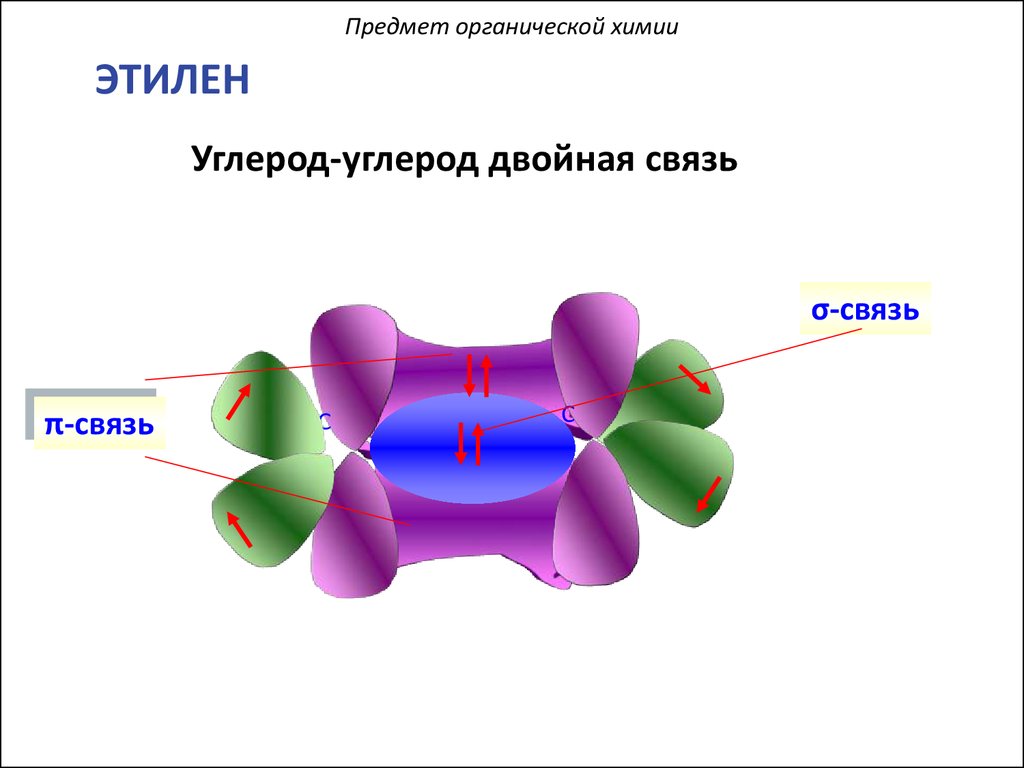
Предмет органической химииЭТИЛЕН
Углерод-углерод двойная связь
σ-связь
π-связь
C
C
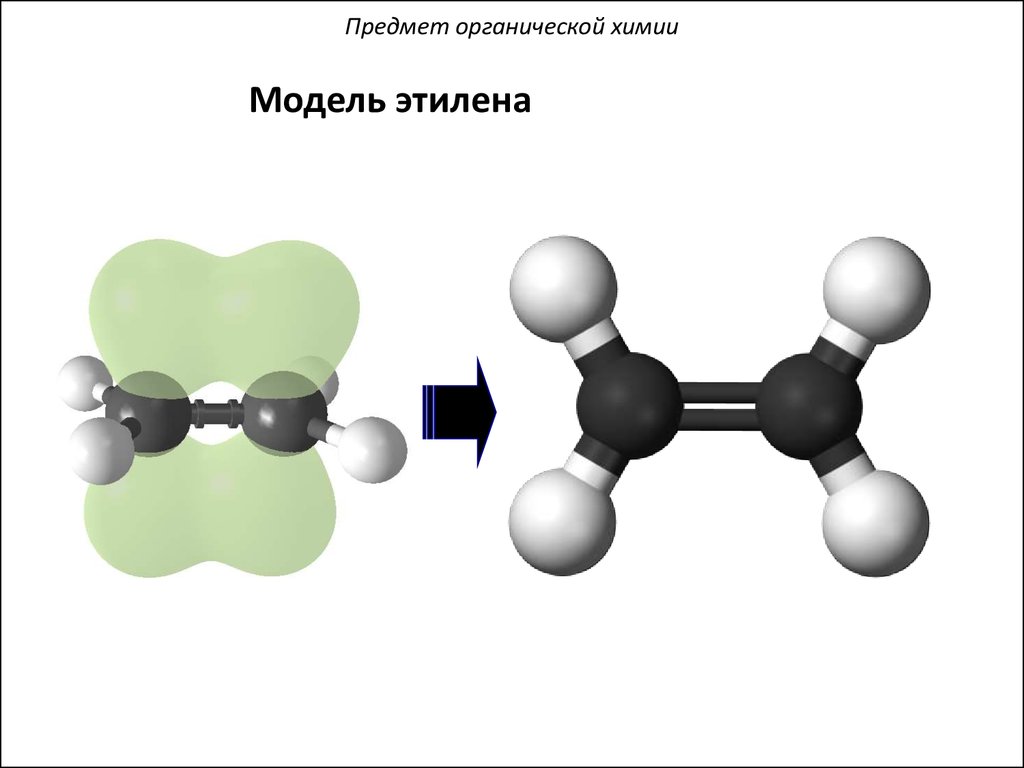
30.
Предмет органической химииМодель этилена
31.
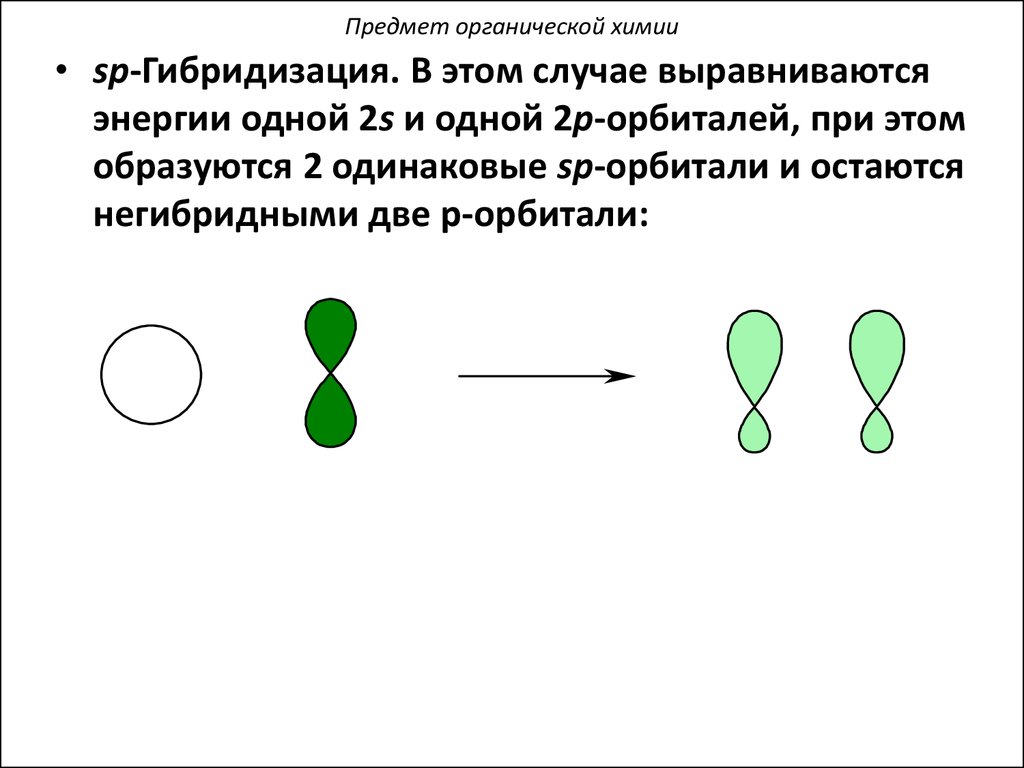
Предмет органической химии• sp-Гибридизация. В этом случае выравниваются
энергии одной 2s и одной 2p-орбиталей, при этом
образуются 2 одинаковые sp-орбитали и остаются
негибридными две p-орбитали:
32.
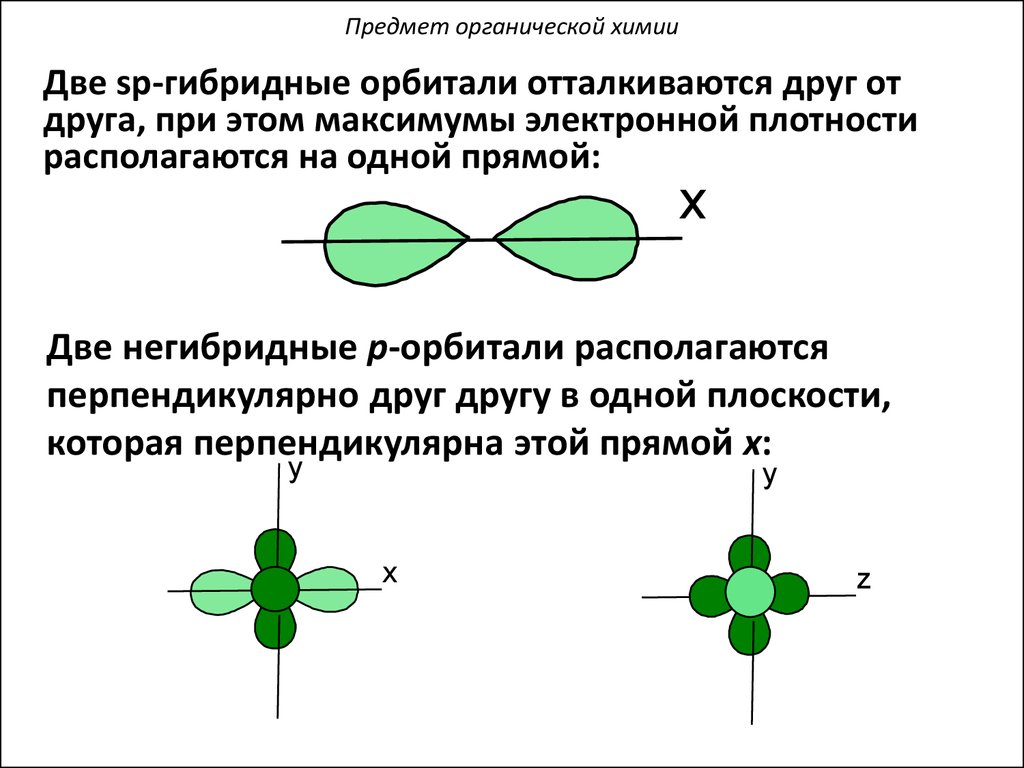
Предмет органической химииДве sp-гибридные орбитали отталкиваются друг от
друга, при этом максимумы электронной плотности
располагаются на одной прямой:
x
Две негибридные p-орбитали располагаются
перпендикулярно друг другу в одной плоскости,
которая перпендикулярна этой прямой x:
y
y
x
z
33.
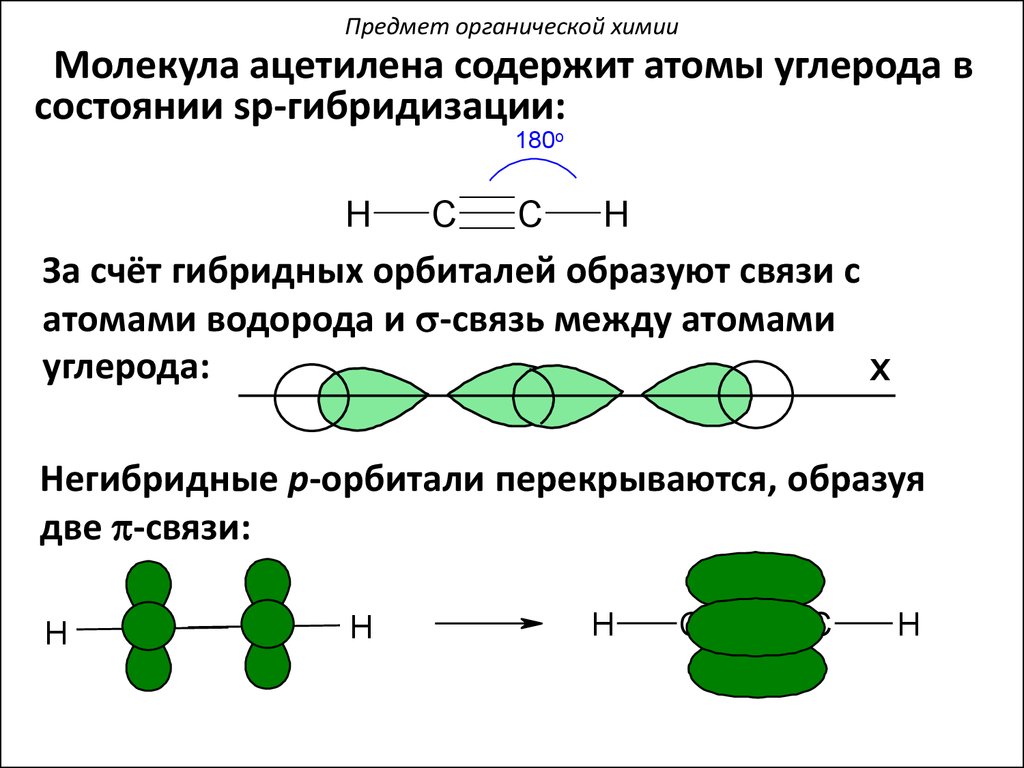
Предмет органической химииМолекула ацетилена содержит атомы углерода в
состоянии sp-гибридизации:
180o
H
C
C
H
За счёт гибридных орбиталей образуют связи с
атомами водорода и s-связь между атомами
углерода:
x
Негибридные p-орбитали перекрываются, образуя
две p-связи:
H
H
H
C
C
H
34. В молекулах алканов атомы углерода находятся в состоянии гибридизации:
ТестыВ молекулах алканов атомы углерода
находятся в состоянии гибридизации:
1) sp2
3) sp
2) sp3
4) sp2d
35. Атомов углерода в состоянии sp2-гибридизации нет в молекуле:
ТестыАтомов углерода в состоянии
sp2-гибридизации нет в молекуле:
а) бромбензола
в) ацетилена
б) толуола
г) бутадиена-1,3
36. Валентный угол и длина связи C-C в молекулах алканов соответственно равны:
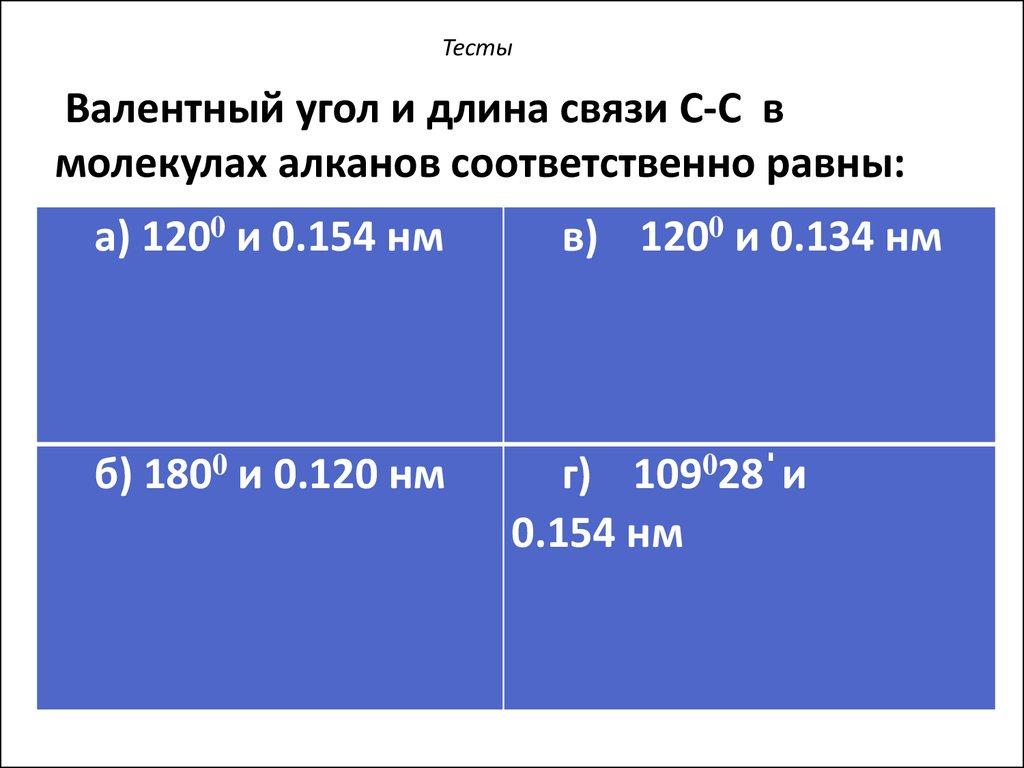
ТестыВалентный угол и длина связи C-C в
молекулах алканов соответственно равны:
а) 1200 и 0.154 нм
б) 1800 и 0.120 нм
в) 1200 и 0.134 нм
г) 109028 и
0.154 нм
37. Какие из приведенных утверждений об алкенах и их свойствах верны? А. В молекулах алкенов все атомы углерода находятся в состоянии sp2-гибрид
ТестыКакие из приведенных утверждений об
алкенах и их свойствах верны?
А. В молекулах алкенов все атомы углерода
находятся в состоянии sp2-гибридизации.
Б.Бутен-1 способен к образованию
цистранс-изомеров.
а) верно только А
б) верно только Б
в) верны оба
утверждения
г) оба утверждения
неверны
38. Классификация органических соединений
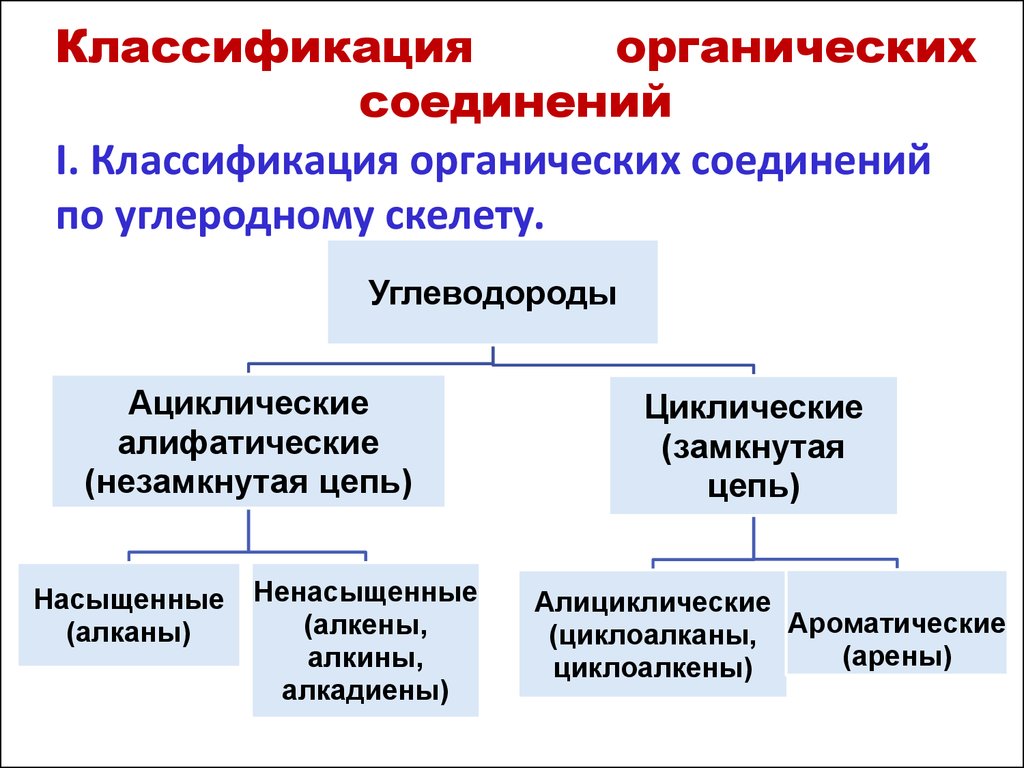
I. Классификация органических соединенийпо углеродному скелету.
Углеводороды
Ациклические
алифатические
(незамкнутая цепь)
Насыщенные
(алканы)
Ненасыщенные
(алкены,
алкины,
алкадиены)
Циклические
(замкнутая
цепь)
Алициклические
(циклоалканы, Ароматические
(арены)
циклоалкены)
39. Классификация органических соединений
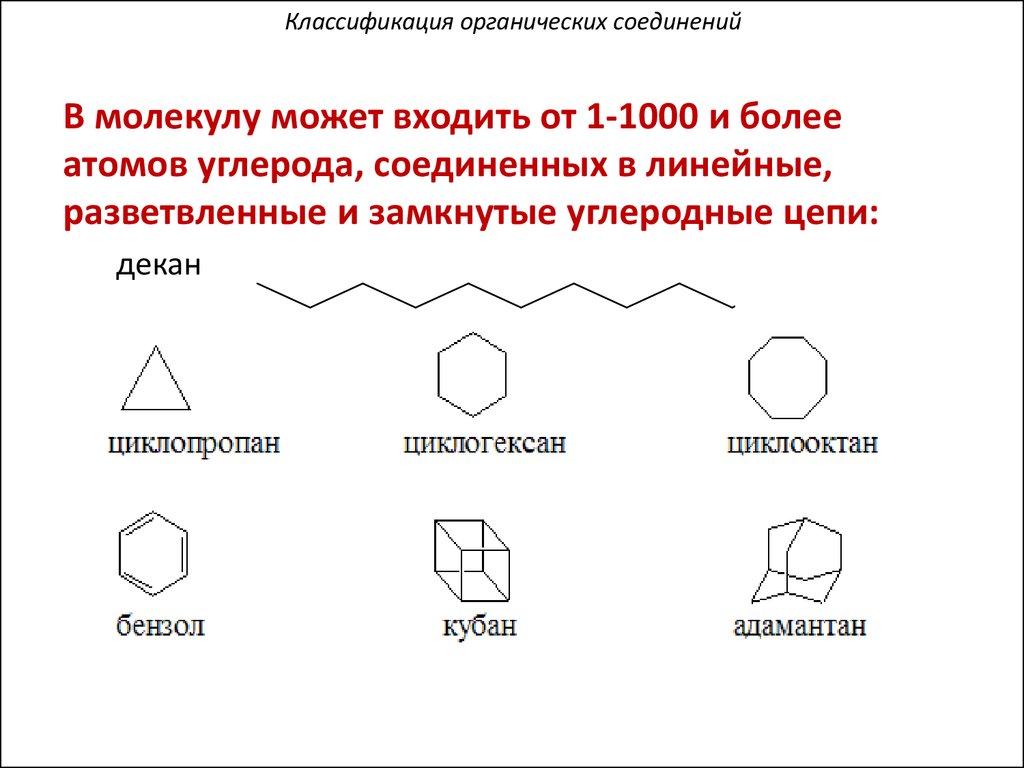
В молекулу может входить от 1-1000 и болееатомов углерода, соединенных в линейные,
разветвленные и замкнутые углеродные цепи:
декан
40. Классификация органических соединений
OHO
H2N
O
O
OH
H2C
OH
OH
HO
OH
OH
O
OH
OH
HO
OH
CH3
OH
OH
OH
OH
OH
O
O
CH3
OH
CH3
HO
OH
O
OH
OH
OH
OH
HO
N
H
N
H
O
CH3
H3C
OH
HO
OH
HO
O
OH
O
OH
H3C
O
CH3
OH
OH
O
OH
OH
HO
OH
OH
OH
OH
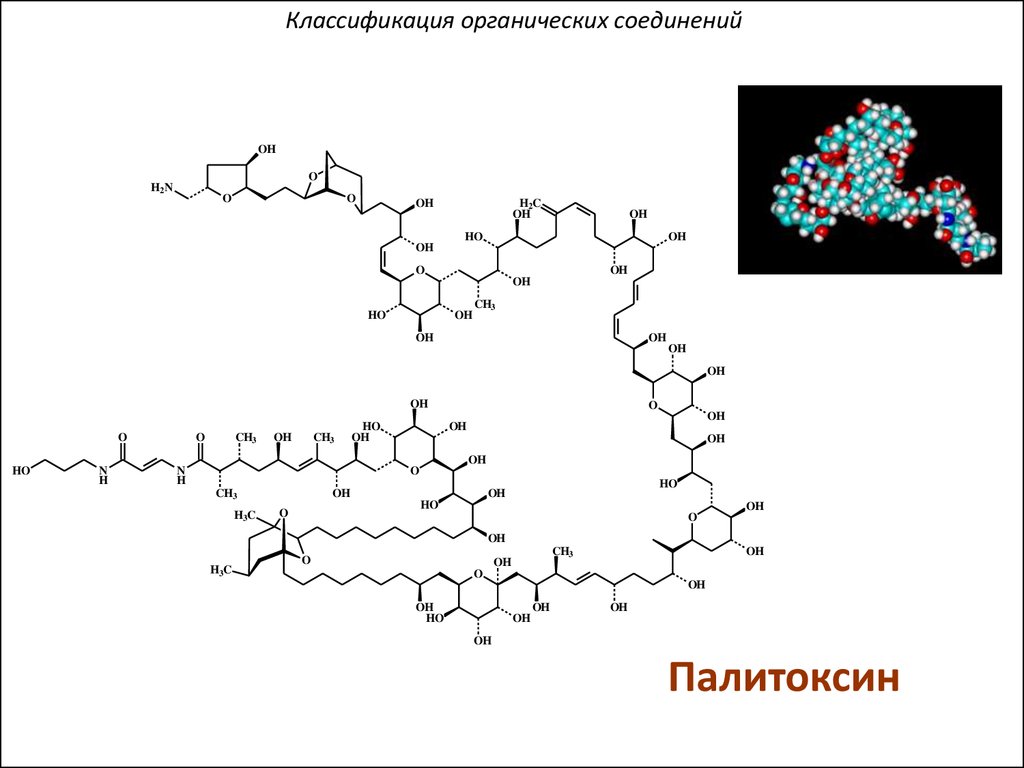
Палитоксин
41. Соединения, содержащие в цикле кроме углерода атомы других элементов называют:
ТестыСоединения, содержащие в цикле кроме
углерода атомы других элементов
называют:
1)
карбоциклические
3)
полициклические
2)
гетероциклические
4)
конденсированные
42.
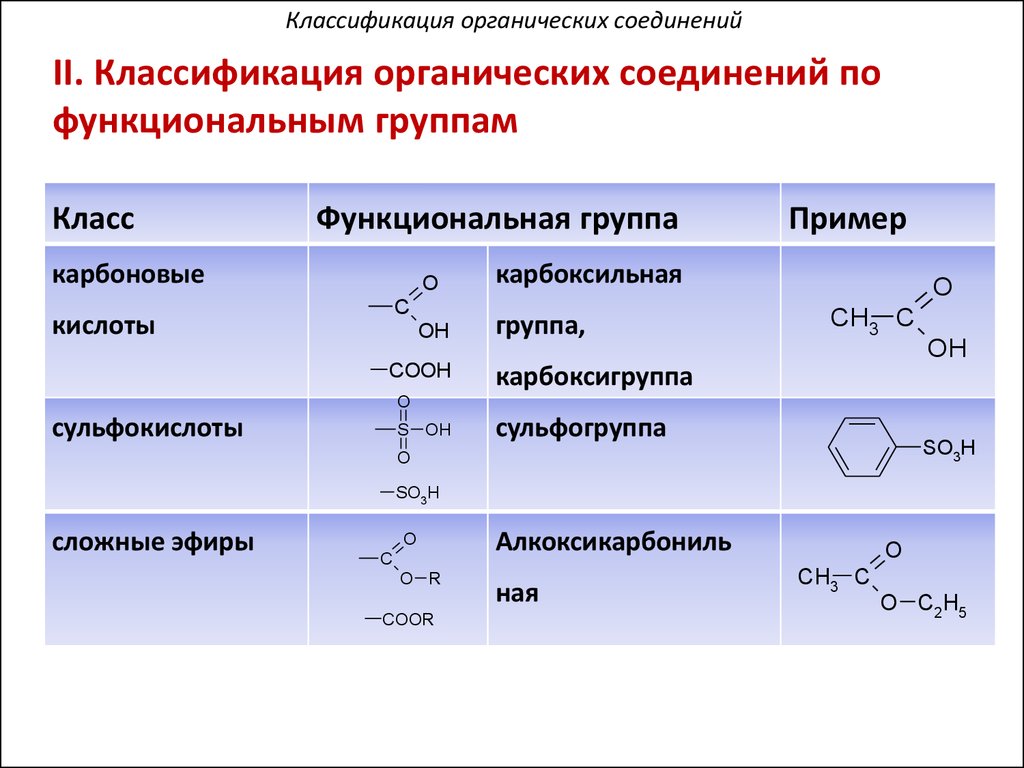
Классификация органических соединенийII. Классификация органических соединений по
функциональным группам
Класс
Функциональная группа
карбоновые
O
карбоксильная
OH
группа,
C
кислоты
COOH
Пример
O
CH3 C
OH
карбоксигруппа
O
сульфокислоты
S OH
сульфогруппа
SO3H
O
SO3H
сложные эфиры
O
Алкоксикарбониль
O R
ная
C
COOR
O
CH3 C
O C2H5
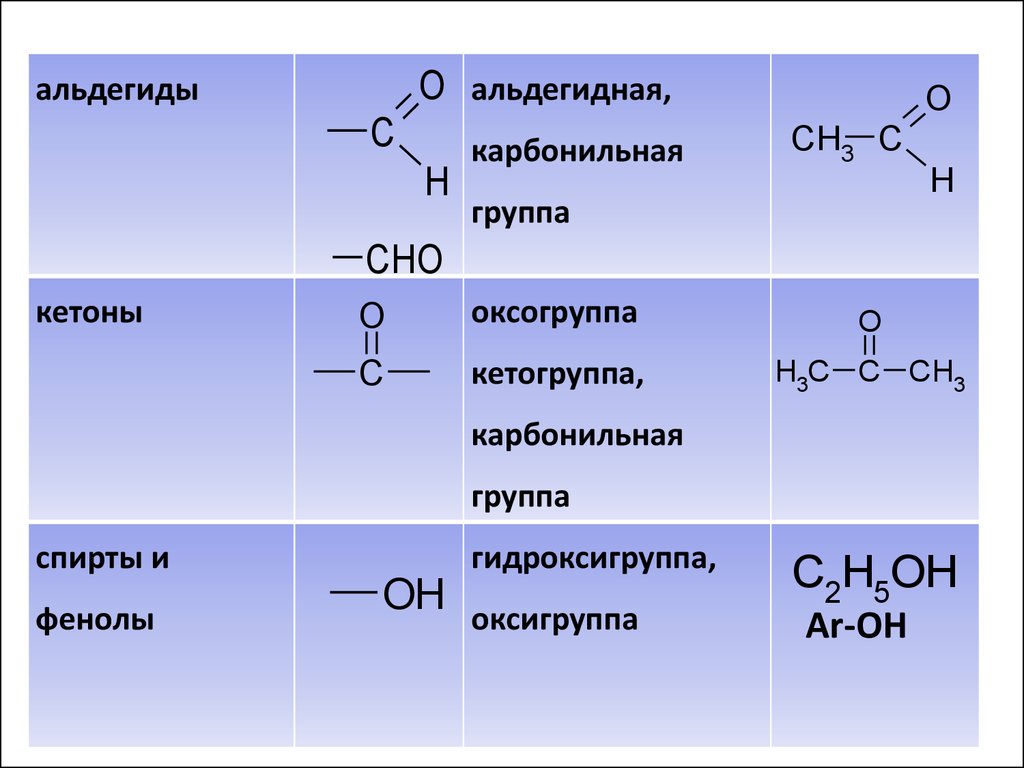
43.
O альдегидная,альдегиды
C
H
карбонильная
O
CH3 C
H
группа
CHO
кетоны
O
оксогруппа
O
C
кетогруппа,
H3C C CH3
карбонильная
группа
спирты и
фенолы
гидроксигруппа,
OH оксигруппа
C2H5OH
Ar-OH
44.
аминыпростые эфиры
нитросоединения
NH2
O R
+ O
N
аминогруппа
алкоксигруппа
C2H5 NH2
C2H5 O
C2H5
нитрогруппа
O
CH3NO2
NO2
галогенопроизводн -F, -Cl, - галоген
ые
Br, -I
C2H5Cl
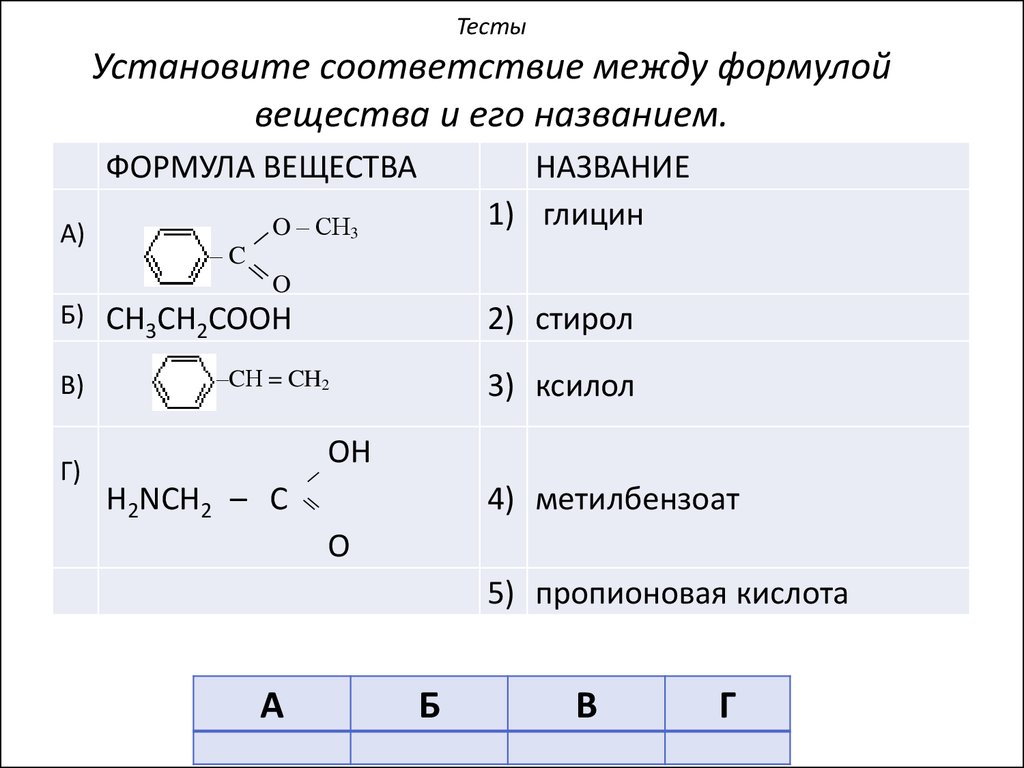
45. Установите соответствие между формулой вещества и его названием.
ТестыУстановите соответствие между формулой
вещества и его названием.
ФОРМУЛА ВЕЩЕСТВА
А)
–C
НАЗВАНИЕ
1) глицин
O – СН3
O
Б) CH3CH2COOH
В)
Г)
2) стирол
–CН = CH2
3) ксилол
OH
H2NCH2 – C
4) метилбензоат
O
5) пропионовая кислота
А
Б
В
Г
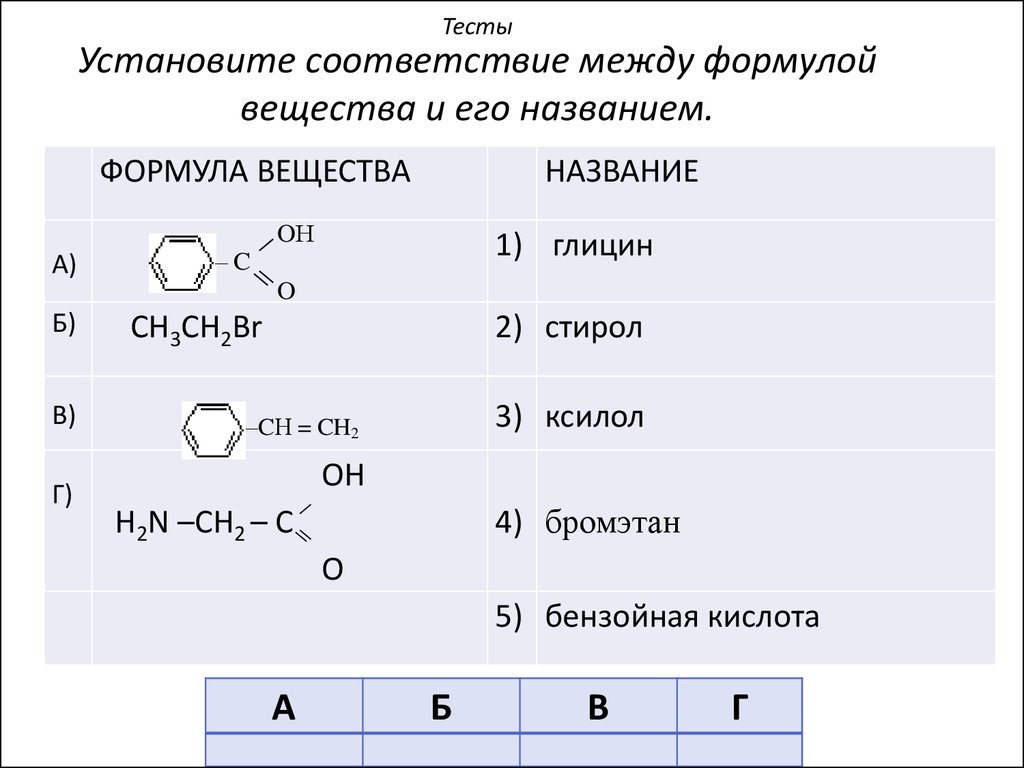
46. Установите соответствие между формулой вещества и его названием.
ТестыУстановите соответствие между формулой
вещества и его названием.
ФОРМУЛА ВЕЩЕСТВА
НАЗВАНИЕ
OН
А)
1) глицин
–C
O
Б)
В)
Г)
CH3CH2Br
2) стирол
3) ксилол
–CН = CH2
OH
4) бромэтан
H2N –CH2 – C
O
5) бензойная кислота
А
Б
В
Г
47. Установите соответствие между формулой вещества и классом соединения.
ТестыУстановите соответствие между формулой
вещества и классом соединения.
ФОРМУЛА ВЕЩЕСТВА
А)
КЛАСС СОЕДИНЕНИЯ
формальдегид
1) арены
Б) пропанол-2
2) альдегиды
В) толуол
3) спирты
Г)
этилен
4) алкены
5) алкины
А
Б
В
Г
48. Установите соответствие между формулой вещества и классом соединения.
ТестыУстановите соответствие между формулой
вещества и классом соединения.
ФОРМУЛА ВЕЩЕСТВА
А)
КЛАСС СОЕДИНЕНИЯ
этиленгликоль
1) арены
Б) пентанол-2
2) фенол
В) бензиловый спирт
3) спирты
Г)
фенол
4) альдегиды
5) карбоновые кислоты
А
Б
В
Г
49. Установите соответствие между формулой вещества и классом соединения.
ТестыУстановите соответствие между формулой
вещества и классом соединения.
ФОРМУЛА ВЕЩЕСТВА
А)
глицерин
КЛАСС СОЕДИНЕНИЯ
1) углеводы
Б) глюкоза
2) фенол
В) глицин
3) спирты
Г)
1,2-диметилбензол
4) о-ксилол
5) аминокислоты
А
Б
В
Г
50.
СПАСИБО ЗАВАШЕ
ВНИМАНИЕ!




















 Химия
Химия