Похожие презентации:
α-Аминокислоты. Белки
1.
α-АминокислотыБелки
Лекция по биоорганической химии
доц. Яглицкой Н.Н.
2.
» R-СН2-СН2-СН-СООН3.
4.
Классификация α- аминокислот1. По природе заряда:
неполярные(гидрофобные)
полярные (гидрофильные)
а) ионогенные
положительно
заряженные
отрицательно
заряженные
б) неионогенные
5.
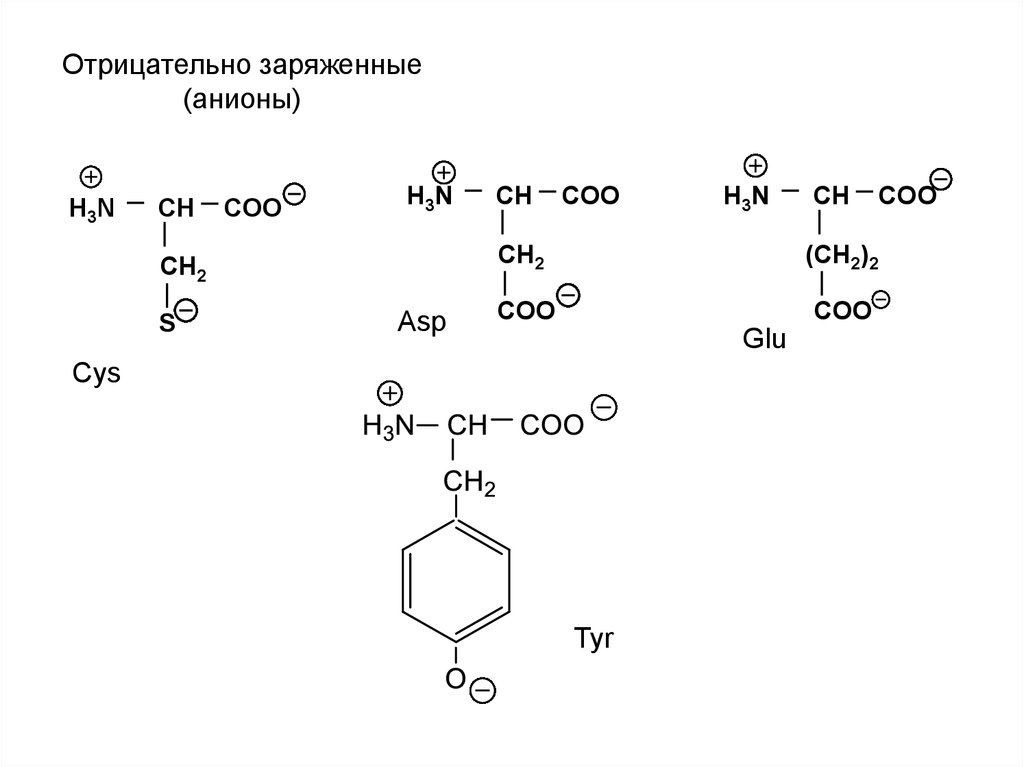
Отрицательно заряженные(анионы)
H3N
CH
COO
H3N
CH2
S
Asp
CH
COO
H3N
CH
COO
CH2
(CH2)2
COO
COO
Glu
Cys
Tyr
6.
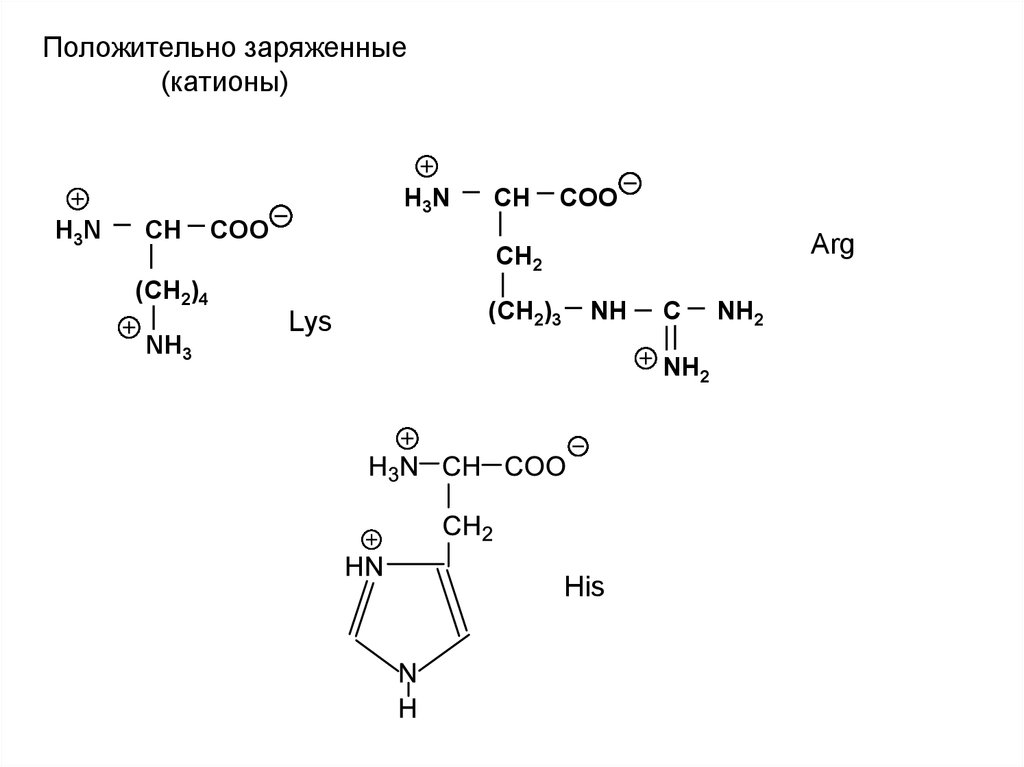
Положительно заряженные(катионы)
H3N
H3N
CH
CH
COO
COO
Arg
CH2
(CH2)4
NH3
Lys
(CH2)3
NH
C
NH2
His
NH2
7.
2. Природа радикала: ароматические (Phe, Tyr)гетероциклические (Trp, His, Pro)
алифатические (Ala, Lys, Asn)
3. Медико-биологическое значение:
незаменимые: Val, Leu, Jle, Lys, Tre, Met, Phe, Trp
заменимые: Ala, Asn, Asp, Gly, Gln, Glu, Pro,Ser, Tyr, Cys
частично заменимые: Arg, His
8.
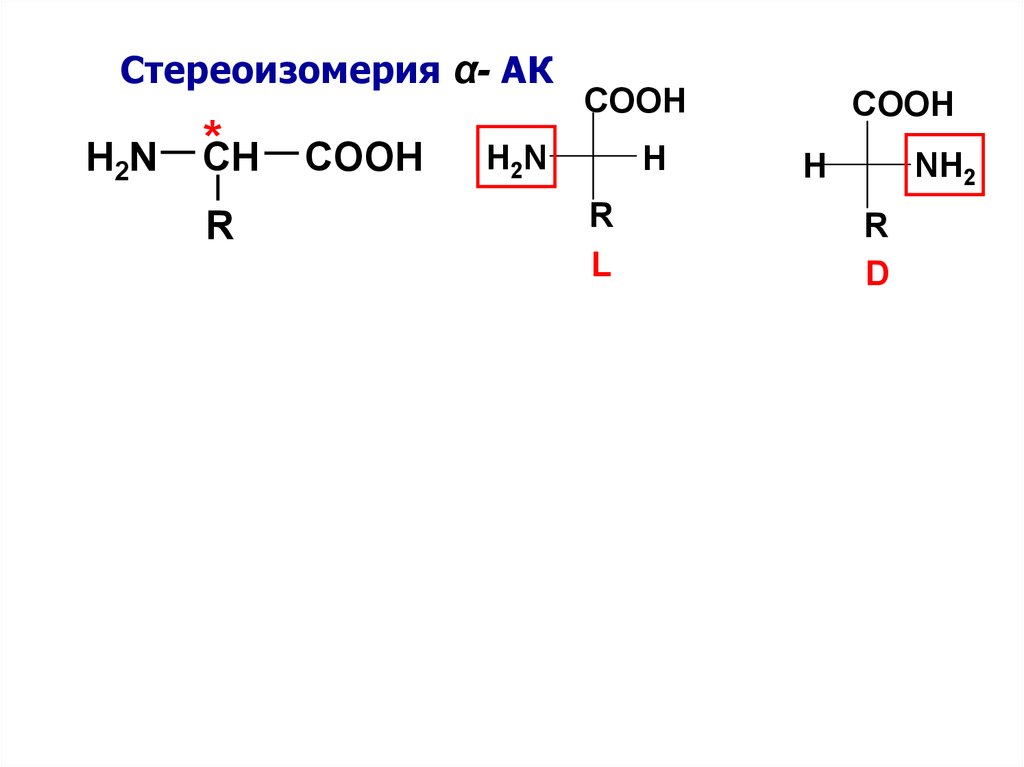
Стереоизомерия α- АКH2N
*
CH
R
COOH
COOH
H2N
H
R
L
COOH
NH2
H
R
D
9.
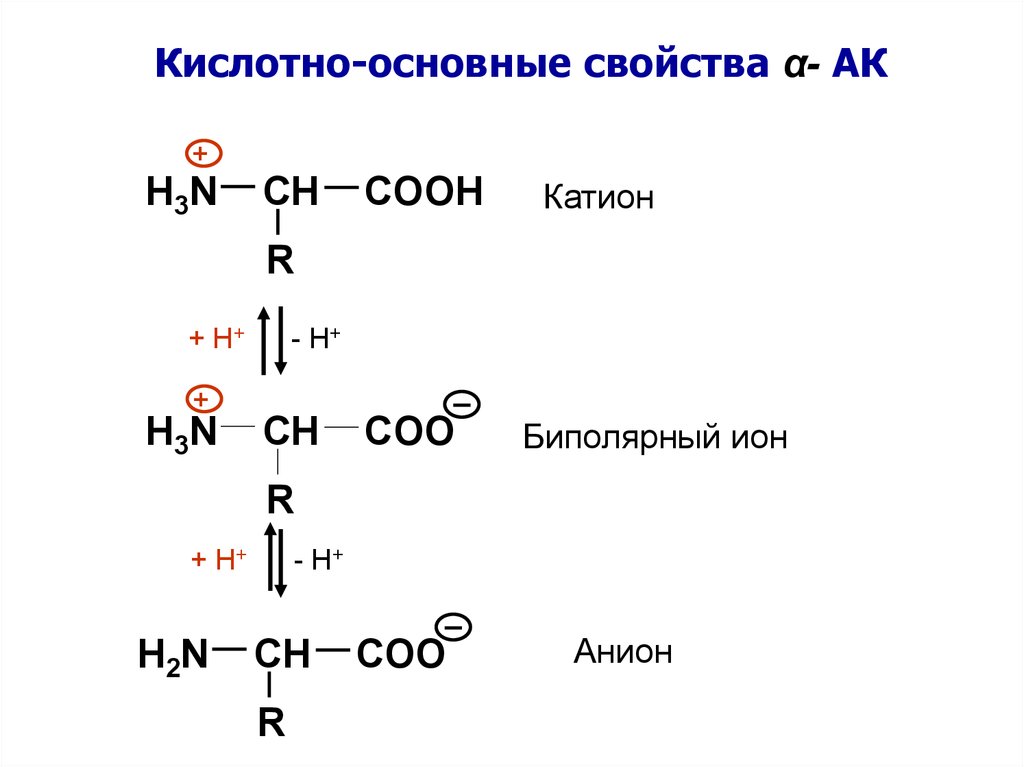
Кислотно-основные свойства α- АК+
H3N
CH
COOH
Катион
R
+ H+
- H+
+
H3N
CH
COO
Биполярный ион
R
+ H+
H2N
- H+
CH
R
COO
Анион
10.
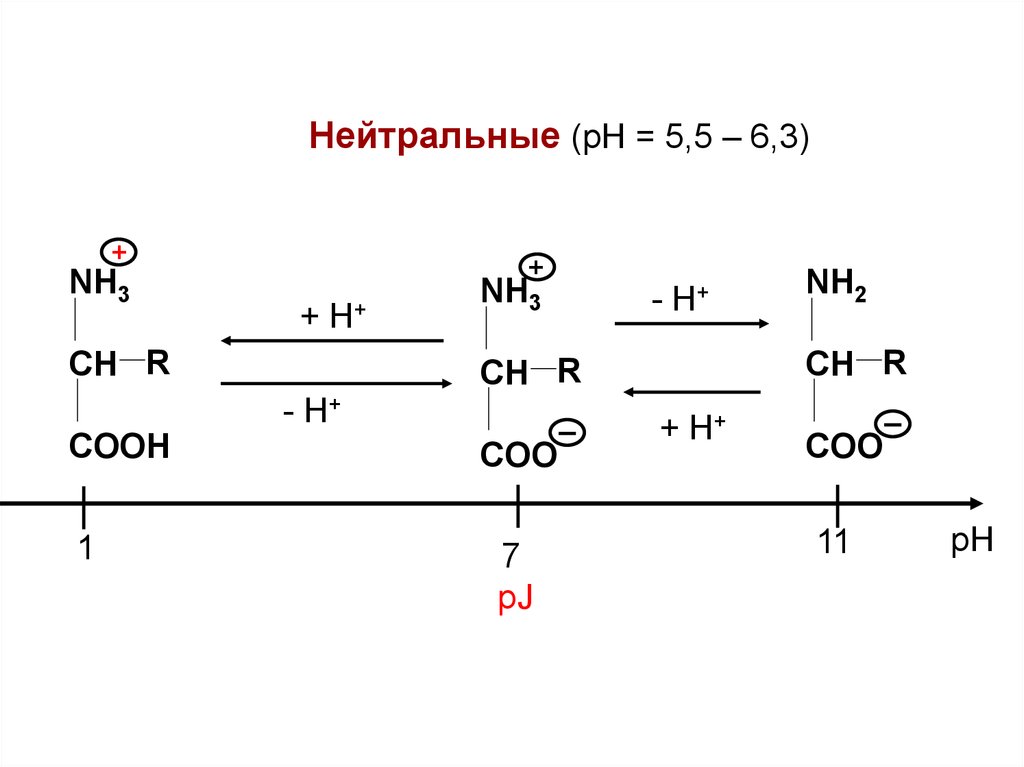
Нейтральные (рН = 5,5 – 6,3)+
NH3
+
+ H+
CH R
NH3
1
COO
7
pJ
NH2
CH R
CH R
- H+
COOH
- H+
+ H+
COO
11
pH
11.
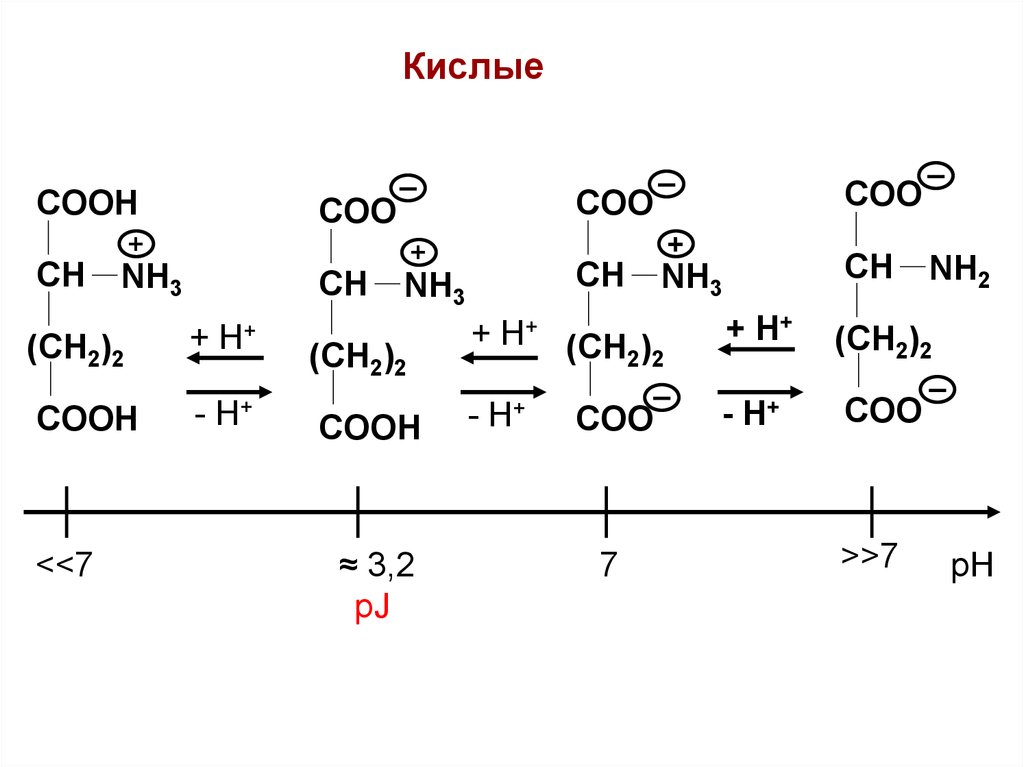
КислыеCOOH
+
CH
CH
(CH2)2
+ H+
COOH
- H+
<<7
+
+
NH3
COO
COO
COO
CH
NH3
CH
NH3
NH2
(CH2)2
+ H+ (CH )
2 2
+ H+
(CH2)2
COOH
- H+
- H+
COO
≈ 3,2
рJ
COO
7
>>7
pH
12.
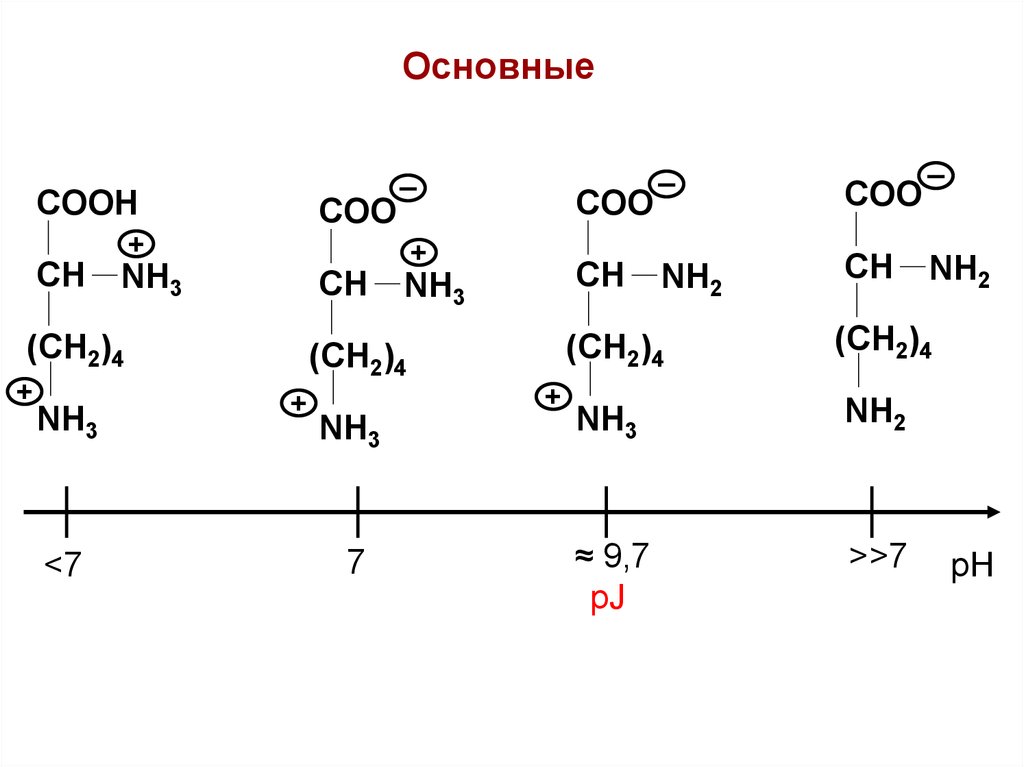
ОсновныеCOOH
+
CH
+
NH3
CH
(CH2)4
+
NH3
<7
CH
NH3
NH2
CH
NH2
(CH2)4
(CH2)4
NH3
NH3
NH2
7
≈ 9,7
рJ
>>7
(CH2)4
+
COO
COO
COO
+
pH
13.
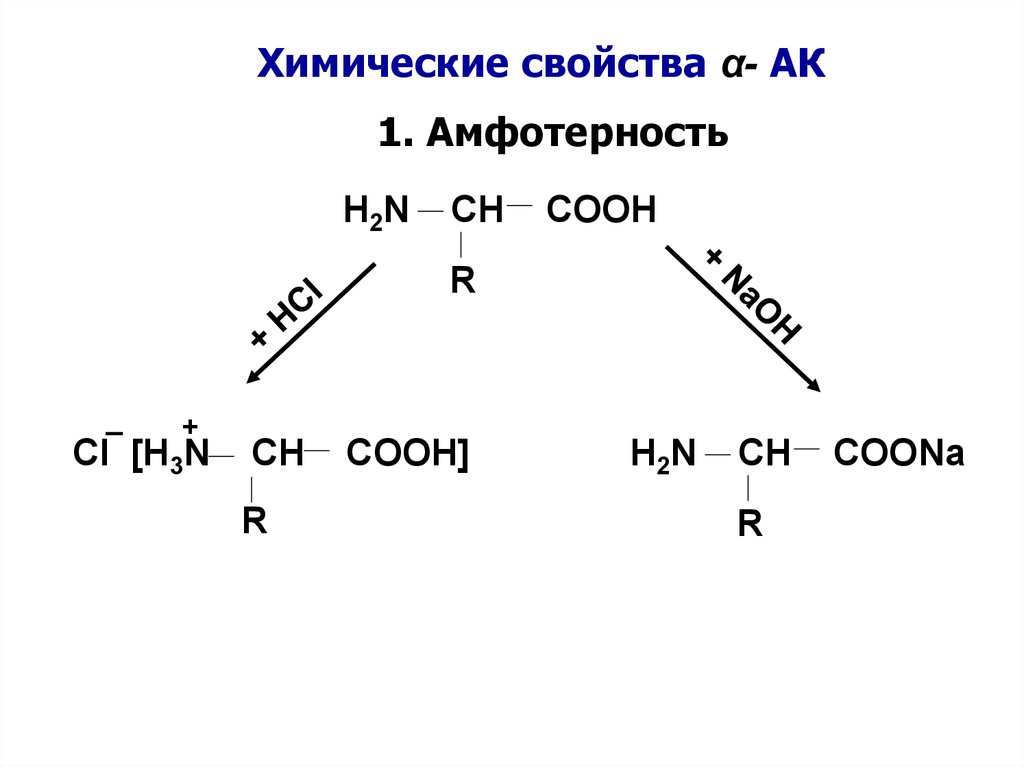
Химические свойства α- АК1. Амфотерность
H2N
CH
COOH
R
+
Cl [H3N
CH
R
COOH]
H2N
CH
R
COONa
14.
2.Реакции по СООН-группеЭтерификация
O
R
CH
C
- NH4Cl
+
R’ OH
OH
NH2
+ NH3
HCl(сух)
H 2О
O
R
CH
C
NH2
сл. эфир
OR’
O
R
CH
+
C
NH3Cl
OR’
15.
3.Реакции по NH2 группеа. Ацилирование
O
R
CH
NH2
COOH + R1
δ+
C
Cl
SN
- HCl
R
CH
COOH
NH
C
O
R1
16.
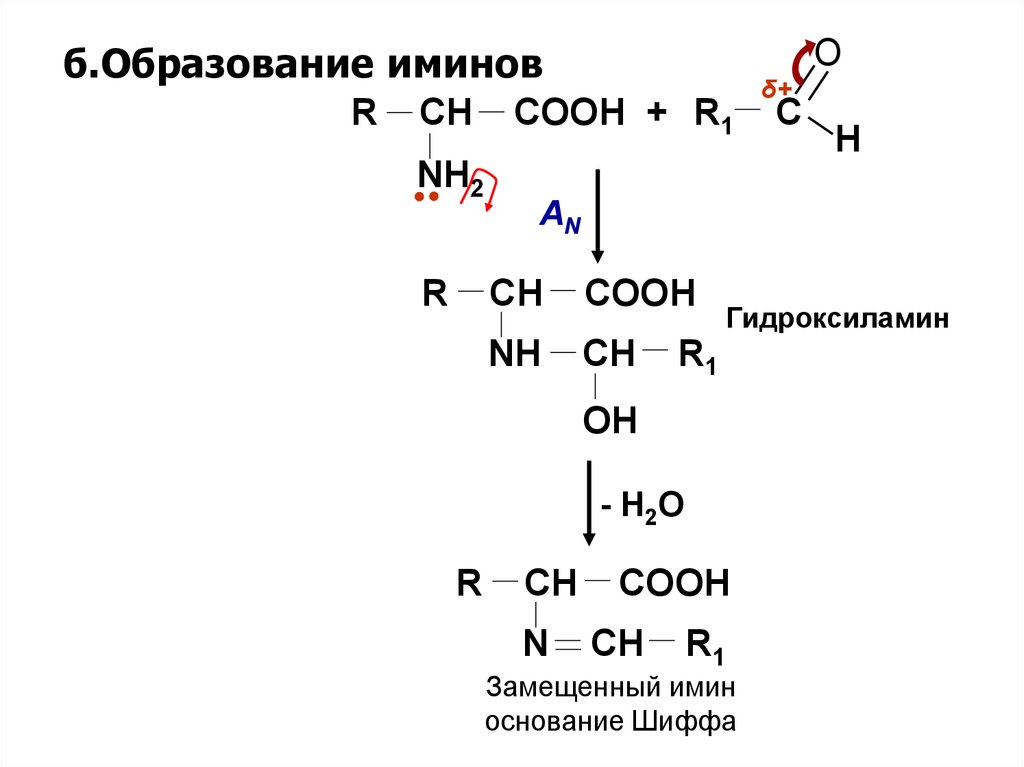
б.Образование иминовR
CH
NH2
R
O
COOH + R1
C
H
AN
CH
COOH
NH
CH
Гидроксиламин
R1
OH
- H2O
R
δ+
CH
N
COOH
CH
R1
Замещенный имин
основание Шиффа
17.
18.
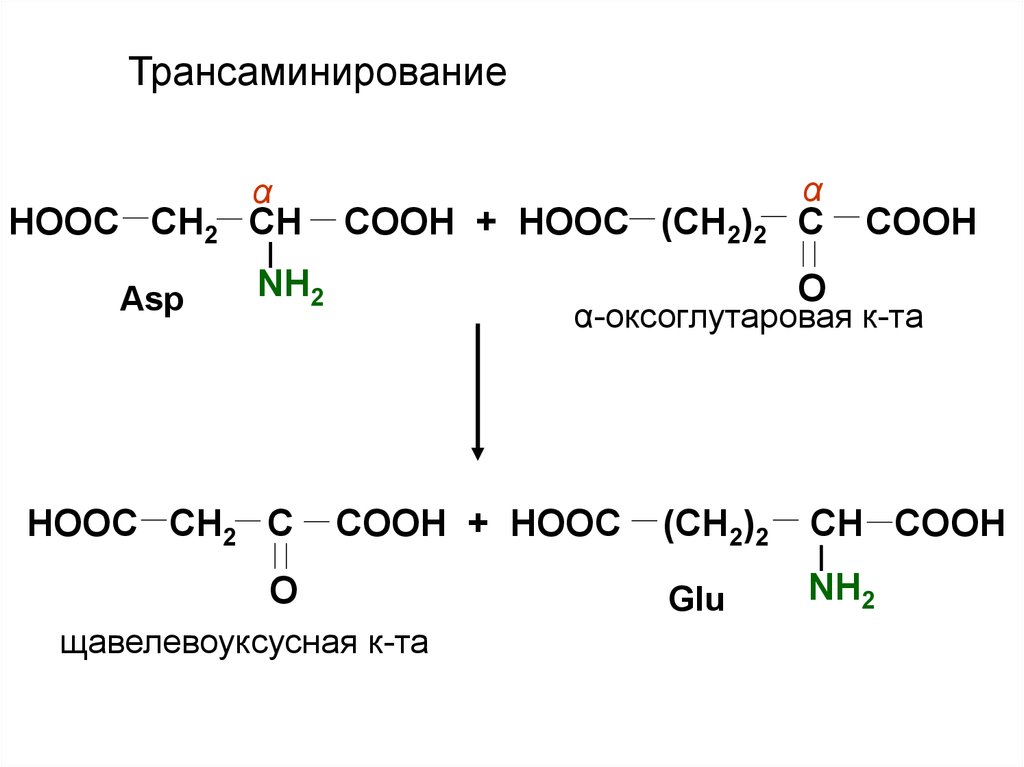
Трансаминированиеα
HOOC CH2 CH
Asp
α
COOH + HOOC (CH2)2 C
NH2
HOOC CH2 C
COOH
O
α-оксоглутаровая к-та
COOH + HOOC
O
щавелевоуксусная к-та
(CH2)2
CH COOH
Glu
NH2
19.
Пиридоксалевый катализO
O
H
C
C
HOCH2
OH
+
N
H
P
OH
OCH2
+
CH3
H
Пиридоксаль (PL)
(витамин В6)
N
CH3
H
Пиридоксальфосфат (PLP)
(витамин В6)
20.
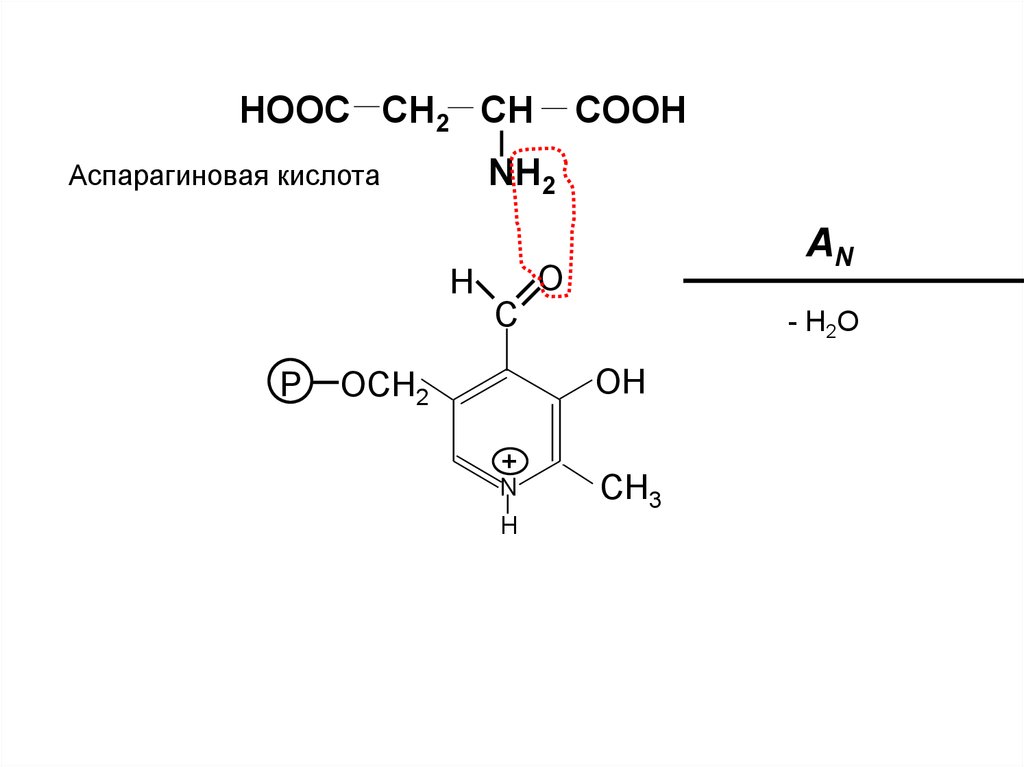
HOOC CH2 CHCOOH
NH2
Аспарагиновая кислота
AN
O
H
C
P
- H 2O
OH
OCH2
+
N
H
CH3
21.
HOOC CH2 CHCOOH
N
H
C
HOOC CH2 C
P
OH
OCH2
N
H
H C
+
N
H
Альдимин 1
CH3
COOH
P
OH
OCH2
+
N
CH3
H
Альдимин 2
+ H2O
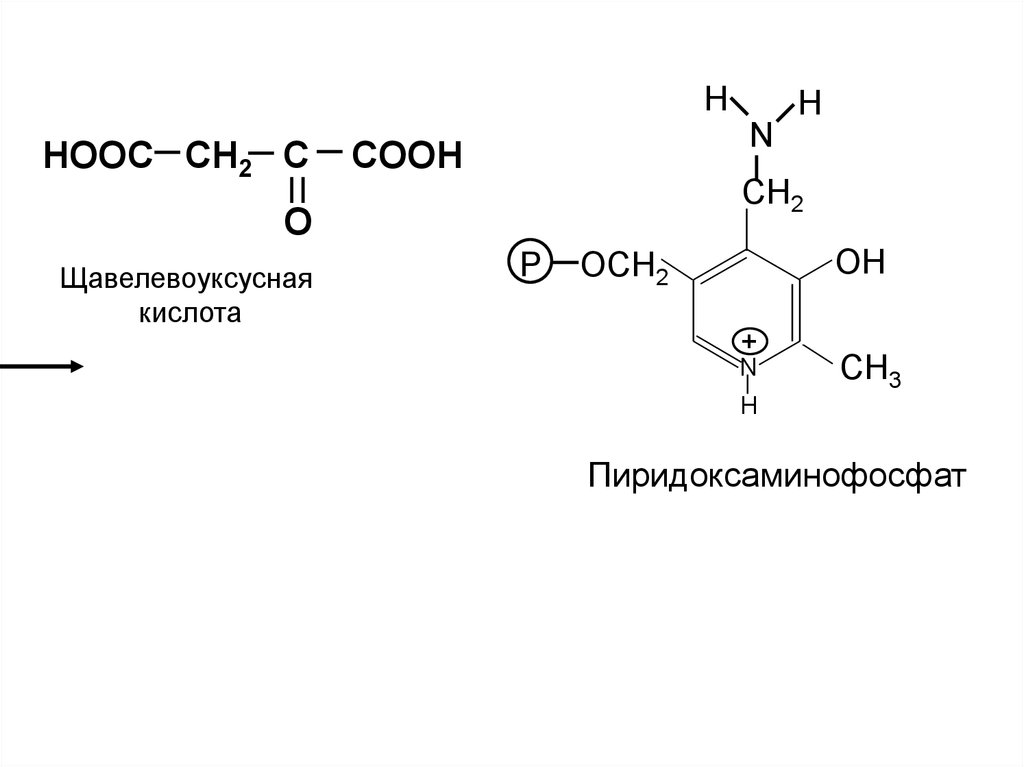
22.
HHOOC CH2 C
N
COOH
CH2
O
Щавелевоуксусная
кислота
H
P
OH
OCH2
+
N
CH3
H
Пиридоксаминофосфат
23.
N H2HOOC (CH2)2
CH2
P
COOH
O
OH
OCH2
C
+
+
N
H
CH3
AN
- H2O
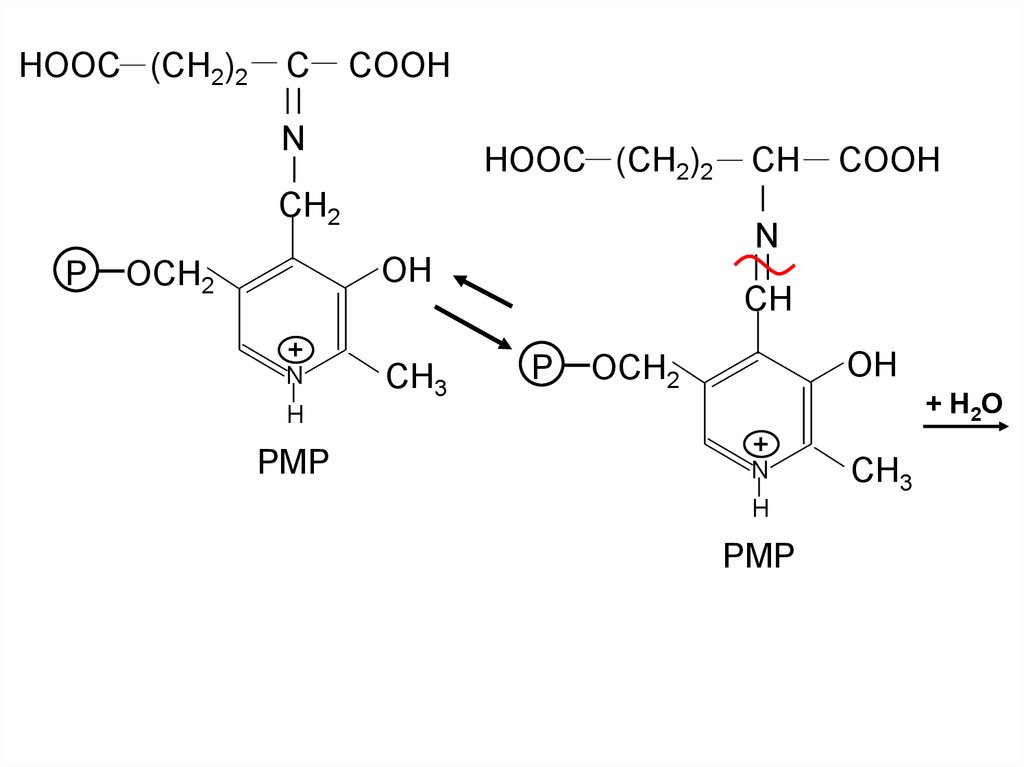
24.
HOOC (CH2)2C
COOH
N
HOOC (CH2)2
CH2
P
+
N
COOH
N
OH
OCH2
CH
CH3
CH
P
OH
OCH2
+ H 2O
H
РМР
+
N
H
РМР
CH3
25.
OH
C
P
HOOC (CH2)2
OH
OCH2
+
N
H
+
CH3
CH
NH2
Глутаминовая
кислота
COOH
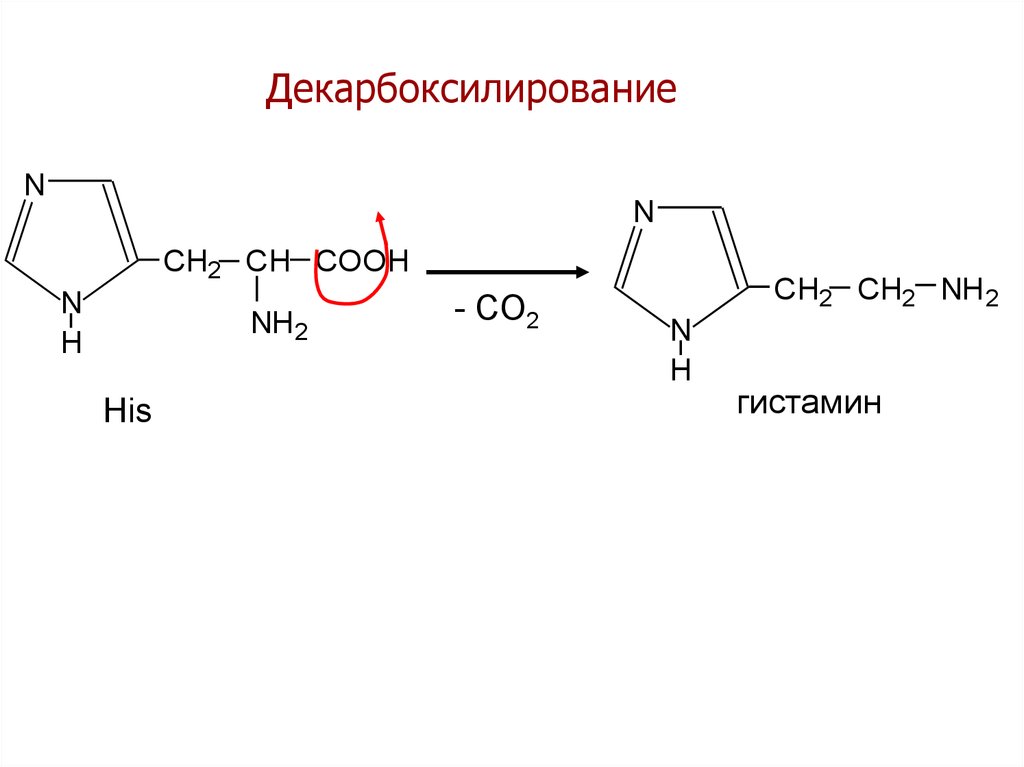
26.
ДекарбоксилированиеN
N
CH2 CH COOH
N
H
NH2
His
- CO2
CH2 CH2 NH 2
N
H
гистамин
27.
OH
C
N
P
CH2 CH COOH
N
H
NH2
OH
OCH2
+
+
N
H
CH3
28.
NN
CH
P
CH
OH
OCH2
+
N
H
+ H 2O
CH3
- CO2
P
OH
OCH2
+
N
H
CH3
29.
OH
C
P
OH
OCH2
+
N
+
CH3
H
Биогенный амин
гистамин
30.
Окислительное дезаминирование-2e, - 2H+
HOOC
(CH2)2
Glu
HOOC
CH COOH
НАД+
NH2
(CH2)2
C
COOH
NH
HOOC
(CH2)2
C
COOH + NH3
O
α-оксоглутаровая к-та
НАДН + Н+
+ H2O
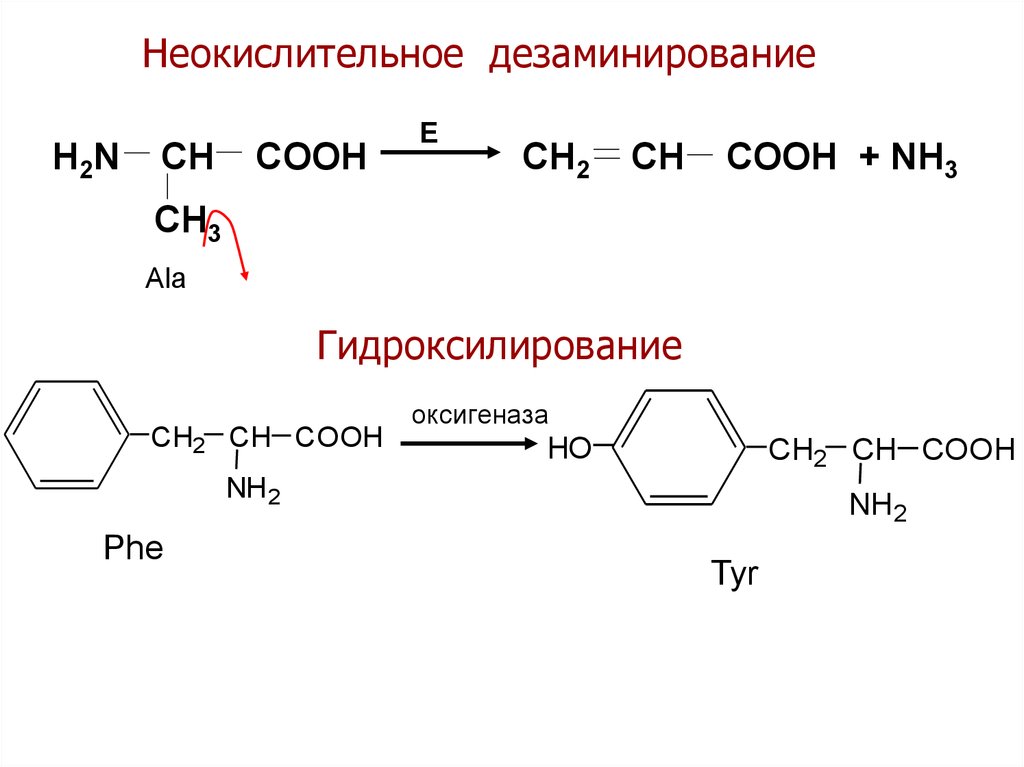
31.
Неокислительное дезаминированиеH2N
CH
COOH
E
CH2
CH
COOH + NH3
CH3
Ala
Гидроксилирование
CH2 CH COOH
оксигеназа
HO
CH2 CH COOH
NH 2
Phe
NH 2
Tyr
32.
Первичная структураδ-
H2N CH
δ+
R
C
O
H2N CH
OH
C
R
Пептидная
группа
O
H2N
N-конец
CH
R
C
O
HN CH
R
Пептидная
связь
C
OH
С-конец
O
OH
33.
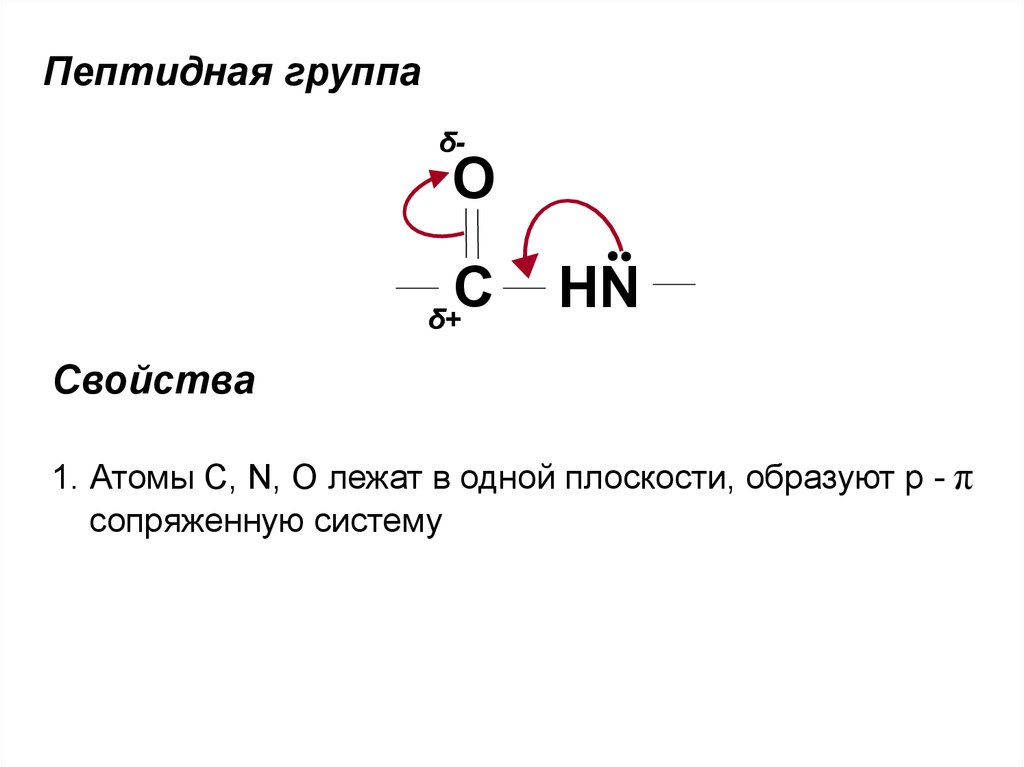
Пептидная группаδ-
O
C
δ+
HN
Свойства
1. Атомы C, N, O лежат в одной плоскости, образуют р - π
сопряженную систему
34.
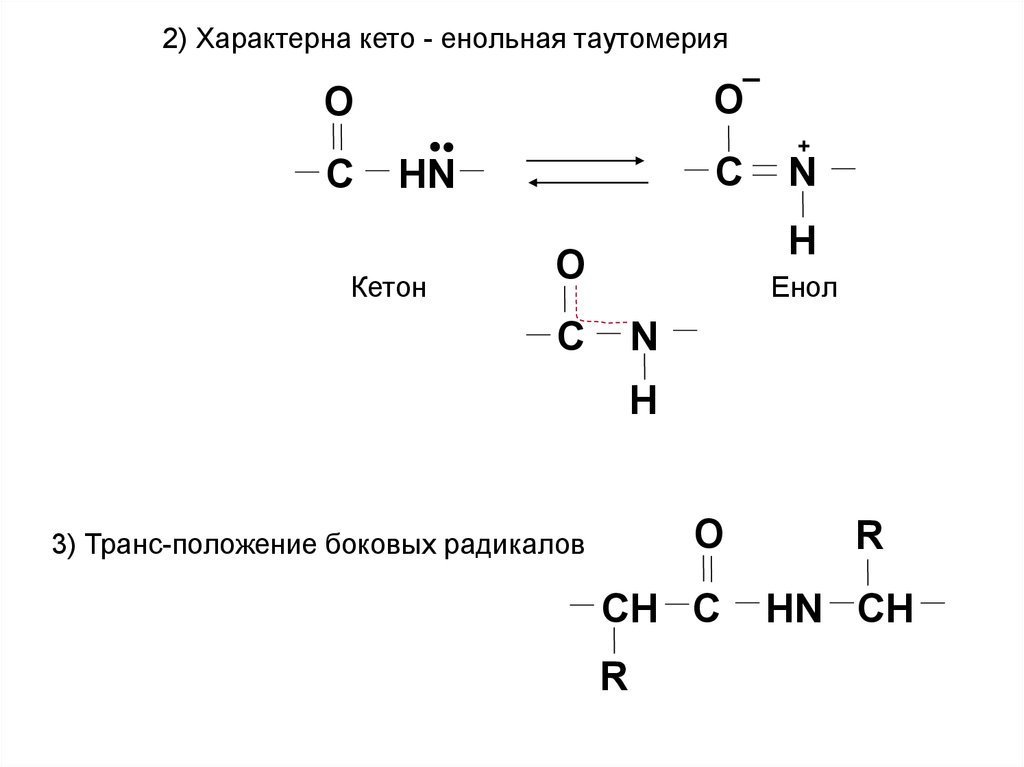
2) Характерна кето - енольная таутомерияO
O
C
C
HN
Кетон
+
N
Н
O
Енол
C
N
Н
O
3) Транс-положение боковых радикалов
CH C
R
R
HN CH
35.
4) Способность к образованию водородной связиO
C
N
Н
••
O
C
N
Н
36.
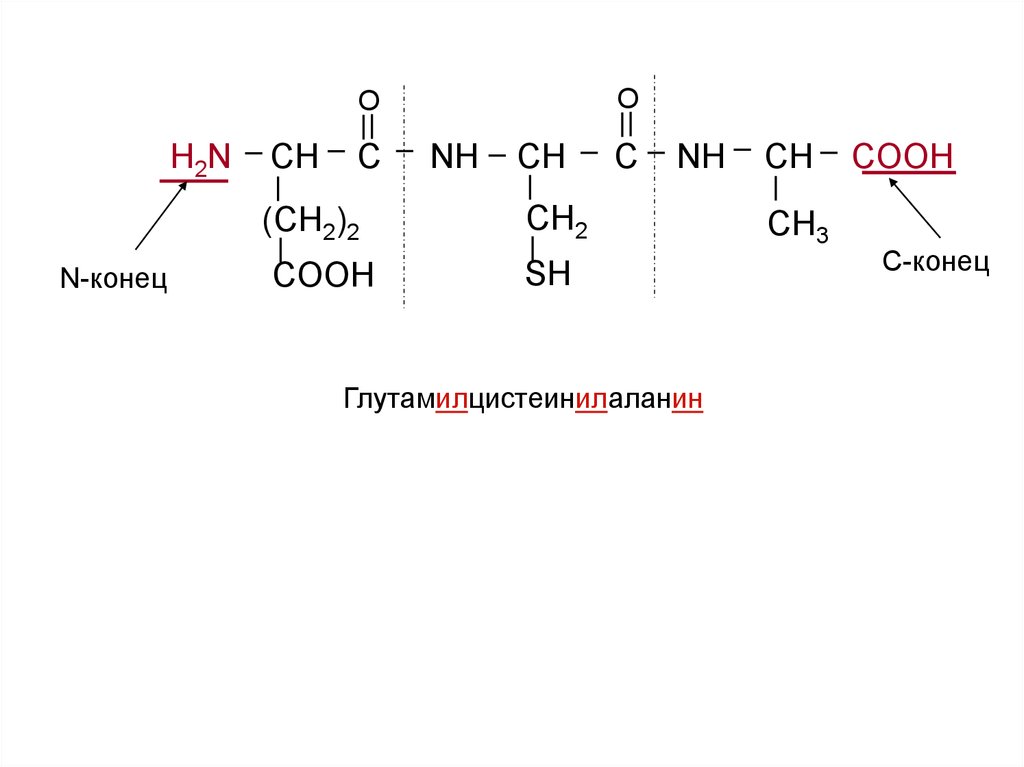
OO
H2N
N-конец
CH
C
NH
CH
(CH2)2
CH2
COOH
SH
C
NH
Глутамилцистеинилаланин
CH
COOH
CH3
C-конец
37.
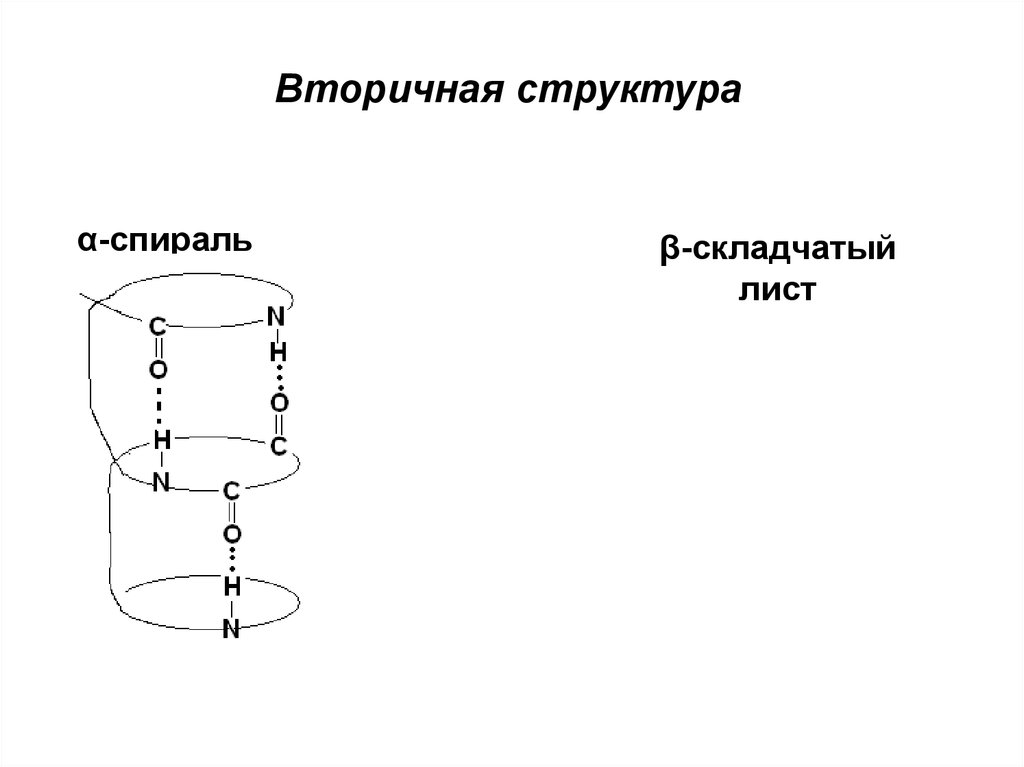
Вторичная структураα-спираль
β-складчатый
лист
38.
Третичная структураO
Ковалентная связь
CH2
Ионное
взаимодействие
Гидрофобное
взаимодействие
CH2 O HHO
COO
CH3
+
H3N
(CH2)3
H3C
CH2
C
CH2
39.
Ковалентная связьВодородная связь
CH2 S
S
CH2 OH
CH2
HO CH2
40.
Качественные реакции наα-АК, пептиды и белки
Универсальные
1 на α-аминокислоты с нингидрином
2. на пептидную связь - биуретовая
41.
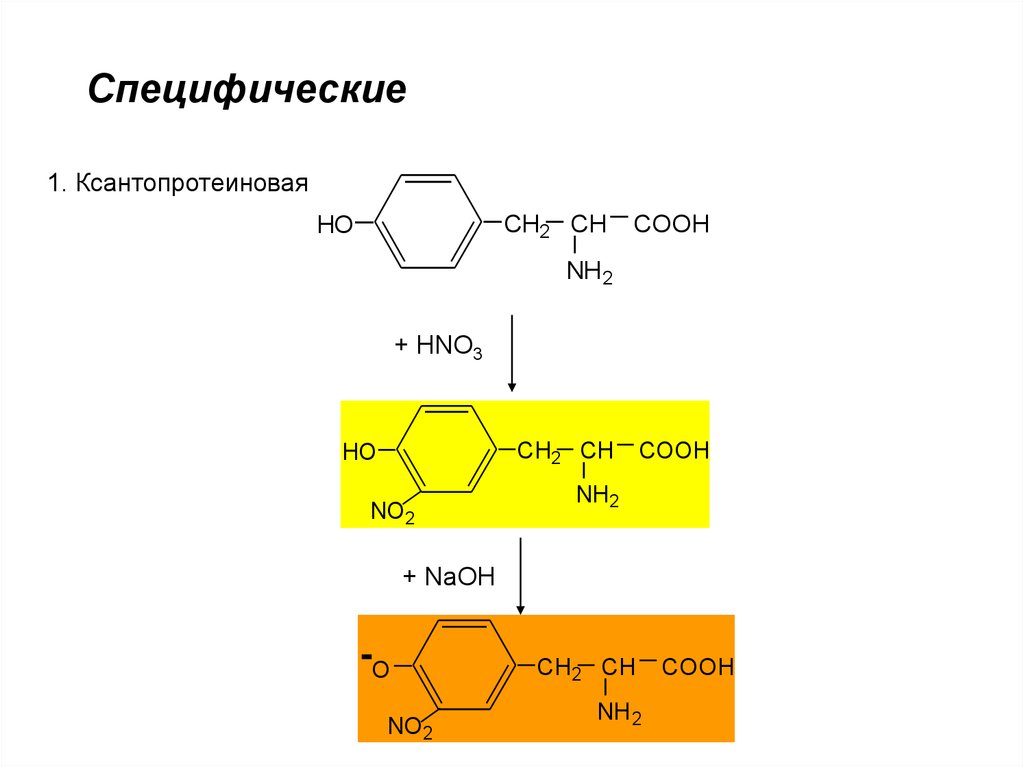
Специфические1. Ксантопротеиновая
CH2 CH
HO
COOH
NH2
+ HNO3
CH2 CH
HO
NO2
COOH
NH 2
+ NaOH
-O
NO2
CH2 CH
NH2
COOH
42.
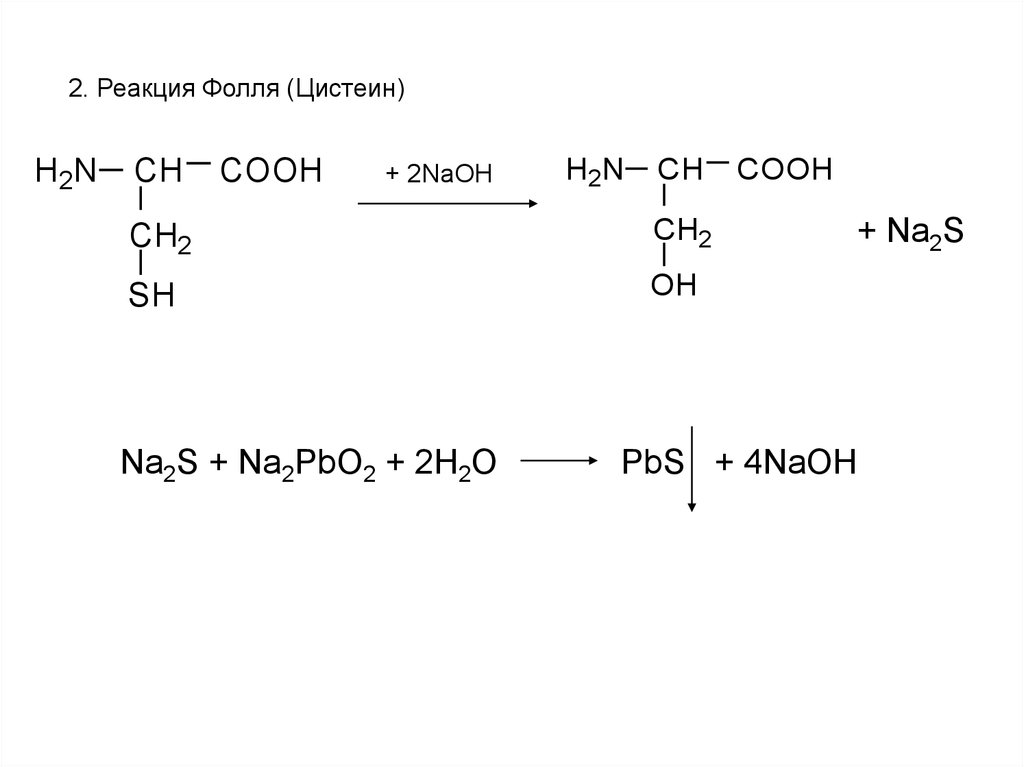
2. Реакция Фолля (Цистеин)H 2N
CH
COOH
+ 2NaOH
H 2N
CH
CH2
CH2
SH
OH
Na2S + Na2PbO2 + 2H2O
COOH
+ Na2S
PbS + 4NaOH
43.
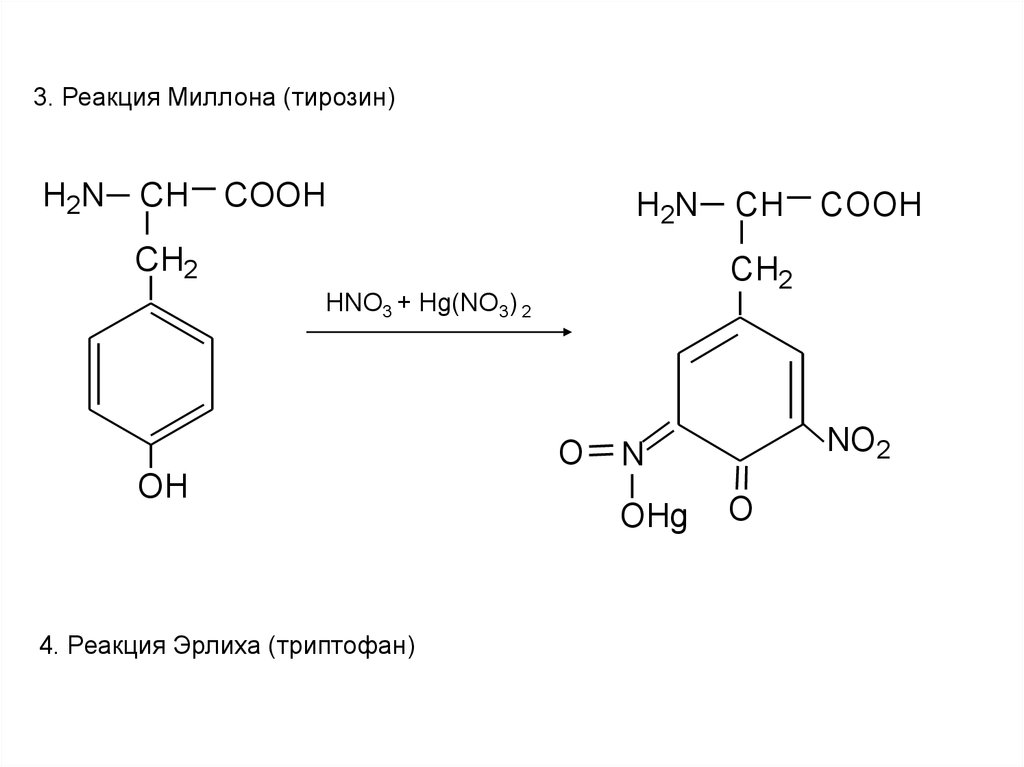
3. Реакция Миллона (тирозин)H 2N
CH
COOH
H 2N
CH2
O
4. Реакция Эрлиха (триптофан)
COOH
CH2
HNO3 + Hg(NO3) 2
OH
CH
NO2
N
OHg
O





















 Химия
Химия