Похожие презентации:
Белки. Структуры белков
1.
2.
Первичная структураδ-
δ+
H2N CH C
O
H2N CH C
OH
R
R
Пептидная
группа
O
H2N CH C HN CH C
N-конец
R
R
Пептидная
связь
O
OH
С-конец
O
OH
3.
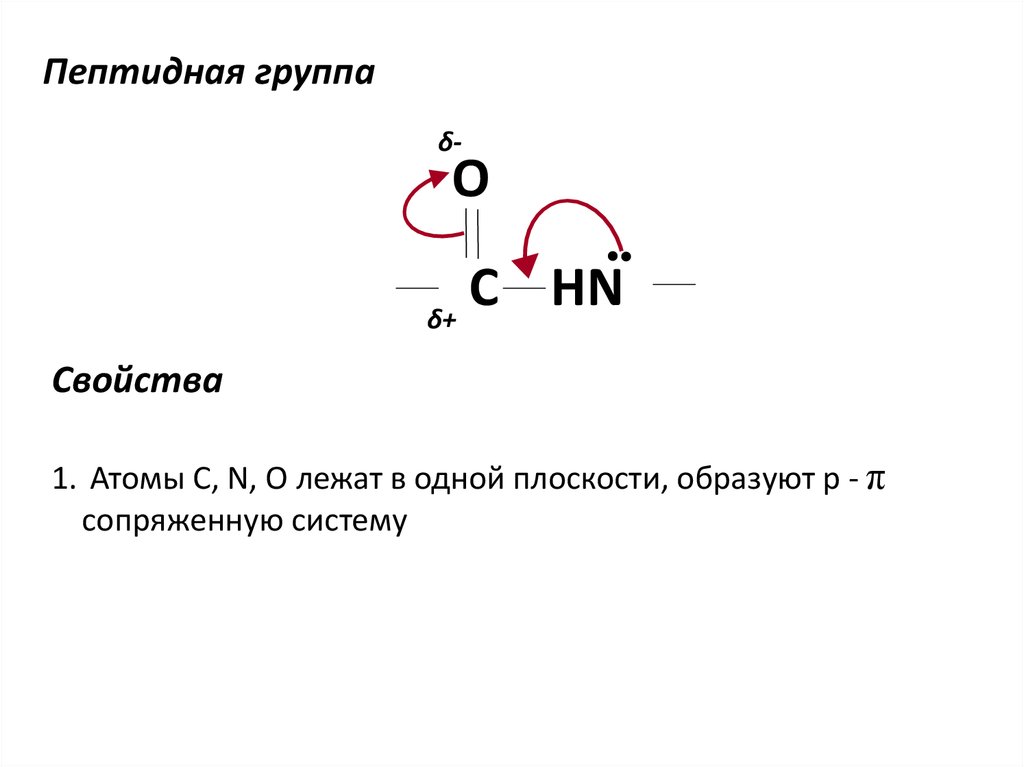
Пептидная группаδ-
O
C
HN
δ+
Свойства
1. Атомы C, N, O лежат в одной плоскости, образуют р - π
сопряженную систему
4.
2) Характерна кето - енольная таутомерияO
O
+
C N
C HN
Кетон
Н
O
Енол
C N
Н
O
3) Транс-положение боковых радикалов
CH C HN CH
R
R
5.
4) Способность к образованию водородной связиO
C N
Н
••
O
C N
Н
6.
OO
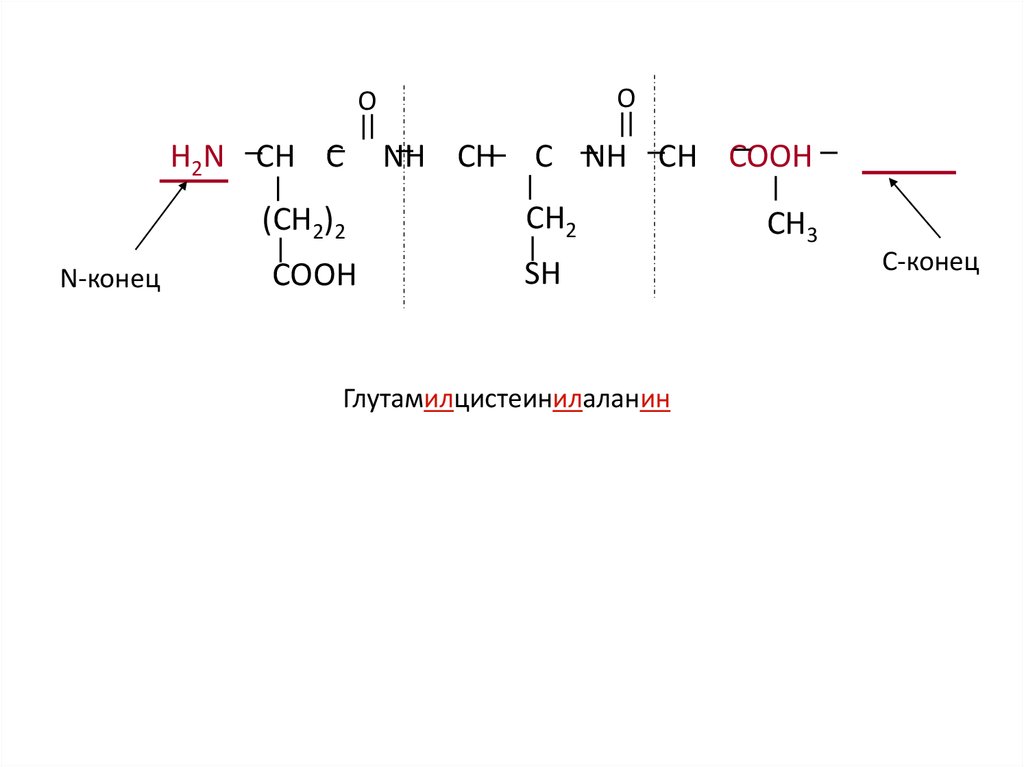
H2N CH C
N-конец
NH CH
C NH CH COOH
(CH2)2
CH2
COOH
SH
Глутамилцистеинилаланин
CH3
C-конец
7.
Вторичная структураα-спираль
β-складчатый
лист
8.
Третичная структураO
CH2 O HHO
Ковалентная связь
Ионное
взаимодействие
Гидрофобное
взаимодействие
CH2
COO
CH3
+
H3N
(CH2)3
H3C
CH2
C
CH2
9.
Ковалентная связьВодородная связь
CH2 S
S
CH2 OH
CH2
HO CH2
10.
Качественные реакции наα-АК, пептиды и белки
Универсальные
1 на α-аминокислоты с нингидрином
2. на пептидную связь - биуретовая
11.
Специфические1. Ксантопротеиновая
CH2 CH
HO
COOH
NH2
+ HNO3
CH2 CH
HO
NO2
COOH
NH 2
+ NaOH
-O
NO2
CH2 CH
NH2
COOH
12.
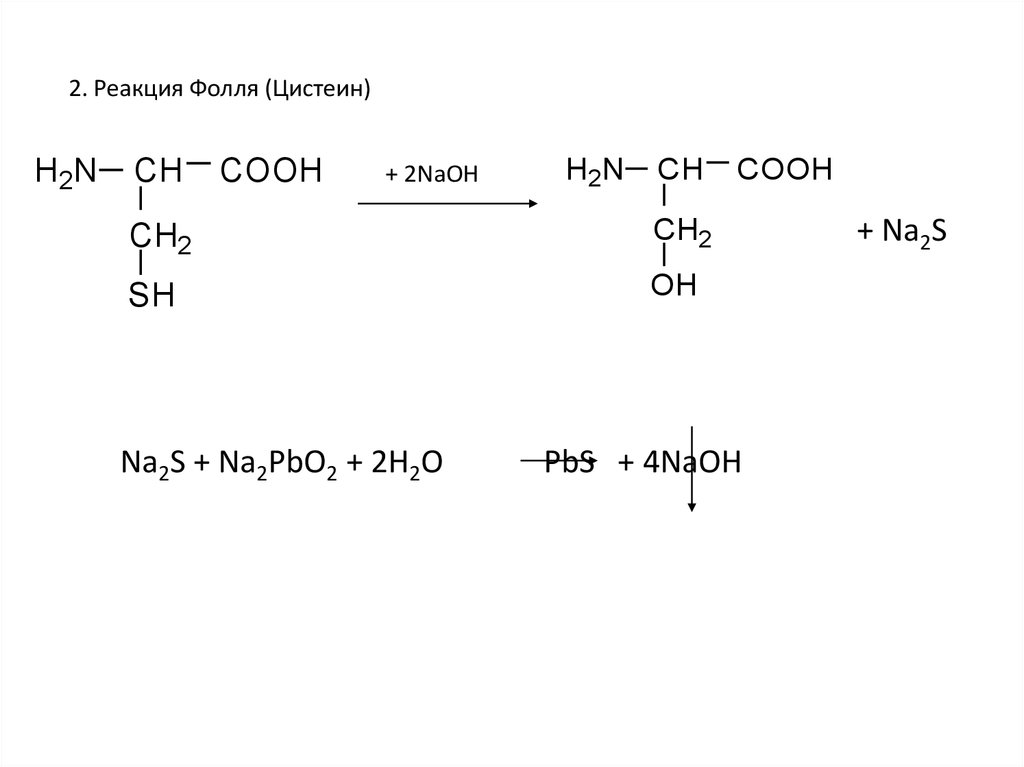
2. Реакция Фолля (Цистеин)H 2N
CH
COOH
+ 2NaOH
H 2N
CH
CH2
CH2
SH
OH
Na2S + Na2PbO2 + 2H2O
COOH
PbS + 4NaOH
+ Na2S
13.
3. Реакция Миллона (тирозин)H 2N
CH
COOH
H 2N
CH2
O
4. Реакция Эрлиха (триптофан)
COOH
CH2
HNO3 + Hg(NO3) 2
OH
CH
NO2
N
OHg
O










 Химия
Химия








