Похожие презентации:
Сопряжение и ароматичность – энергетический фактор стабилизации молекул биологически активных соединений
1. Сопряжение и ароматичность – энергетический фактор стабилизации молекул биологически активных соединений
2. Классификация полиненасыщенных соединений
Изолированные СН2=СН-(СН2)n-СН=СН2Кумулированные СН=С=СН-(СН2)n-СН3
Сопряженные СН2=СН-СН=СН-(СН2)n-СН3
n≥1
2
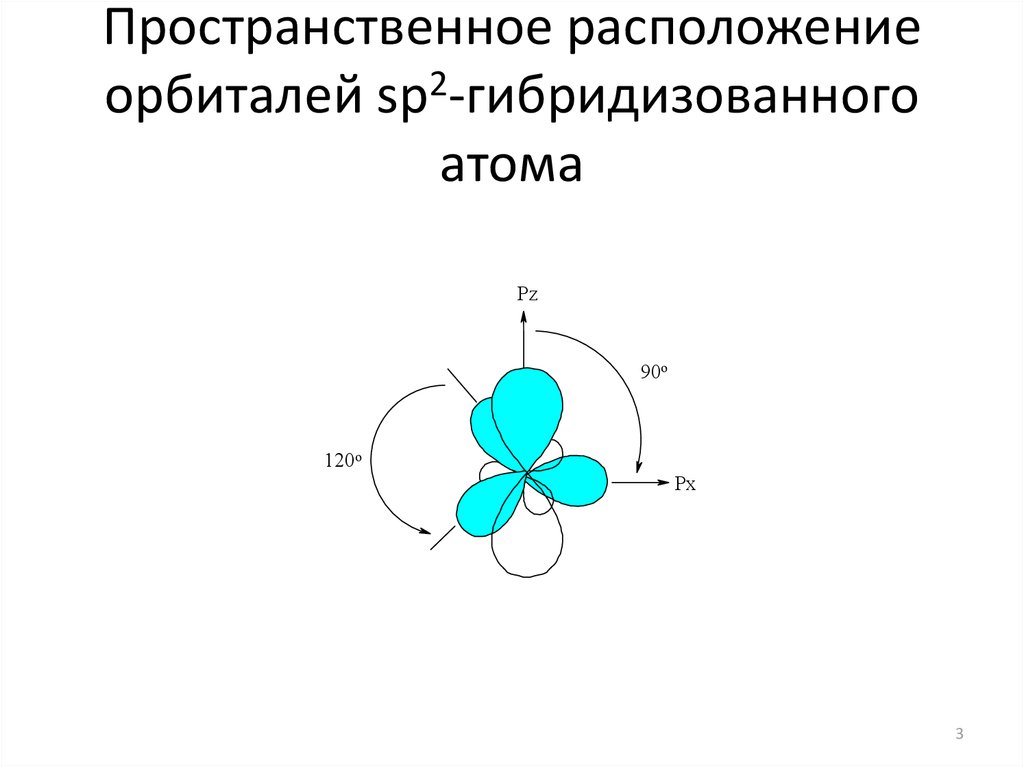
3. Пространственное расположение орбиталей sp2-гибридизованного атома
Pz90o
120o
Px
3
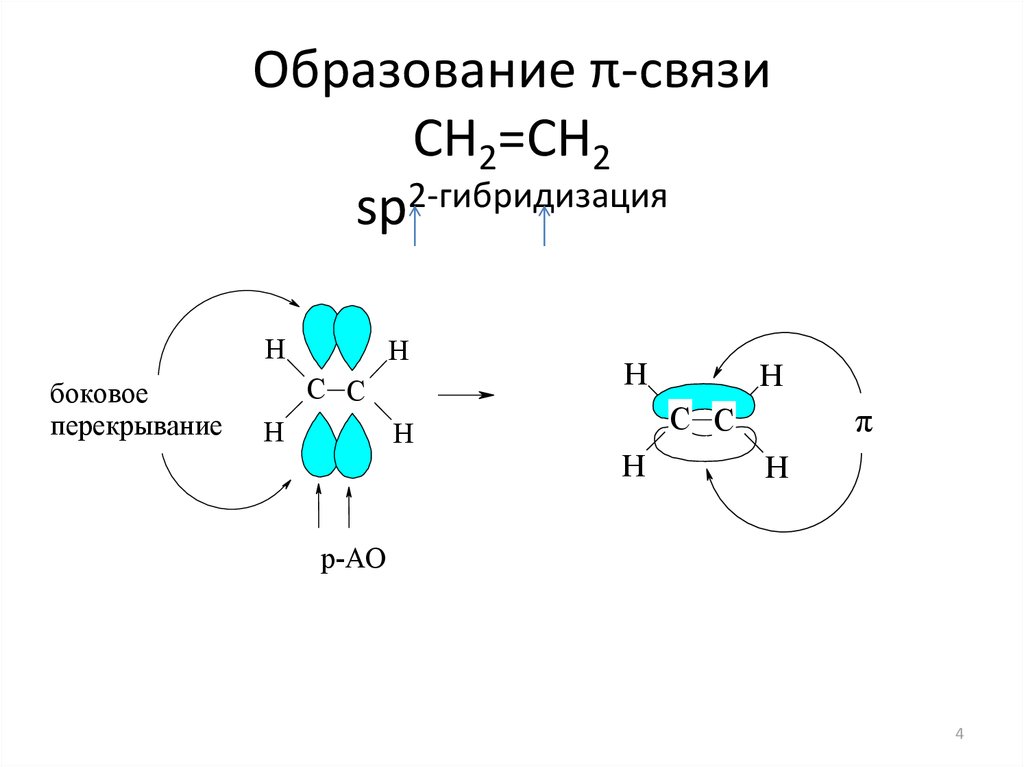
4. Образование π-связи СН2=СН2 sp2-гибридизация
Нбоковое
перекрывание
Н
С С
Н
Н
Н
Н
π
С С
Н
Н
p-AO
4
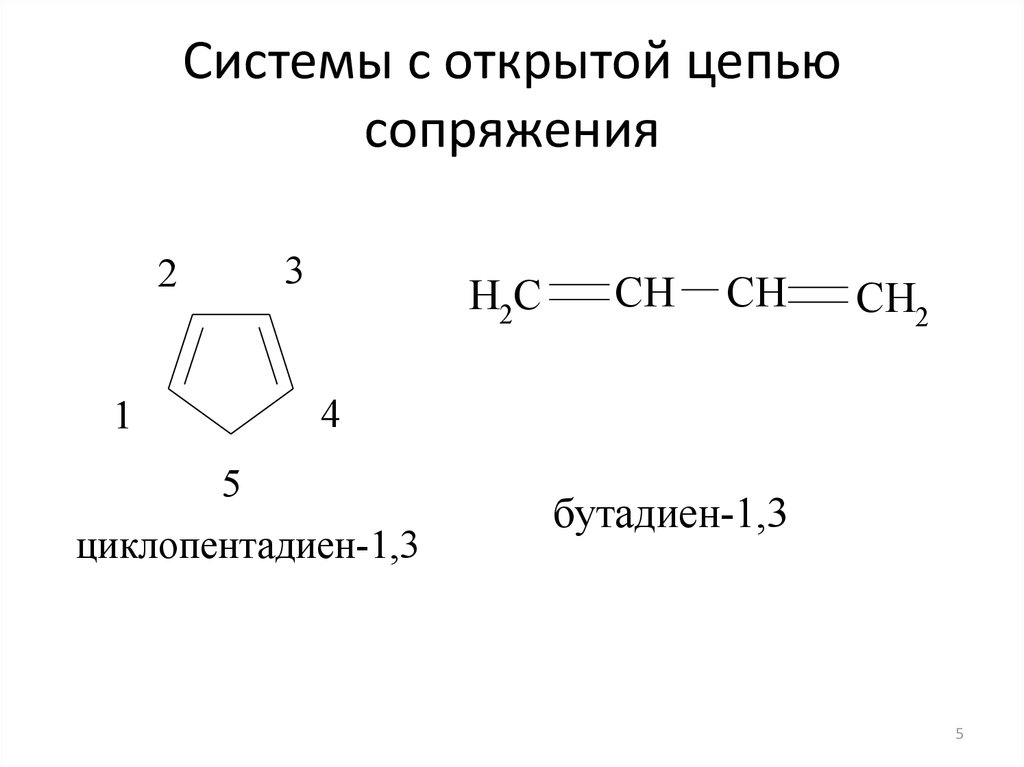
5. Системы с открытой цепью сопряжения
32
H2C
CH
CH
CH2
4
1
5
циклопентадиен-1,3
бутадиен-1,3
5
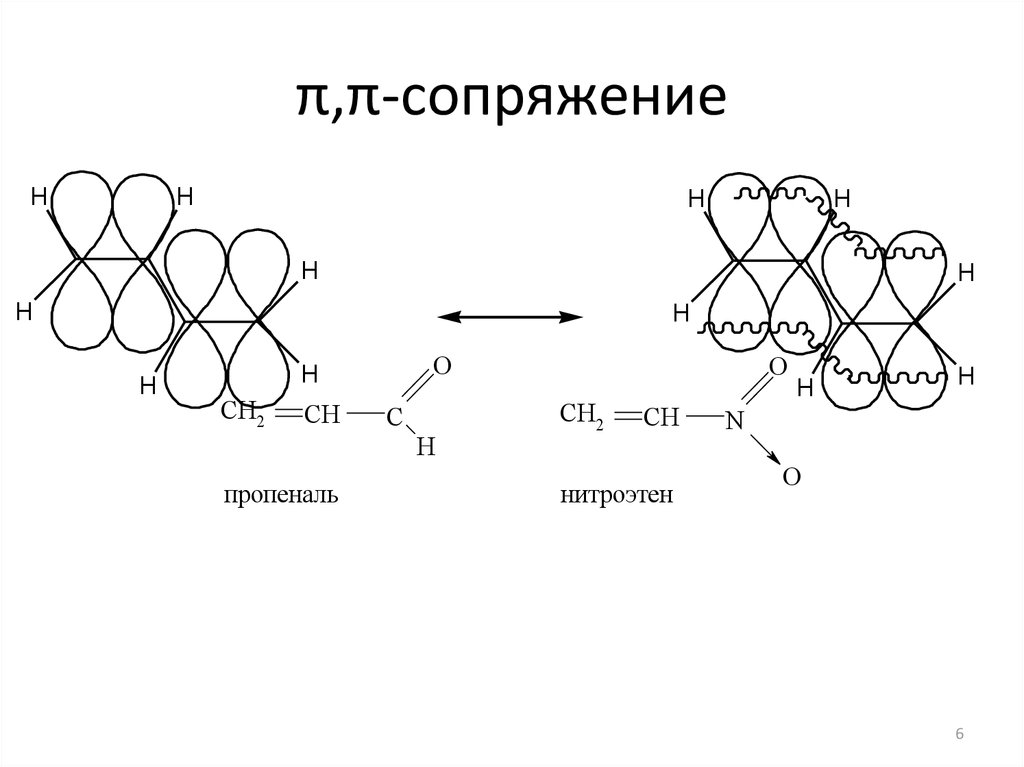
6. π,π-сопряжение
HH
H
H
H
H
H
H
H
O
H
CH2
CH
C
H
пропеналь
O
CH2
CH
нитроэтен
H
H
N
O
6
7.
β-каротин (провитамин А)O
C
CH2OH
H
ретинол (витамин А)
ретиналь
7
8. р,π-сопряжение
HCH2=CH-Cl
..
CH2=CH-NH2
H
C
H
C
Cl
..
OH
8
9. Системы с замкнутой цепью сопряжения
бензолароматическая
система
циклооктатетраен
неароматическая
система
9
10. Критерий ароматичности
• Плоский цикл• Замкнутая система сопряжения
• Правило Хюккеля: число π-электронов,
делокализованных в системе сопряжения
равно 4n+2
n-целое положительное число
10
11. Арены и их производные Бензол
1112.
нафталин4.2+2=10
n=2
антрацен
4.3+2=14
n=3
фенантрен
4.3+2=14
n=3
12
13. Фридрих Август Кекуле
Немецкий химик –органик
В 1865 году предложил
циклическую
структурную формулу
бензола
13
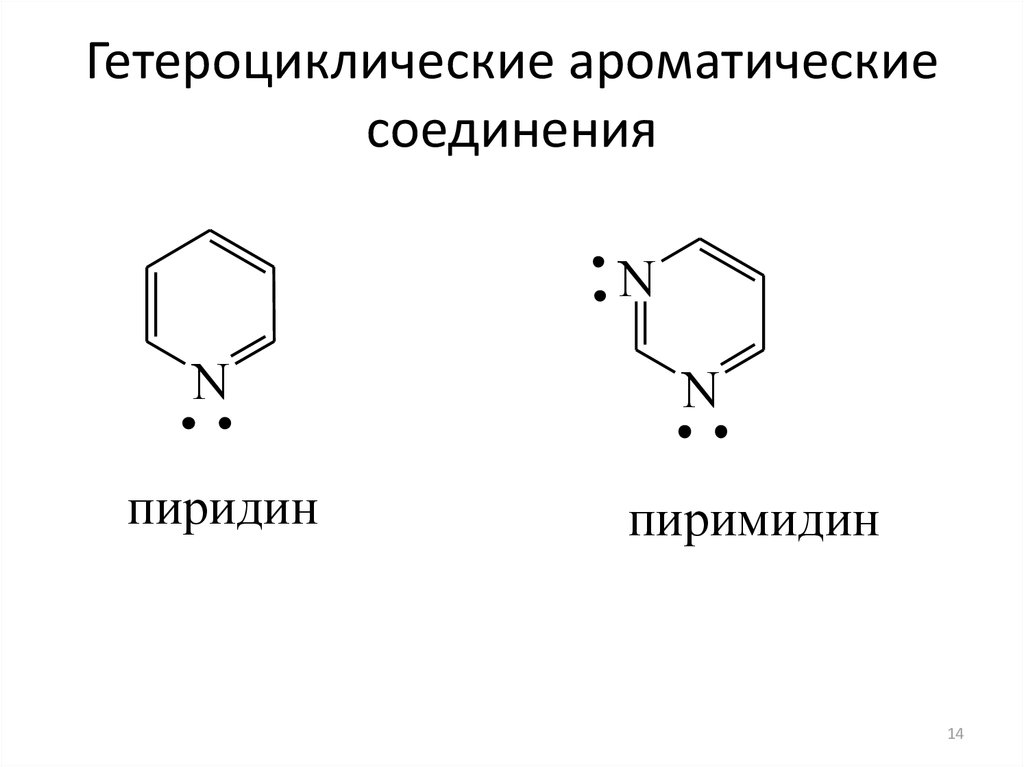
14. Гетероциклические ароматические соединения
NN
пиридин
N
пиримидин
14
15. р,π-сопряженная система в гетероциклах
NH
пиррол
O
фуран
S
тиофен
15
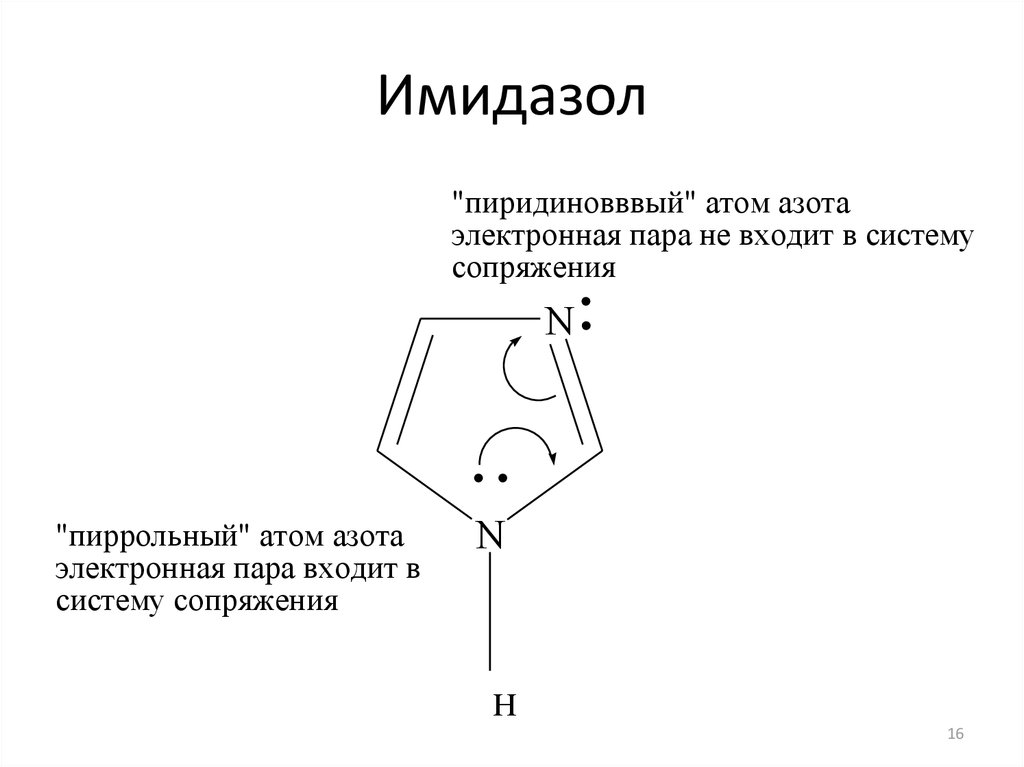
16. Имидазол
"пиридиновввый" атом азотаэлектронная пара не входит в систему
сопряжения
N
"пиррольный" атом азота
электронная пара входит в
систему сопряжения
N
H
16
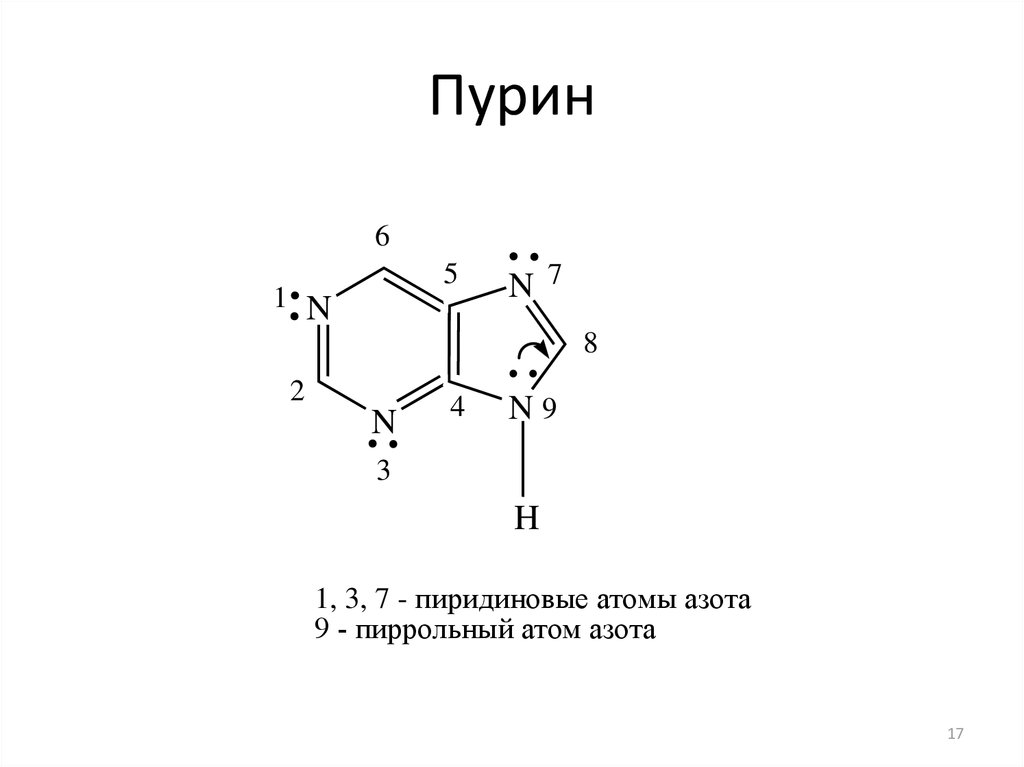
17. Пурин
65
1 N
N7
8
2
N
4
N9
3
H
1, 3, 7 - пиридиновые атомы азота
9 - пиррольный атом азота
17
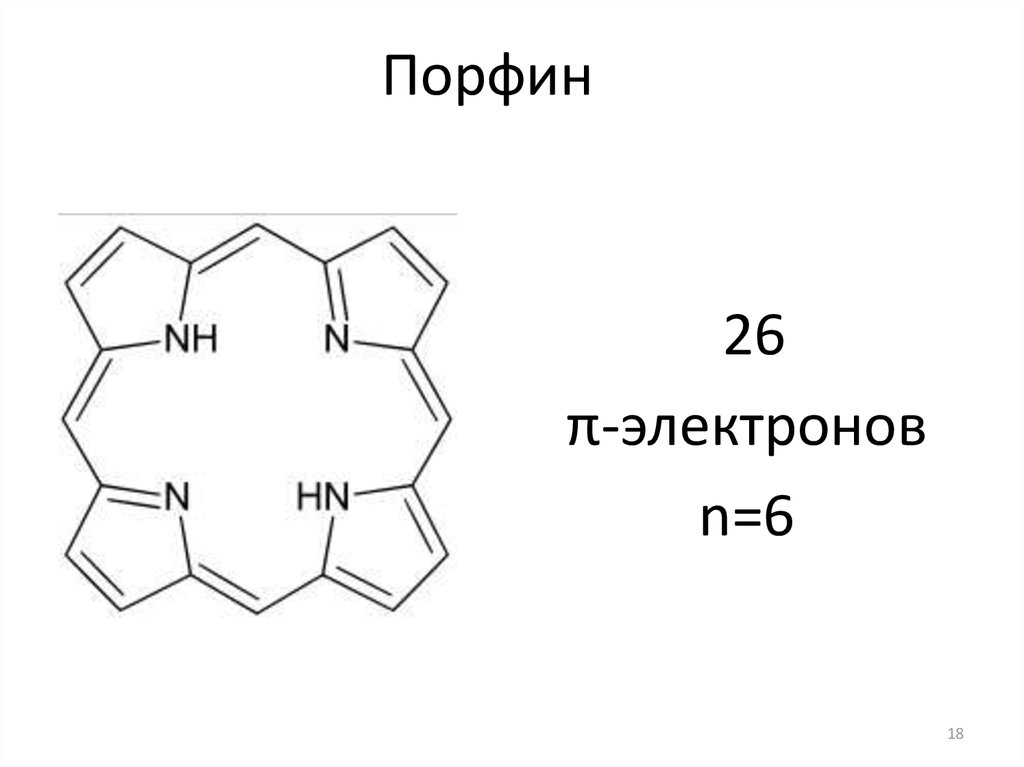
18. Порфин
26π-электронов
n=6
18
19. Реакции электрофильного замещения атома водорода в ароматических системах
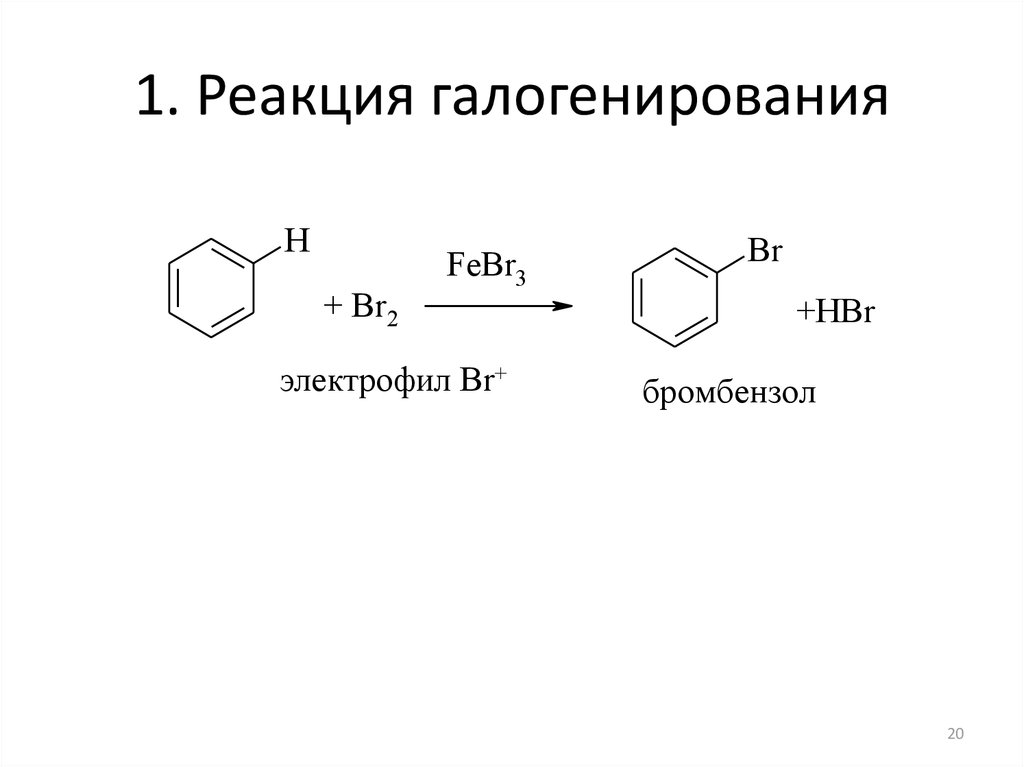
1920. 1. Реакция галогенирования
H+ Br2
FeBr3
электрофил Br+
Br
+HBr
бромбензол
20
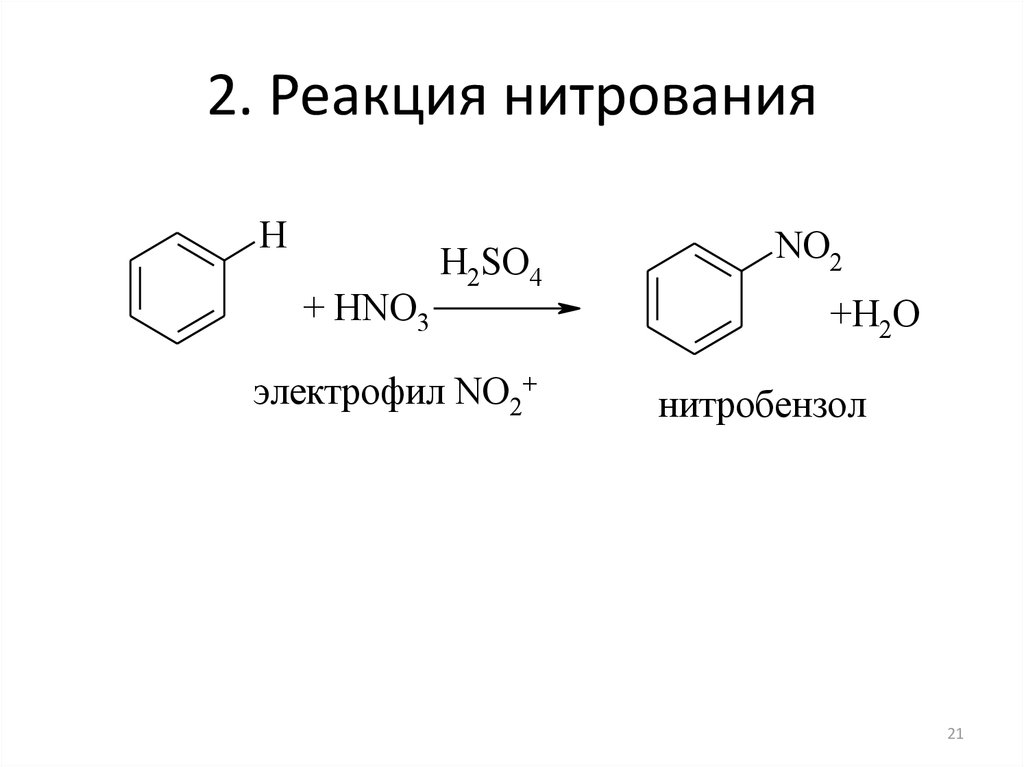
21. 2. Реакция нитрования
H+ HNO3
H2SO4
электрофил NO2+
NO2
+H2O
нитробензол
21
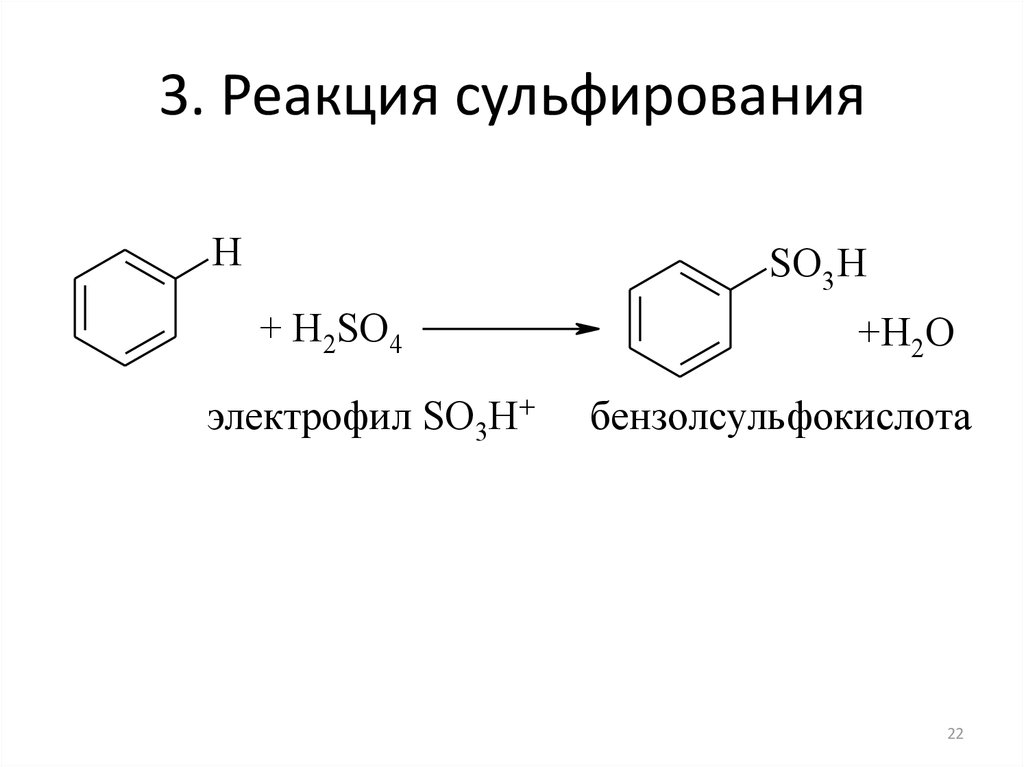
22. 3. Реакция сульфирования
HSO3 H
+ H2SO4
электрофил SO3H+
+H2O
бензолсульфокислота
22
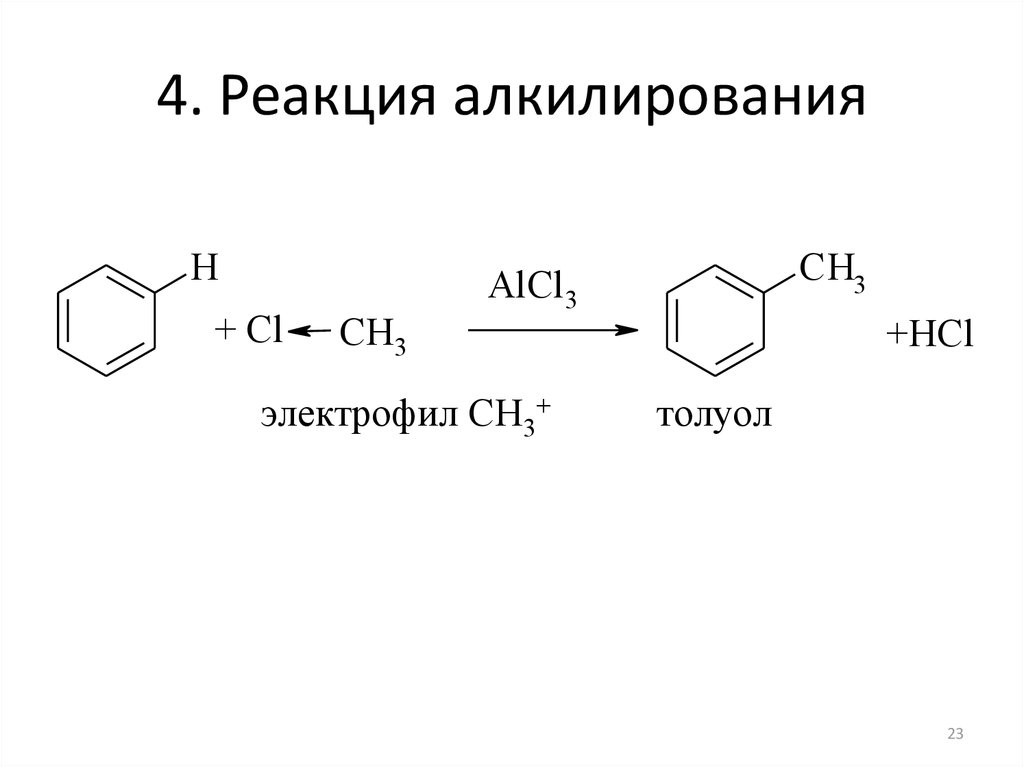
23. 4. Реакция алкилирования
H+ Cl
CH3
CH3
AlCl3
электрофил CH3+
+HCl
толуол
23
24. Реакционная способность ароматических гетероциклических соединений
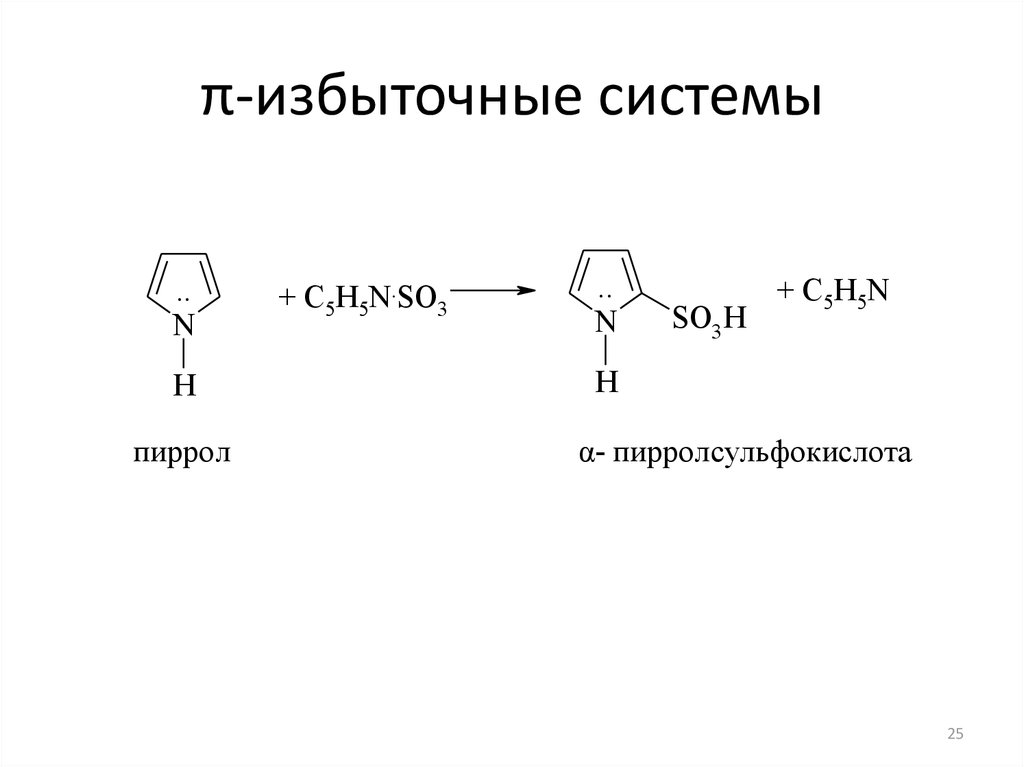
2425. π-избыточные системы
..N
H
пиррол
+ C5H5N.SO3
..
N
SO3 H
+ C5H5N
H
α- пирролсульфокислота
25
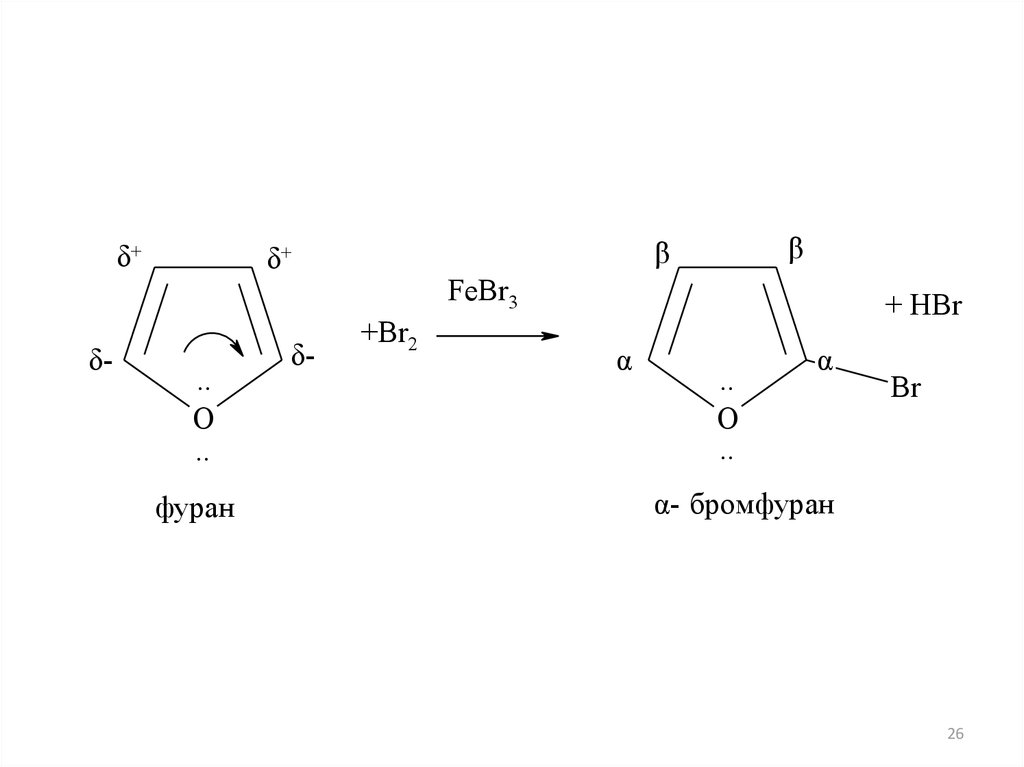
26.
δ+δ-
..
O
..
фуран
δ-
β
β
δ+
FeBr3
+Br2
+ HBr
α
..
O
..
α
Br
α- бромфуран
26
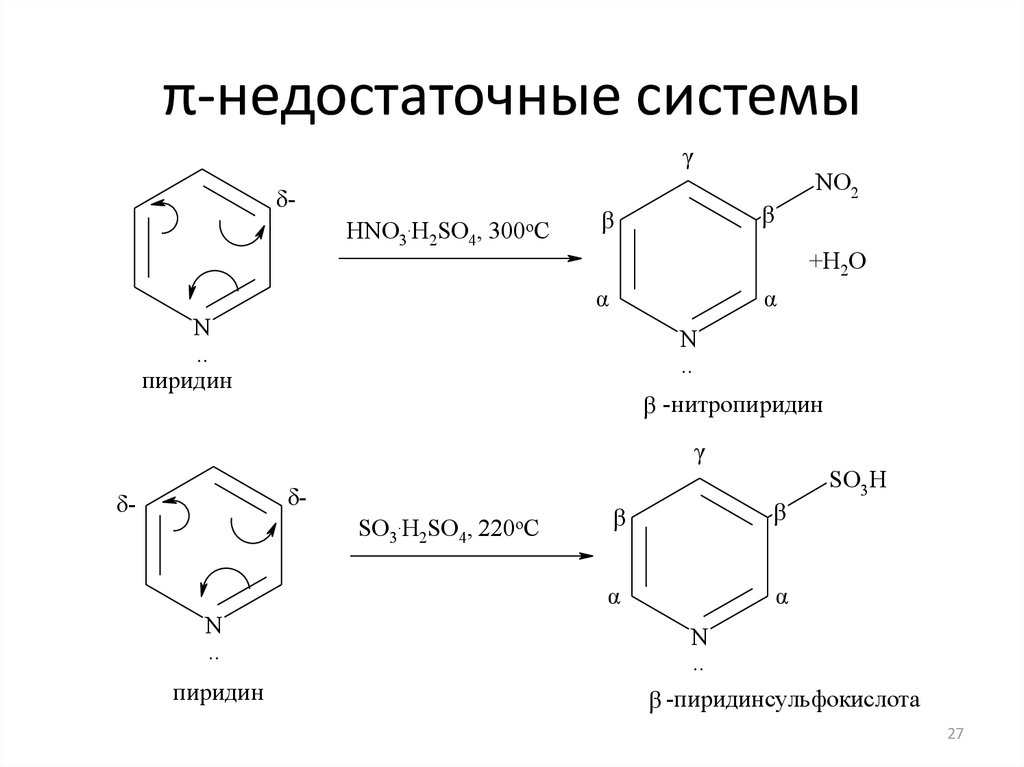
27. π-недостаточные системы
γδHNO3.H2SO4, 300oC
NO2
β
β
+H2O
α
α
N
..
пиридин
N
..
β -нитропиридин
γ
SO3 H
δ-
δ-
SO3.H2SO4, 220oC
N
..
пиридин
β
β
α
α
N
..
β -пиридинсульфокислота
27
28. Кето-енольная и лактим-лактамная таутомерия гетерофункциональных соединений
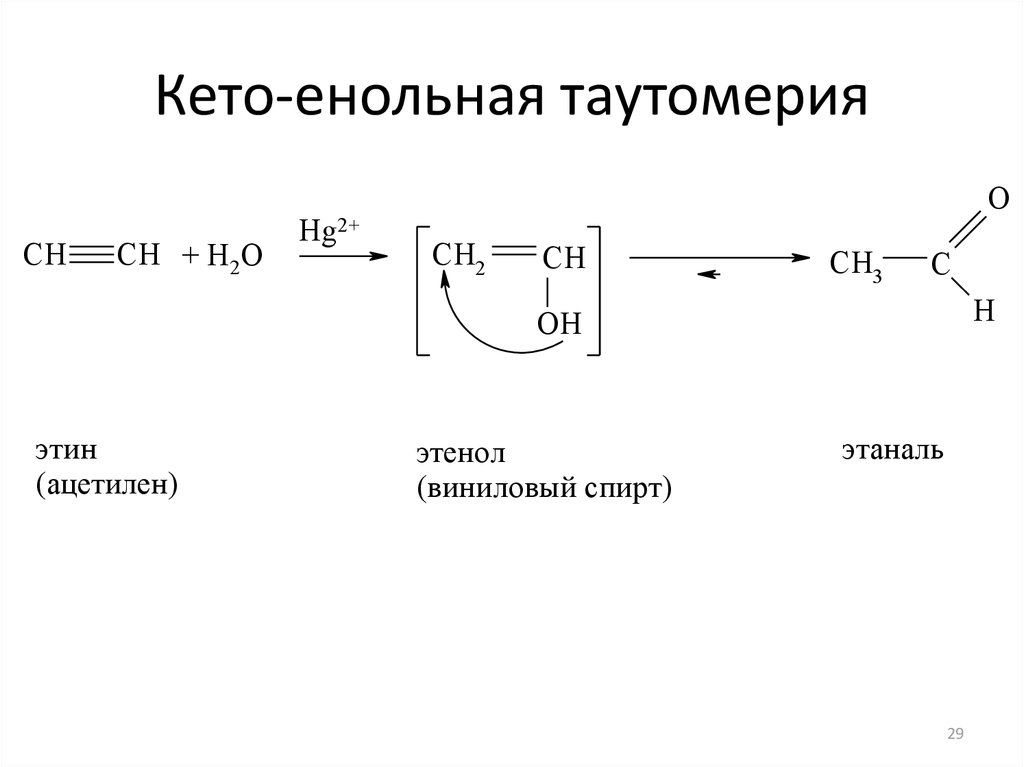
2829. Кето-енольная таутомерия
CHCH + H2O
Hg2+
O
CH2
CH
CH3
C
H
OH
этин
(ацетилен)
этенол
(виниловый спирт)
этаналь
29
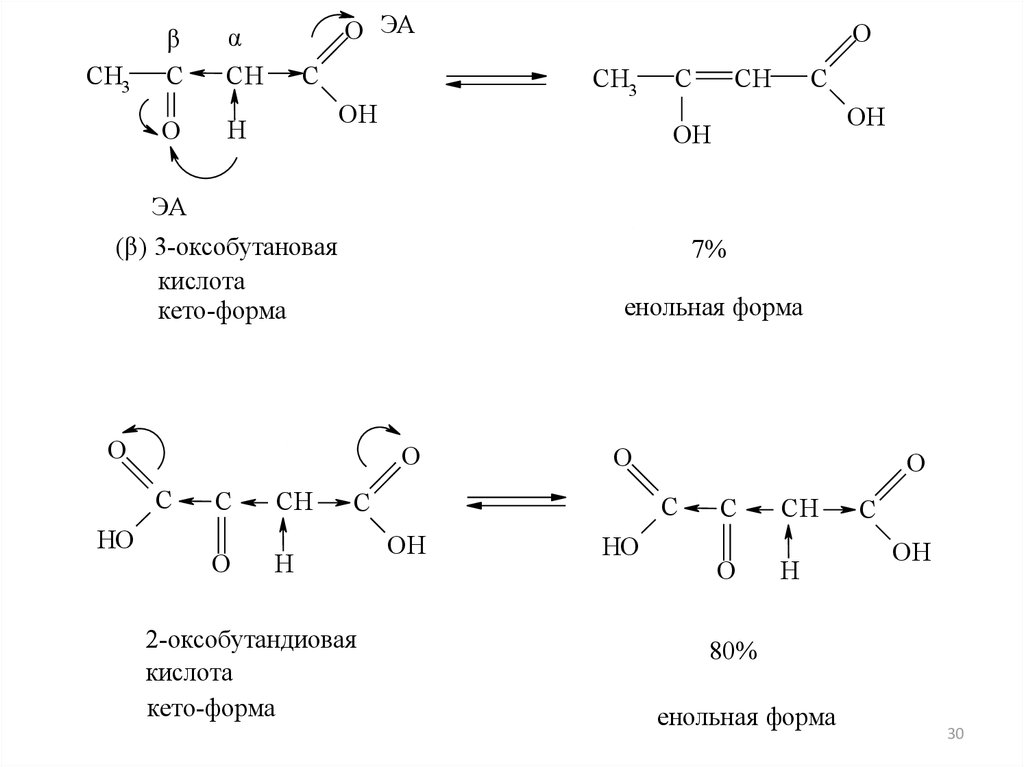
30.
CH3β
C
α
CH
O
H
O ЭА
C
O
CH3
OH
CH
C
C
OH
OH
ЭА
(β) 3-оксобутановая
кислота
кето-форма
7%
енольная форма
O
O
C
HO
C
CH
O
H
O
C
2-оксобутандиовая
кислота
кето-форма
O
C
OH
HO
C
CH
O
H
C
OH
80%
енольная форма
30
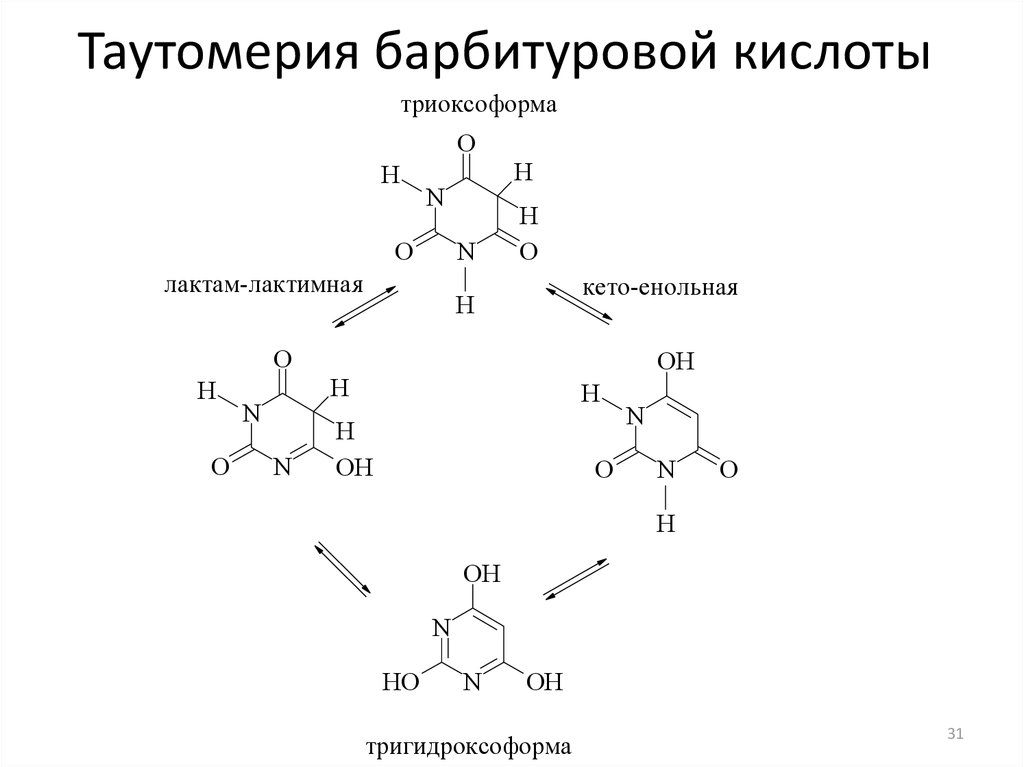
31. Таутомерия барбитуровой кислоты
триоксоформаO
H
H
N
O
N
лактам-лактимная
H
O
кето-енольная
H
O
H
O
OH
H
N
N
H
H
OH
O
N
N
O
H
OH
N
HO
N
OH
тригидроксоформа
31













 Химия
Химия








