Похожие презентации:
Реакции деструкции макромолекул
1. СИНТЕЗ РЕАКЦИОННОСПОСОБНЫХ ОЛИГОМЕРОВ И ПОЛИМЕРОВ НА ИХ ОСНОВЕ
ЛЕКЦИЯ № 62. План лекции
1. Деструкция полимеров, как способполучения олигомеров.
2. Виды деструкции: термическая,
термоокислительная и химическая.
3. Деградация полимерных материалов.
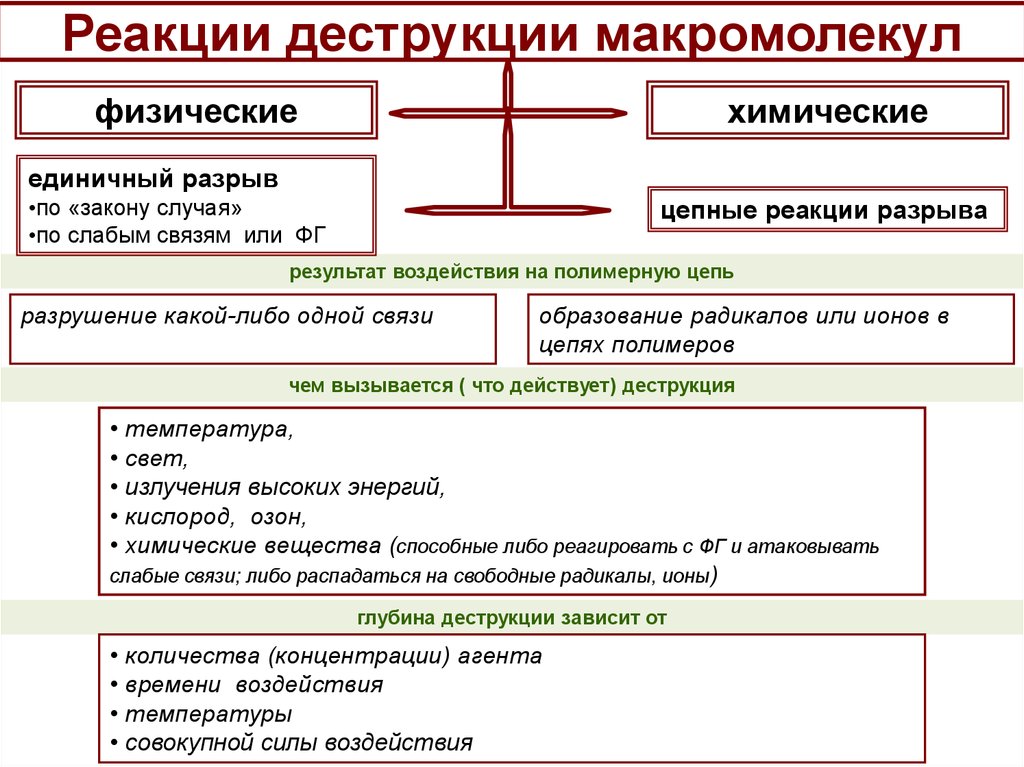
3. Реакции деструкции макромолекул
физическиехимические
единичный разрыв
•по «закону случая»
•по слабым связям или ФГ
цепные реакции разрыва
результат воздействия на полимерную цепь
разрушение какой-либо одной связи
образование радикалов или ионов в
цепях полимеров
чем вызывается ( что действует) деструкция
• температура,
• свет,
• излучения высоких энергий,
• кислород, озон,
• химические вещества (способные либо реагировать с ФГ и атаковывать
слабые связи; либо распадаться на свободные радикалы, ионы)
глубина деструкции зависит от
• количества (концентрации) агента
• времени воздействия
• температуры
• совокупной силы воздействия
4. Реакции термодеструкции макромолекул
Слабые связи в полимерных цепях1. Углерод-углерод связь в ß-положении к двойной связи
2. Концевые звенья цепи
3. Аномальные связи
Реакции термодеструкции макромолекул
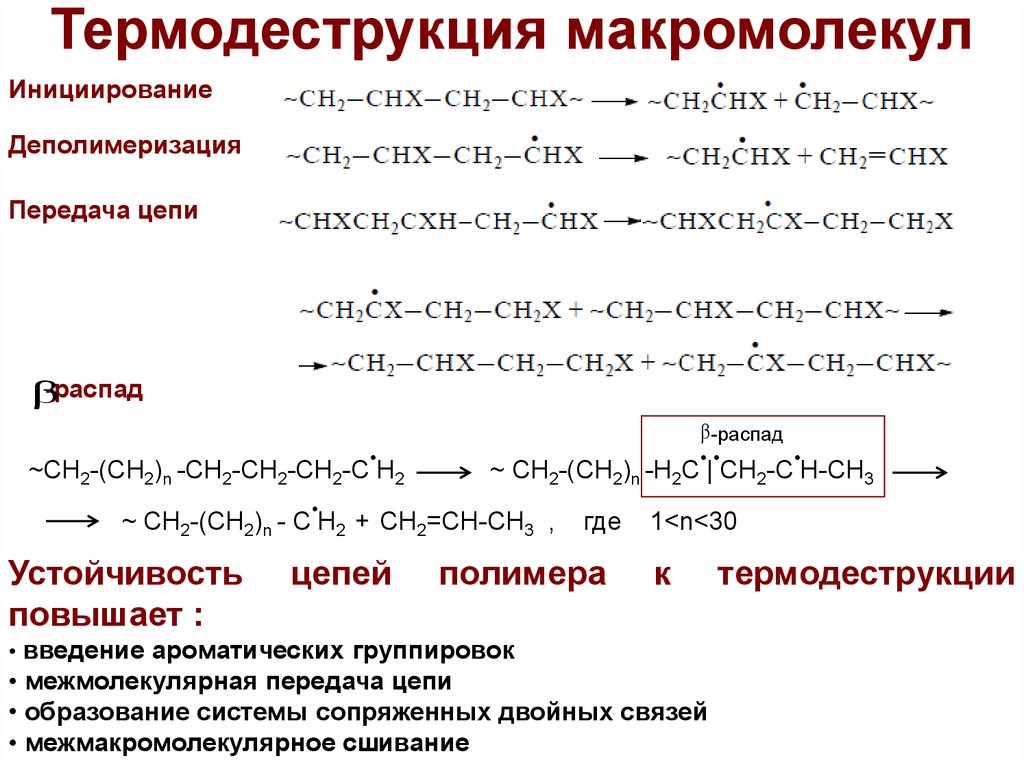
5. Термодеструкция макромолекул
ИнициированиеДеполимеризация
Передача цепи
β-распад
β-распад
~СH2-(CH2)n -СH2-СH2-СH2-C H2
•
~ СH2-(CH2)n - C H2 + СH2=СH-CH3 ,
Устойчивость
повышает :
цепей
~ СH2-(CH2)n -H2C | СH2-С H-CH3
где
полимера
1<n<30
к
• введение ароматических группировок
• межмолекулярная передача цепи
• образование системы сопряженных двойных связей
• межмакромолекулярное сшивание
термодеструкции
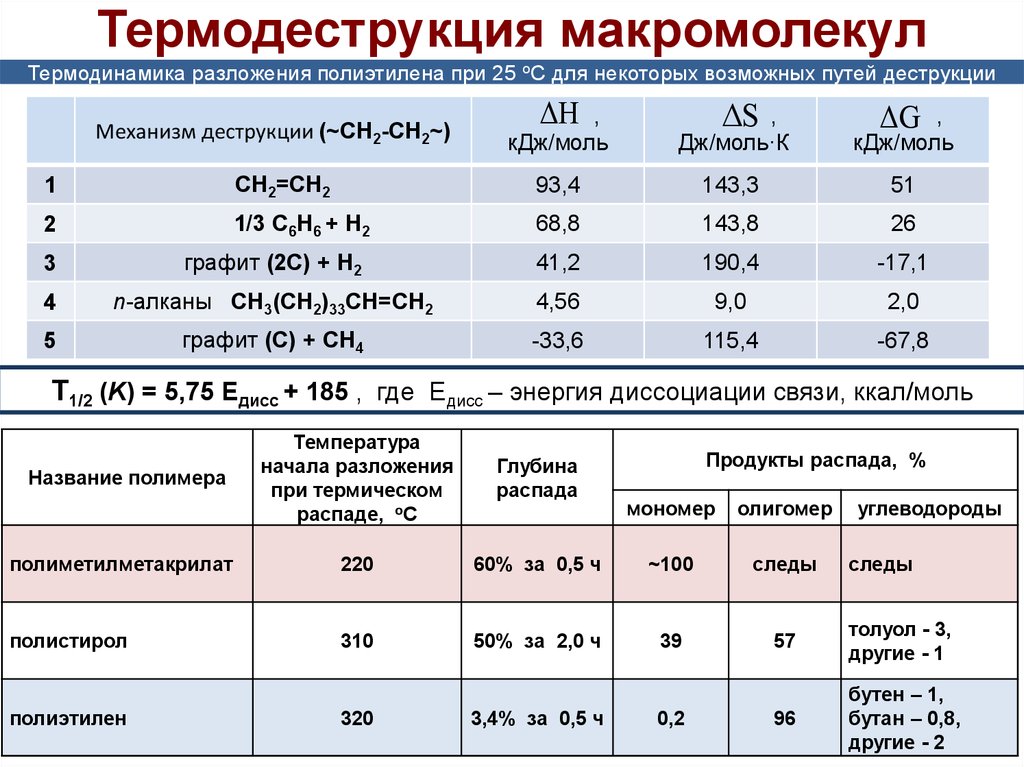
6. Термодеструкция макромолекул
Термодинамика разложения полиэтилена при 25 oC для некоторых возможных путей деструкцииМеханизм деструкции (~CH2-CH2~)
ΔH
ΔS
ΔG
,
кДж/моль
,
Дж/моль·К
,
кДж/моль
1
CH2=CH2
93,4
143,3
51
2
1/3 C6H6 + H2
68,8
143,8
26
3
графит (2С) + H2
41,2
190,4
-17,1
4
n-алканы CH3(CH2)33CH=CH2
4,56
9,0
2,0
5
графит (С) + CH4
-33,6
115,4
-67,8
T1/2 (K) = 5,75 Eдисс + 185 , где Eдисс – энергия диссоциации связи, ккал/моль
Температура
начала разложения
при термическом
распаде, oC
Глубина
распада
полиметилметакрилат
220
полистирол
310
Название полимера
полиэтилен
320
Продукты распада, %
мономер
олигомер
60% за 0,5 ч
~100
следы
50% за 2,0 ч
39
57
толуол - 3,
другие - 1
96
бутен – 1,
бутан – 0,8,
другие - 2
3,4% за 0,5 ч
0,2
углеводороды
следы
7. Термодеструкция макромолекул
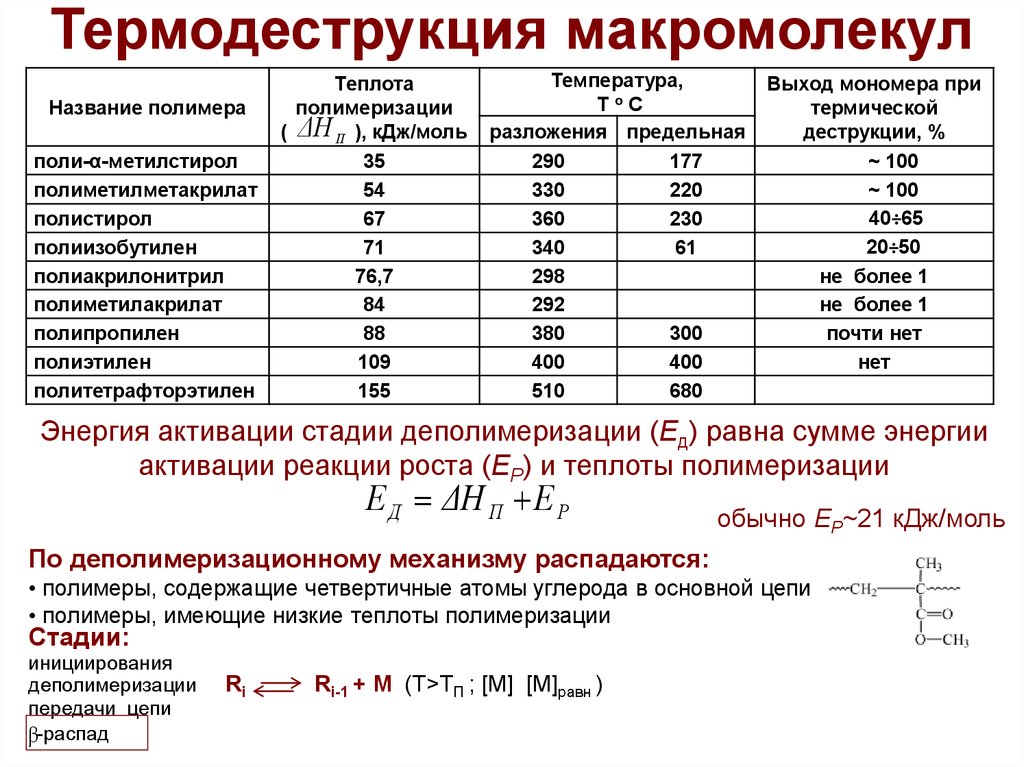
Название полимераполи-α-метилстирол
полиметилметакрилат
полистирол
полиизобутилен
полиакрилонитрил
полиметилакрилат
полипропилен
полиэтилен
политетрафторэтилен
Теплота
полимеризации
( ΔH П ), кДж/моль
35
54
67
71
76,7
84
88
109
155
Температура,
ToC
разложения предельная
290
177
330
220
360
230
340
61
298
292
380
300
400
400
510
680
Выход мономера при
термической
деструкции, %
~ 100
~ 100
40÷65
20÷50
не более 1
не более 1
почти нет
нет
Энергия активации стадии деполимеризации (Eд) равна сумме энергии
активации реакции роста (ЕР) и теплоты полимеризации
Е Д ΔH П Е Р
обычно ЕР~21 кДж/моль
По деполимеризационному механизму распадаются:
• полимеры, содержащие четвертичные атомы углерода в основной цепи
• полимеры, имеющие низкие теплоты полимеризации
Стадии:
инициирования
деполимеризации
передачи цепи
β-распад
Ri
Ri-1 + M (Т>ТП ; [М] [М]равн )
8.
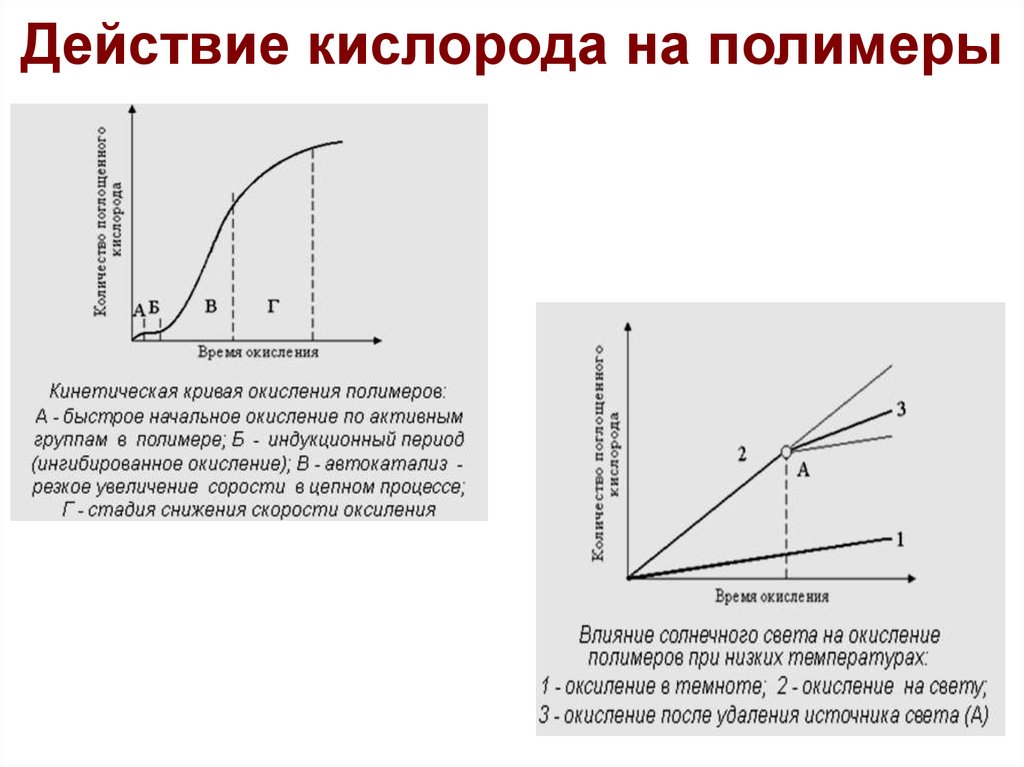
Действие кислорода на полимеры9.
(Термо)окислительная деструкцияпроисходит под действием: кислорода, озона, свободных радикалов
зависит от природы полимера
W– скорость окисления полимеров;
Wi – скорость инициирования процесса
окисления, которая складывается из
скоростей зарождения и вырожденного
разветвления цепей
10.
Действие кислорода на полимерыОкисление ненасыщенных полимеров
11.
Действие кислорода на полимерыОкисление насыщенных полимеров
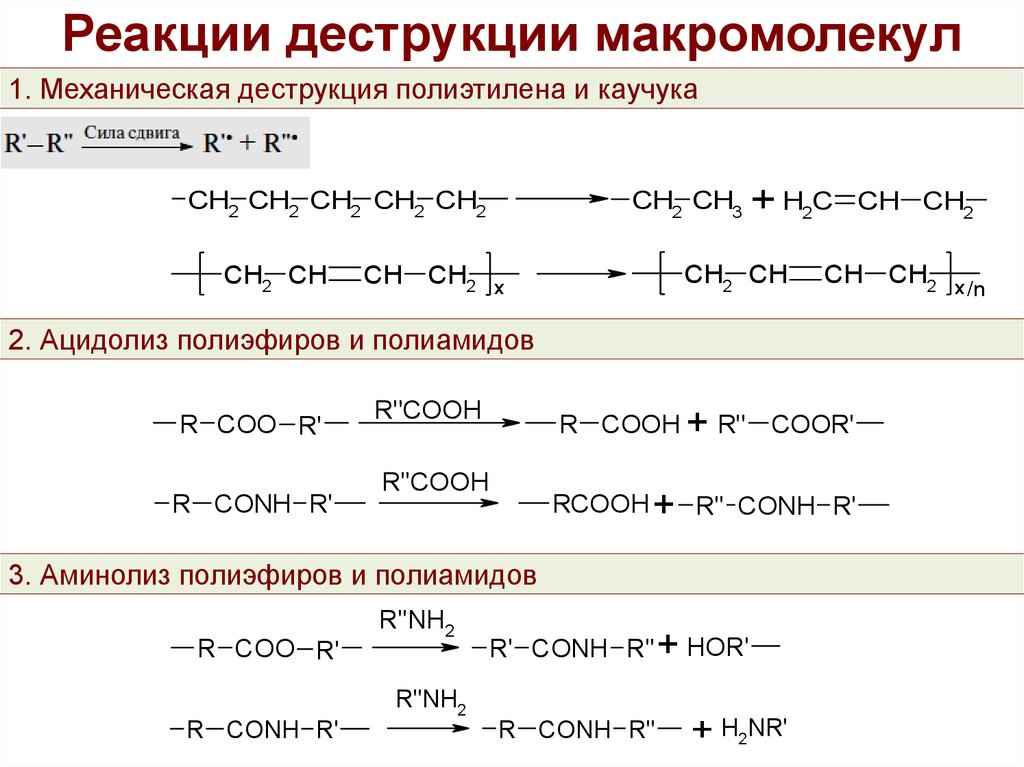
12. Реакции деструкции макромолекул
1. Механическая деструкция полиэтилена и каучукаCH2 CH3 + H2C CH CH2
CH2 CH2 CH2 CH2 CH2
CH2 CH
CH CH2
CH2 CH
x
CH CH2
2. Ацидолиз полиэфиров и полиамидов
R COO R'
R CONH R'
R''COOH
R COOH + R'' COOR'
R''COOH
RCOOH + R'' CONH R'
3. Аминолиз полиэфиров и полиамидов
R COO R'
R''NH2
R' CONH R'' + HOR'
R''NH2
R CONH R'
R CONH R''
+ H2NR'
x /n
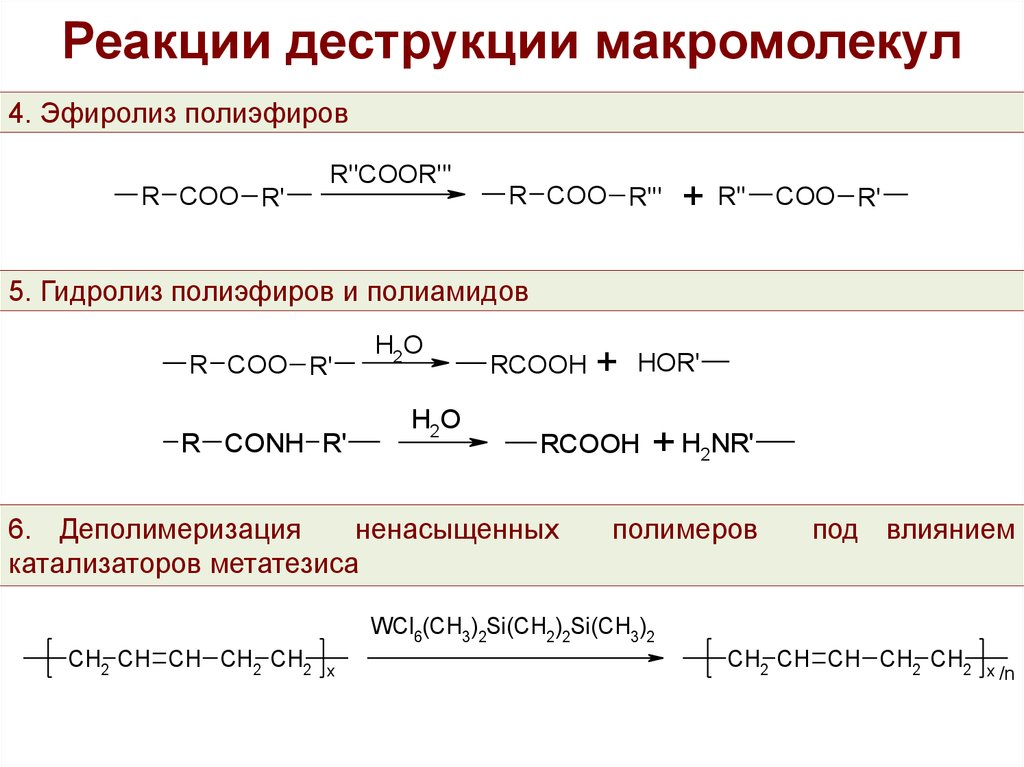
13. Реакции деструкции макромолекул
4. Эфиролиз полиэфировR COO R'
R''COOR'''
R COO R'''
+
R''
COO R'
5. Гидролиз полиэфиров и полиамидов
R COO R'
R CONH R'
H2O
H2O
RCOOH
+
HOR'
RCOOH
6. Деполимеризация
ненасыщенных
катализаторов метатезиса
+ H2NR'
полимеров
под влиянием
WCl6(CH3)2Si(CH2)2Si(CH3)2
CH2 CH CH CH2 CH2
x
CH2 CH CH CH2 CH2
x /n
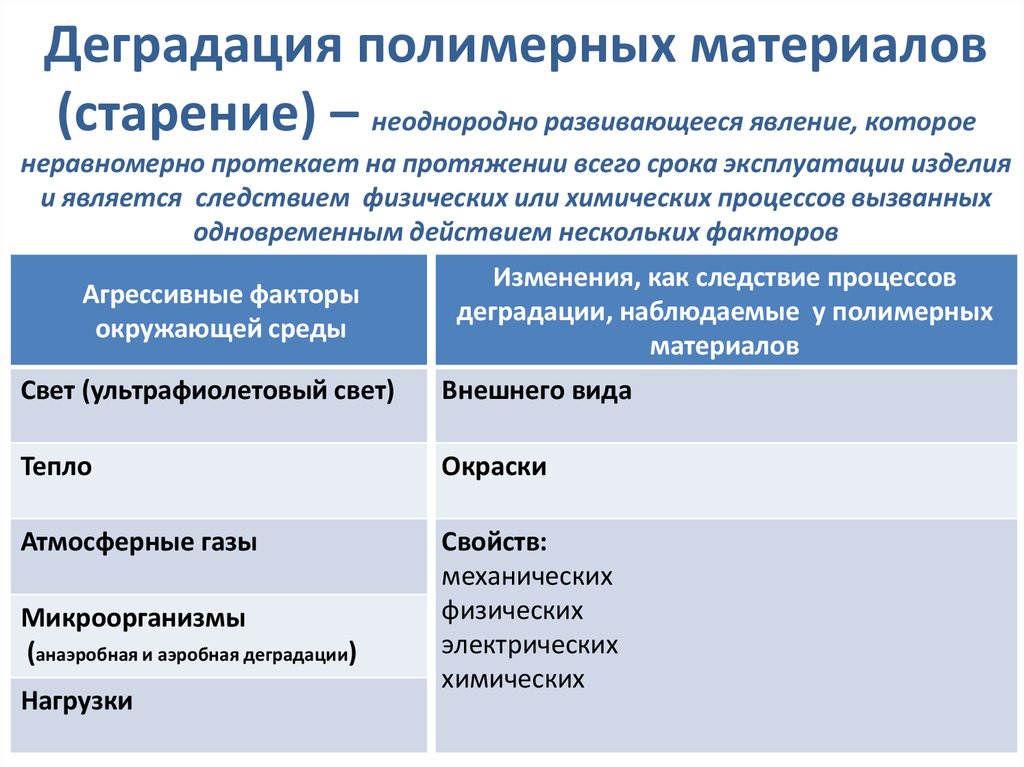
14. Деградация полимерных материалов (старение) – неоднородно развивающееся явление, которое неравномерно протекает на протяжении
всего срока эксплуатации изделияи является следствием физических или химических процессов вызванных
одновременным действием нескольких факторов
Агрессивные факторы
окружающей среды
Изменения, как следствие процессов
деградации, наблюдаемые у полимерных
материалов
Свет (ультрафиолетовый свет)
Внешнего вида
Тепло
Окраски
Атмосферные газы
Свойств:
механических
физических
электрических
химических
Микроорганизмы
(анаэробная и аэробная деградации)
Нагрузки
15.
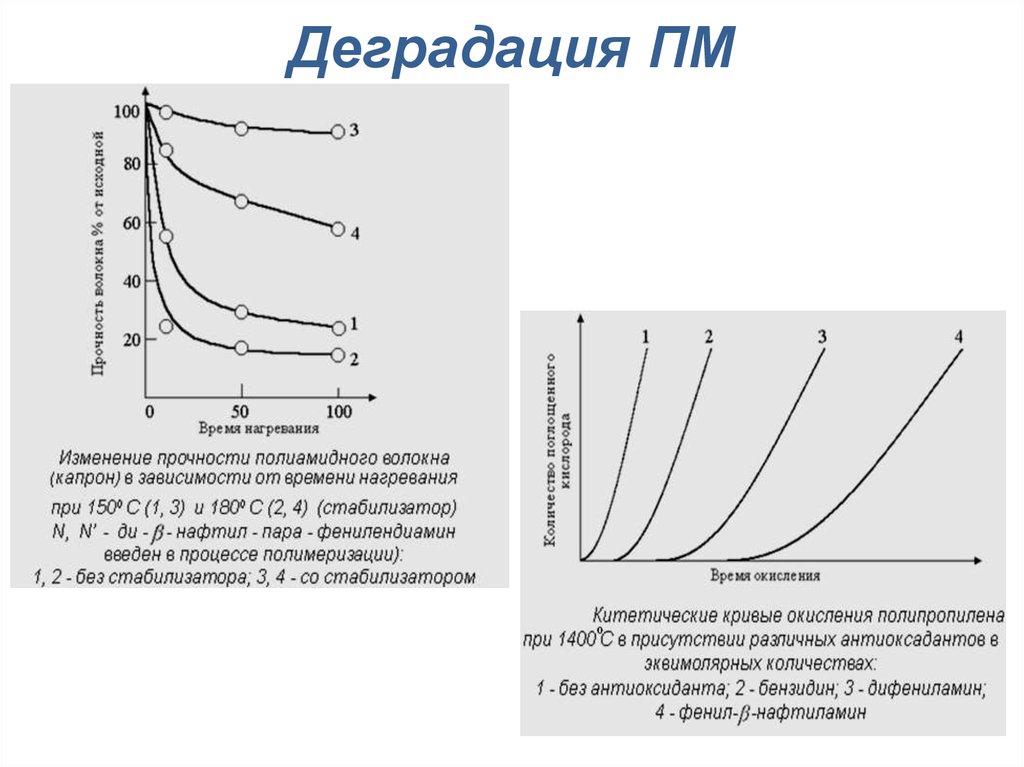
Деградация ПМ16. Деградация ПМ
Подходы к исследованию деградации:• Интенсифицируют параметры окружающих факторов
• Получают экспериментальные результаты
• Обрабатывают результаты с помощью предсказуемых
моделей
Это позволяет:
• Определить агрессивные условия
• Выявить наиболее чувствительные функциональные свойства
ПМ
• Определить места, где зарождается деградация и степень
реальной деградации ПМ
• Прогнозировать для определенных условий эксплуатации
сроки службы изделий из ПМ
Действия:
Введение антиоксидантов
Защита поверхности ПМ
Усиление физико-механических характеристик
Изменение толщины изделия
Усовершенствование процесса изготовления (допрессовка)







 Химия
Химия