Похожие презентации:
Ароматичні сульфонові кислоти (аренсульфокислоти) та їх похідні
1. Ароматичні сульфонові кислоти (аренсульфокислоти) та їх похідні
АРОМАТИЧНІ СУЛЬФОНОВІ КИСЛОТИ(АРЕНСУЛЬФОКИСЛОТИ) ТА ЇХ ПОХІДНІ
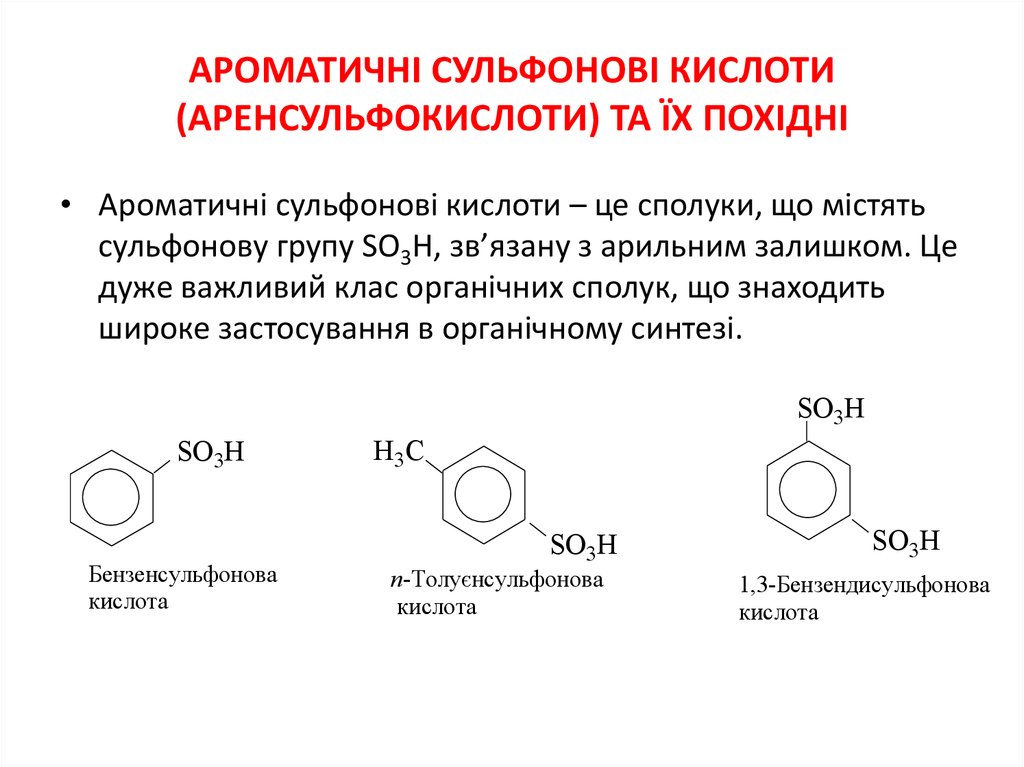
• Ароматичні сульфонові кислоти – це сполуки, що містять
сульфонову групу SO3H, зв’язану з арильним залишком. Це
дуже важливий клас органічних сполук, що знаходить
широке застосування в органічному синтезі.
SO3H
SO3H
Бензенсульфонова
кислота
H3C
SO3H
п-Толуєнсульфонова
кислота
SO3H
1,3-Бензендисульфонова
кислота
2. СПОСОБИ ОДЕРЖАННЯ
1. Дія концентрованої Н2SO4 на бензен та його гомологиo
C6H6
HO SO2 OH
t
C6H5 SO2 OH
H2O
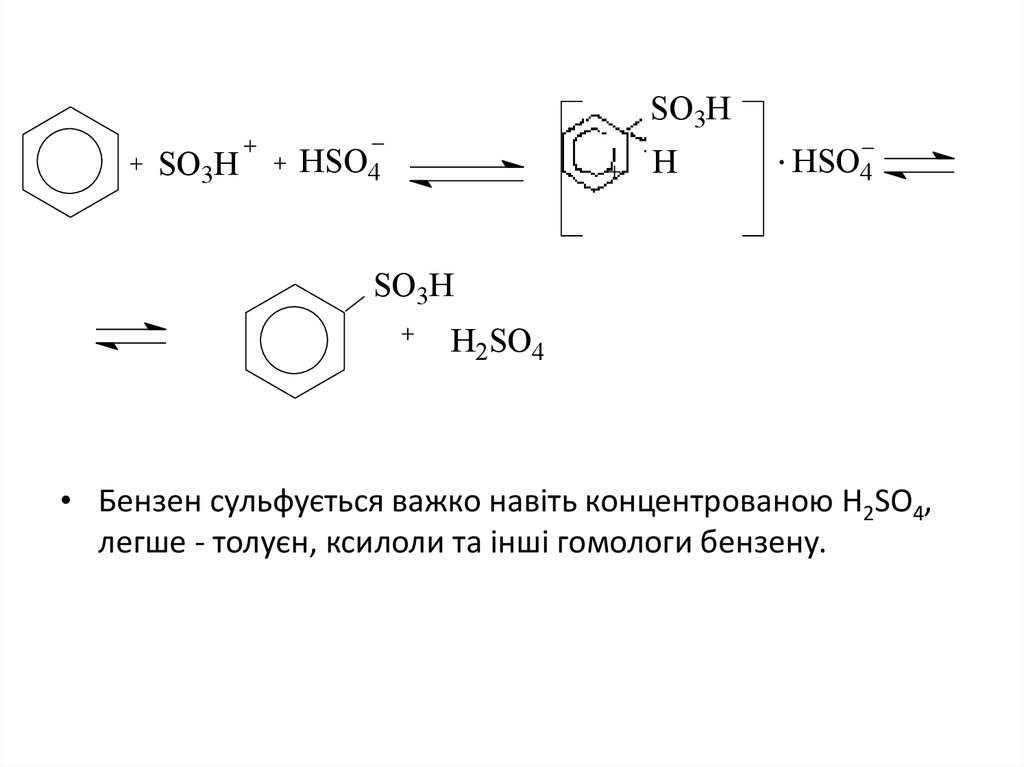
Реакція протікає за механізмом електрофільного заміщення (SE).
Очевидно, електрофільний реагент утворюється за реакцією:
H O SO3H
H O SO3H
H O SO3H
H3O
2 HSO4
SO3H
Гідросульфонієвий йон
(електрофіл)
3.
SO3HSO3H
HSO4
H
HSO4
SO3H
H2SO4
• Бензен сульфується важко навіть концентрованою Н2SО4,
легше - толуєн, ксилоли та інші гомологи бензену.
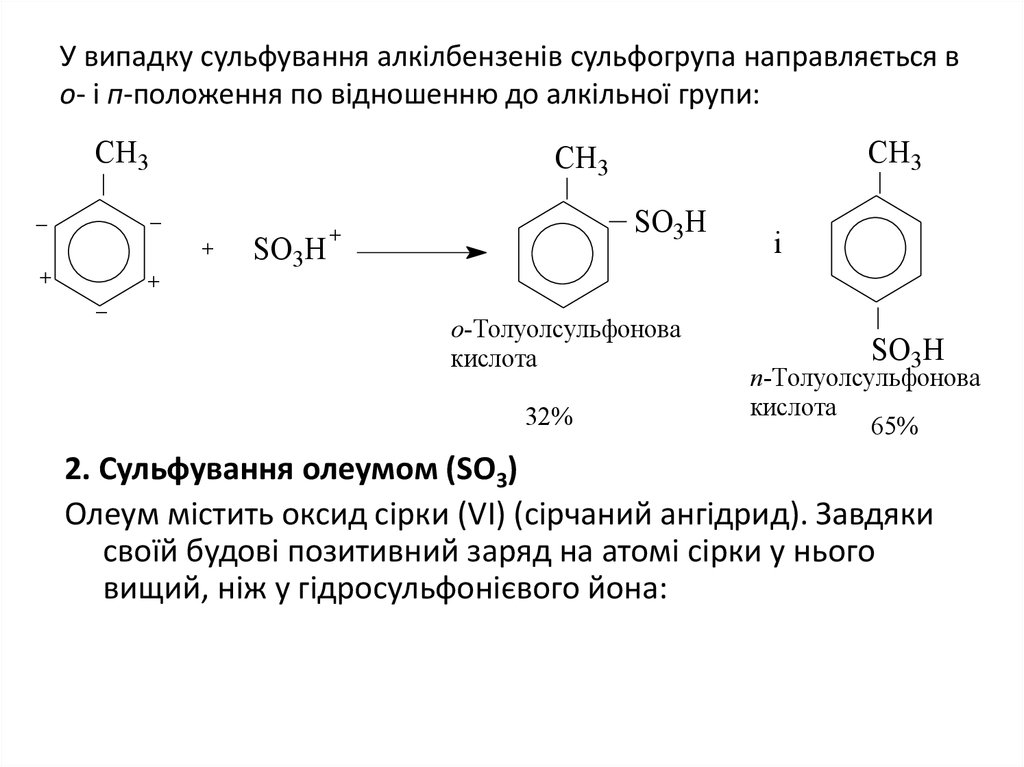
4. У випадку сульфування алкілбензенів сульфогрупа направляється в о- і п-положення по відношенню до алкільної групи:
CH3СН3
СН3
SO3H
SO3H
о-Толуолсульфонова
кислота
32%
і
SO3H
п-Толуолсульфонова
кислота
65%
2. Сульфування олеумом (SО3)
Олеум містить оксид сірки (VІ) (сірчаний ангідрид). Завдяки
своїй будові позитивний заряд на атомі сірки у нього
вищий, ніж у гідросульфонієвого йона:
5.
SO3Повільно
SO3
H
H
SO3
H
Швидко
SO3H
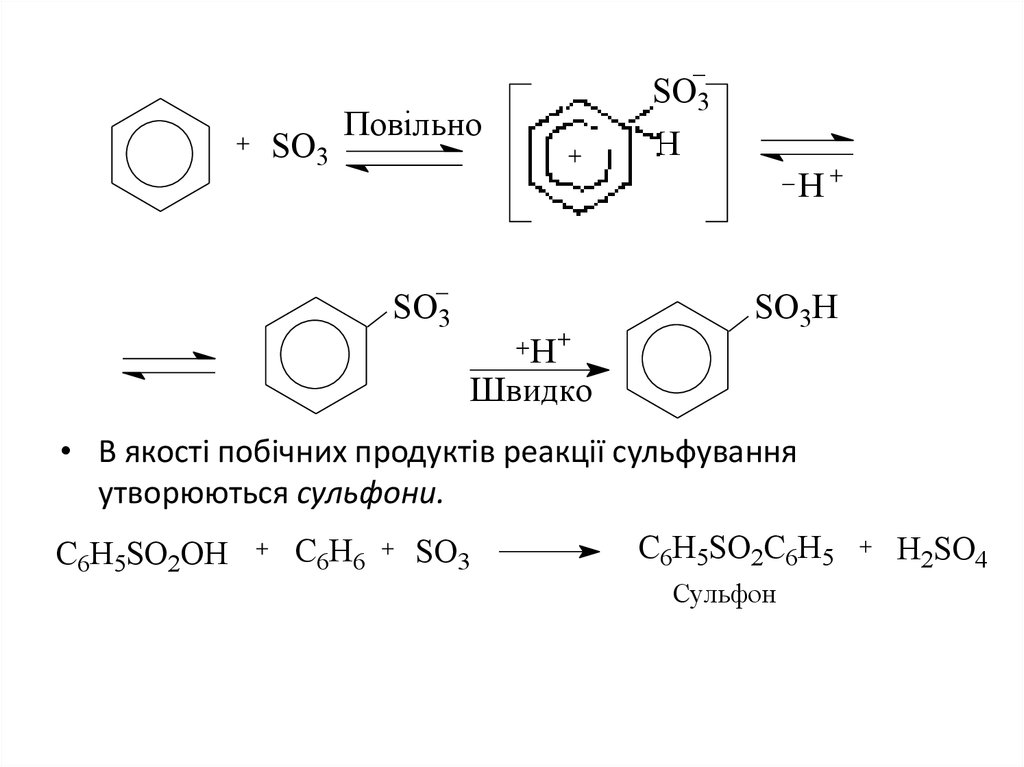
• В якості побічних продуктів реакції сульфування
утворюються сульфони.
С6Н5SO2ОH
C6H6
SO3
С6Н5SO2С6H5
Сульфон
H2SO4
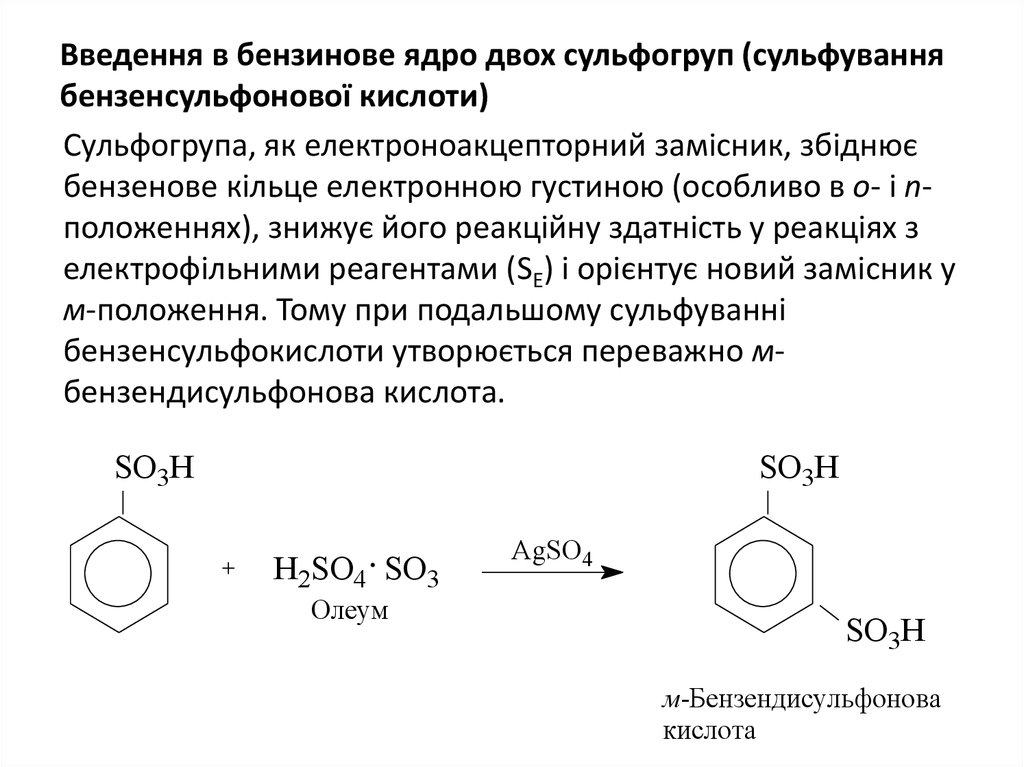
6. Введення в бензинове ядро двох сульфогруп (сульфування бензенсульфонової кислоти)
Сульфогрупа, як електроноакцепторний замісник, збіднюєбензенове кільце електронною густиною (особливо в o- і nположеннях), знижує його реакційну здатність у реакціях з
електрофільними реагентами (SE) і орієнтує новий замісник у
м-положення. Тому при подальшому сульфуванні
бензенсульфокислоти утворюється переважно мбензендисульфонова кислота.
SO3H
SO3H
H2SO4 SO3
Олеум
AgSO4
SO3H
м-Бензендисульфонова
кислота
7. Фізичні і хімічні властивості
ФІЗИЧНІ І ХІМІЧНІ ВЛАСТИВОСТІ• Аренсульфонові кислоти - переважно кристалічні
речовини, розчинні у воді. Це – сильні кислоти і у водному
середовищі вони повністю йонізовані.
• Сульфогрупа є дуже реакційноздатною і для
аренсульфонових кислот характерні такі типи
перетворень:
• 1.Реакції сульфогрупи;
• 2.Реакції заміщення сульфогрупи на інші функціональні
групи;
• 3.Реакції заміщення водню в бензеновому кільці.
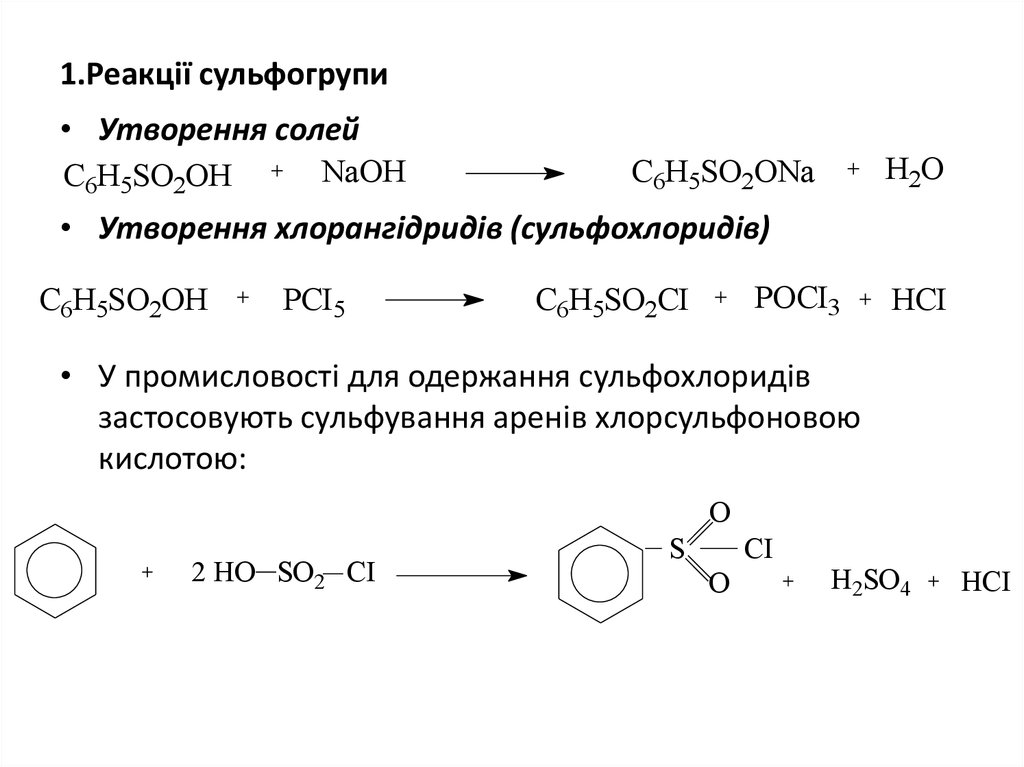
8. 1.Реакції сульфогрупи
• Утворення солейС6Н5SO2ОH
NaOH
H2O
С6Н5SO2ONa
• Утворення хлорангідридів (сульфохлоридів)
С6Н5SO2ОH
PCI5
PОCI3
С6Н5SO2CI
HCI
• У промисловості для одержання сульфохлоридів
застосовують сульфування аренів хлорсульфоновою
кислотою:
О
2 HO SO2 CI
S
CI
O
H2SO4
HCI
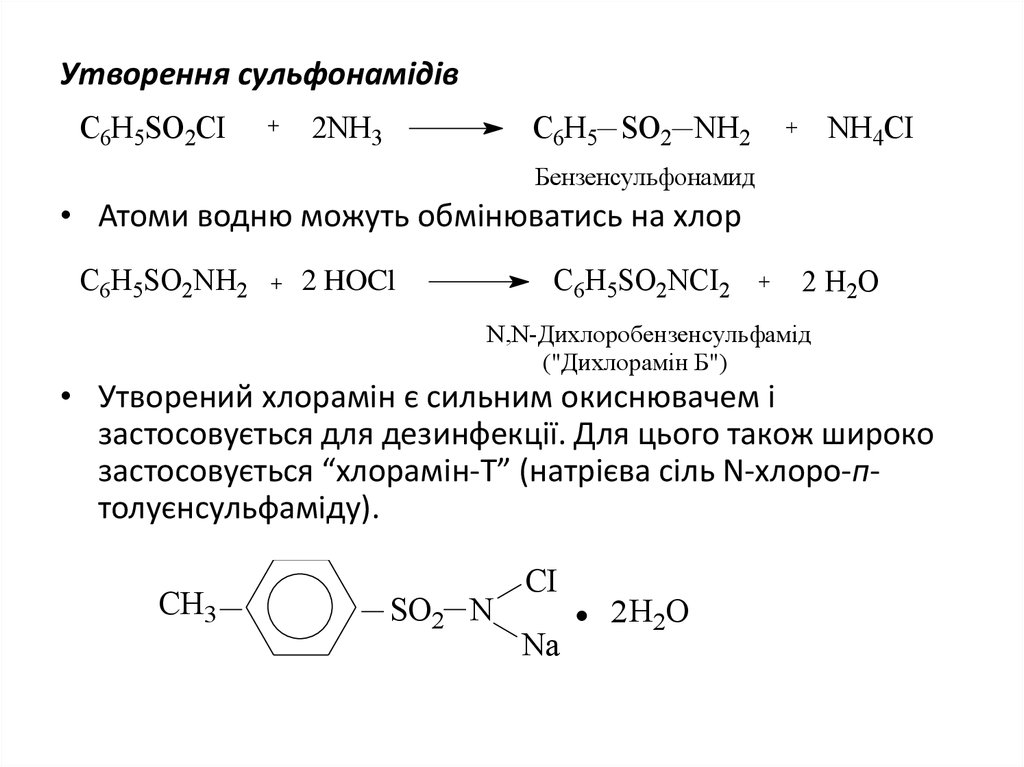
9. Утворення сульфонамідів
С6Н5SO2CI2NH3
NH4CI
С6Н5 SO2 NH2
Бензенсульфонамид
• Атоми водню можуть обмінюватись на хлор
С6Н5SO2NH2
С6Н5SO2NCI2
2 HOCl
2 H2O
N,N-Дихлоробензенсульфамід
("Дихлорамін Б")
• Утворений хлорамін є сильним окиснювачем і
застосовується для дезинфекції. Для цього також широко
застосовується “хлорамін-Т” (натрієва сіль N-хлоро-птолуєнсульфаміду).
CH3
SO2 N
CI
Na
2 H2O
10. Відновлення сульфогрупи
С6Н5SO2OHZn + H2SO4
3 H2O
С6Н5SH
Тіофенол
2. Реакції заміщення сульфогрупи
Сульфогрупа зв’язана з вуглецевим атомом бензенового
кільця доволі полярним зв’язком і може бути відщеплена
за допомогою як електрофільних, так і нуклеофільних
реагентів
Реакції гідролізу
о
С6Н5SO3H
H2O
120-150 C
H
С6Н6
H2SO4
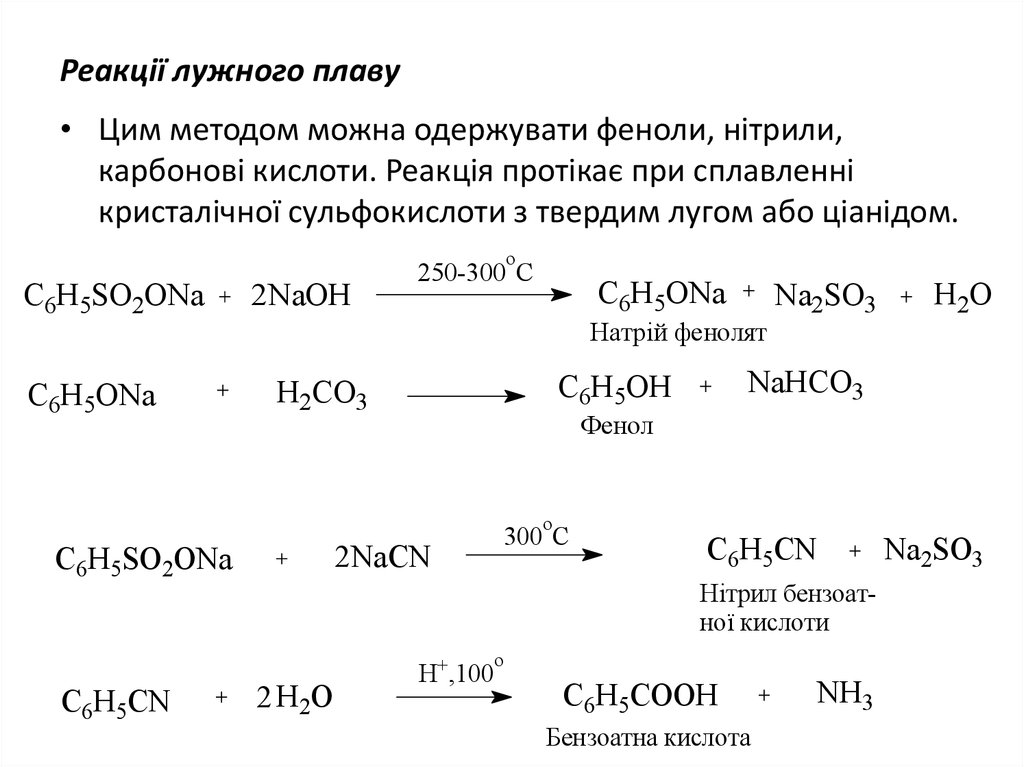
11. Реакції лужного плаву
• Цим методом можна одержувати феноли, нітрили,карбонові кислоти. Реакція протікає при сплавленні
кристалічної сульфокислоти з твердим лугом або ціанідом.
о
С6Н5SO2ONa
С6Н5ONa
2NaOH
250-300 C
С6Н5ONa
Натрій фенолят
Фенол
о
300 C
2 NaСN
С6Н5SO2ONa
С6Н5CN
Нітрил бензоатної кислоти
o
С6Н5СN
2 H2O
H2O
NaHCO3
С6Н5OH
H2CO3
Na2SO3
H+,100
С6Н5COOH
Бензоатна кислота
NH3
Na2SO3
12. 3. Реакції заміщення водню у бензеновому кільці
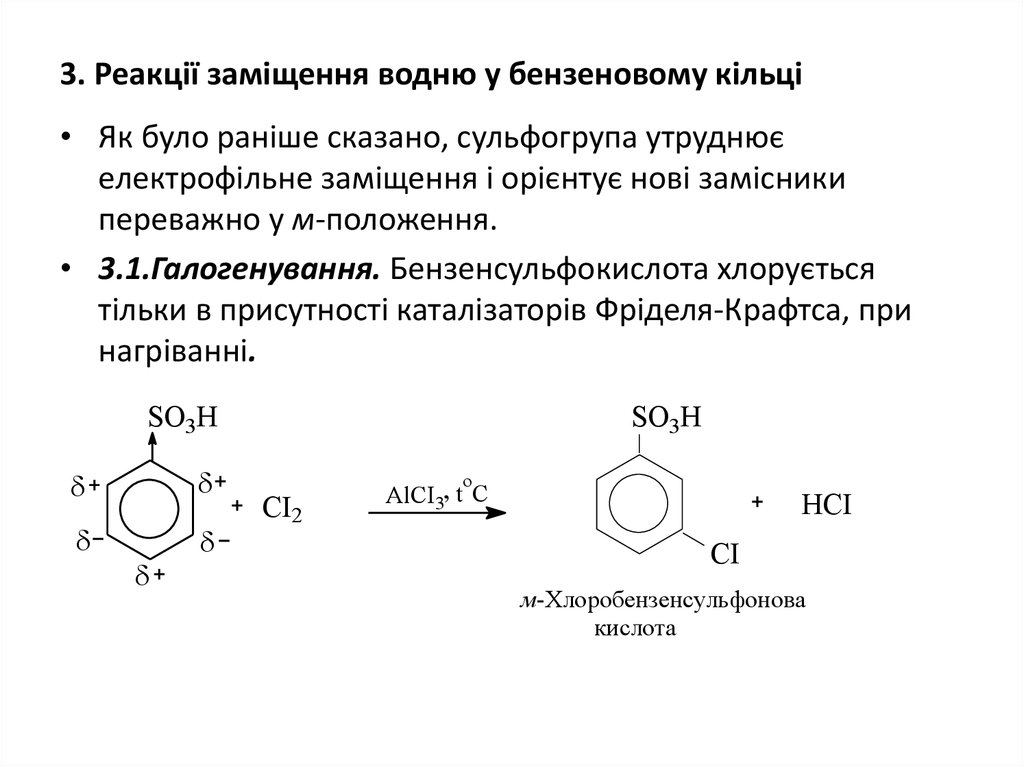
• Як було раніше сказано, сульфогрупа утруднюєелектрофільне заміщення і орієнтує нові замісники
переважно у м-положення.
• 3.1.Галогенування. Бензенсульфокислота хлорується
тільки в присутності каталізаторів Фріделя-Крафтса, при
нагріванні.
SO3H
SO3H
CI2
о
AlCI3, t C
HCI
CI
м-Хлоробензенсульфонова
кислота
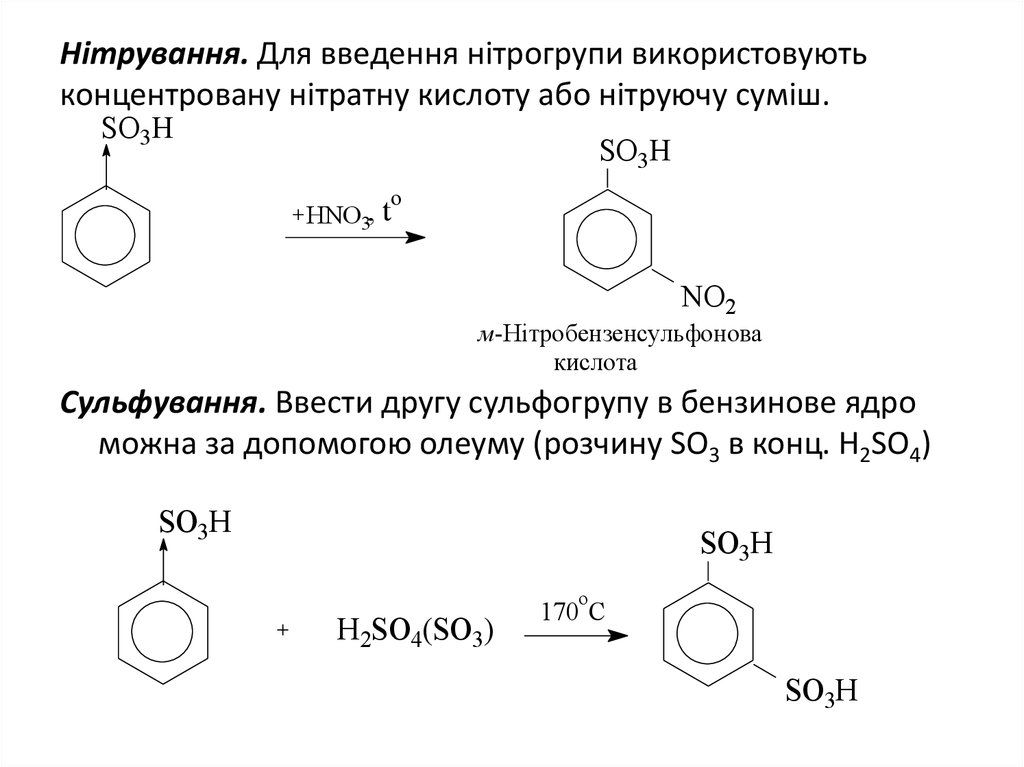
13. Нітрування. Для введення нітрогрупи використовують концентровану нітратну кислоту або нітруючу суміш.
SO3HSO3H
o
HNO3, t
NO2
м-Нітробензенсульфонова
кислота
Сульфування. Ввести другу сульфогрупу в бензинове ядро
можна за допомогою олеуму (розчину SO3 в конц. H2SO4)
SO3H
SO3H
о
H2SO4(SO3)
170 C
SO3H
14. Ароматичні нітросполуки (нітроарени)
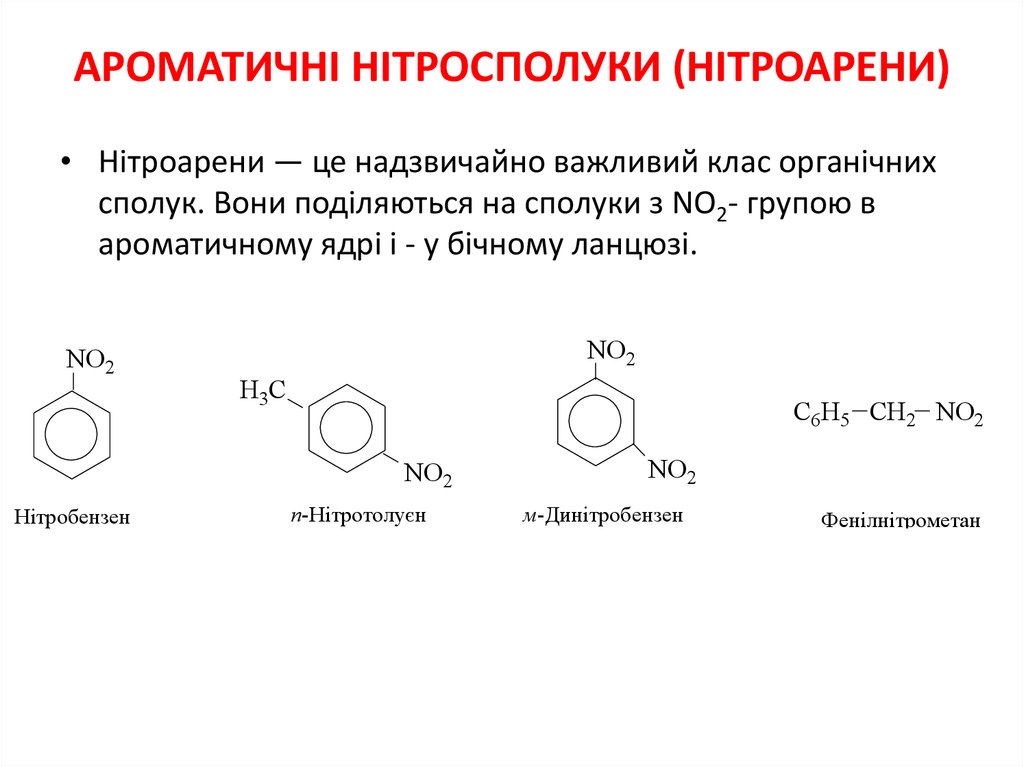
АРОМАТИЧНІ НІТРОСПОЛУКИ (НІТРОАРЕНИ)• Нітроарени ― це надзвичайно важливий клас органічних
сполук. Вони поділяються на сполуки з NO2- групою в
ароматичному ядрі і - у бічному ланцюзі.
NO2
NO2
Н3С
C6H5 CH2 NO2
NO2
Нітробензен
п-Нітротолуєн
NO2
м-Динітробензен
Фенілнітрометан
15. Методи одержання
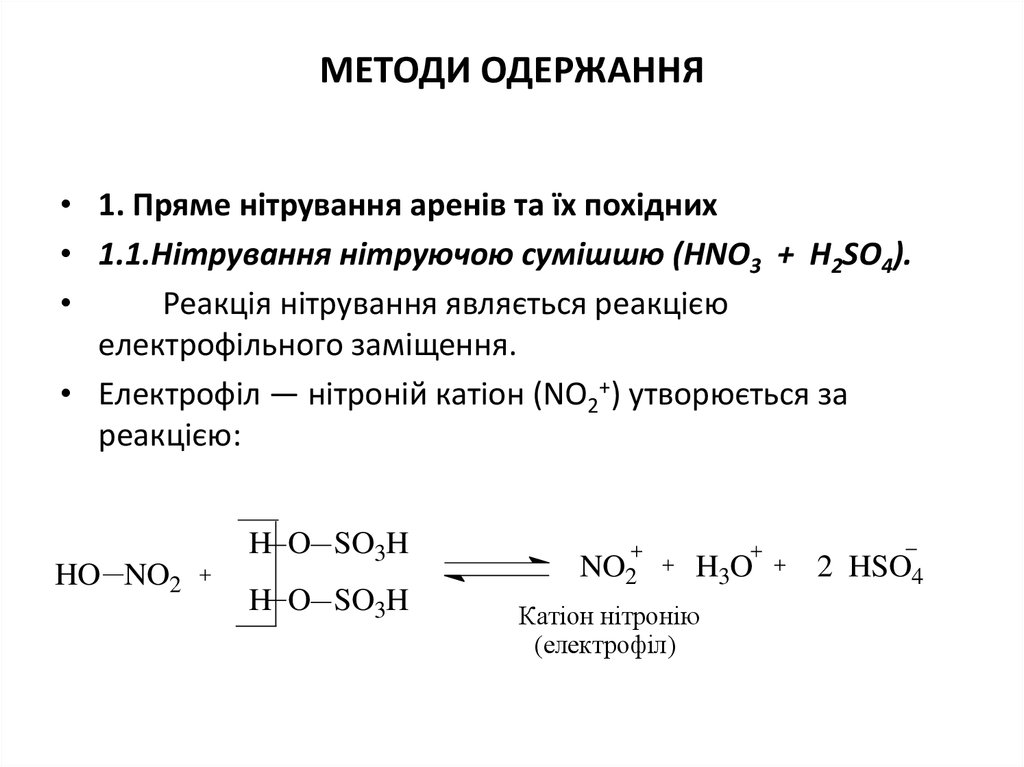
МЕТОДИ ОДЕРЖАННЯ• 1. Пряме нітрування аренів та їх похідних
• 1.1.Нітрування нітруючою сумішшю (HNO3 + H2SO4).
Реакція нітрування являється реакцією
електрофільного заміщення.
• Електрофіл ― нітроній катіон (NO2+) утворюється за
реакцією:
HO NO2
H O SO3H
H O SO3H
NO2
H3O
Катіон нітронію
(електрофіл)
2 HSO4
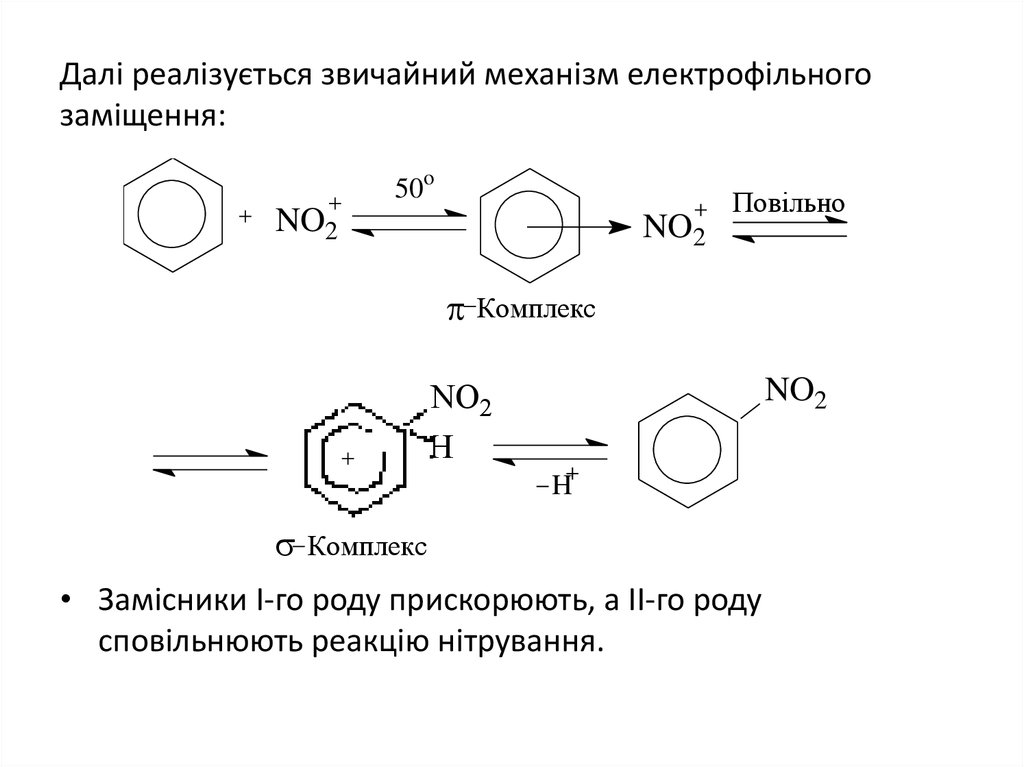
16. Далі реалізується звичайний механізм електрофільного заміщення:
50oNO2
NO2
Повільно
Комплекс
NO2
NO2
H
H
Комплекс
• Замісники І-го роду прискорюють, а ІІ-го роду
сповільнюють реакцію нітрування.
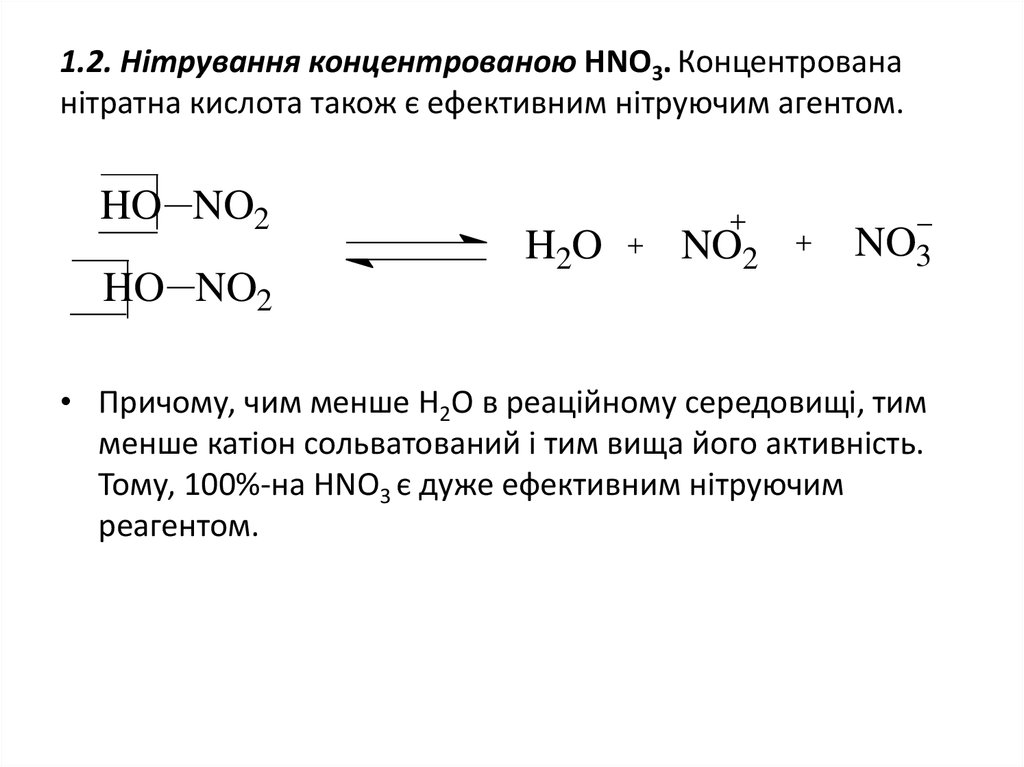
17. 1.2. Нітрування концентрованою HNO3. Концентрована нітратна кислота також є ефективним нітруючим агентом.
HO NO2HO NO2
H2O
NO2
NO3
• Причому, чим менше Н2О в реаційному середовищі, тим
менше катіон сольватований і тим вища його активність.
Тому, 100%-на HNO3 є дуже ефективним нітруючим
реагентом.
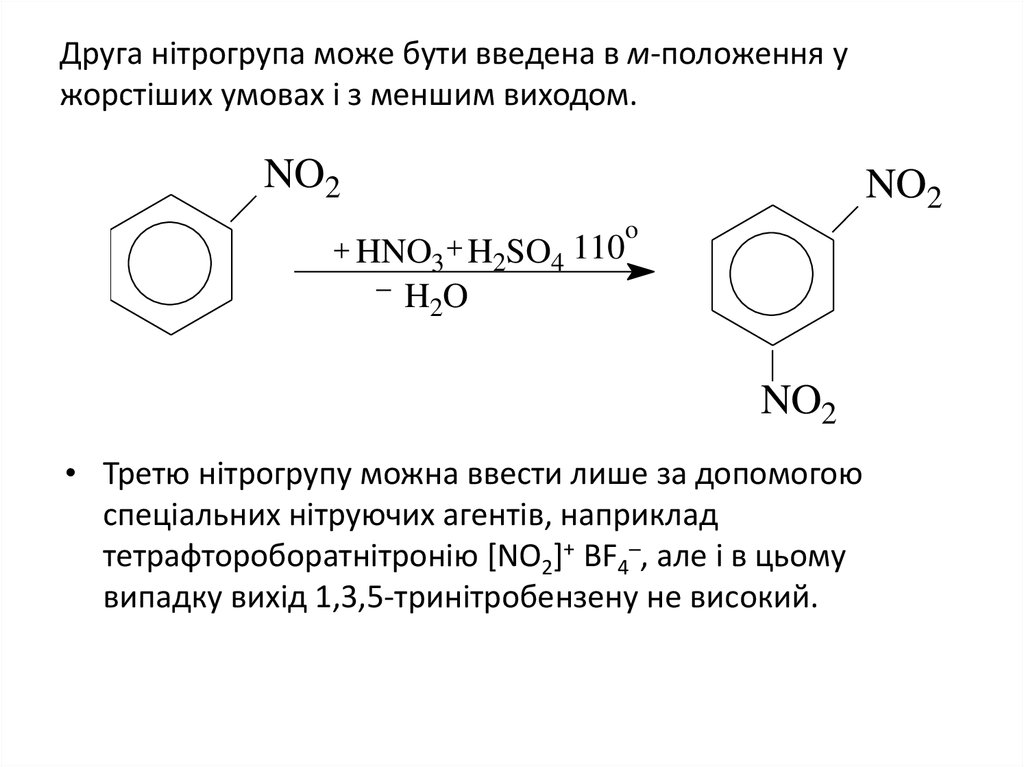
18. Друга нітрогрупа може бути введена в м-положення у жорстіших умовах і з меншим виходом.
NO2NO2
o
HNO3 H2SO4 110
H2O
NO2
• Третю нітрогрупу можна ввести лише за допомогою
спеціальних нітруючих агентів, наприклад
тетрафтороборатнітронію [NO2]+ BF4─, але і в цьому
випадку вихід 1,3,5-тринітробензену не високий.
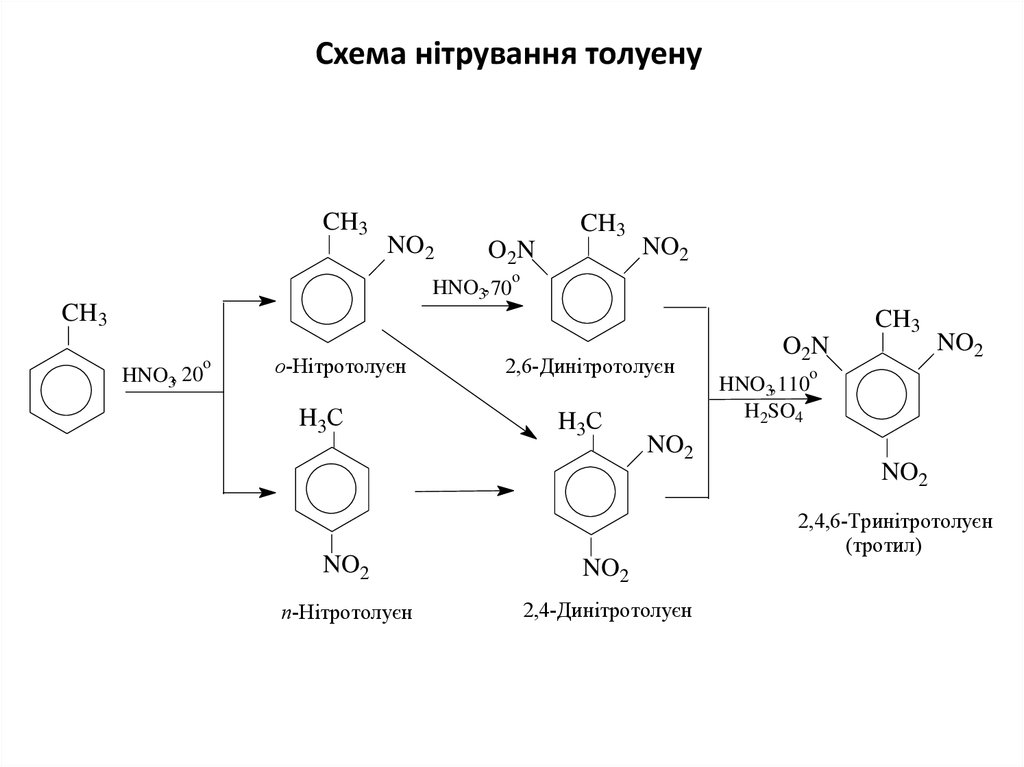
19. Схема нітрування толуену
Схема нітрування толуенуCH3
NO2
CH3
O 2N
o
HNO3, 70
NO2
CH3
CH3
HNO3, 20
o
о-Нітротолуєн
H 3С
2,6-Динітротолуєн
H 3С
NO2
O2N
NO2
o
HNO3, 110
H2SO4
NO2
2,4,6-Тринітротолуєн
(тротил)
NO2
NO2
n-Нітротолуєн
2,4-Динітротолуєн
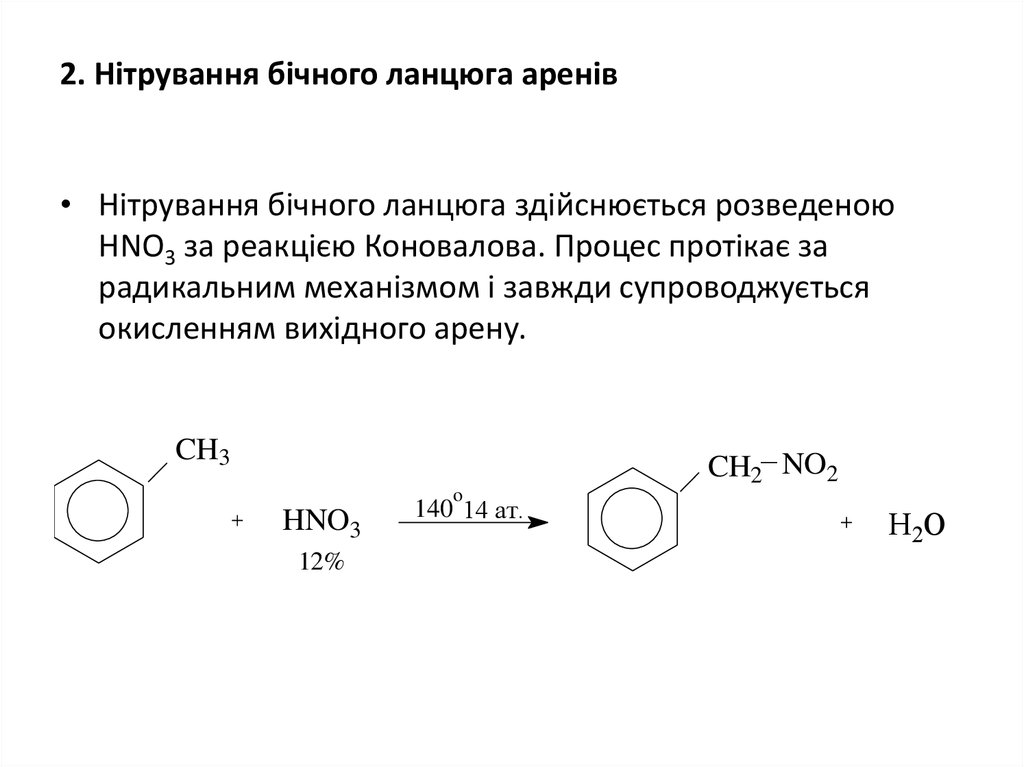
20. 2. Нітрування бічного ланцюга аренів
• Нітрування бічного ланцюга здійснюється розведеноюНNO3 за реакцією Коновалова. Процес протікає за
радикальним механізмом і завжди супроводжується
окисленням вихідного арену.
CH3
CH2 NO2
o
HNO3
12%
140 14 ат.
H2O
21. Фізичні та хімічні властивості
ФІЗИЧНІ ТА ХІМІЧНІ ВЛАСТИВОСТІ• Мононітроарени – рідкі або тверді речовини, мають запах
мигдалю і дуже отруйні. У воді не розчиняються, є сильно
полярними розчинниками. Ди- і полінітроарени –
кристалічні речовини.
• 1. Реакції відновлення нітрогрупи
• Відновлення NО2-групи в NH2 - це складний процес,
напрямок протікання якого залежить, в основному, від рНсередовища. Вперше вказану реакцію відкрив Зінін М.М. у
1842 р.
C6H5NO2
3(NH4)2S
C6H5NH2
6NH3 3S
2H2O
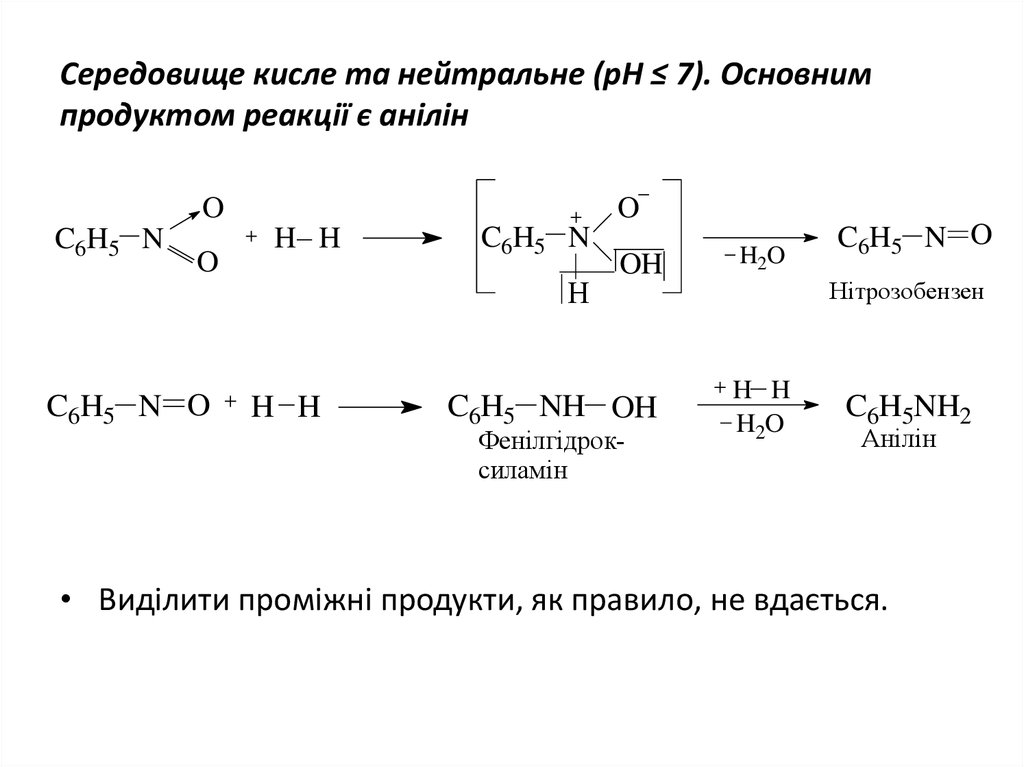
22. Середовище кисле та нейтральне (рН ≤ 7). Основним продуктом реакції є анілін
OC6H5 N
O
C6H5 N O
O
H H
C6H5 N
OH
H2O
C6H5 NH OH
H H
H2O
H
H H
Фенілгідроксиламін
C6H5 N O
Нітрозобензен
C6H5NH2
Анілін
• Виділити проміжні продукти, як правило, не вдається.
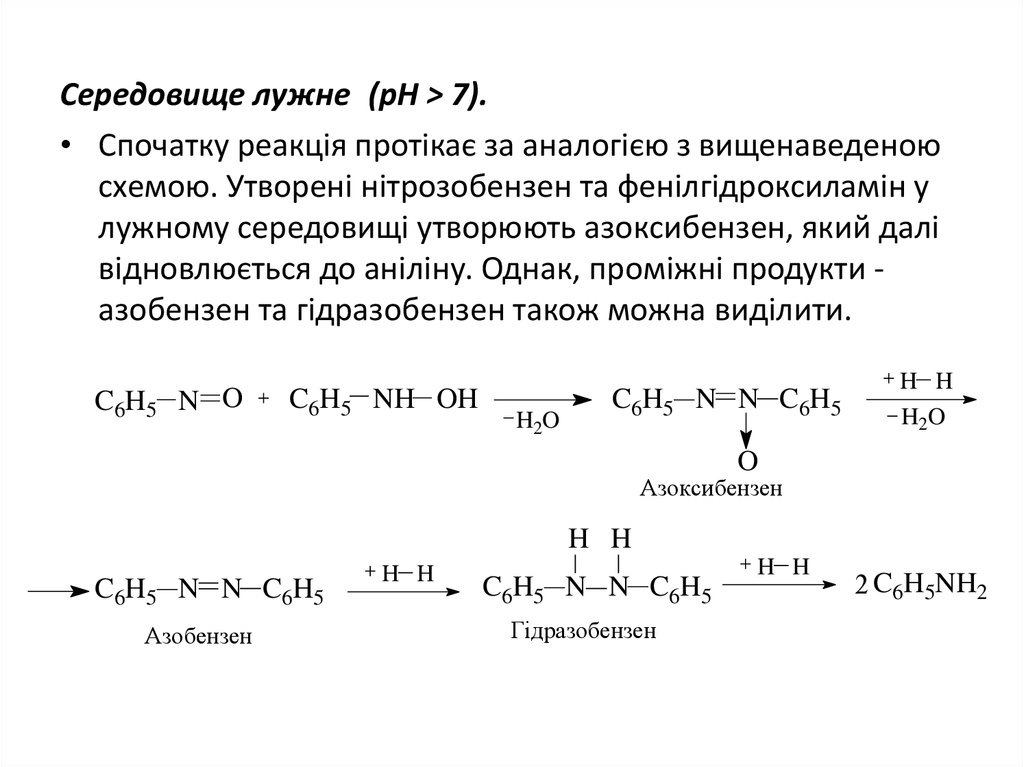
23. Середовище лужне (рН > 7).
Середовище лужне (рН > 7).• Спочатку реакція протікає за аналогією з вищенаведеною
схемою. Утворені нітрозобензен та фенілгідроксиламін у
лужному середовищі утворюють азоксибензен, який далі
відновлюється до аніліну. Однак, проміжні продукти азобензен та гідразобензен також можна виділити.
C6H5
N O
C6H5 NH OH
H2O
C6H5 N N C6H5
H H
H2O
O
Азоксибензен
H H
C6H5 N N C6H5
Азобензен
H H
C6H5 N N C6H5
Гідразобензен
H H
2 C6H5NH2
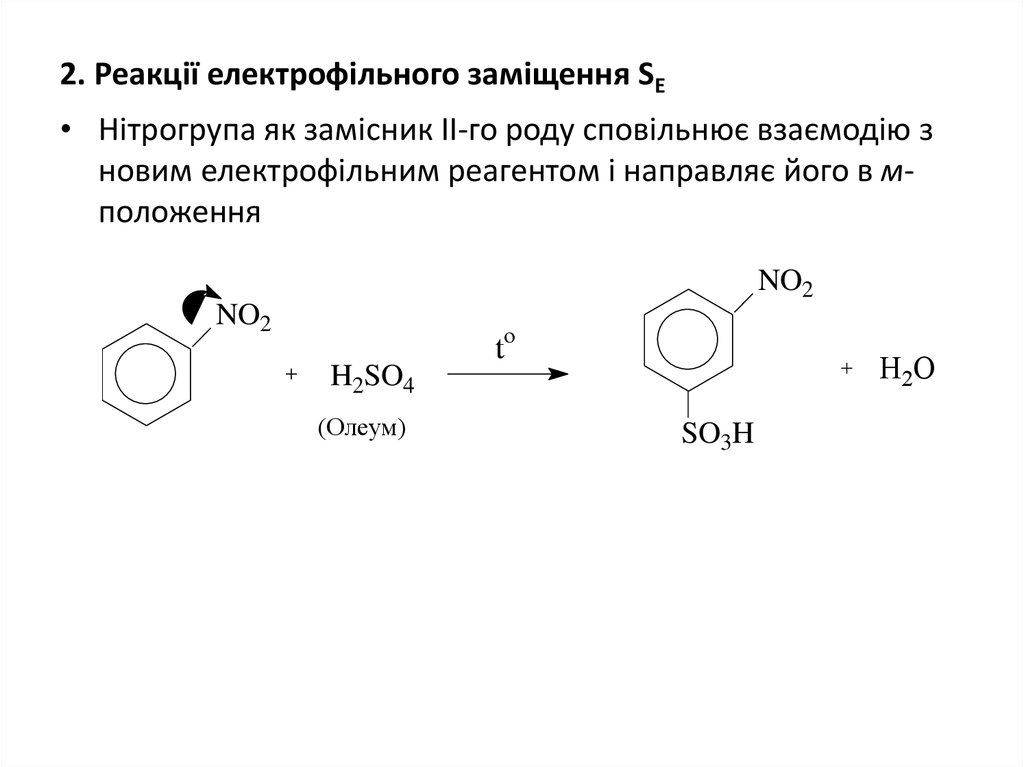
24. 2. Реакції електрофільного заміщення SE
• Нітрогрупа як замісник ІІ-го роду сповільнює взаємодію зновим електрофільним реагентом і направляє його в мположення
NO2
NO2
o
H2SO4
(Олеум)
t
H2O
SO3H
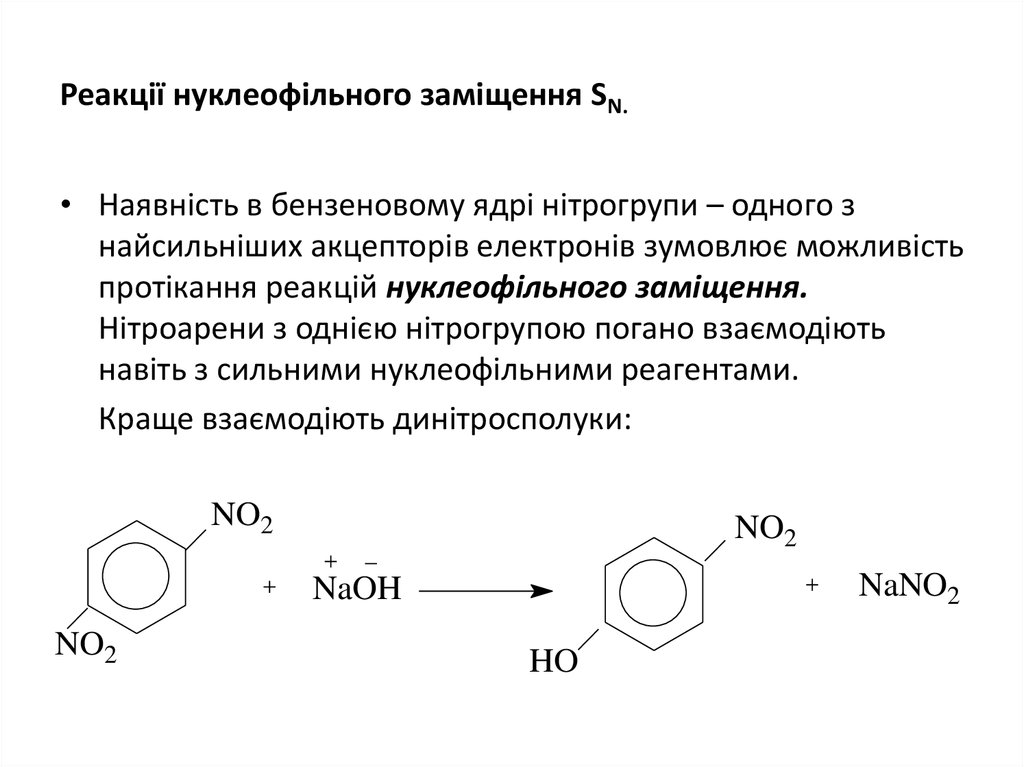
25. Реакції нуклеофільного заміщення SN.
• Наявність в бензеновому ядрі нітрогрупи – одного знайсильніших акцепторів електронів зумовлює можливість
протікання реакцій нуклеофільного заміщення.
Нітроарени з однією нітрогрупою погано взаємодіють
навіть з сильними нуклеофільними реагентами.
Краще взаємодіють динітросполуки:
NO2
NO2
NaNO2
NaOH
NO2
HO
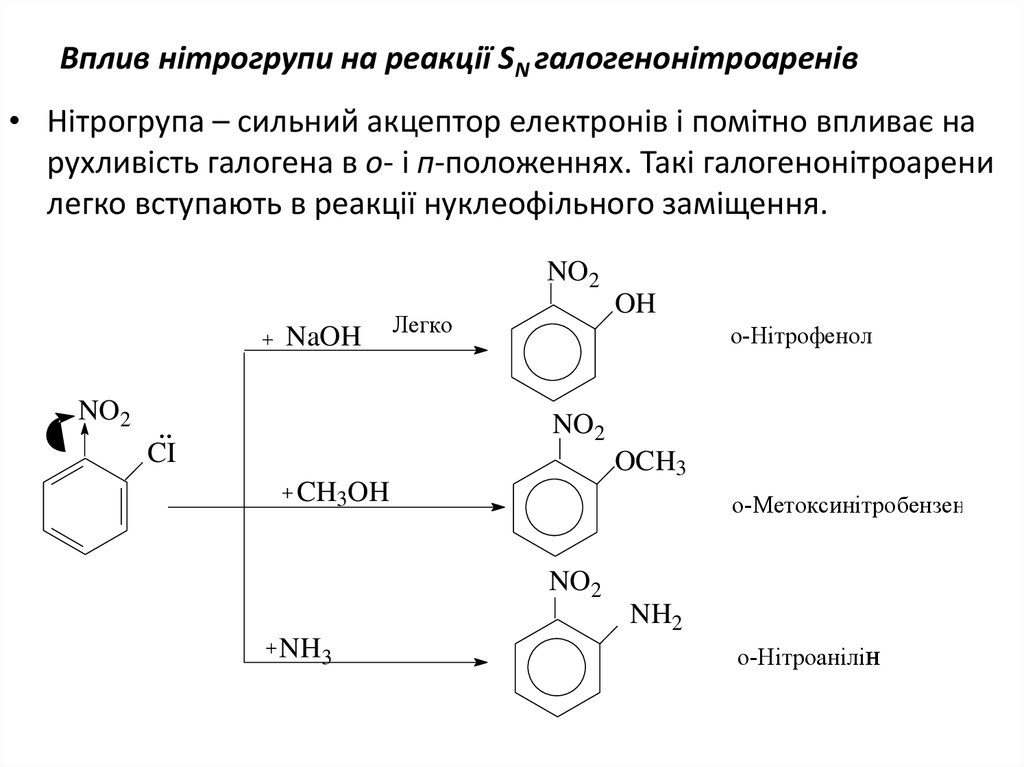
26. Вплив нітрогрупи на реакції SN галогенонітроаренів
• Нітрогрупа – сильний акцептор електронів і помітно впливає нарухливість галогена в о- і п-положеннях. Такі галогенонітроарени
легко вступають в реакції нуклеофільного заміщення.
NO2
NaOH
NO2
OH
Легко
о-Нітрофенол
NO2
CI
OCH3
CH3OH
о-Метоксинітробензен
NO2
NH2
NH3
о-Нітроанілін




 Химия
Химия








