Похожие презентации:
Превращения алкенов при каталитическом кренинге
1.
Превращения алкенов при К.К.Расщепление
Изомеризация
Перераспределениеводорода
Циклизация
Расщепление - крекинг
Происходит расщепление по связи С-С в -положение к двой
RCH2CH2CH2 CH2CH=CH2
RCH2CH=CH2 + CH3CH=CH2
2.
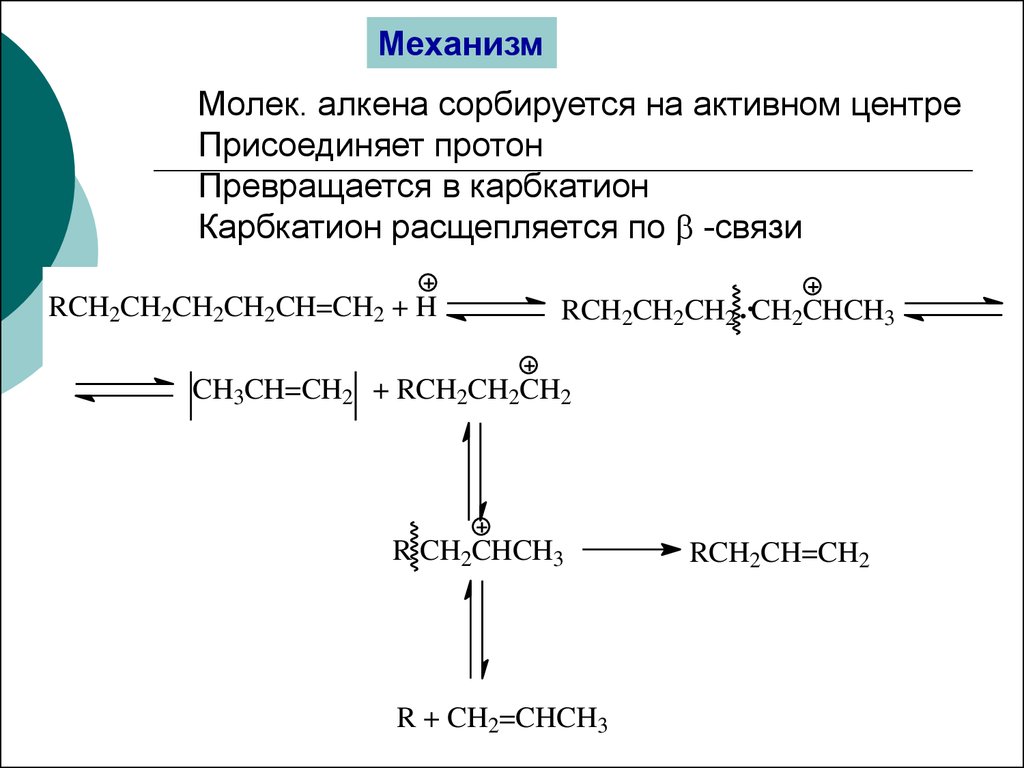
МеханизмМолек. алкена сорбируется на активном центре
Присоединяет протон
Превращается в карбкатион
Карбкатион расщепляется по -связи
RCH2CH2CH2CH2CH=CH2 + H
RCH2CH2CH2 CH2CHCH3
CH3CH=CH2 + RCH2CH2CH2
R CH2CHCH3
R + CH2=CHCH3
RCH2CH=CH2
3.
Изомеризация алкеновИзомеризация с перемещением кратной связи и
скелетная изомеризация
а)миграция кратной связи
H
CH2=CHCH2CH3 + H
CH3CHCHCH3
-H
CH3CH=CHCH3
4.
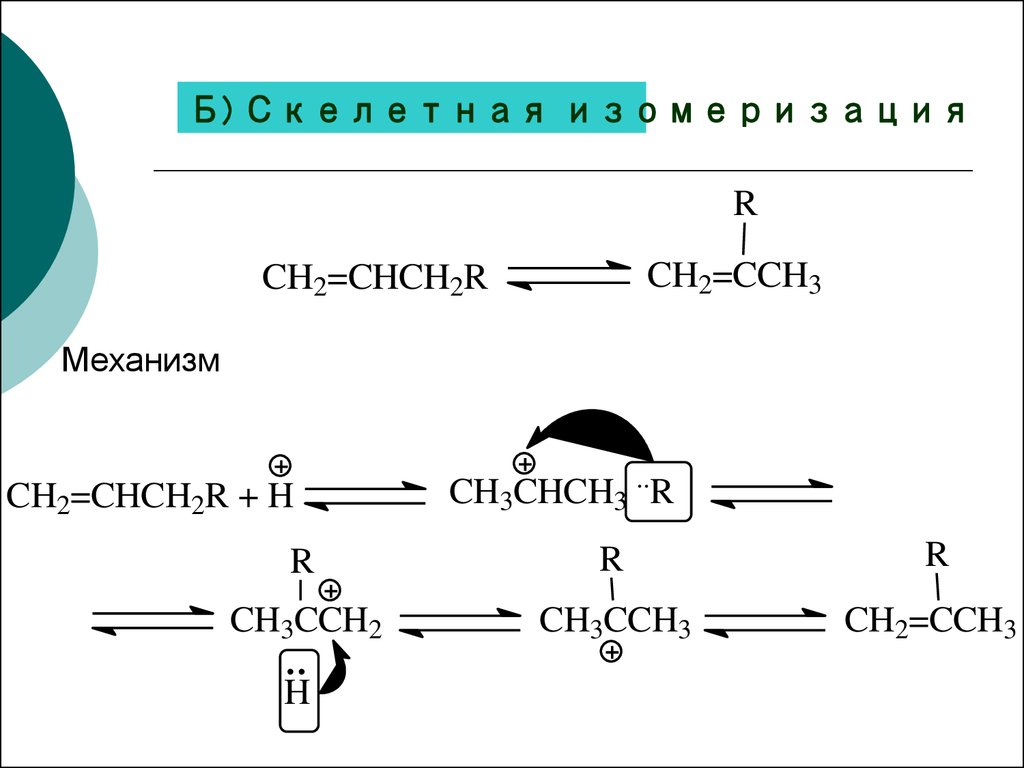
Б) Скелетная изомеризацияR
CH2=CCH3
CH2=CHCH2R
Механизм
CH2=CHCH2R + H
CH3CHCH3 ..R
R
R
R
CH3CCH2
CH3CCH3
CH2=CCH3
H
5.
В) Перераспределение водоС.С.Наметкин ЖОХ 1932.Т2, С 608 (cat H2SO4)
4CH8
2C8H16
C8H14 + C8H18
Диен
Реакция дегидро гидро полимеризации
Ионный механизм
трие
н
алкан
смолы
6.
В условиях Кат. крекингаОлефин адсорбированный на поверхности теряет водор
Ненасыщ У.В. полимеризуются
Полимеры обедняясь водородом превращаются в кокс
Длительный контакт алкена с А.сил кат. приводит к получению
кокса и алкана
C-C-C-C-C-C + C=C-C=C-C-C
2C=C-C-C-C-C
кокс
полимеры
7.
МеханизмH3C-CH(CH2)3CH3
1) H2C=CHCH2CH2CH2CH3 + H
2) H2C=CHCH(CH2)2CH3 + CH3CH(CH2)CH3
H
H2C=CHCH(CH2)2CH3 + CH3(CH2)4CH3
гексан
3) H2C=CHCHCHCH2CH3
H
-H
H2C=CHCH=CHCH2CH3
гексадиен
гексатриен
полимеры
8.
ЦиклизацияCH3
C-C-C-C-C=C
CH3 + H2
+ 3H2
циклоалканы
циклоалкены
Ароматические У.В.
9.
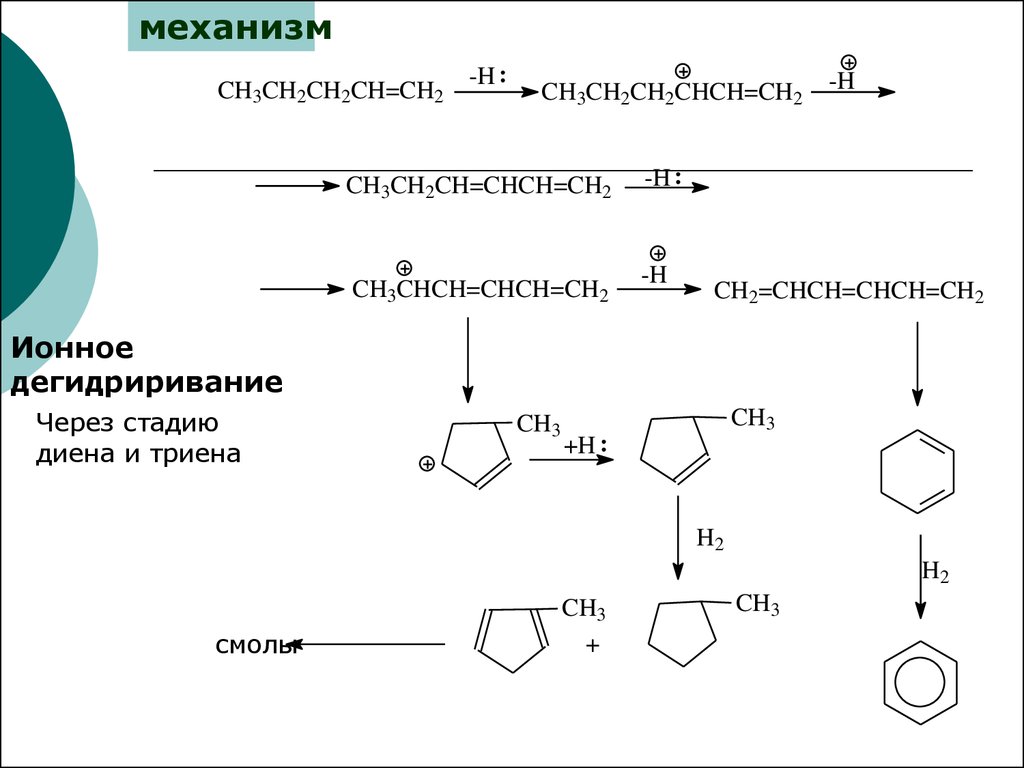
механизмCH3CH2CH2CH=CH2
-H
CH3CH2CH2CHCH=CH2
CH3CH2CH=CHCH=CH2
CH3CHCH=CHCH=CH2
-H
-H
-H
CH2=CHCH=CHCH=CH2
Ионное
дегидриривание
Через стадию
диена и триена
CH3
CH3
+H
H2
H2
смолы
CH3
+
CH3
10.
Превращения нафтеновпри каталитическом крекинге
К.К. нафтенов протекает в 1000 раз
быстрее, чем термический
Расщепление
Изомеризация
Дегидрогенизация
Расщепление
нафтенов
2CH3CH=CH2
CH3CH2CH2CH2CH=CH2
11.
Механизм1 стадия
CH2
CH2
CH2
CH2
H
CH2
CH2
CH2
CH2
CH
+ H2
CH2
CH2
CH2
2 стадия
CH
CH2CH2CH2CH2CH=CH2
CH3CHCH2 CH2CH=CH2
H3CCH=CH2 + CH2CH=CH2
Расщепление по -связи циклич. К.к.,
Изомеризация перв. карбкатиона во втор., Расщепление по -связи
12.
3 стадияH2C CH2
CH2CH=CH2 + H CH
CH2
H2C
H2C
CH2
CH2
CH
CH2 + H3CCH=CH2
H2C
CH2
13.
Образование гексена возможно также в в результатеИзомеризации ненасыщенного первичного карбкатиона
H2C-CH2CH2CH2CH=CH2
CH3CH2CH2-CH-CH=CH2
H2C CH2
CH2
CH3CH2CH2CHCH=CH2 + H CH
H2C
CH2
H2C
CH2
CH2
CH3CH2CH2CH2CH=CH2 + CH
H2C
CH2
14.
Дегидрогенизация нафтенов-H2
-H2
-H2
Механизм дегидрогенизации
CH2
CH2
H2C
CH H
H2C
CH2
H
H2C
CH2
H2C
CH2
CH2
CH2
CH2
H2C
CH
+H
CH
H2C
CH2
15.
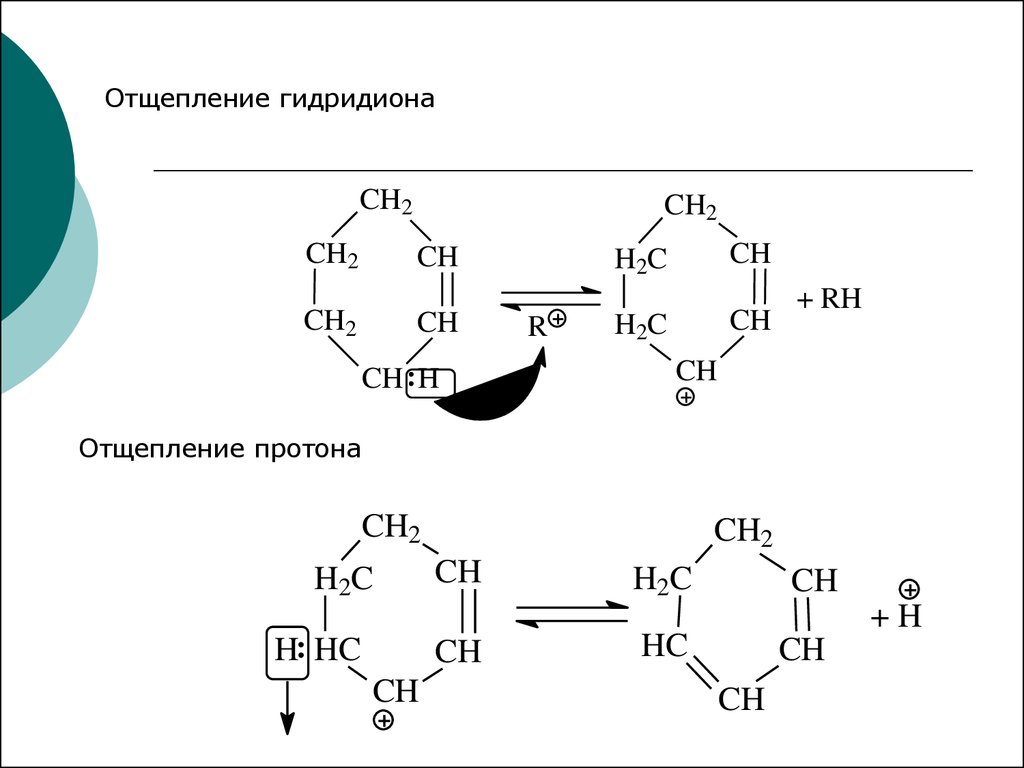
Отщепление гидридионаCH2
CH2
CH2
CH
CH2
CH
CH H
CH
H2C
R
CH
H2C
+ RH
CH
Отщепление протона
CH2
H2C
H HC
CH2
CH
CH
CH
H2C
CH
+H
HC
CH
CH
16.
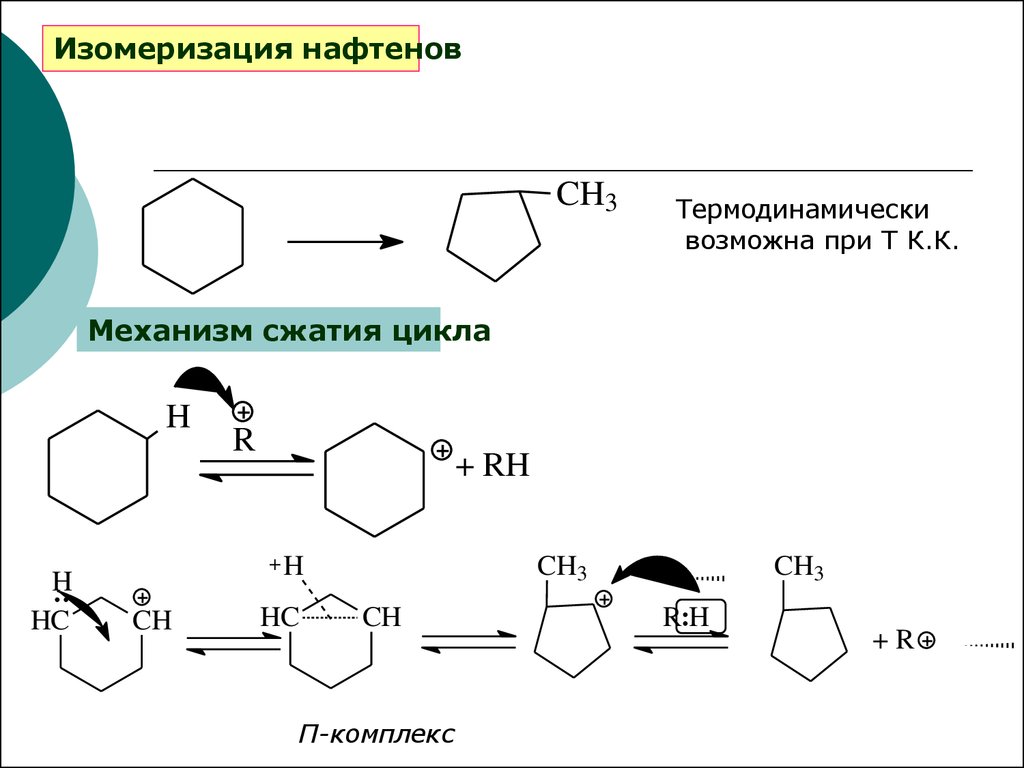
Изомеризация нафтеновCH3
Термодинамически
возможна при Т К.К.
Механизм сжатия цикла
H
H
HC
R
+ RH
+H
CH
HC
CH3
CH
П-комплекс
CH3
RH
+R
17.
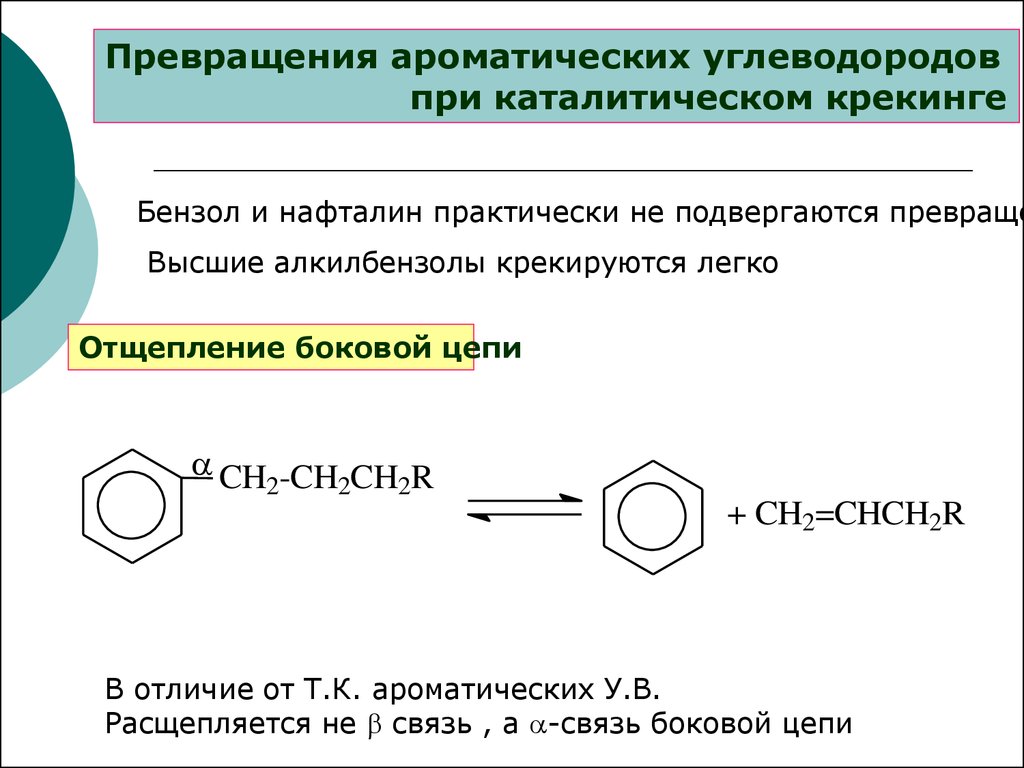
Превращения ароматических углеводородовпри каталитическом крекинге
Бензол и нафталин практически не подвергаются превраще
Высшие алкилбензолы крекируются легко
Отщепление боковой цепи
CH -CH CH R
2
2
2
+ CH2=CHCH2R
В отличие от Т.К. ароматических У.В.
Расщепляется не связь , а -связь боковой цепи
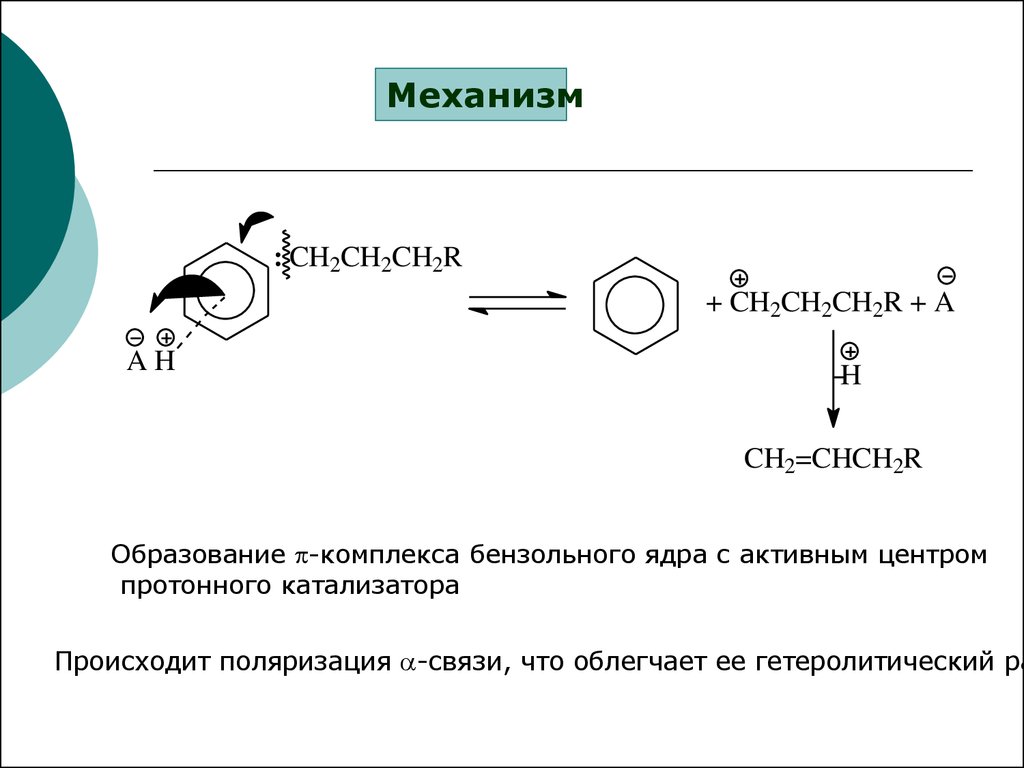
18.
МеханизмCH2CH2CH2R
+ CH2CH2CH2R + A
AH
H
CH2=CHCH2R
Образование -комплекса бензольного ядра с активным центром
протонного катализатора
Происходит поляризация -связи, что облегчает ее гетеролитический ра
19.
Изомеризация алкилбензоловПеремещение алкильных заместителей по кольц
Карбений-ионная теория
CH3
CH3
CH3
H
H
CH3
C
H
CH3
C
H
C
CH3
H
H
CH3
+H
CH
CH3
CH3
м-ксилол изомеризуется в п-ксилол
C
C
CH3
20.
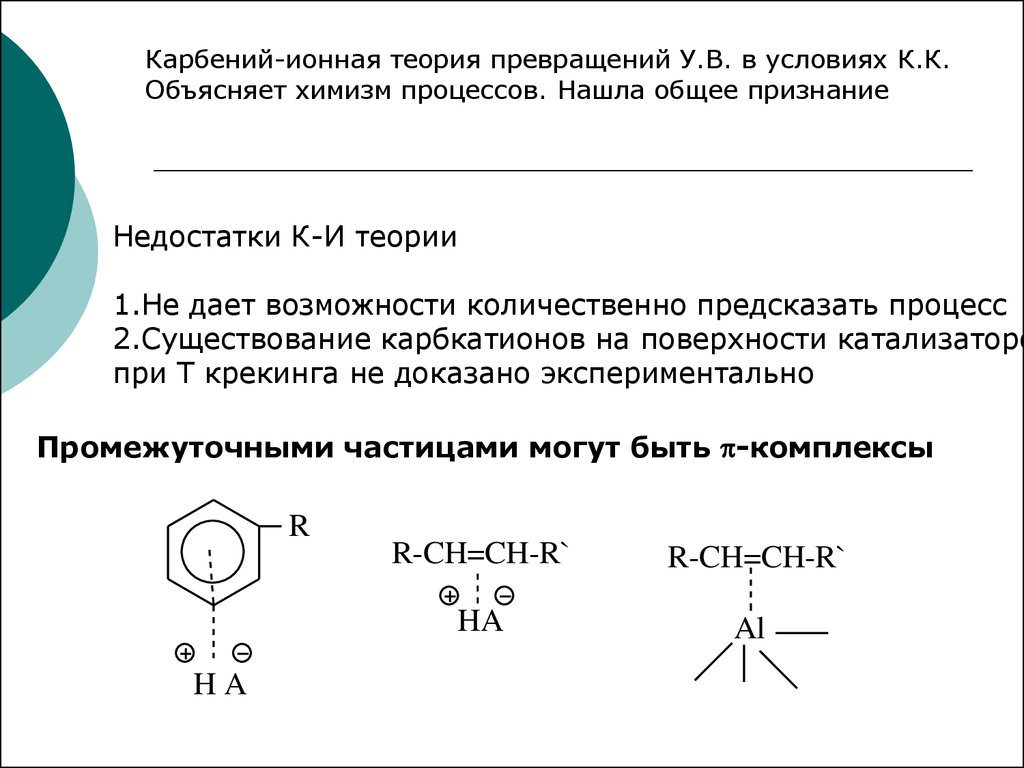
Карбений-ионная теория превращений У.В. в условиях К.К.Объясняет химизм процессов. Нашла общее признание
Недостатки К-И теории
1.Не дает возможности количественно предсказать процесс
2.Существование карбкатионов на поверхности катализаторо
при Т крекинга не доказано экспериментально
Промежуточными частицами могут быть -комплексы
R
HA
R-CH=CH-R`
R-CH=CH-R`
HA
Al
21.
Промежуточными частицами могут быть также катион-раe
+
R + Al
CH3
HC
CH3
_
Al
CH3
CH3
-e
+ CH
CH
Al
Al
CH3
CH3
Al
22.
CAl
C
+ Al
CH3CHCH3
H + CH2=CHCH3
+ HR
+R














 Химия
Химия








