Похожие презентации:
Соединения галогенов
1.
2.
1.Рассмотреть свойства иприменение важнейших соединений
галогенов.
2.Изучить качественные реакции на
галогенид –ионы.
3.Познакомиться со способами
получения галогеноводородов.
05.02.2017
4.Рассмотреть природные соединения
галогенов.
Водолазская О.А.
2
3.
К.П.С.Общая
формула -
H+1Г -1
F 18,99849
Фтор
17
Cl 35,453
Хлор
35
Вч79,904
Бром
I
53
126,904
Иод
At
HF
HCl
H+δ Г-δ
Свойства HГ
HF – жидкость;
HCl,HBr,HI - газы
Токсичные !!!
Хорошо растворимы
в воде
Соляная
HCl
кислота
HBr
HI
В 1 V H2O - 450 V HCl↑
85
[210]
Астат
05.02.2017
Водолазская О.А.
главная
3
4.
ФтороводороднаяHF
кислота –
плавиковая кислота
Хлороводородная
кислота –
соляная кислота.
Бромоводородная
кислота Иодоводородная
кислота -
05.02.2017
HCl
HBr
HI
С
И
Л
А
К
И
С
Л
О
Т
У
В
Е
Л
И
Ч
И
В
А
Е
Т
С
Я
Водолазская О.А.
???
+9
-1
F ))
28
+17
-1
Cl )))
288
+35 -1
Br ))))
2 8188
+53 -1
I )))))
2 818188
У
В
Е
Л
И
Ч
И
В
А
Е
Т
С
Я
R
и
о
н
а
У
М
Е
Н
Ь
Ш
А
Е
Т
С
Я
У
М
Е
Н
Ь
Ш
А
Е
Т
С
Я
П
Р
О
Ч
Н
О
С
Т
Ь
П
О
Л
Я
Р
Н
О
С
Т
Ь
С
В
Я
З
И
У
С
И
Л
Е
Н
И
Е
В
О
С
С
Т
А
Н
О
В
И
Т
Е
Л
Ь
Н
Ы
Х
С
В
Я
З
И
4
С
В
О
Й
С
Т
В
главная
5.
- HCLБесцветная жидкость, с резким
Свойства запахом, дымит на воздухе
HCl
1.Изменяет Мч = ?
Лакмус – красный
цвет
индикаторов Метиловый оранжевый - розовый
2.Ме(до Н2)
3.Основные
оксиды
4.Основания
Домашнее задание:
Составить уравнения реакций,
подтверждающие химические
свойства соляной кислоты
5.Соли
(более слабых
кислот)
05.02.2017
Водолазская О.А.
главная
5
6.
Вещество, при реакциисскоторым
которым HBr
HCl
HI даст
даст
осадок
1.
2.
1.Ba(NO
1.
1.AgNO
CuSO334)2 4.Ba(NO3)2
3.Ba(NO
3.CuSO34)2
2.
2.AgNO
NaOH3
2.NaOH
3.
HCL + AgNO3 → HNO3 + AgCl↓
HBr + AgNO3 → HNO3 + AgBr↓
HI + AgNO3 → HNO3 + AgI↓
HF ???
05.02.2017
CaF2↓
Водолазская О.А.
4.CuSO
4.NaOH
3.AgNO
4 3
К
А
Ч
Е
С
Т
В
Е
Н
Н
Ы
Е
Р
Е
А
К
Ц
И
И
главная
6
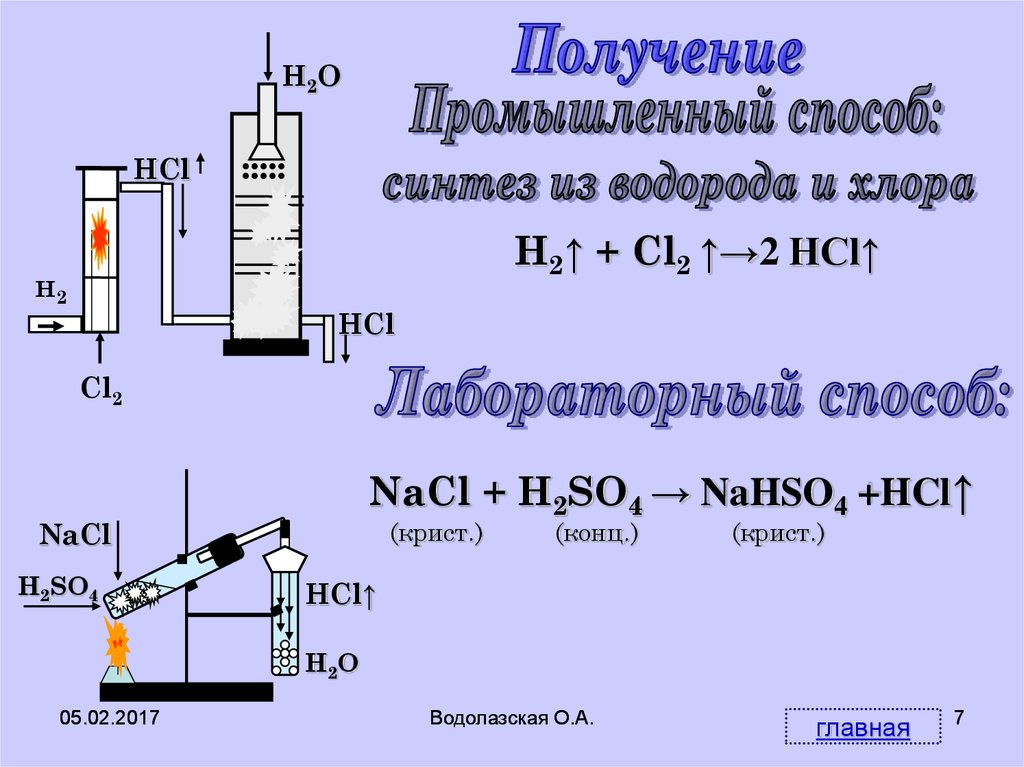
7.
H2OHCl
••••
••••
H2↑ + Cl2 ↑→2 HCl↑
н2
HCl
Cl2
NaCl + H2SO4 → NaHSO4 +HCl↑
(крист.)
NaCl
H2SO4
(конц.)
(крист.)
HCl↑
H2O
05.02.2017
Водолазская О.А.
главная
7
8.
Получениесолей
05.02.2017
HCl
Приготовление
лекарств
При паянии
Производство
красок
Очистка
поверхности
металлов в
гальваностегии
Производство
пластмасс,
синтетических
материалов
Водолазская О.А.
8
главная
9.
2.Х
Л
1.
О
И
Р
3. Ф Т О Р И Д Ы
Д
Д
И
Ы
4. Б Р О М И Д
Ы
По вертикали:
1.Соли иодоводородной
кислоты
2.Соли соляной кислоты
По горизонтали:
Дать названия:
BaBr2, CaF2
AlCl3, AgI
3.Соли фтороводородной
кислоты
4.Соли бромоводородной
кислоты
Определить
растворимость в воде.
05.02.2017
Водолазская О.А.
главная
9
10.
NaClNa
NaOH
Мыло
Фториды
Производство
зубных паст.
Получение исск.
криолита.
Бромиды
В медицине - для
лечения истерии,
бессонницы,
неврастении.
В фотоделе.
Cl2
HCl
Сода
Иодиды
Приправа к пище
Пищевая
05.02.2017 промышленность
Водолазская О.А.
Фармацевтическая ,
химическая
промышленность.
Производство
светочувствительных
материалов
10
главная
11.
CaF2Флуорит- составная часть
апатитов и фосфоритов,
а также криолита.
NaCl
KCl
F - 0,027
Cl - 0,045
Br - 0,00016
I - 0.00003
NaCl –галит (каменная,
поваренная соль),
KCl-сильвин,
(Na, K) Cl –сильвинит.
05.02.2017
NaBr
KBr
Содержание в земной
коре(%)
Бромиды– в морской
воде, буровых водах
нефтяных скважин.
NaI
KI
ламинария
Иодиды – в морской воде,
буровых водах нефтяных
скважин.
Водолазская О.А.
главная
11
12.
Составить уравнения реакций,подтверждающие химические
свойства соляной кислоты.
§18, №1, №2
05.02.2017
Водолазская О.А.
главная
12
13.
Ваше настроение ???1
2
3
4
05.02.2017
Водолазская О.А.
главная
13












 Химия
Химия








