Похожие презентации:
Вебинар. Гидролиз солей
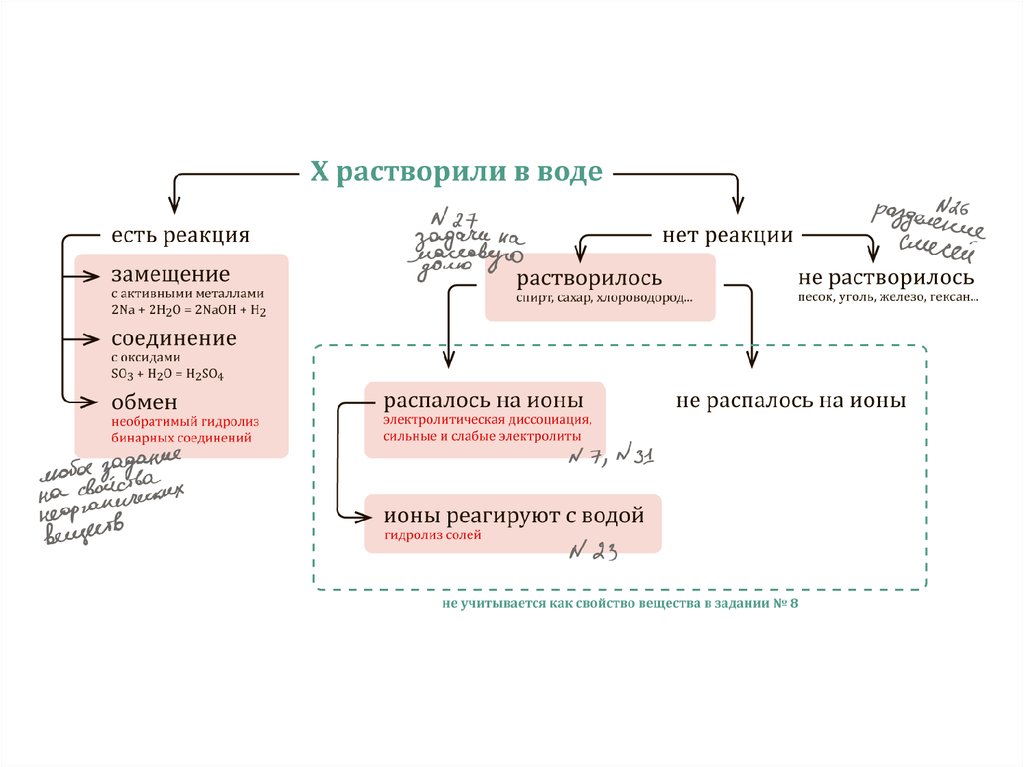
1.
2.
3.
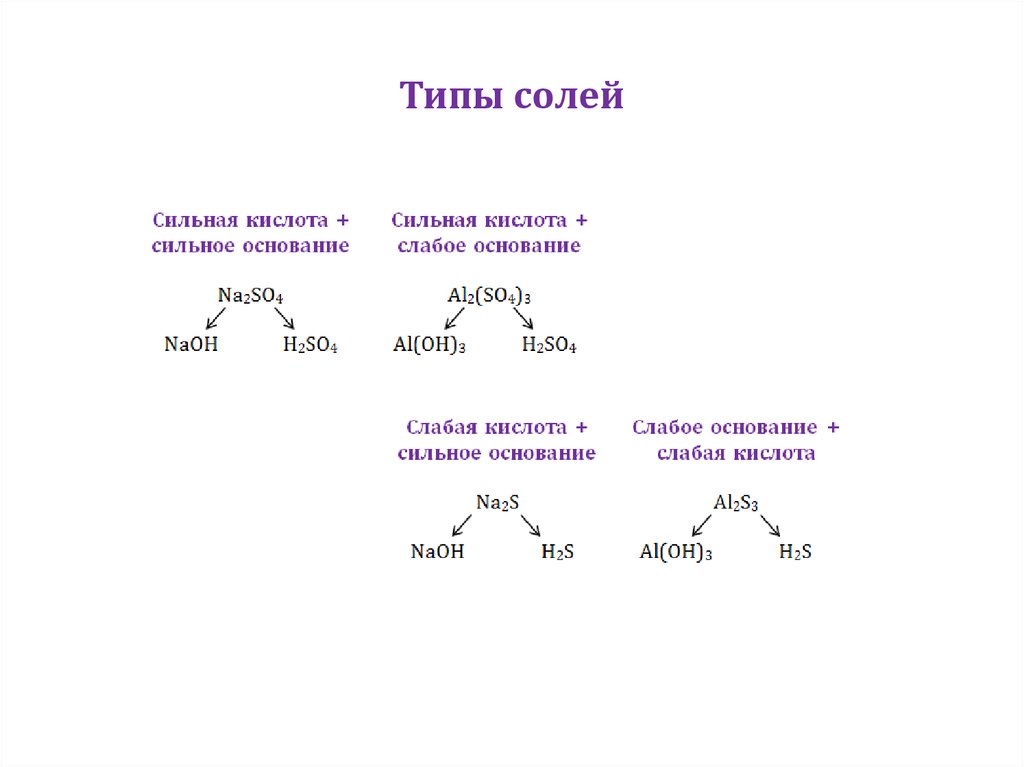
4. Типы солей
5.
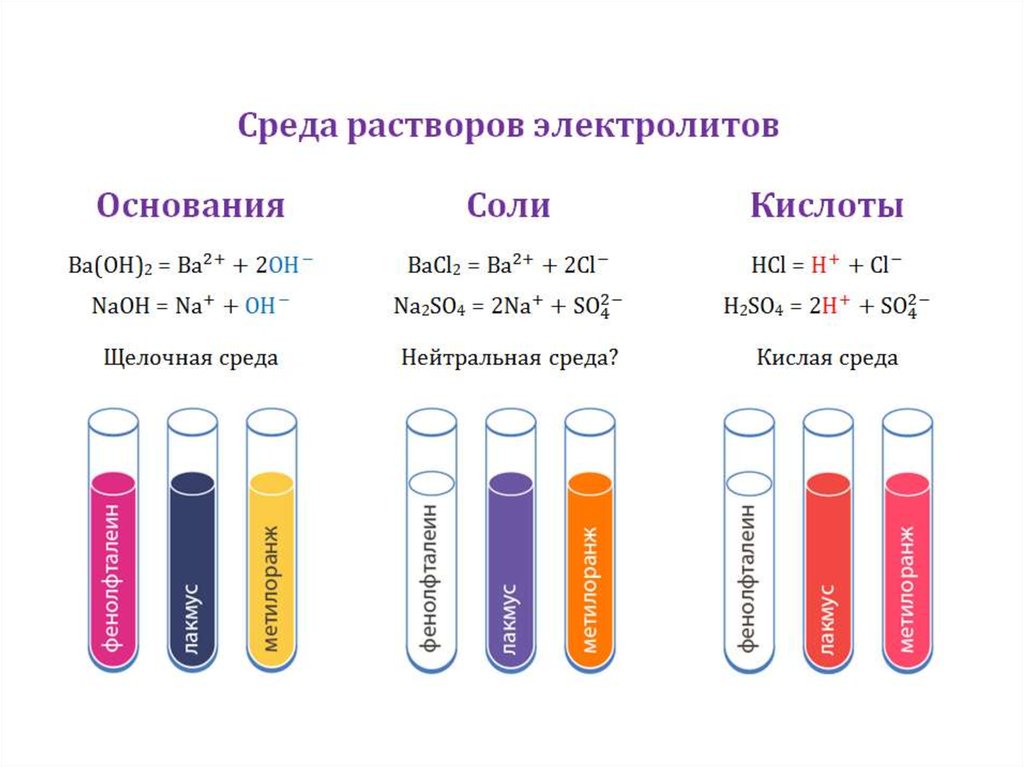
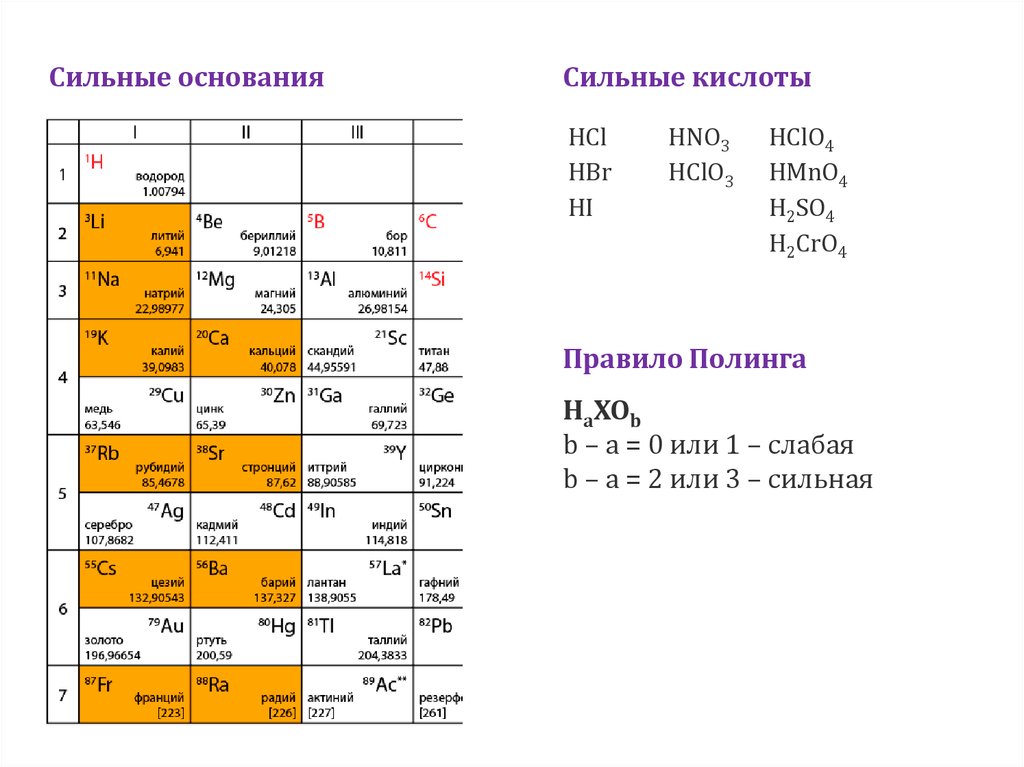
Сильные основанияСильные кислоты
HCl
HBr
HI
HNO3
HClO3
HClO4
HMnO4
H2SO4
H2CrO4
Правило Полинга
HaXOb
b – a = 0 или 1 – слабая
b – a = 2 или 3 – сильная
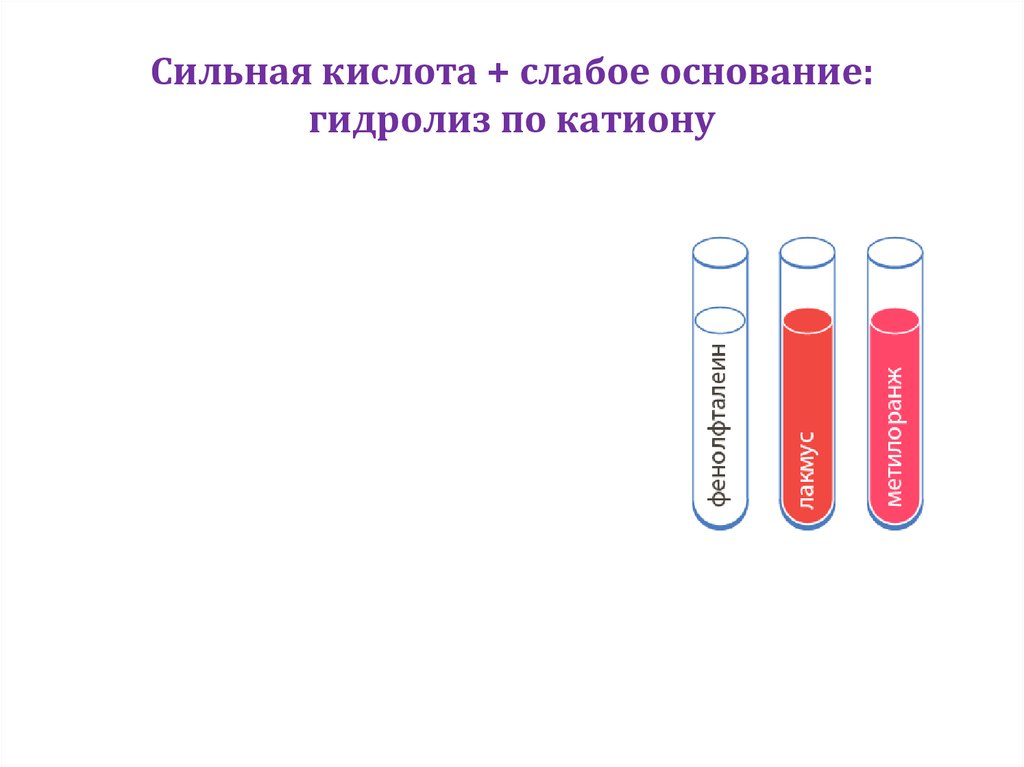
6. Сильная кислота + слабое основание: гидролиз по катиону
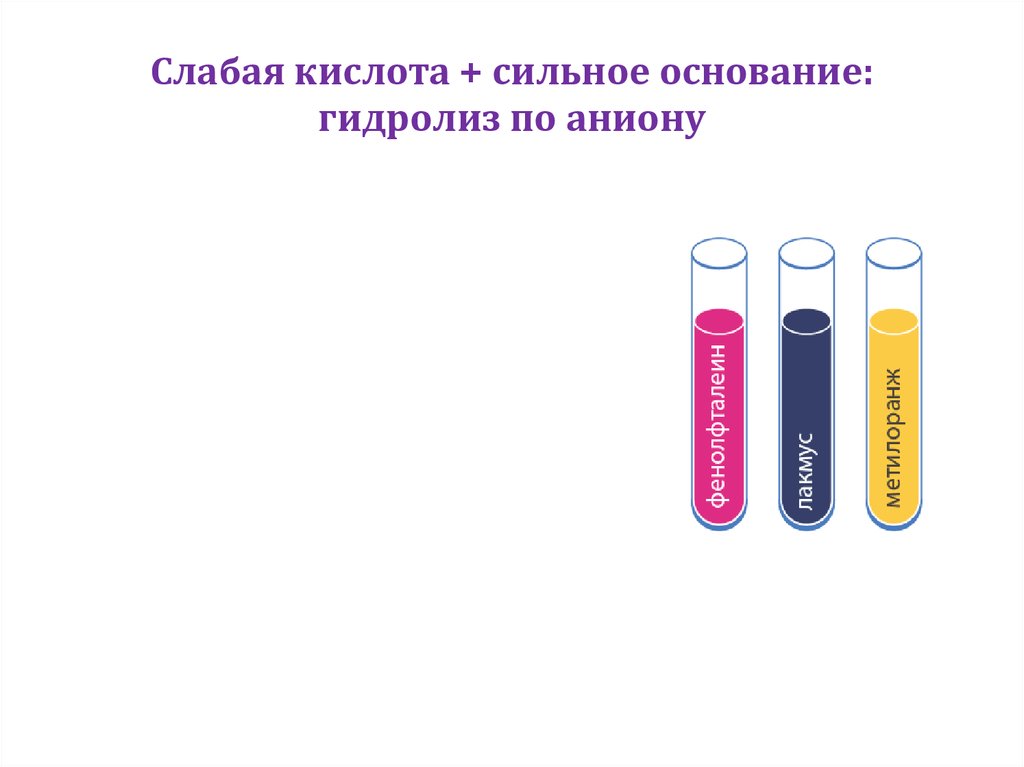
7. Слабая кислота + сильное основание: гидролиз по аниону
8.
Слабая кислота + слабое основание:гидролиз по аниону и по катиону
• Существующие соли
• Некоторые «?» и «–» соли
9. Ловушки в тестах
• «Н» соли не гидролизуются10. Ловушки в тестах
• среда растворов кислых солей активных металлов:кислая
щелочная
HSO4–, H2PO4–
HS –, HCO3–, HPO42–…
11.
12.
13.
14.
15.
16. Распознавание солей
17.
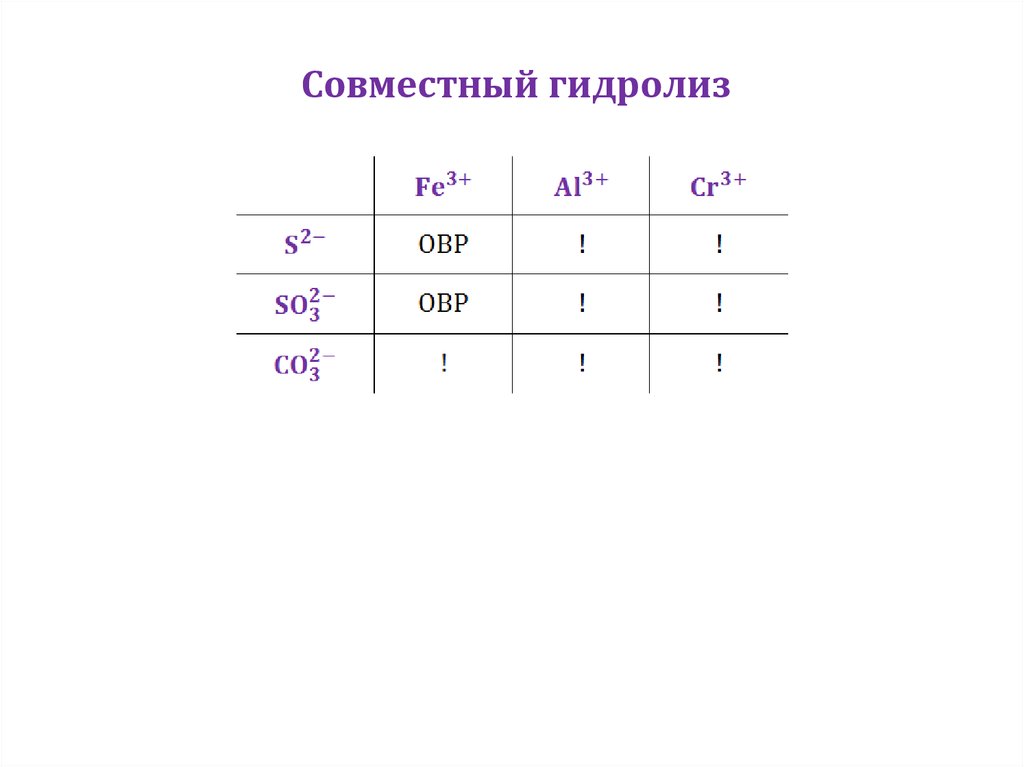
Совместный гидролиз18. Совместный гидролиз в заданиях ЕГЭ
№ 32. Оксид железа (III) растворили в соляной кислоте. Кполученному раствору добавили карбонат калия. Выпавший осадок
отделили и прокалили. Над полученным веществом пропустили
водород при нагревании.
19. Совместный гидролиз в заданиях ЕГЭ
№ 32. Натрий растворили в воде. Через полученный растворпропустили недостаток сернистого газа, а затем добавили бромид
алюминия. Выпавший осадок отделили и прокалили.














 Химия
Химия