Похожие презентации:
Азотсодержащие соединения
1. Азотсодержащие соединения
128.03.2019
2.
N1s2
2s2
2
2p3
28.03.2019
3.
Классификация азотосодержащих соединений1. Нитросоединения:
R – NO2, Ar – NO2;
2. Нитрозосоединения: R – NO, Ar – NO;
3. Аминосоединения:
R – NH2, R2NH, R3N, Ar – NH2, Ar2NH, Ar3N ;
4. Гидразины:
R – NH – NH2, Ar – NH – NH2;
5. Функциональные производные карб. кислот:
а) амиды
R – C = O,
Ar – C = O;
|
|
NH2
NH2
б) нитрилы
R – C ≡ N, Ar – C ≡ N;
6. Азо - , диазосоединения:
азосоединения;
N=N
-
N
N X
диазосоединения [Ar - N ≡ N] Х
+
‒
Х – остаток неорганической кислоты.
3
28.03.2019
4. Нитросоединения
428.03.2019
5.
I. Классификация1. В зависимости от строения углеводородного скелета
нитросоединения бывают:
1) алифатические:
а) насыщенные;
б) ненасыщенные;
2) циклические;
3) ароматические;
4) гетероциклические;
5
28.03.2019
6.
2. В зависимости от характера атома, соединенного снитрогруппой:
1) первичные нитросоединения
CH3 – CH2 – NO2
2) вторичные нитросоединения
CH3 – CH – CH3
|
NO2
3) третичные нитросоединения
6
CH3
|
CH3 – C – CH3
|
NO2
28.03.2019
7.
3. В зависимости от количества нитрогрупп в соединении:1) мононитросоединения;
2) динитросоединения;
3) полинитросоединения.
7
28.03.2019
8.
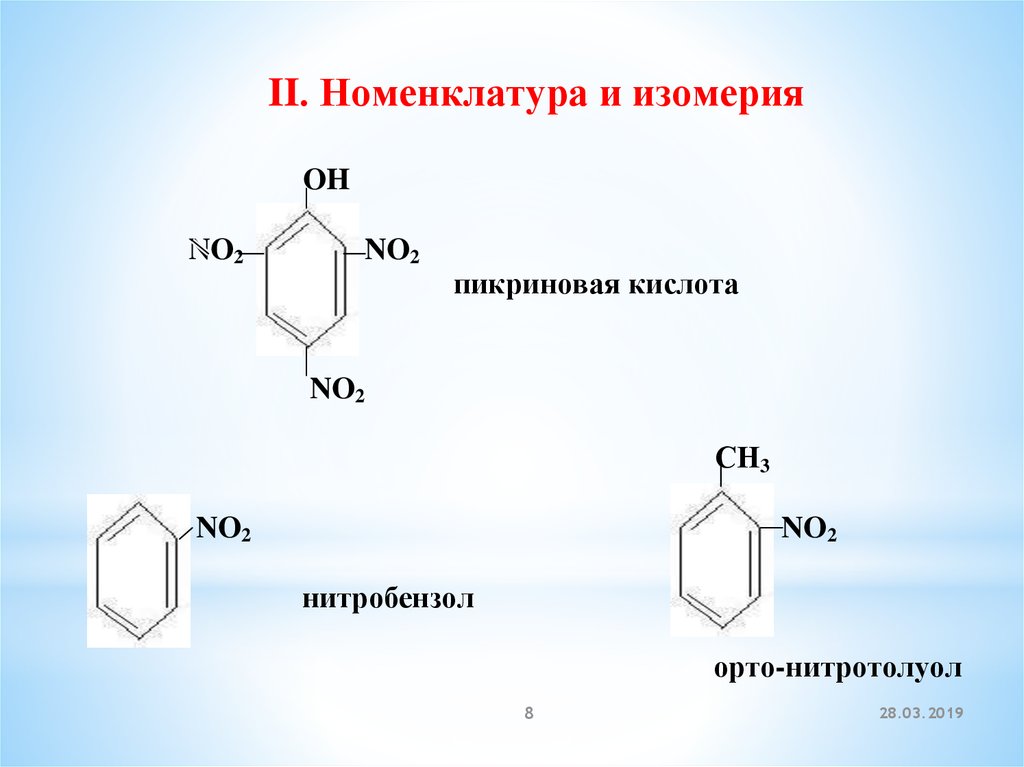
II. Номенклатура и изомерияOH
NO2
NO2
пикриновая кислота
NO2
СН3
NO2
NO2
нитробензол
орто-нитротолуол
8
28.03.2019
9.
12
3
4
CH3 – CH – CH2 – CH – CH3
|
|5
6
NO2 CH3 – CH – CH3
4
3
2
2 – нитро – 4, 5 - диметилгексан
1
CH3 – CH – CH = CH2
|
NO2
3 – нитробутен – 1
9
28.03.2019
10.
III. Способы получения1. Реакция жидкофазного нитрования (реакция Коновалова):
110-140°C
CH3 – CH2 – CH3 +
HNO3
6-12%
COOH
|
CH2 +
HNO3
|
6-12%
COOH
малоновая
кислота
CH3 – CH – CH3
|
NO2
+
H2O
COOH
|
t
CH – NO2
NO2 – CH2 – COOH
-Н2О
|
-CO2
COOH
нитромалоновая
нитроуксусная кислота
кислота
10
28.03.2019
11.
2.Парофазное нитрование:300 - 350°C
CH3–CH–CH2–CH3+HNO3
|
конц
CH3
CH3 – NO2 + CH3 – CH – CH2 – CH3
|
NO2
NO2 – CH – CH3
|
CH3
+ CH3 – CH2 – NO2
Образуется смесь нитропродуктов
11
28.03.2019
12.
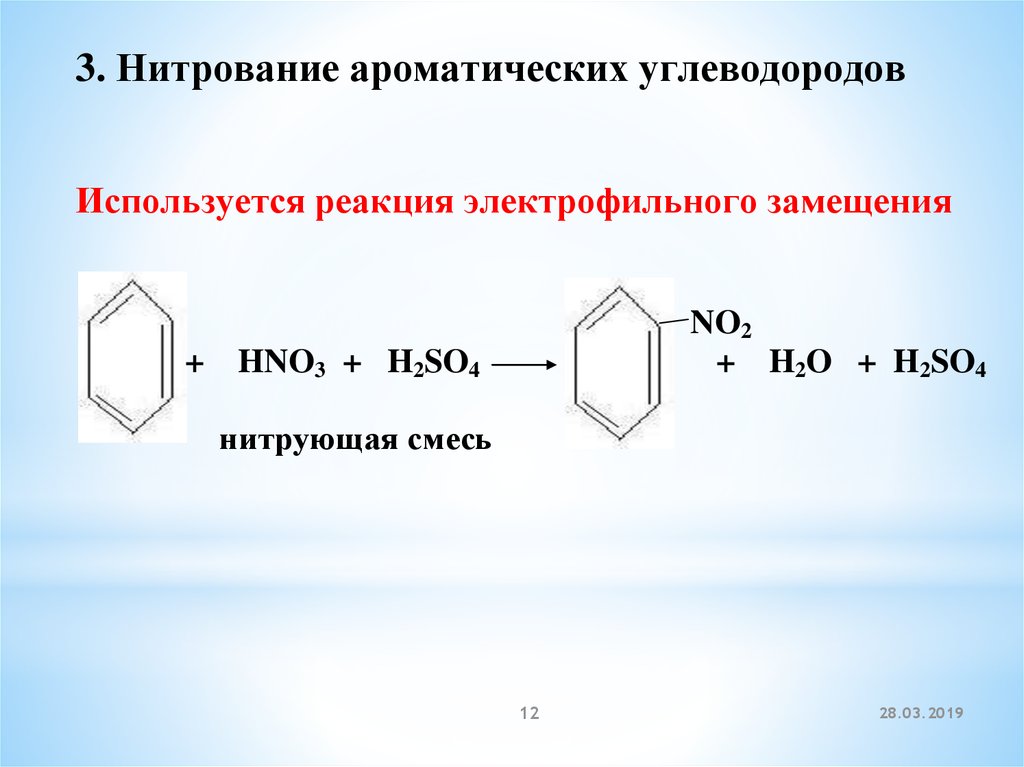
3. Нитрование ароматических углеводородовИспользуется реакция электрофильного замещения
NO2
+ H2O + H2SO4
+ HNO3 + H2SO4
нитрующая смесь
12
28.03.2019
13.
4. Нитрование олефинов оксидами азота:CH3 – CH = CH2
+
N2O4
CH3 – CH – CH2
|
|
NO2 NO2
1,2- динитропропан
13
28.03.2019
14.
IV. Строение нитросоединений и физические свойстваO
R
N+
O–
Обе связи N-O равноценны.
Связь N+-O- семиполярная.
Дипольный момент 3.5-4.0 D
O
R
N
O
O
R = Alk алифатические
= Ar ароматические
N+
R
O–
Изомеры:
R-O-N=O эфиры азотистой кислоты
алкил(арил)нитриты
14
Нитросоединения
15.
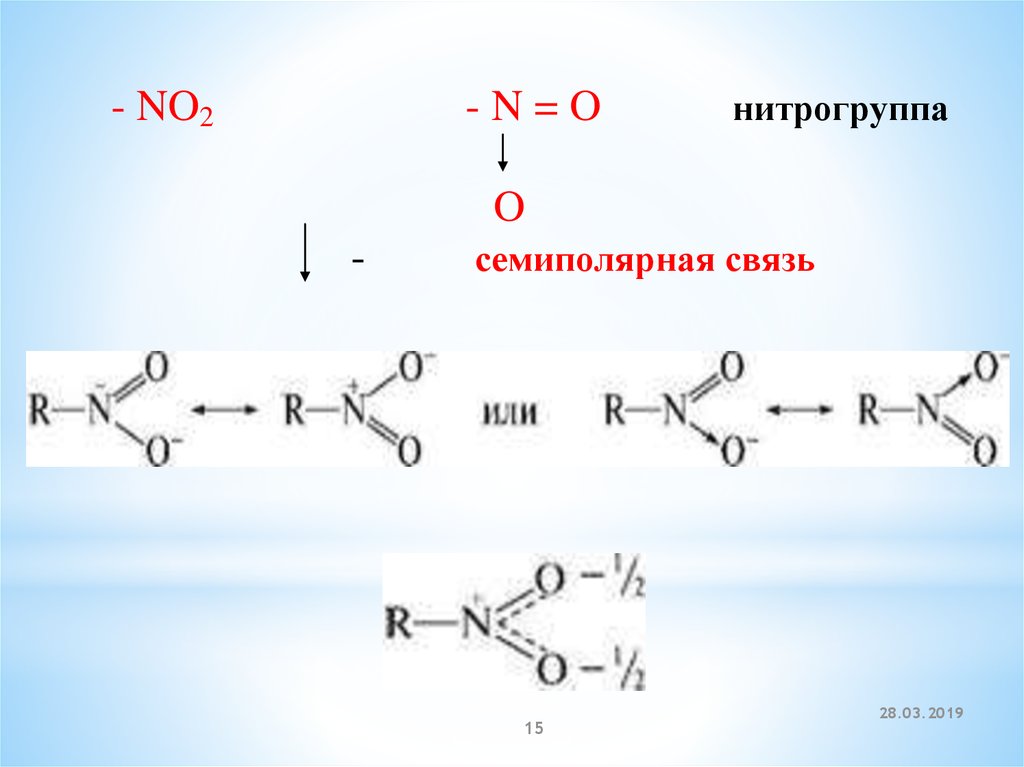
- NO2-N=O
нитрогруппа
O
-
семиполярная связь
15
28.03.2019
16.
Вещества с семиполярнымисвязями имеют довольно
большой дипольный момент,
они обычно кипят при более
высоких температурах, чем
изомерные им вещества, в
молекулах которых
семиполярная связь отсутствует
16
28.03.2019
17.
V. Химические свойства1.Восстановление алифатических нитросоединений:
СН3 – СН2 – NO2 + 6H
CH3 – CH2 – NH2 + 2H2O
аминоэтан
17
28.03.2019
18.
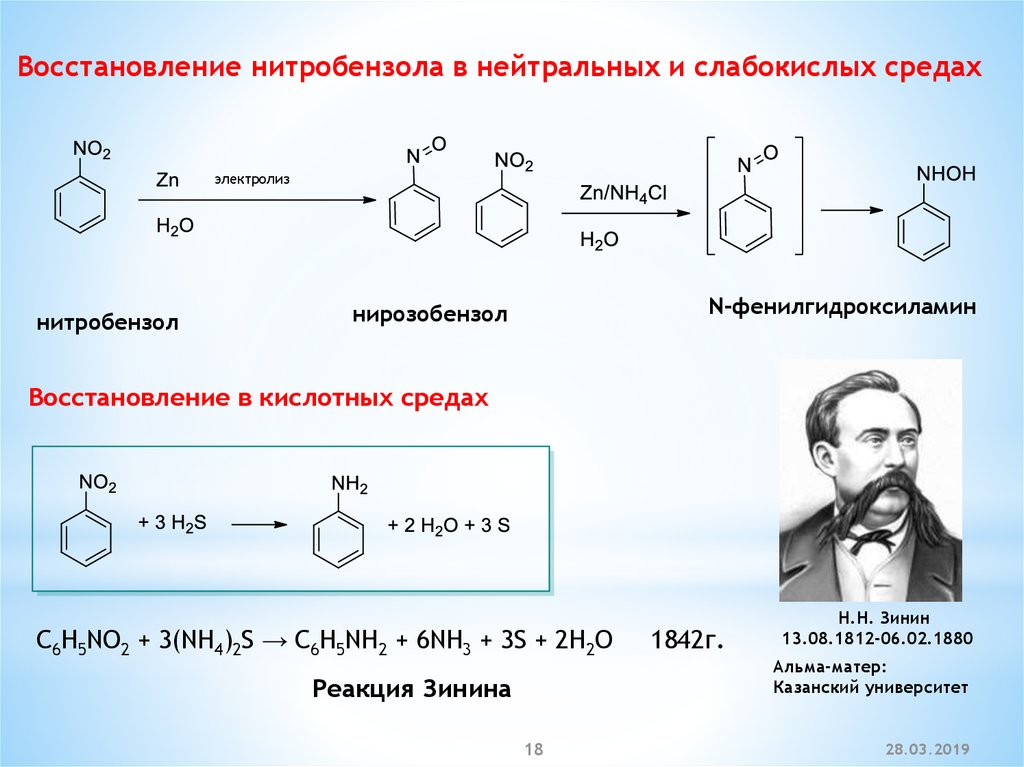
Восстановление нитробензола в нейтральных и слабокислых средахэлектролиз
нитробензол
N-фенилгидроксиламин
нирозобензол
Восстановление в кислотных средах
C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O
Реакция Зинина
18
1842г.
Н.Н. Зинин
13.08.1812-06.02.1880
Альма-матер:
Казанский университет
28.03.2019
19.
2. Реакции со щелочами:а) первичные нитросоединения
в реакцию вступает водород, находящийся при углероде в αположении относительно нитрогруппы
α
2
2CH3 – CH2 – N = O
+
1
+HCl
2CH3 – CH = N – ONa
2NaOH
-H2O
O
2CH3 – CH = N – OH
-NaCl
О
аци-нитроформа
О
натриевая соль аци-нитроформы этана
1-натрийаци-нитроэтан
2 CH3 – CH2 – NO2
нитроформа
2СН3 – С = О
|
H
альдегид
19
+
N2O
+
H2O
28.03.2019
20.
б) вторичные нитросоединенияα
+ NaOH 1
CH3 – CH – CH3
|
N=O
О
2
3
+НСl
CH3 – C – CH3
||
N – ONa
CH3 – C – CH3
||
N – OН
О
CH3 – CН – CH3
|
NО2
О
2 – натрийаци-нитропропан
20
28.03.2019
21.
в) третичные нитросоединенияCH3
|α
CH3 – C – CH3
|
N=O
+
NaOH
O
нет водорода при углероде в α-положении относительно
нитрогруппы
21
28.03.2019
22.
3. Реакция с азотистой кислотой:а) первичные нитросоединения
α
2
1
CH3 – CH2 – N = O + HONO
CH3 – CH – N=O
- H2O
|
O
NO О
1,1-нитрозонитроэтан
NaOH
CH3 – C = N – ONa
|
NO О
1 – нитрозо – 1 – натрийаци-нитроэтан
Осадок красного цвета – качественная реакция на
первичные нитросоединения
В реакцию вступает водород при углероде в α-положении
относительно нитрогруппы
22
28.03.2019
23.
б) вторичные нитросоединениякачественная реакция на вторичные нитросоединения
α
CH3 –CH – CH3 + HONO
|
N=O
O
N=O
|
CH3 – C – CH3
|
N=O
в эфире
синий цвет
O
2, 2 – нитрозонитропропан
образуются псевдонитроловые кислоты
23
28.03.2019
24.
в) третичные нитросоединенияCH3
|α
CH3 – C – CH3
|
N=O
+
HONO
O
нет водорода при углероде в α- положении
24
28.03.2019
25.
4. Взаимодействие с карбонильными соединениями:а) первичные нитросоединения
В реакцию вступает водород при углероде в α положении относительно нитрогруппы
α
CH3 – CH2 + CH3 – C = O
|
|
N=O
H
OH
4
3
2|
1
CH3 – CH – CH – CH3
|
NO2
3 – нитробутанол – 2
О
CH3 – C = CH – CH3
|
NO2
25
2 – нитробутен
–2
28.03.2019
26.
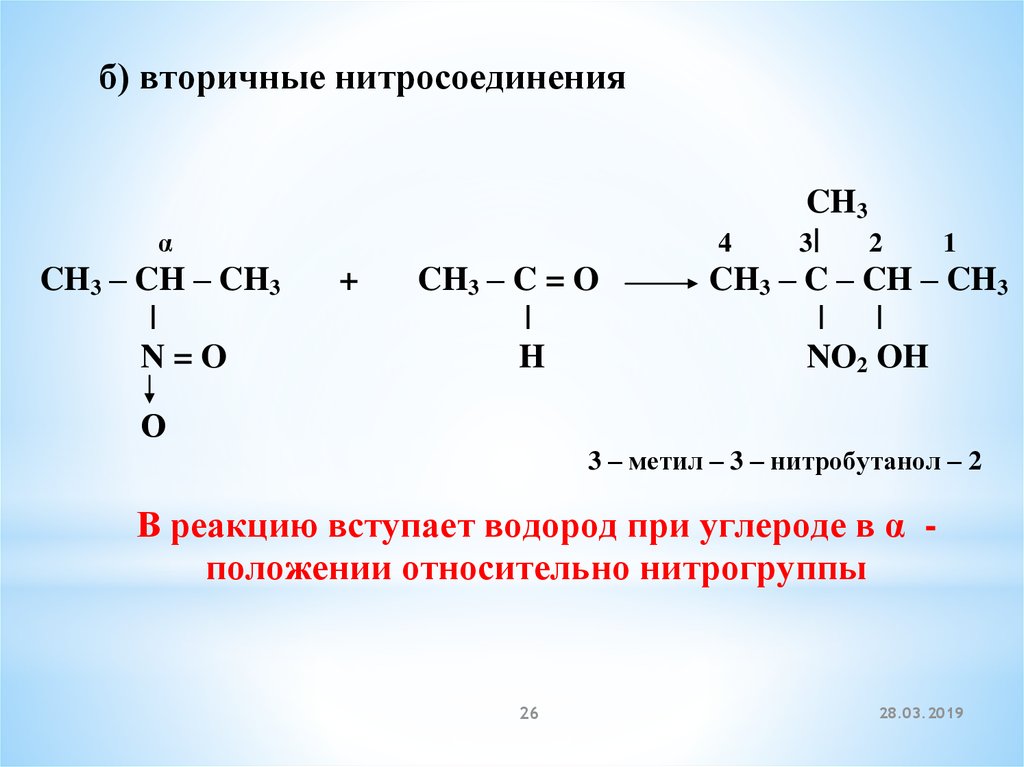
б) вторичные нитросоединенияα
CH3 – CH – CH3
|
N=O
+
CH3 – C = O
|
H
CH3
4
3|
2
1
CH3 – C – CH – CH3
| |
NO2 OH
О
3 – метил – 3 – нитробутанол – 2
В реакцию вступает водород при углероде в α положении относительно нитрогруппы
26
28.03.2019
27.
в) третичные нитросоединенияCH3
|α
CH3 – C – CH3
|
N=O
+
CH3 – C = O
|
H
O
водорода при углероде в α - положении относительно
нитрогруппы нет
27
28.03.2019
28.
5. Реакции бензольного кольца:Все реакции электрофильного замещения
1) галогенирование
Cl
AlCl3
+
Cl2
NO2
+
HCl
NO2
мета-нитрохлорбензол
2) алкилирование;
3) нитрование;
4) сульфирование;
5) ацилирование.
Нитрогруппа – заместитель 2-го рода (дезактивирующий)
Направляет следующий заместитель в мета-положение
28
28.03.2019
29.
Использование нитросоединенийНитросоединения широко применяются в
органическом синтезе для получения различных
веществ, используемых в производстве
азокрасителей, лекарственных препаратов и др.
Некоторые из нитросоединений обладают
фунгицидными свойствами и применяются в
качестве противогрибковых и противомикробных
средств.
Полинитропроизводные – тротил (тринитротолуол),
пикриновая кислота (тринитрофенол) и ее соли –
используются как взрывчатые вещества.
29
28.03.2019
30. Спасибо за Ваше внимание!
3028.03.2019

























 Химия
Химия








