Похожие презентации:
Противомикробные препараты антибиотики
1. Антибиотики
противомикробные препараты биологического происхождения, их полусинтетические производные илисинтетические
аналоги,
обладающие
высокой
физиологической активностью по отношению к определенным группам микроорганизмов или к злокачественным опухолям, избирательно задерживая их рост
или полностью подавляя развитие.
В настоящее время известно около
антибиотиков, применяется примерно 60.
40.000
1
2. История
• 1887г. – Л. Пастер наблюдал явление антагонизма бактерий и плесени.• В 1897 Эрнест Дюшен сделал «открытие», наблюдая за тем, как арабские мальчишкиконюхи применяют плесень с ещё сырых седел для обработки ран на спинах лошадей,
натертых этими же самыми седлами. Дюшен тщательно исследовал взятую плесень,
определил её как Penicillium glaucum, опробовал на морских свинках для лечения тифа и
обнаружил её разрушающее действие на бактерии E.coli. Это было первое в истории
клиническое испытание того, что вскоре станет известным всему миру пенициллином.
• 1928-29гг. - А. Флеминг открыл, что вещество, выделяемое Penicillum notatum в
культуральную жидкость, задерживает рост стафилококка.
• 1940г. – Х. Флори и Э. Чейн получили стабилизированный препарат очищенного
пенициллина.
• 14 марта 1942 г впервые в клинической практике применен пенициллин промышленного
производства (Merck & Co)
• 1942 г. – под руководством З.В. Ермольевой в СССР создается препарат Пенициллинкрустозин ВИЭМ, который был получен из штамма гриба вида Penicillium crustosum
• Термин «Антибиотик»предложен С. Ваксманом в 1942г.
• 1945г. – А.Флемминг, Х.Флори и Э.Чейн получили Нобелевскую премию за открытие
Пенициллина.
• 1945г. – расшифрована химическая структура пенициллина (Дороти Ходжкин)
2
3.
В начале 40-х, когда первый антибиотикПенициллин стал только появляться в арсенале
врачей, он был исключительно дефицитным
лекарством. Нужно было вырастить огромное
количество плесени для производства всего одной
дозы. А учитывая, что это был разгар Второй
мировой войны, необходимость в нем была
огромна. На помощь ученым пришла смекалка:
они знали, что до 95% введенного пенициллина
экскретируется мочой в неизмененном состоянии.
Таким образом, в 1943 году, когда каждый
миллиграмм ценного антибиотика был дороже
золота, стали практиковать повторное его
использование после экстракции из мочи
больного. Оказалось, что таким путем дозу
антибиотика получить быстрее, чем выращивать
культуру
http://blogs.discovermagazine.com/bodyhorrors/2014/12/31/penicillin-urine/#.VfiDmBHtlBf
3
4. как производился пенициллин в 40-х
45. Зинаида Ермольева
Первый советский пенициллин выделила ТамараБалезина, сотрудница лаборатории Зинаиды
Ермольевой:
Зинаида Ермольева
"Устав от напрасного ожидания (помощи
от союзников. — "Наука"), весной 1942 года
я с помощью друзей стала собирать плесени.
Несли самую разнообразную плесень из самых
невероятных мест. 93-м по счету образцом был
грибок, случайно выросший в другой лаборатории
на культуре микроорганизма, над которым там
работали. Этот штамм был идентифицирован
как "близкий к Penicillium crustosum". Из него мы
и стали получать советский препарат, который
назвали "пенициллин-крустозин ВИЭМ".
Сотрудники
Всесоюзного
института
экспериментальной медицины (ВИЭМ) проверили
антибиотик на себе, после чего передали его для
клинических испытаний.
Штамм
Балезиной
имел
пенициллиновую
активность в 4-8 раз больше, чем штамм Флеминга.
Зинаиде Ермольевой дали для опытов палату
раненых в 25 человек в госпитале под
Сталинградом. Все они считались обреченными,
поэтому Ермольевой разрешили пробовать на них
новое лекарство. Абсолютно все выжили, после
этого штамм Балезиной стал основой для серийного
производства
пенициллина
в
СССР.
Подробнее:http://www.kommersant.ru/doc/2717610
5
6. продуценты антибиотиков
Актиномицетыпримерно 80% АБ
Бактерии
полимиксины, бацитрацин и др.
(бациллы, псевдомонады)
Плесневые грибы
β-лактамы
6
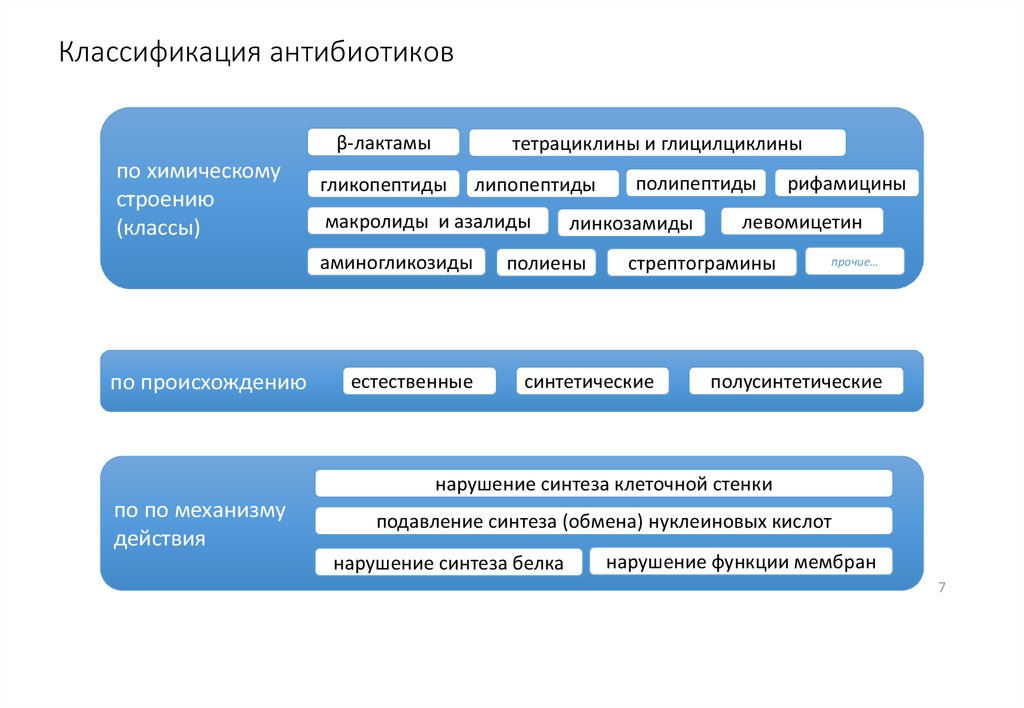
7. Классификация антибиотиков
β-лактамыпо химическому
строению
(классы)
тетрациклины и глицилциклины
гликопептиды
макролиды и азалиды
аминогликозиды
по происхождению
липопептиды
естественные
полипептиды
линкозамиды
полиены
левомицетин
стрептограмины
синтетические
рифамицины
прочие…
полусинтетические
нарушение синтеза клеточной стенки
по по механизму
действия
подавление синтеза (обмена) нуклеиновых кислот
нарушение синтеза белка
нарушение функции мембран
7
8. Классификация антибиотиков по химическому строению
β-лактамыКлассификация антибиотиков по химическому строению
Пенициллины
пенициллин, бициллин, амоксициллин
Цефалоспорины
I-IV поколений
1.
2.
3.
4.
Карбапенемы
имипенем*, меропенем* - По сравнению с другими β-лактамами карбапенемы
способны быстрее проникать через наружную мембрану грамотрицательных бактерий,
оказывают мощное бактерицидное действие, эффективны против G+ и G-
цефазолин
цефуроксим
цефотаксим*, цефтриаксон*
цефепим*
*уст. к β-лактамазам!
Гликопептиды
ванкомицин, тейкопланин. крупные молекулы, действ. только на
G+, используют при резистентности или аллергии к β-лактамам
Аминогликозиды
стрептомицин, гентамицин, тобрамицин. бактерицидные, широкого
спектра (особенно G-, на некоторых простейших). Нефро- и ототоксичны.
Тетрациклины
тетрациклин, доксициклин. бактериостатические, широкий спектр, действуют на внутриклеточные
паразиты (риккетсии, хламидии, микоплазмы, бруцеллы). Препарат выбора при лечении чумы.
Макролиды
эритромицин, азитромицин, кларитромицин. бактериостатические и бактерицидные,
макроциклические молекулы, широкий спектр (внутрикл. паразиты, напр. Helicobacter pylori)
Линкозамиды
линкомицин, клиндамицин. бактериостатические, спектр как у макролидов, особенно активны против
анаэробных бактерий. Применяются в гнойной хирургии (напр. при остеомиелитах)
Хлорамфеникол
Левомицетин. бактериостатические, токсичные,
широкий спектр (в т.ч. на внутриклеточные паразиты).
Полипептиды
полимиксины. узкий спектр (G-)
очень токсичны
Рифамицины
Полиены
нистатин. противогрибковая
активность. токсичны
рифампицин. используется в основном
для лечения TBC
8
9. Способы получения антибиотиков
биологический синтездля получения природных антибиотиков
биосинтез с последующими химическими модификациями
Сначала путем биосинтеза получают природный антибиотик, а затем его молекулу
изменяют путем химических модификаций, например присоединяют определенные
радикалы, в результате чего улучшаются антимикробные и фармакологические свойства
препарата
химический синтез
антибиотик синтезируется на 100% химическим путем
9
10. β-лактамы
пенициллины, цефалоспорины, монобактамы, карбапенемыБета-лактамы (β-лактамы, азетидин-2-оны) — лактамы, содержащие
гетероциклическое кольцо из трёх атомов углерода и одного атома азота
• Мишень для β-лактамных антибиотиков в микробной клетке - Пенициллинсвязывающие белки (ПСБ), ферменты, участвующие в синтезе основного
компонента наружной мембраны микроорганизмов – пептидогликана.
• β-Лактамы свободно проникают через капсулу и пептидогликан внутрь клетки
G(+) микроорганизмов.
• β-Лактамы не проходят через наружную мембрану G(–) бактерий, и
проникновение в клетку осуществляется через пориновые каналы внешней
мембраны.
• β-лактамы не действуют на микоплазмы, внутриклеточные микроорганизмы,
метициллин-резистентные стафилококки и на анаэробы (большинство βлактамов)
10
11. Резистентность к β-лактамам
Доступ β-лактамных антибиотиков к ПСБ ограничивают ферменты - β-лактамазы,инактивирующие антибиотики.
Созданы специальные вещества, предохраняющие β-лактамные антибиотики от
разрушающего действия β-лактамаз.
Лекарственные формы, в которых соединены антибиотики и ингибиторы β-лактамаз,
получили название "ингибиторозащищенные β-лактамы» (Амоксиклав)
Кроме природной чувствительности (или резистентности), клиническую
эффективность β-лактамов определяет приобретенная устойчивость, механизмами
которой могут быть:
• снижение аффинности ПСБ к β-лактамам;
• снижение проницаемости внешних структур микроорганизма для β-лактамов;
• появление новых β-лактамаз или изменение экспрессии имеющихся.
11
12. β-лактамы: противопоказания и предостережения
Аллергические реакции – наиболее частый и опасный побочный эффектПри указании в анамнезе на тяжелые реакции гиперчувствительности к пенициллину
(анафилактический шок, ангионевротический отек, бронхоспазм) применение других b-лактамов
не допускается; при умеренных реакциях (крапивница, дерматит) возможно осторожное
назначение цефалоспоринов и карбапенемов под прикрытием блокаторов Н1-гистаминовых
рецепторов
Транзиторное повышение уровня трансаминаз и щелочной фосфатазы.
Эти реакции проходят самостоятельно и не требуют отмены лекарственного средства (ЛС)
Тошнота, рвота и диарея могут наблюдаться при применении всех b-лактамов
Геморрагический синдром при приеме цефалоспоринов I поколения возникает
вследствие нарушения всасывания витамина К в кишечнике
Карбенициллин и тикарциллин следует назначать с осторожностью перед операциями из-за
возможности развития геморрагического синдрома, связанного с нарушением функции
мембран тромбоцитов
Цефалоспорины I поколения могут вызывать нарушение толерантности к алкоголю
12
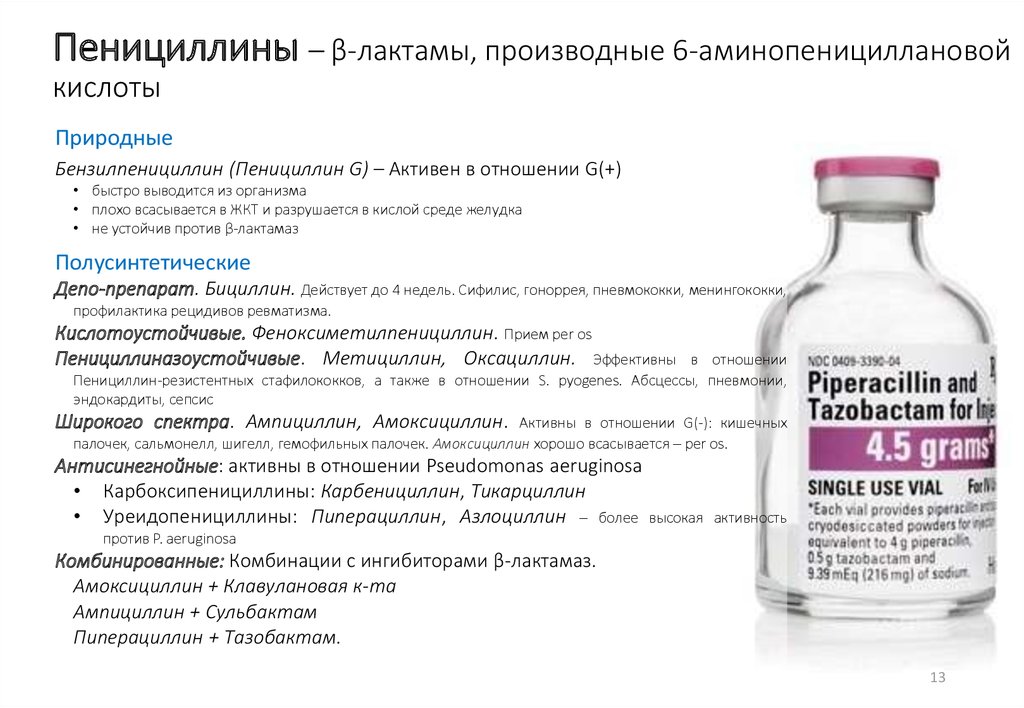
13. Пенициллины – β-лактамы, производные 6-аминопенициллановой кислоты
ПриродныеБензилпенициллин (Пенициллин G) – Активен в отношении G(+)
• быстро выводится из организма
• плохо всасывается в ЖКТ и разрушается в кислой среде желудка
• не устойчив против β-лактамаз
Полусинтетические
Депо-препарат. Бициллин. Действует до 4 недель. Сифилис, гоноррея, пневмококки, менингококки,
профилактика рецидивов ревматизма.
Кислотоустойчивые. Феноксиметилпенициллин. Прием per os
Пенициллиназоустойчивые. Метициллин, Оксациллин. Эффективны
в отношении
Пенициллин-резистентных стафилококков, а также в отношении S. pyogenes. Абсцессы, пневмонии,
эндокардиты, сепсис
Широкого спектра. Ампициллин, Амоксициллин.
Активны в отношении G(-): кишечных
палочек, сальмонелл, шигелл, гемофильных палочек. Амоксициллин хорошо всасывается – per os.
Антисинегнойные: активны в отношении Pseudomonas aeruginosa
• Карбоксипенициллины: Карбенициллин, Тикарциллин
• Уреидопенициллины: Пиперациллин, Азлоциллин – более высокая
активность
против P. aeruginosa
Комбинированные: Комбинации с ингибиторами β-лактамаз.
Амоксициллин + Клавулановая к-та
Ампициллин + Сульбактам
Пиперациллин + Тазобактам.
13
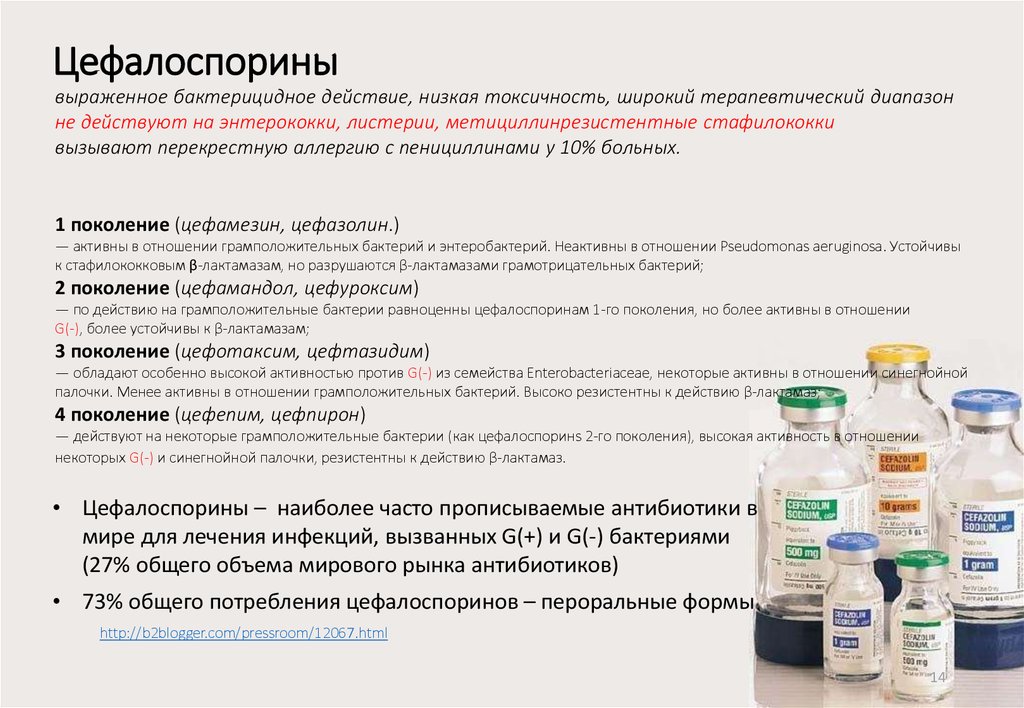
14. Цефалоспорины
выраженное бактерицидное действие, низкая токсичность, широкий терапевтический диапазонне действуют на энтерококки, листерии, метициллинрезистентные стафилококки
вызывают перекрестную аллергию с пенициллинами у 10% больных.
1 поколение (цефамезин, цефазолин.)
— активны в отношении грамположительных бактерий и энтеробактерий. Неактивны в отношении Pseudomonas aeruginosa. Устойчивы
к стафилококковым β-лактамазам, но разрушаются β-лактамазами грамотрицательных бактерий;
2 поколение (цефамандол, цефуроксим)
— по действию на грамположительные бактерии равноценны цефалоспоринам 1-го поколения, но более активны в отношении
G(-), более устойчивы к β-лактамазам;
3 поколение (цефотаксим, цефтазидим)
— обладают особенно высокой активностью против G(-) из семейства Enterobacteriaceae, некоторые активны в отношении синегнойной
палочки. Менее активны в отношении грамположительных бактерий. Высоко резистентны к действию β-лактамаз;
4 поколение (цефепим, цефпирон)
— действуют на некоторые грамположительные бактерии (как цефалоспоринs 2-го поколения), высокая активность в отношении
некоторых G(-) и синегнойной палочки, резистентны к действию β-лактамаз.
• Цефалоспорины – наиболее часто прописываемые антибиотики в
мире для лечения инфекций, вызванных G(+) и G(-) бактериями
(27% общего объема мирового рынка антибиотиков)
• 73% общего потребления цефалоспоринов – пероральные формы
http://b2blogger.com/pressroom/12067.html
14
15. Монобактамы — моноциклические β-лактамы
азтреонам• узкая специфичность:
активность против G(-), включая P. aeruginosa и колиформных бактерий
• выраженное бактерицидное действие
• устойчив к β-лактамазам G(-) бактерий, но в то же время
разрушается β-лактамазами G(+)
• только парентеральное введение
• препарат резерва при инфекциях, вызванных аэробными G(-)
бактериями.
15
16. Карбапенемы — антибиотики ультраширокого спектра действия
Имипенем, Меропенем• из всех β-лактамов имеют самый широкий спектр действия за
исключением метициллинрезистентных штаммов S.aureus и E.faecium
• устойчивы к β-лактамазам, включая β-лактамазы расширенного спектра
действия, которые инактивируют цефалоспорины всех поколений
• выраженное бактерицидное действие
• только парентеральное введение
• препарат резерва при инфекциях, вызванных полирезистентными
штаммами или при смешаных инфекциях
• самый быстрый рост потребления в последние 10 лет
16
17.
Гликопептиды — антибиотики, специфичныепротив G(+)
Ванкомицин
• Не действуют на G(-) бактерии
гликопептиды — очень крупные молекулы, не могут проникнуть через поры G(-) бактерий
• Высокая токсичность
ототоксичность, нефротоксичность, флебиты
• Используют при лечении тяжелых инфекций, вызванных
стафилококками, устойчивыми к другим антибиотикам
(метициллинрезистентные стафиллококки)
• Эффективны при лечении псевдомембранозного колита,
вызванного Clostridium difficile
• Только парентеральное введение
17
18.
Циклические Липопептиды — новый класс антибиотиковДаптомицин (Кубицин)
• высокая эффективность против G(+), в т.ч. против
полирезистентных стафилококков
• одобрен для лечения осложненных инфекций кожи и мягких
тканей и бактериемии при эндокардите
• не действуют на G(-) бактерии
очень крупные молекулы, не могут проникнуть через поры G(-) бактерий
• редкий, но опасный побочный эффект — рабдомиолиз
• уникальный механизм действия
посредством кальций-зависимого механизма необратимо связывается с клеточной мембраной грам(+) бактерий.
Формирует трансмембранный канал, приводящий к быстрой деполяризации клеточной мембраны из-за выхода калия.
В результате грубого нарушения процессов синтеза макромолекул наступает гибель бактериальной клетки. В отличие от
бета-лактамных антибиотиков, бактерицидное действие даптомицина не связано с разрушением клетки.
18
19.
Аминогликозиды — гроза аэробных G(-) бактерий с 1943 гСтрептомицин, Канамицин; Гентамицин, Тобрамицин, Нетилмицин; Амикацин
• механизм действия – угнетение 30S-субъединиц рибосом
• Стрептомицин активен против возбудителей чумы, туляремии,
бруцеллеза. Один из первых препаратов для лечения TBC.
• основное клиническое значение — лечение нозокомиальных
инфекций, вызванных аэробными G(-) возбудителями
• антибактериальный синергизм при совместном использовании с
пенициллинами и цефалоспоринами (но нельзя смешивать в
одном шприце!)
• Все аминогликозиды нефро- и ототоксичны.
19
20.
Тетрациклины — бактериостатики внутриклеточных микробовТетрациклин, Доксициклин, Тигециклин
механизм действия – угнетение 30S-субъединиц рибосом
активны против внутриклеточных возбудителей: хламидий, риккетсий,
микоплазм, а также против ряда G(+) (бациллы, клостридии,
пневмококки) и G(-) – бруцелл, легионелл, лептоспир, холерного
вибриона, йерсиний.
Доксициклин широко используется в венерологической практике.
Тетрациклин широко применяется в ветеринарии
неактивны против P.aeruginosa
используются пероральные и наружные формы
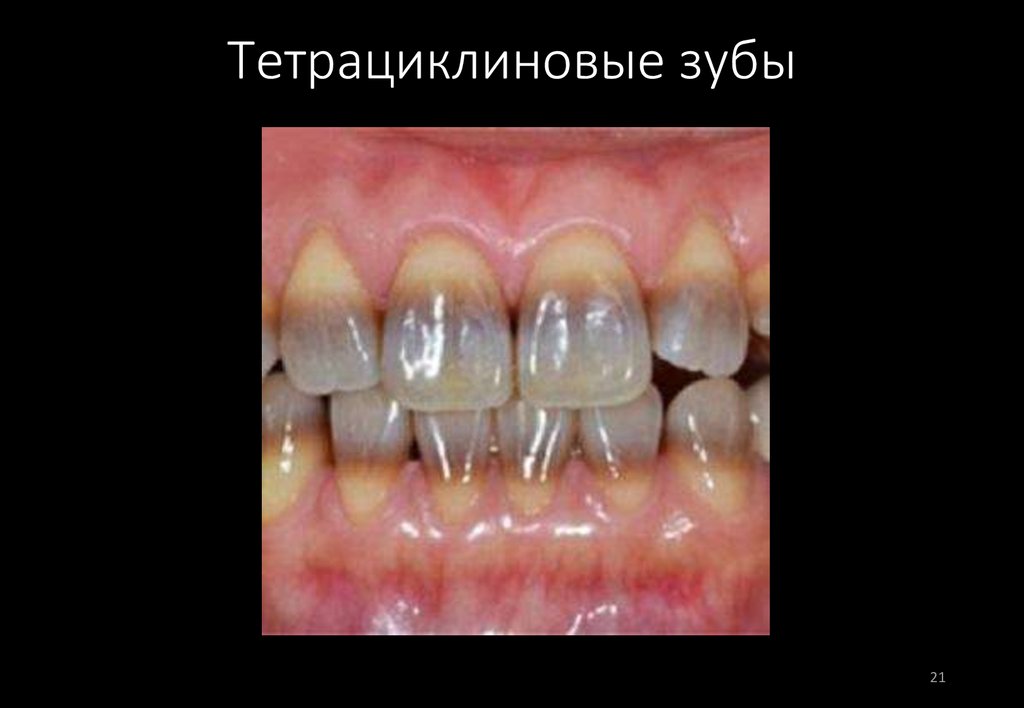
противопоказаны детям до 18 лет из-за способности накапливаться в
зубной ткани (синдром «черных зубов»)
* Methicillin-resistant Staphylococcus Aureus
** Vancomycin-Resistant Enterococci
*** Penicillin Resistant Pneumonia
20
21. Тетрациклиновые зубы
2122.
Глицилциклины — современные аналоги тетрациклиновТигециклин (Тигaцил)
высокая эффективность против широкого спектра микроорганизмов:
G(-), G(+), MRSA*, VRE**, PRP***, Acinetobacter и др.
Согласно заключению FDA от 2010 г, использование Тигацила показывает
более высокую смертность, чем при лечении другими современными
антибиотиками. Применение ограничено осложненными
абдоминальными и кожными инфекциями.
* Methicillin-resistant Staphylococcus Aureus
** Vancomycin-Resistant Enterococci
*** Penicillin Resistant Pneumonia
22
23.
Макролиды — 14-, 15- и 16-членные макроциклическиесоединения
Эритромицин, Джозамицин, Спирамицин, Кларитромицин, Азитромицин
бактериостатический, иммуномодулирующий и умеренный
противовоспалительный эффект
механизм действия – подавление синтеза белка за счет связывания с
50S-субъединицей рибосом
эффективны против гемофильной палочки, хеликобактера, кокков и
некоторых простейших (токсоплазма, криптоспоридии)
в высоких концентрациях бактерицидны для G(+) кокков,
возбудетелей дифтерии и коклюша.
микроорганизмы семейств
Enterobacteriaceae, Pseudomonas и Acinetobacter обладают природной
устойчивостью ко всем макролидам.
23
24.
Линкозамиды — узкоспецифичное оружие против анаэробовЛинкомицин - природный, Клиндамицин - полусинтетический
бактериостатическое действие, вызванное ингибированием синтеза
белка за счет связывания с 50S-субъединицей рибосом
наибольшая активность против кокков и неспорообразующих
анаэробов – клостридий, бактероидов
в основном применяются в гнойной хирургии: сепсис, остеомиелит,
абсцесс лёгкого, эмпиема плевры, раневая инфекция
серьезные побочные реакции: лейко- и тромбоцитопения, отек
квинке, псевдомембранозный колит, эксфолиативный дерматит,
эпидидимит(!) и лишай в области паха и яичек (Клиндамицин)
противопоказаны при беременности
несовместимы с ампициллином и канамицином
24
25.
Фузидины — антибиотики резерва против G(+)Фузидин, Фузидиевая кислота
продуцируется грибом F. coccineum, впервые выделен в 1960 г.
стероидоподобная структура молекулы
бактериостатическое действие, вызванное образованием комплекса
фактора элонгации (50S-субъединица рибосомы) с органическими
фосфатами клетки, нарушением функции фактора элонгации,
гидролизом гуанозинфосфатов и прекращением процесса удлинения
пептидной связи и синтеза белка.
антибиотик резерва против G(+) MRSA
резистентность бактерий к фузидиевой кислоте развивается
достаточно редко и медленно и, несмотря на длительное
использование лекарственного средства, не имеет клинического
значения.
проявляет антагонизм или несовместимость с большинством других
антибиотиков
25
26.
Стрептограмины — производные пристиномицинахинупристин/далфопристин
подавляют синтез белка, взаимодействуя с 50S-субъединицей
рибосом, препятствуя наращиванию полипептидной цепи и вызывая
преждевременную остановку синтеза белка
применяется в комбинации хинупристин/далфопристин в
соотношении 3:7
наибольшая активность против стрептококков и стафилококков,
включая метицилинрезистентные (MRSA)
пролонгированный постантибиотический эффект
рекомендовано назначать только при тяжелых инфекциях, вызванных
полирезистентными грамположительными бактериями (такими, как
устойчивые к ванкомицину штаммы Enterococcus faecium)
26
27.
Хлорамфеникол — устаревший токсичный бактериостатиклевомицетин
механизм противомикробного действия связан с нарушением синтеза
белков микроорганизмов за счёт блокирования
пептидилтрансферазной активности путём связывания с 23S рРНК 50S
субъединицы рибосомы бактерий
широкий спектр действия: G(+), G(-), внутриклеточные паразиты
применяют для лечения сыпного тифа, ку-лихорадки (Q-риккетсиоз) и
других заболеваний, вызванных риккетсиями
крайне токсичен и часто оставляет тяжёлые побочные эффекты при
применении внутрь: миелосупрессия, апластическая анемия (редко),
вымывание кальция из организма
синдром «серого ребенка»
при врожденном дефиците фермента глюкуронилтрансферазы препарат накапливается в крови в
токсических концентрациях, в результате чего возникают серый цвет кожи, увеличение печени, боли в
сердце, отеки, рвота, общая слабость
27
28.
Рифамицины — против туберкулеза, лепры, холеры и чумырифампицин
механизм – подавление ДНК-зависимой РНК-полимеразы
микроорганизмов
противотуберкулезный препарат первого ряда
окрашивает билогические жидкости - от желтого до красного цвета в
зависимости от концентрации в организме
гепатотоксичен, может вызывать лейкопению
28
29.
Полимиксины — полипептидные антибиотикиполимиксин Б
механизм: нарушение цитоплазматической мембраны
узкий спектр антибактериального действия – только G(-) бактерии
основное клиническое значение имеет активность полимиксинов в
отношении P. aeruginosa
не всасываются в ЖКТ, а также при местном применении
выраженная нефро- и нейротоксичность; возможно развитие острого
тубулярного некроза с выраженной протеинурией и гематурией.
в настоящее время используются крайне ограниченно, в виде
местного средства в офтальмологии и оториноларингологии
29
30.
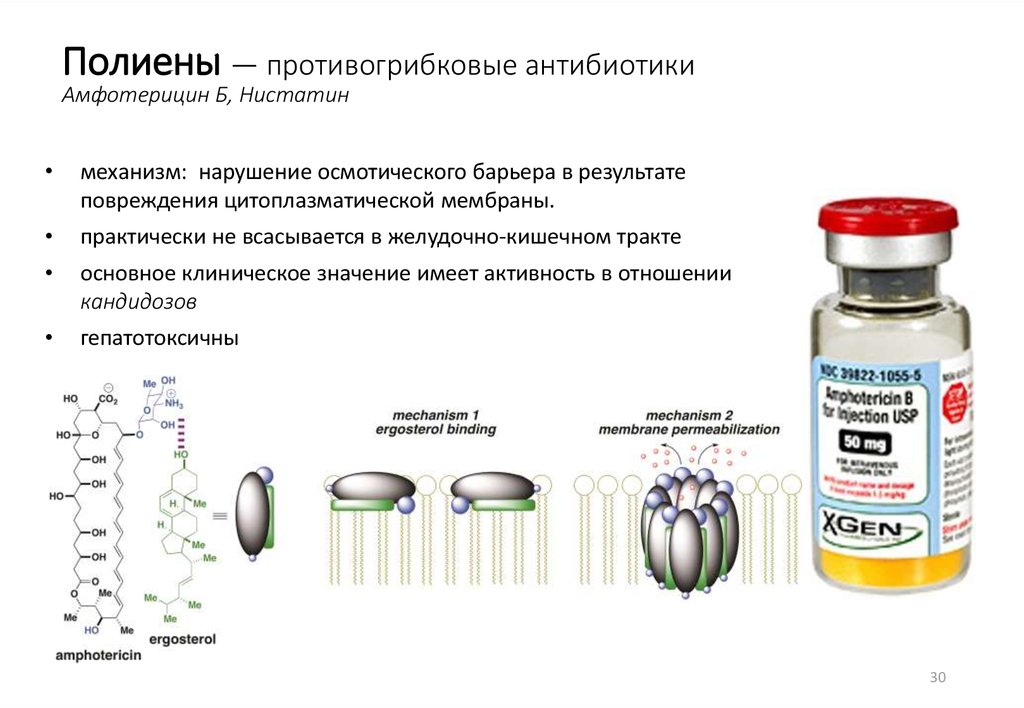
Полиены — противогрибковые антибиотикиАмфотерицин Б, Нистатин
механизм: нарушение осмотического барьера в результате
повреждения цитоплазматической мембраны.
практически не всасывается в желудочно-кишечном тракте
основное клиническое значение имеет активность в отношении
кандидозов
гепатотоксичны
30
31. Синтетические антимикробные химиотерапевтические препараты
антимикробные вещества с избирательным действием, которые не встречаются вживой природе, но похожи на антибиотики по механизму, типу и спектру действия
Сальварсан и сульфаниламид – первые химиотерапевтические средства
сульфаниламиды
хинолоны
нитроимидазолы
нитрофураны
оксазолидиноны
имидазолы
31
32.
Сульфаниламиды — производные парааминобензойной кислотыСульфодимезин, Ко-тримоксазол (Сульфометоксазол+Триметоприм)
механизм: нарушение синтеза фолиевой кислоты
бактериостатическое действие (Ко-тримоксазол – бактерицдное)
широкий спектр активности
устаревший класс, слабый клинический эффект из-за распространения
устойчивых штаммов
используется в основном для лечения инфекций мочеполового тракта,
вызванных G(-) бактериями
32
33.
Хинолоны и Фторхинолоны — ингибиторы ДНК-гиразыНалидиксовая кислота, Офлоксацин, Левофлоксацин, Моксифлоксацин
широкий спектр, бактерицидное действие
механизм: нарушение синтеза ДНК за счет ингибирования ДНКгиразы и топоизомеразы IV
хинолоны 1 поколения активны в отношении G(-) бактерий.
современные фторхинолоны проявляют активность в отношении
грамположительных бактерий (прежде всего пневмококков),
внутриклеточных патогенов, анаэробов (IV поколение)
широкое клиническое применение: респираторные, кишечные,
хирургические инфекции, менингит, туберкулез, инфекции глаз,
уроинфекции, сибирская язва и др.
3 место в мире по объему реализации среди антибактериальных
препаратов
из-за хондропатического побочного действия противопоказан детям
33
34.
Нитроимидазолы — против анаэробов и простейшихМетронидазол (Трихопол)
бактерицидное действие в отношении анэробных бактерий и
простейших (трихомонады, лямблии, дизентерийная амеба)
механизм: активируется бактериальной нитроредуктазой, расщепляет
ДНК
широко используется в челюстно-лицевой и абдоминальной хирургии
(антибактериальная терапия после операций на толстой кишке), а
также в дерматовенерологии
гепатотоксичны
34
35.
Имидазолы — противогрибковые химиопрепаратыКлотримазол
действуют на уровне эргостеролов цитоплазматической мембраны.
проявляют активность в отношении различных видов грибков
(Trichophyton, Microsporum, Epidermophyton, Candida), наибольшее
распространение получили для лечения кандидозов
применяются как наружное средство и интравагинально в виде
таблеток, порошка, свечей и кремов
несовместимы с полиеновыми антибиотиками
35
36.
Нитрофураны — уросептики широкого спектраФуразолидон, Фурагин, Нифурател, Фурацилин, Нифуроксазид (Эрсефурил)
тип действия – бактерицидный, спектр – широкий: G(+), G(-), некторые
анаэробы и грибы Candida, некоторые простейшие
являясь акцепторами кислорода, нитрофураны ингибируют МАО,
блокируют цикл Кребса, нарушают процесс клеточного дыхания
бактерий и биосинтез нуклеиновых кислот.
накапливаются в моче в высоких концентрациях
применяются для лечения уро- и кишечных инфекций, а также в
хирургии для промывания ран и полостей
лекарственная резистентность микроорганизмов не характерна
36
37.
Оксазолидиноны — новая группа синтетических АМПЛинезолид
основное значение имеет как препарат для терапии инфекций,
вызванных полирезистентными грамположительными кокками MRSA
и MRSE; Enterococcus spp., включая ванкомицинорезистентные
штаммы; S.pneumoniae.
преимущественно бактериостатическое действие за счет нарушения
синтеза белка
в отношении пневмококка, B.fragilis и C. perfringens действует
бактерицидно
37
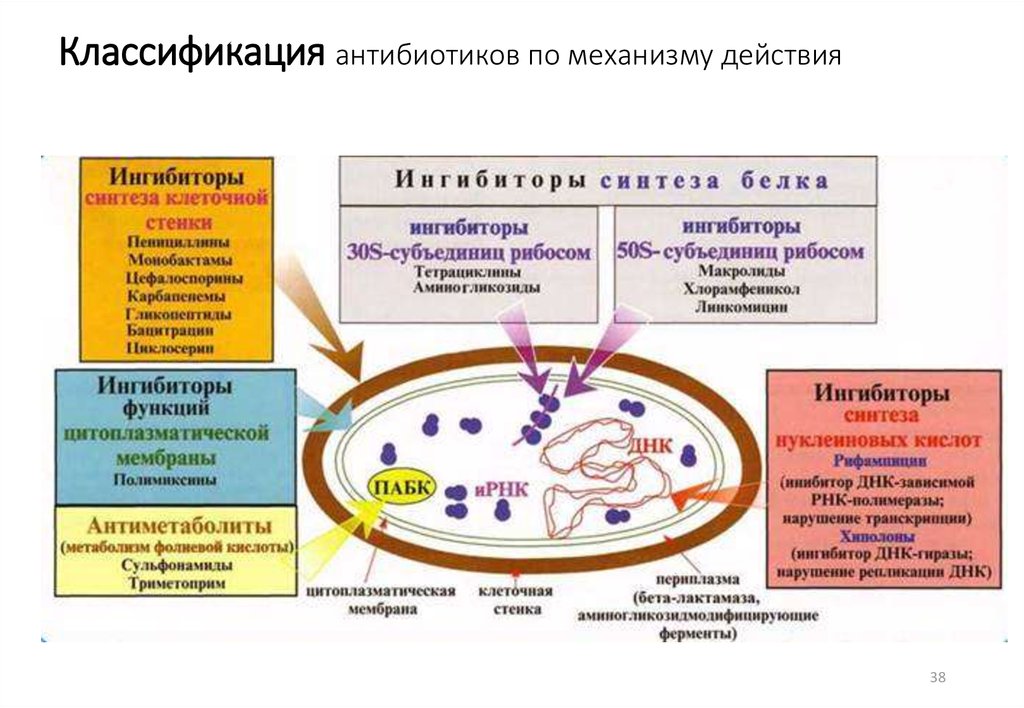
38. Классификация антибиотиков по механизму действия
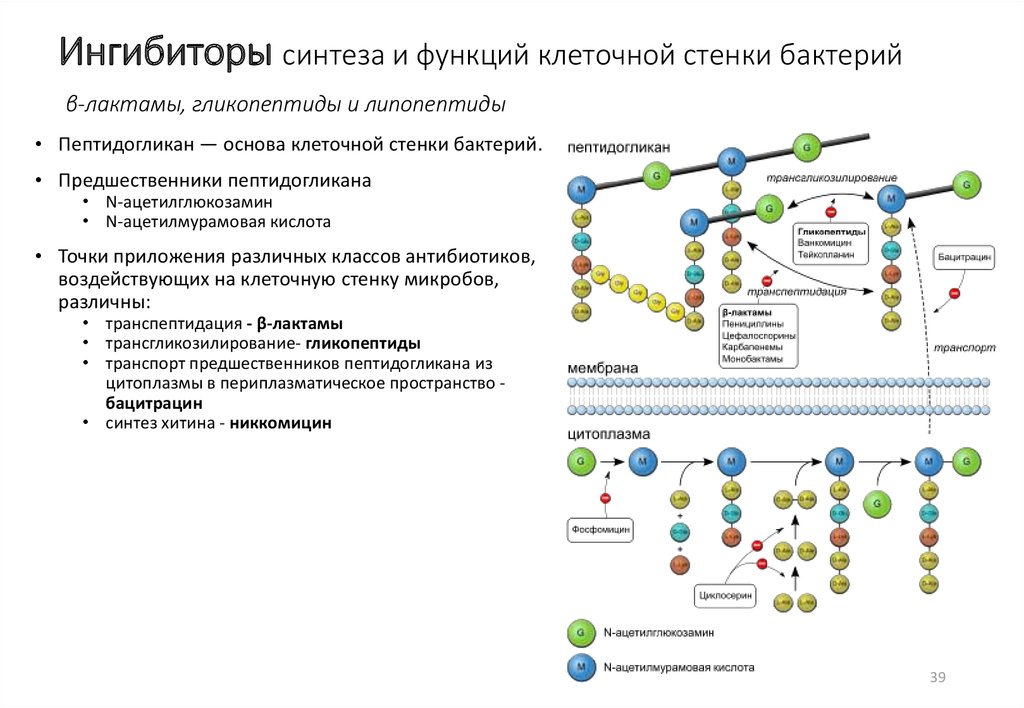
3839. Ингибиторы синтеза и функций клеточной стенки бактерий
β-лактамы, гликопептиды и липопептиды• Пептидогликан — основа клеточной стенки бактерий.
• Предшественники пептидогликана
• N-ацетилглюкозамин
• N-ацетилмурамовая кислота
• Точки приложения различных классов антибиотиков,
воздействующих на клеточную стенку микробов,
различны:
• транспептидация - β-лактамы
• трансгликозилирование- гликопептиды
• транспорт предшественников пептидогликана из
цитоплазмы в периплазматическое пространство бацитрацин
• синтез хитина - никкомицин
39
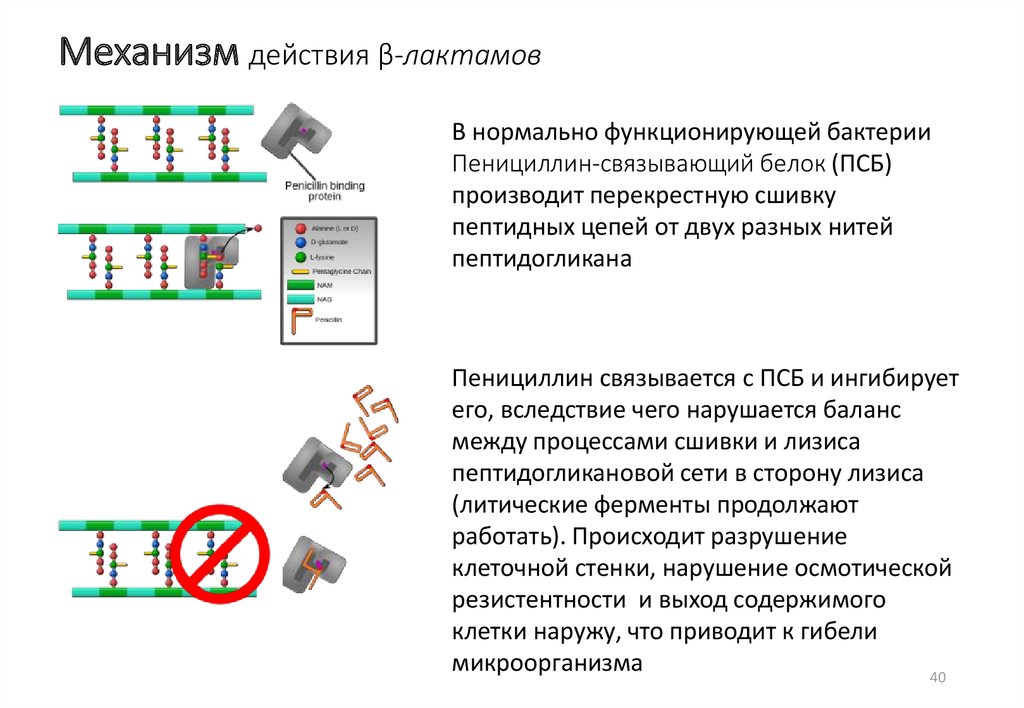
40. Механизм действия β-лактамов
В нормально функционирующей бактерииПенициллин-связывающий белок (ПСБ)
производит перекрестную сшивку
пептидных цепей от двух разных нитей
пептидогликана
Пенициллин связывается с ПСБ и ингибирует
его, вследствие чего нарушается баланс
между процессами сшивки и лизиса
пептидогликановой сети в сторону лизиса
(литические ферменты продолжают
работать). Происходит разрушение
клеточной стенки, нарушение осмотической
резистентности и выход содержимого
клетки наружу, что приводит к гибели
микроорганизма
40
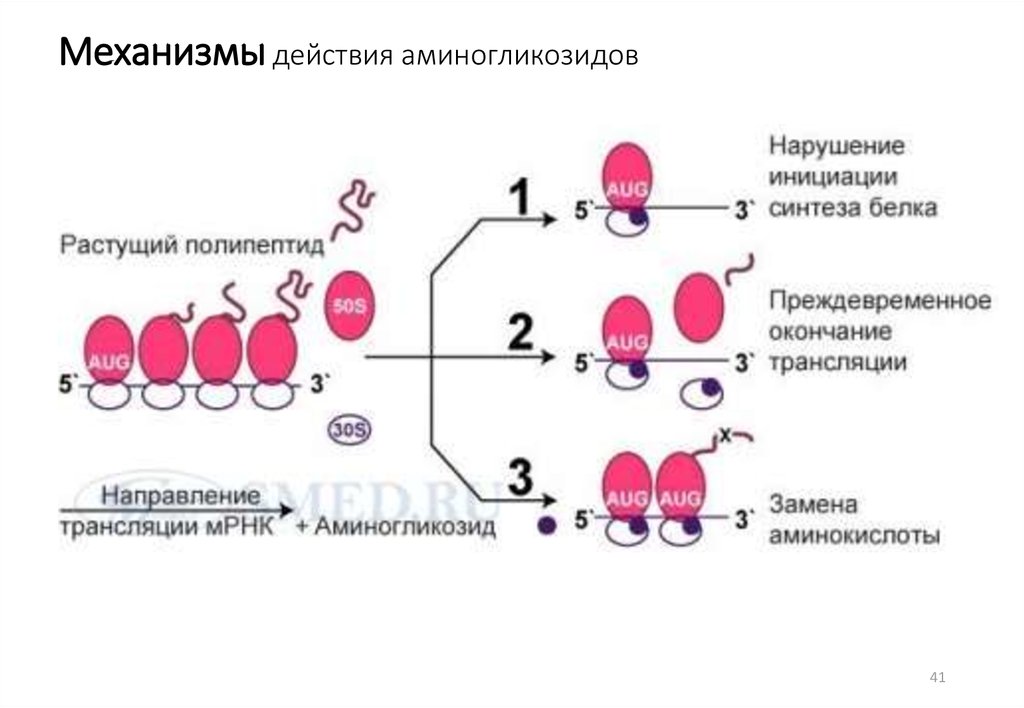
41. Механизмы действия аминогликозидов
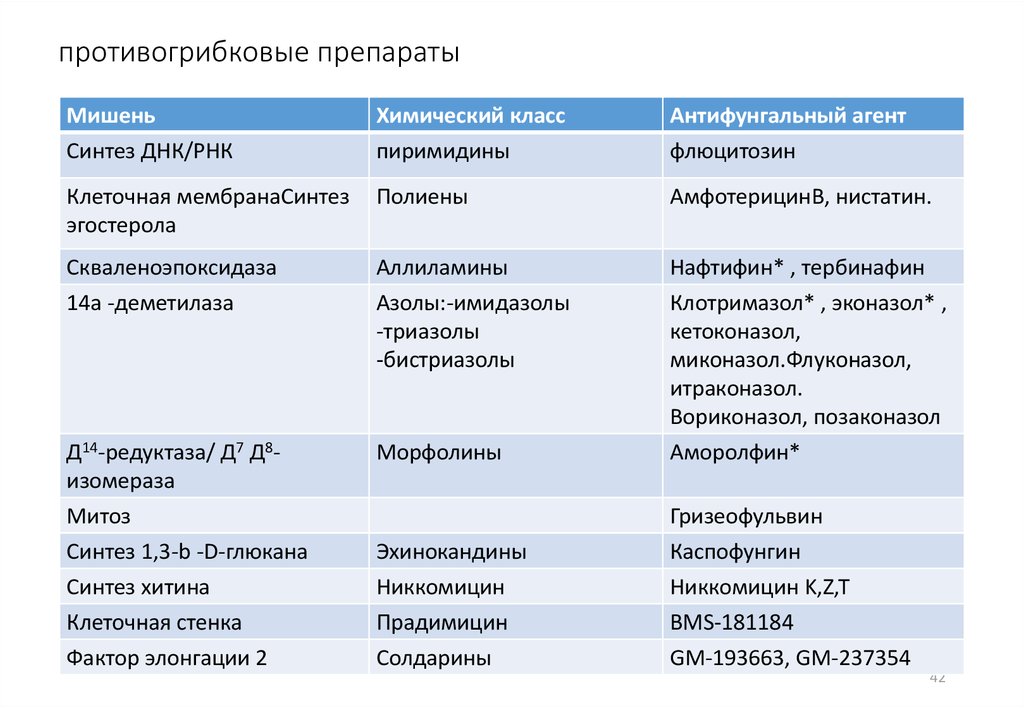
4142. противогрибковые препараты
МишеньСинтез ДНК/РНК
Химический класс
пиримидины
Антифунгальный агент
флюцитозин
Клеточная мембранаСинтез
эгостерола
Полиены
АмфотерицинВ, нистатин.
Скваленоэпоксидаза
14a -деметилаза
Аллиламины
Азолы:-имидазолы
-триазолы
-бистриазолы
Д14-редуктаза/ Д7 Д8изомераза
Митоз
Синтез 1,3-b -D-глюкана
Синтез хитина
Клеточная стенка
Фактор элонгации 2
Морфолины
Нафтифин* , тербинафин
Клотримазол* , эконазол* ,
кетоконазол,
миконазол.Флуконазол,
итраконазол.
Вориконазол, позаконазол
Аморолфин*
Эхинокандины
Никкомицин
Прадимицин
Солдарины
Гризеофульвин
Каспофунгин
Никкомицин K,Z,T
BMS-181184
GM-193663, GM-237354
42
43. противовирусные химиопрепараты
4344.
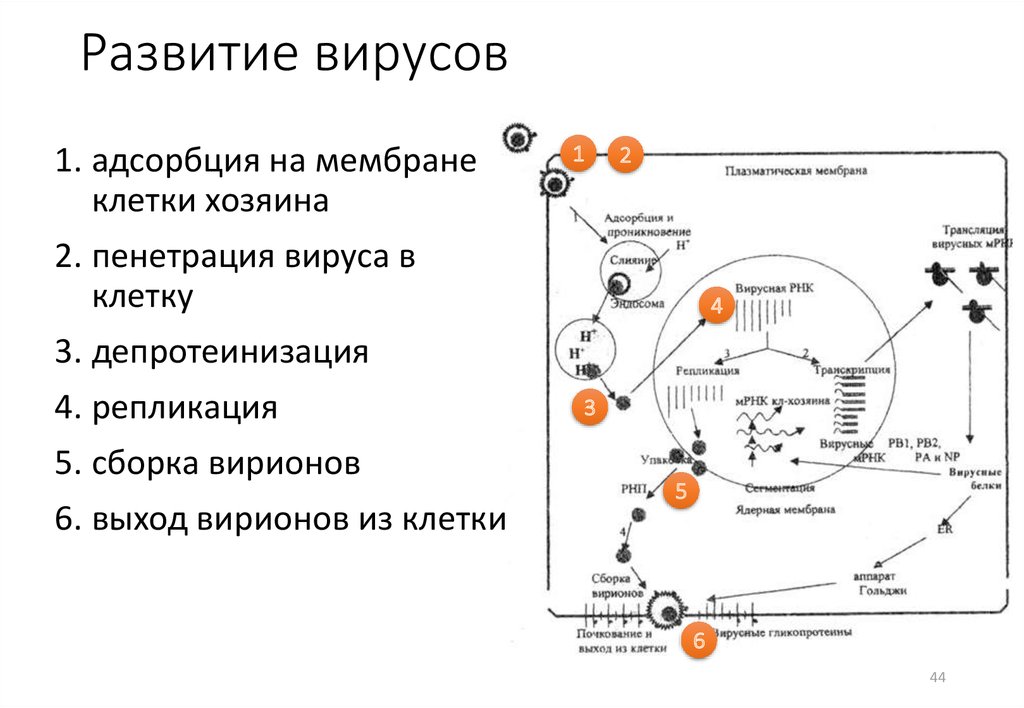
Развитие вирусов1. адсорбция на мембране
клетки хозяина
1
2
2. пенетрация вируса в
клетку
4
3. депротеинизация
4. репликация
5. сборка вирионов
6. выход вирионов из клетки
3
5
6
44
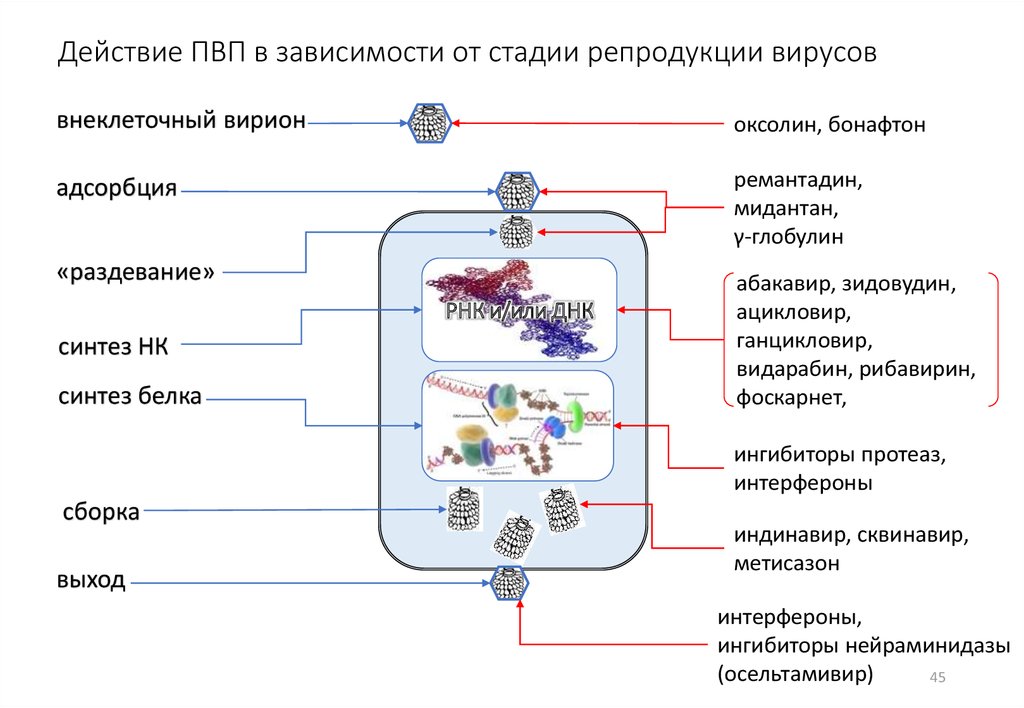
45. Действие ПВП в зависимости от стадии репродукции вирусов
внеклеточный вирионоксолин, бонафтон
адсорбция
ремантадин,
мидантан,
γ-глобулин
«раздевание»
РНК и/или ДНК
синтез НК
синтез белка
абакавир, зидовудин,
ацикловир,
ганцикловир,
видарабин, рибавирин,
фоскарнет,
ингибиторы протеаз,
интерфероны
сборка
выход
индинавир, сквинавир,
метисазон
интерфероны,
ингибиторы нейраминидазы
(осельтамивир)
45
46. препараты, нарушающие проникновение вируса в клетку и его депротеинизацию
— производные амантадина: Ремантадин— блокируют транспорт протонов через липидную мембрану вириона,
что нарушает процесс депротеинизации вирусной РНК
— Арбидол – лекарственное средство с недоказанной эффективностью
— подавляет слияние липидной оболочки вируса с мембранами эндосом,
происходящее внутри клеток
— обладает интерферониндуцирующими свойствами, стимулирует
гуморальные и клеточные реакции иммунитета
46
47. ингибиторы репликации вирусных нуклеиновых кислот
— аналоги нуклеозидов— ингибиторы вирусной ДНК-полимеразы: АЦИКЛОВИР, ГАНЦИКЛОВИР,
РИБАВИРИН, ВИДАРАБИН
— ингибиторы обратной транскриптазы ВИЧ: ЗИДОВУДИН, ЛАМИВУДИН,
АБАКАВИР
— аналоги пирофосфата: ФОСКАРНЕТ
47
48. препараты, ингибирующие стадии сборки вириона
— ингибиторы протеаз: ингибируют расщепление предшественниковструктурныхвирусных белков на функционально-активные
фрагменты
— Индинавир, Ритонавир, Саквинавир – против ВИЧ
— Метисазон – против натуральной оспы
48
49. препараты, нарушающие выход вирионов из клетки
— ингибиторы нейраминидаз вирусов гриппа А и Б:синтетические пептиды Осельтамивир, Занамивир
*данные исследований последних лет показали низкую
эффективность ингибиторов нейраминидазы при лечении гриппа
49
50. Ингибиторы внеклеточных форм вируса
— Оксолиниспользуется в виде мази для профилактики и лечения
гриппа и других вирусных ринитов
50
51. механизмы резистентности микроорганизмов к антимикробным химиопрепаратам
5152.
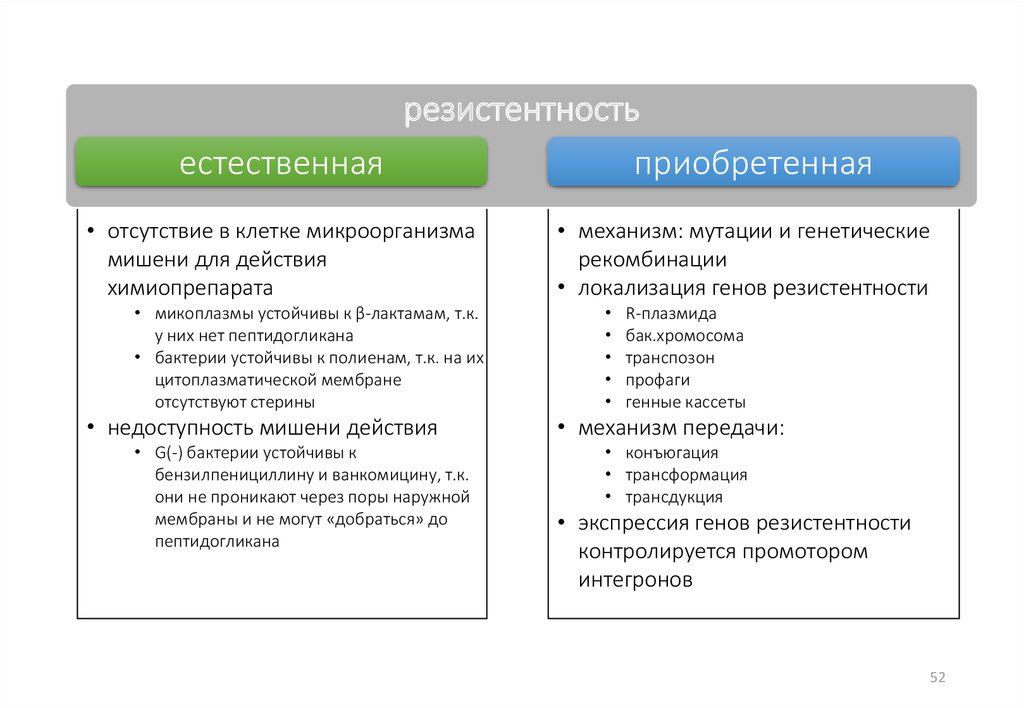
резистентностьестественная
приобретенная
• отсутствие в клетке микроорганизма
мишени для действия
химиопрепарата
• микоплазмы устойчивы к β-лактамам, т.к.
у них нет пептидогликана
• бактерии устойчивы к полиенам, т.к. на их
цитоплазматической мембране
отсутствуют стерины
• недоступность мишени действия
• G(-) бактерии устойчивы к
бензилпенициллину и ванкомицину, т.к.
они не проникают через поры наружной
мембраны и не могут «добраться» до
пептидогликана
• механизм: мутации и генетические
рекомбинации
• локализация генов резистентности
R-плазмида
бак.хромосома
транспозон
профаги
генные кассеты
• механизм передачи:
• конъюгация
• трансформация
• трансдукция
• экспрессия генов резистентности
контролируется промотором
интегронов
52
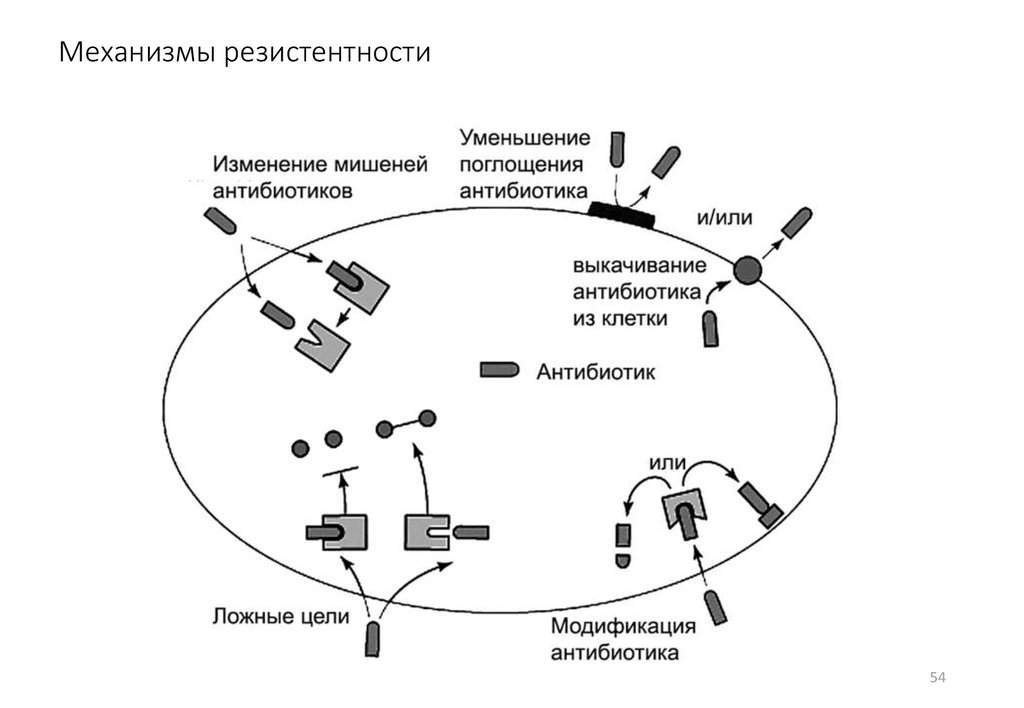
53. механизмы реализации приобретенной резистентности
• модификация структуры мишени—мутации, пориводящие к изменению структуры белка рибосом, делают бактерии
устойчивыми к аминогликозидам, макролидам, тетрациклинам
—изменение структуры ДНК-гиразы делает бактерии устойчивыми к
фторхинолонам
—изменение структуры ПСБ приводит к развитию устойчивости к β-лактамам
• недоступность мишени для действия химиопрепарата
—изменение проницаемости клеточных структур для препарата,
например, белков поринов в наружной мембране (G-) бактерий
—активное выведение препарата из клетки
• образование бак.ферментов, инактивирующих антибиотики
—β-лактамазы инактивируют пенициллины и цефалоспорины
—трансферазы (ацетилирующие или фосфорилирующие) инактивируют
такие антибиотики, как аминогликозиды, линкозамиды, макролиды
53
54. Механизмы резистентности
5455. группа наиболее опасных микроорганизмов, сочетающих высокую патогенность и высокий уровень резистентности и приводящие к
высокому уровню смертельных исходовESKAPE
Enterococcus Faecium
Staphylococcus aureus
Klebsiella pneumoniae
Acinetobacter baumanni
Pseudomonas aeruginosa
Enterobacter spp.
55
56.
BACKUP56
57.
http://b2blogger.com/pressroom/12067.htmlhttp://www.antibiotic.ru/cmac/pdf/12_2_127.pdf
http://www.fda.gov/Drugs/DrugSafety/ucm224370.htm
https://ru.wikipedia.org/wiki/
https://en.wikipedia.org/wiki/Penicillin
Научная библиотека диссертаций и авторефератов
disserCat http://www.dissercat.com/content/mekhanizm-virusspetsificheskogodeistviya-preparata-arbidol#ixzz3mJcD3TaZ
57
58.
«Арбидол» (Аrbidolum, химическое название: метилфенилтиометил-диметиламинометилгидроксиброминдол карбоновой кислоты этиловый эфир, МНН не присваивалось) —российский противовирусный препарат, оказывает иммуномодулирующее и
противогриппозное действие, специфически подавляя вирусы гриппа А и В.[3] Наименование
«Арбидол» / «Аrbidolum» присвоено разработчиком — ВНИХФИ как производное от слов
«карбэтокси» и «броминдол», и одобрено номенклатурной комиссией Фармакологического
комитета Минздрава СССР. Клинические исследования препарата проводились одновременно
во Всесоюзном Научно-исследовательском институте гриппа и НИИ эпидемиологии и
микробиологии им. Пастера в Ленинграде, а также в НИИ вирусологии им. Ивановского в г
Москве. На базе данных клинических учреждений проведено сравнительное двойное слепое
плацебо-контролируемое исследование. В исследовании принимали участие 7646 человек в
организованных взрослых коллективах и на промышленных предприятиях, из которых 4695
человек получали арбидол, 111 — получали ремантадин и 2840 — плацебо. Результаты этих
исследований неизвестны. Однако клинические испытания препарата в соответствии с
современными требованиями доказательной медицины не проводились, поэтому арбидол
следует классифицировать как лекарственное средство с недоказанной эффективностью. ВОЗ
не рассматривает арбидол, либо иные химически-родственные субстанции в качестве
перспективных противовирусных препаратов. Механизм действия препарата Арбидол
действует на ранних стадиях вирусной репродукции и ингибирует слияние вирусной липидной
оболочки с внутриклеточными мембранами, предотвращая проникновение вируса внутрь
клетки. Арбидол по механизму действия отличается от применяемых противогриппозных
препаратов: амантадина и ремантадина, являющихся блокаторами ионных каналов,
образованных М2 белком вируса гриппа, и ингибиторов нейраминидазы (NA) — занамивира и
озельтамивира. Применение Арбидол разрешён к медицинскому применению в СССР на
основании приказа Министерства здравоохранения СССР № 229 от 23 марта 1988 года.
58






































 Медицина
Медицина








