Похожие презентации:
Биохимия крови
1. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:Биохимия крови
Краснодар
2016
2. Функции крови
1. Транспортная:а) дыхательная
б) питательная (трофическая)
в) выделительная (экскреторная)
2. Регуляторная:
а) КОС – буферные системы
б) осмотическое давление Росм
в) онкотическое давление Ронк
г) гормональная
д) терморегуляторная
3. Защитная:
а) коллоидная защита
б) иммунохимическая
в) гемостаз
3. Физико-химические свойства
КРОВЬплазма 55%
□
□
□
□
□
форменные элементы
- эритроциты
- лейкоциты
- тромбоциты
рН 7,36-7,42
Росм 7,8-8,1 атм
Ронк 0,03-0,04 атм
Δ t -0,56-(-0,58) °С
Удельные вес 1,050-1,060 г/см3
(плотность)
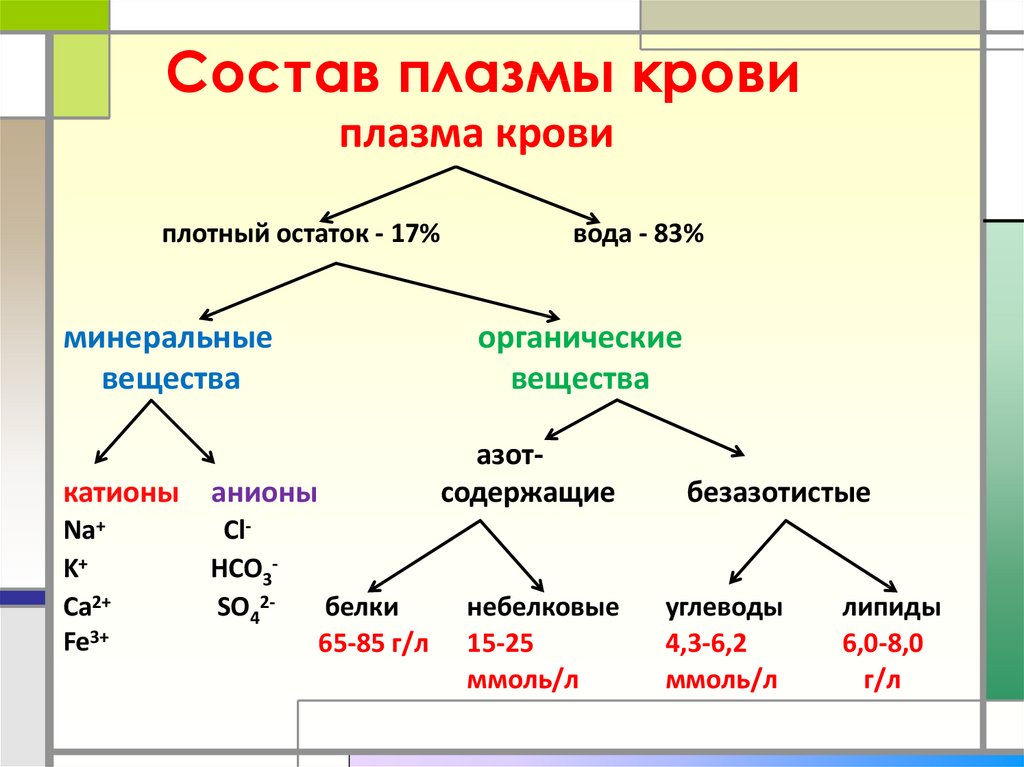
4. Состав плазмы крови
плазма кровиплотный остаток - 17%
минеральные
вещества
катионы
анионы
Na+
K+
Ca2+
Fe3+
ClHCO3SO42-
вода - 83%
органические
вещества
азотсодержащие
белки
65-85 г/л
небелковые
15-25
ммоль/л
безазотистые
углеводы
4,3-6,2
ммоль/л
липиды
6,0-8,0
г/л
5. Минеральный состав крови
□ Берёзов, Коровкин. Биологическаяхимия (стр. 582-584)
□ Бышевский, Терсенов. Биохимия для
врача (стр.208-209, 297-301)
□ Чиркин, Данченко. Биологическая
химия (стр.497-501)
6. Жизненный цикл эритроцита
1. пролиферация, клеточнаядифференцировка, созревание:
Нb
исчезновение белоксинтезирующей системы
исчезновение клеточных органелл (ядра,
митохондрий)
резкое ослабление дыхательного
метаболизма
2. период активного
функционирования (90-120 дней)
транспорт газов
поддержание КОС
3. деградация
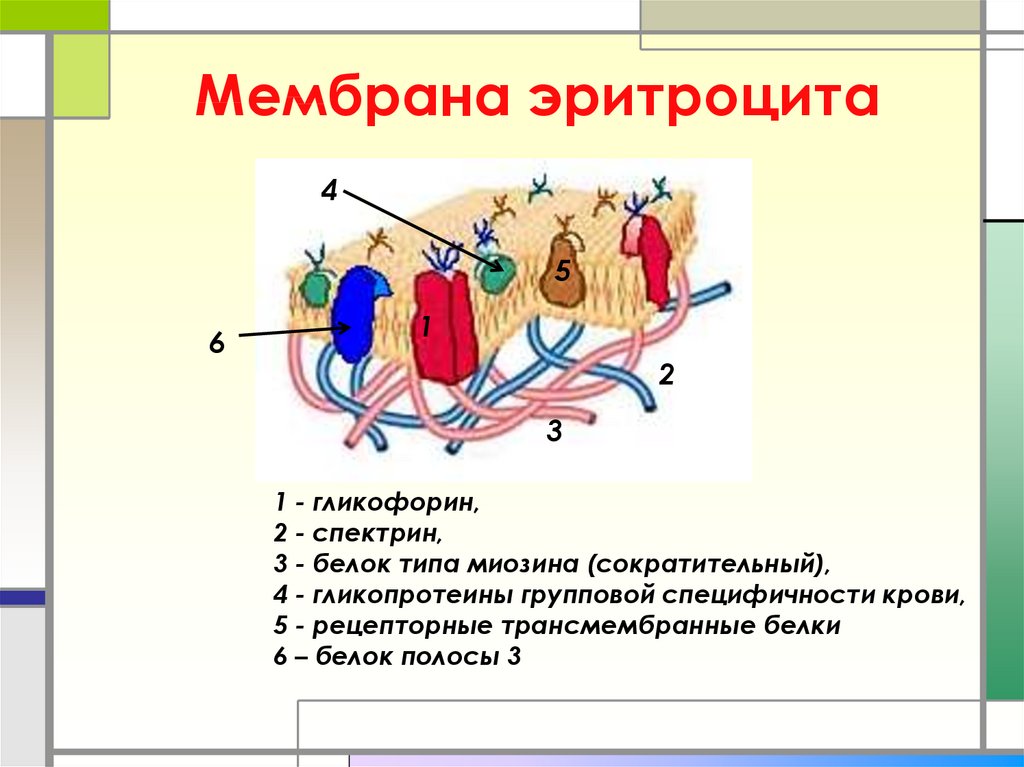
7. Мембрана эритроцита
45
6
1
2
3
1 - гликофорин,
2 - спектрин,
3 - белок типа миозина (сократительный),
4 - гликопротеины групповой специфичности крови,
5 - рецепторные трансмембранные белки
6 – белок полосы 3
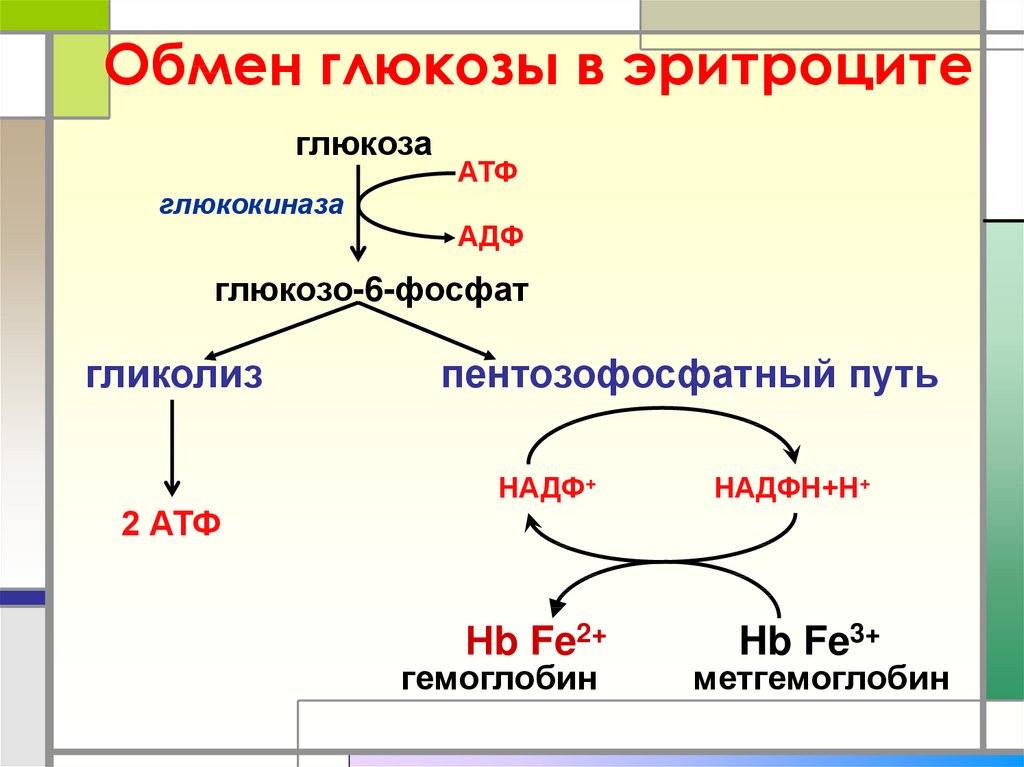
8. Обмен глюкозы в эритроците
глюкозаАТФ
глюкокиназа
АДФ
глюкозо-6-фосфат
гликолиз
пентозофосфатный путь
НАДФ+
НАДФН+Н+
2 АТФ
Нb Fe2+
гемоглобин
Hb Fe3+
метгемоглобин
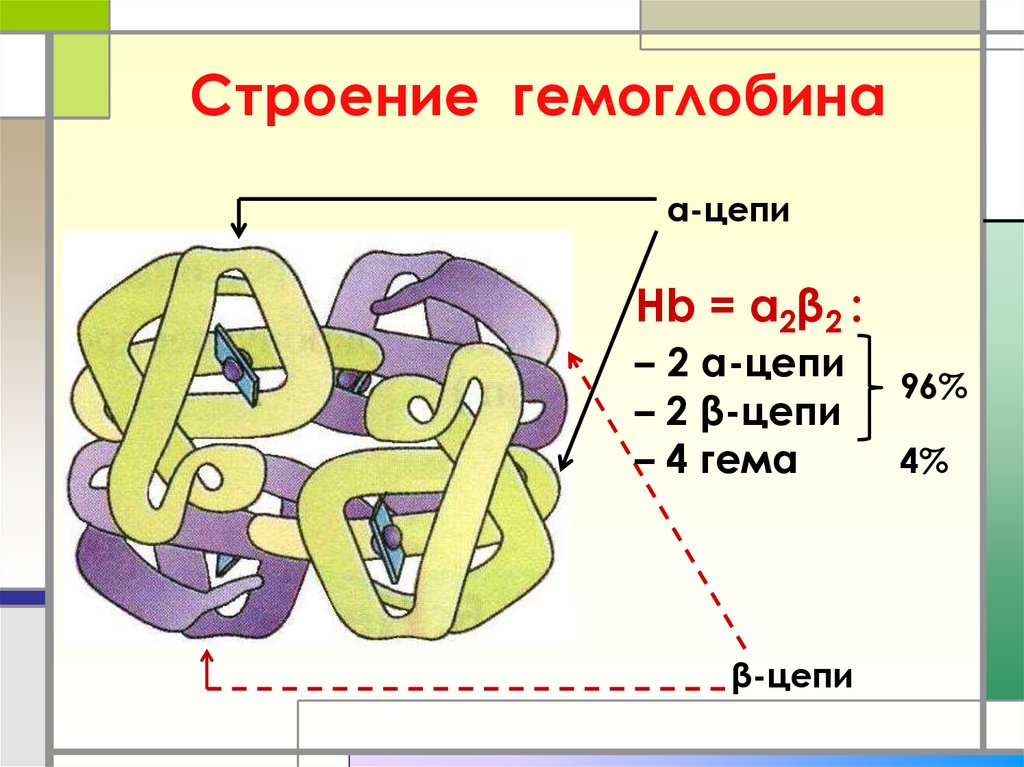
9. Строение гемоглобина
α-цепиHb = α2β2 :
– 2 α-цепи
– 2 β-цепи
– 4 гема
β-цепи
96%
4%
10. Транспортная форма О2
Кислород транспортируетсятолько в связанном с
гемоглобином виде (в виде
оксигемоглобина) –
Hb(Fe2+)•4 О2
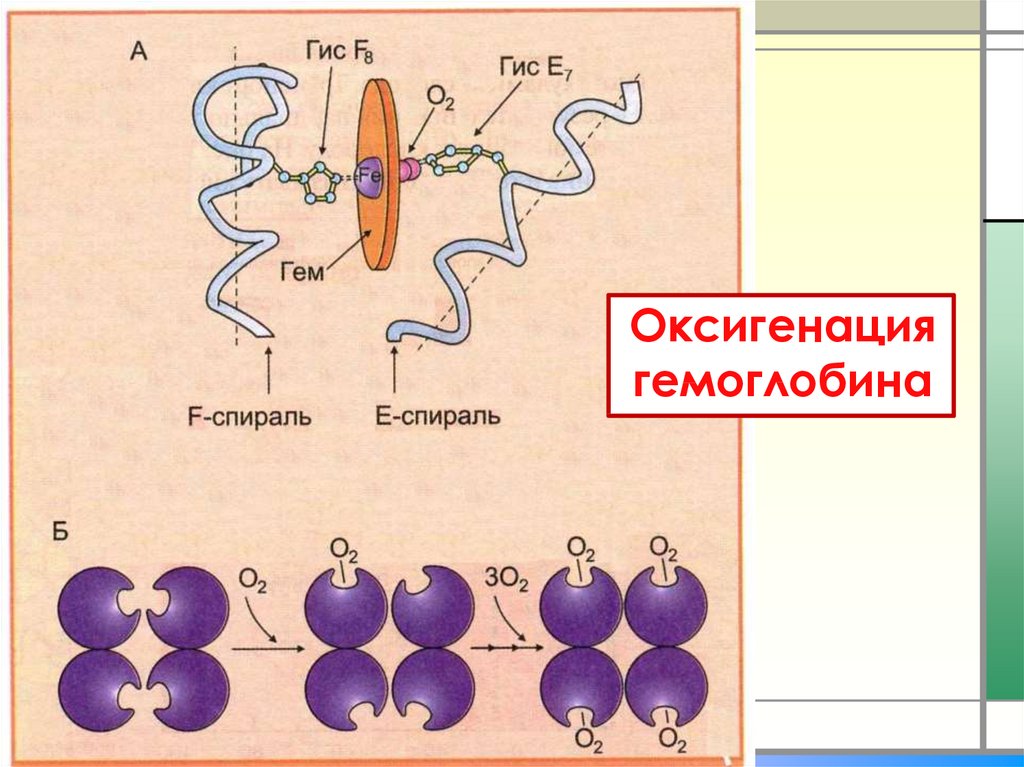
11. Оксигенация гемоглобина
12. Транспортные формы СО2
□ Физически растворённый - 7-8%□ Карбгемоглобин – 12-13%
HHb + CO2
HHb-NH-C
O
OH
□ Бикарбонаты – 80%
NaHCO3 в плазме
КНCO3 в эритроците
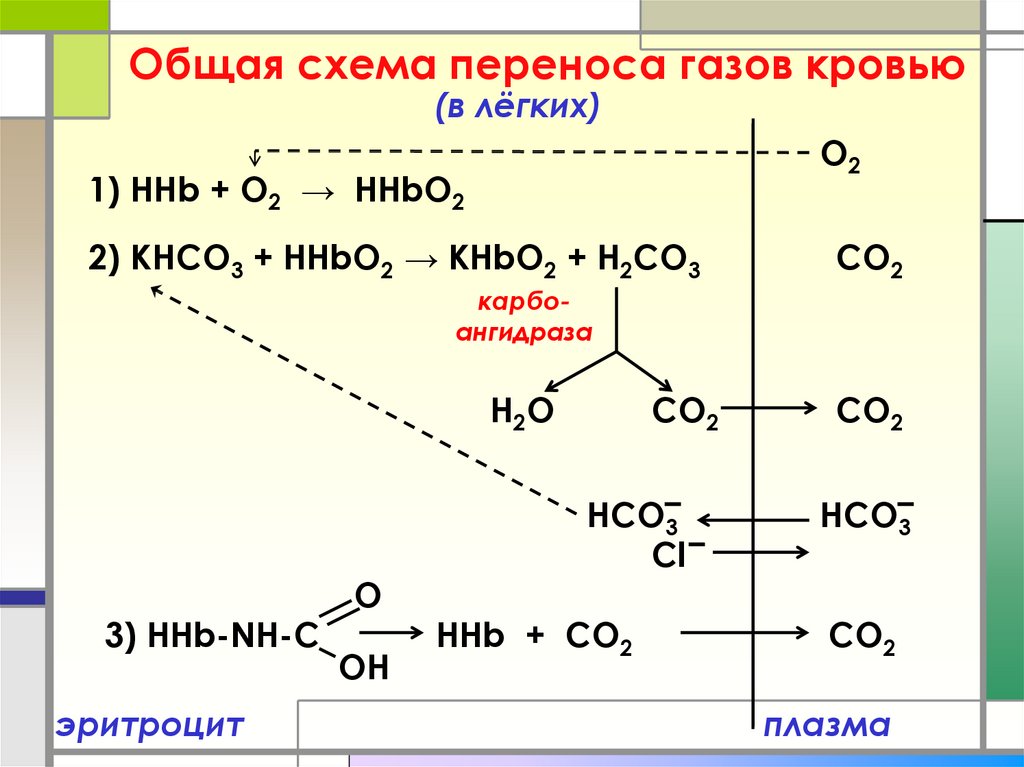
13. Общая схема переноса газов кровью
(в лёгких)O2
1) ННb + O2 → HHbO2
2) KНCO3 + HHbO2 → KHbO2 + Н2CO3
CO2
карбоангидраза
H2O
3) HHb-NH-C
эритроцит
O
OH
CO2
HCO3
Cl
HHb + CO2
CO2
HCO3
CO2
плазма
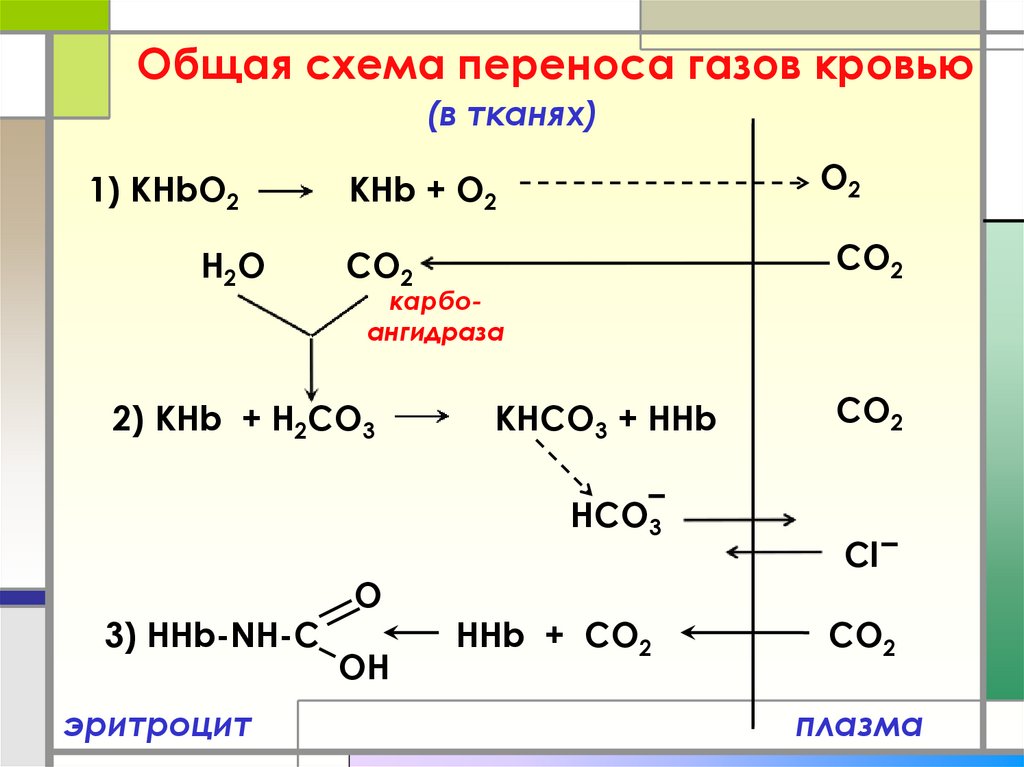
14. Общая схема переноса газов кровью
(в тканях)1) КHbO2
H2O
O2
КНb + O2
CO2
CO2
карбоангидраза
2) KHb + Н2CO3
KНCO3 + HHb
HCO3
3) HHb-NH-C
эритроцит
O
OH
HHb + CO2
CO2
Cl
CO2
плазма
15. Связывание газов гемоглобином
□ ОксигемоглобинHb O2 (Fe2+)
□ Карбоксигемоглобин Hb CO (Fe2+)
□ Карбгемоглобин Hb-NH-COOH (Fe2+)
□ Метгемоглобин Мet Hb(Fe3+)
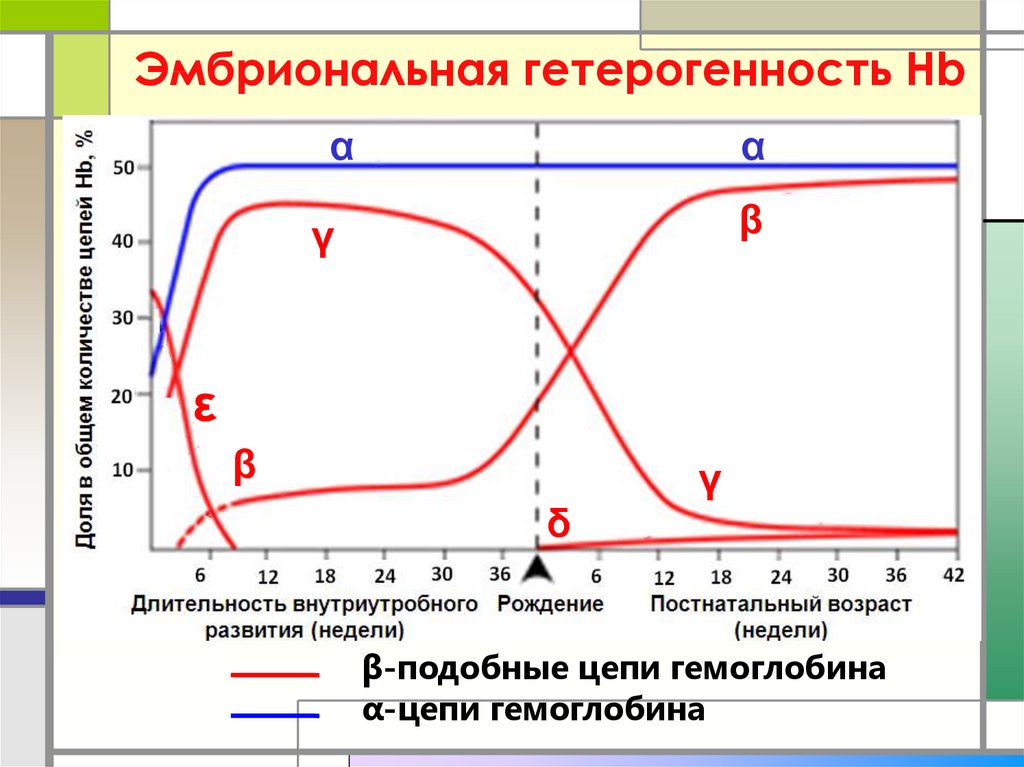
16. Эмбриональная гетерогенность Нb
Нb P = α2 ε2Hb F = α2 γ2
Hb A = α2 β2
Hb A2 = α2 δ2
17. Эмбриональная гетерогенность Нb
αα
β
γ
ε
β
δ
γ
β-подобные цепи гемоглобина
α-цепи гемоглобина
18. Гетерогенность, обусловленная минорными компонентами
Hb A = α2 β296-98%
Hb F = α2 γ2
1-2%
Hb A2 = α2 δ2
1-2%
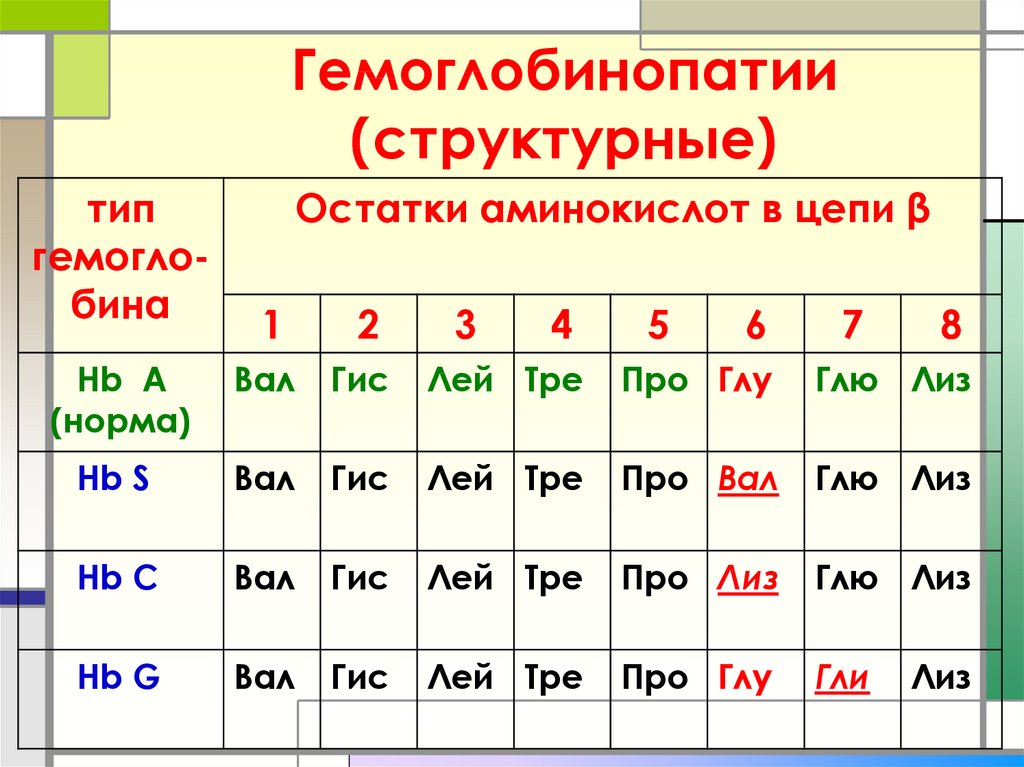
19. Гемоглобинопатии (структурные)
типгемоглобина
Остатки аминокислот в цепи β
1
2
3
4
5
6
7
8
Hb A
(норма)
Вал
Гис
Лей Тре
Про Глу
Глю Лиз
Hb S
Вал
Гис
Лей Тре
Про Вал
Глю Лиз
Hb C
Вал
Гис
Лей Тре
Про Лиз
Глю Лиз
Hb G
Вал
Гис
Лей Тре
Про Глу
Гли
Лиз
20. Гемоглобинопатии
Hb A = α2 β2HbKansas = β 102асп→тре
HbHiroshima = β 146гис→асп
Hb F = α2 γ2
HbBart = γ4
Hb H = β4
талассемии
(регуляторные)
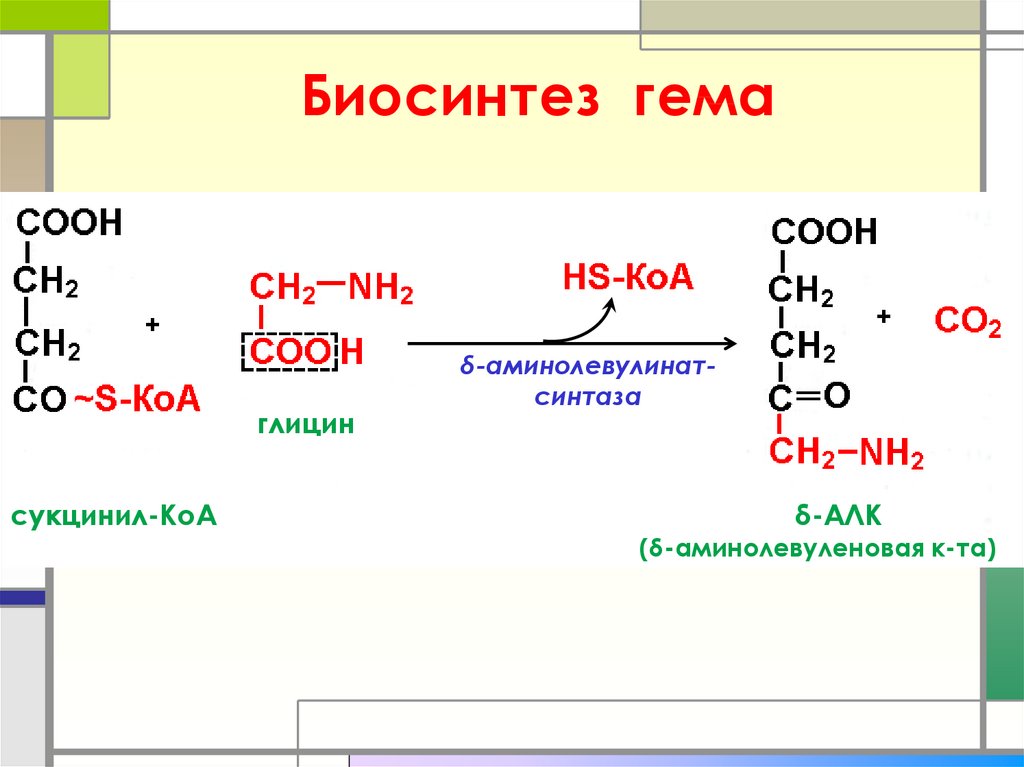
21. Биосинтез гема
++
глицин
сукцинил-КоА
δ-аминолевулинатсинтаза
δ-АЛК
(δ-аминолевуленовая к-та)
22.
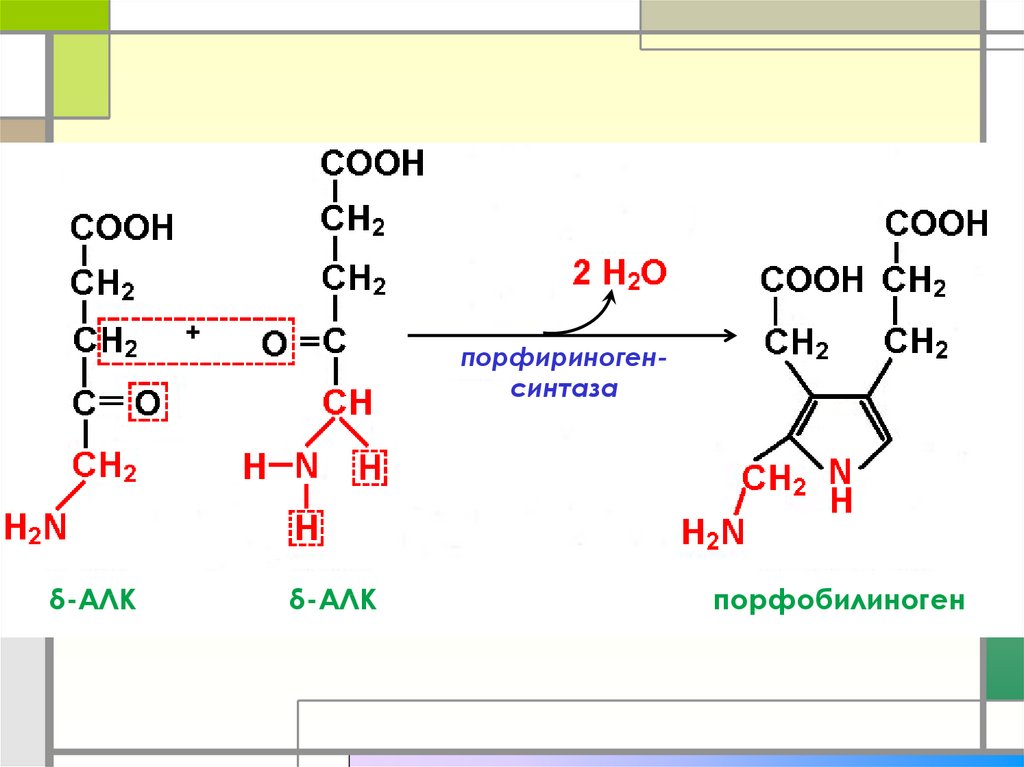
+δ-АЛК
порфириногенсинтаза
δ-АЛК
порфобилиноген
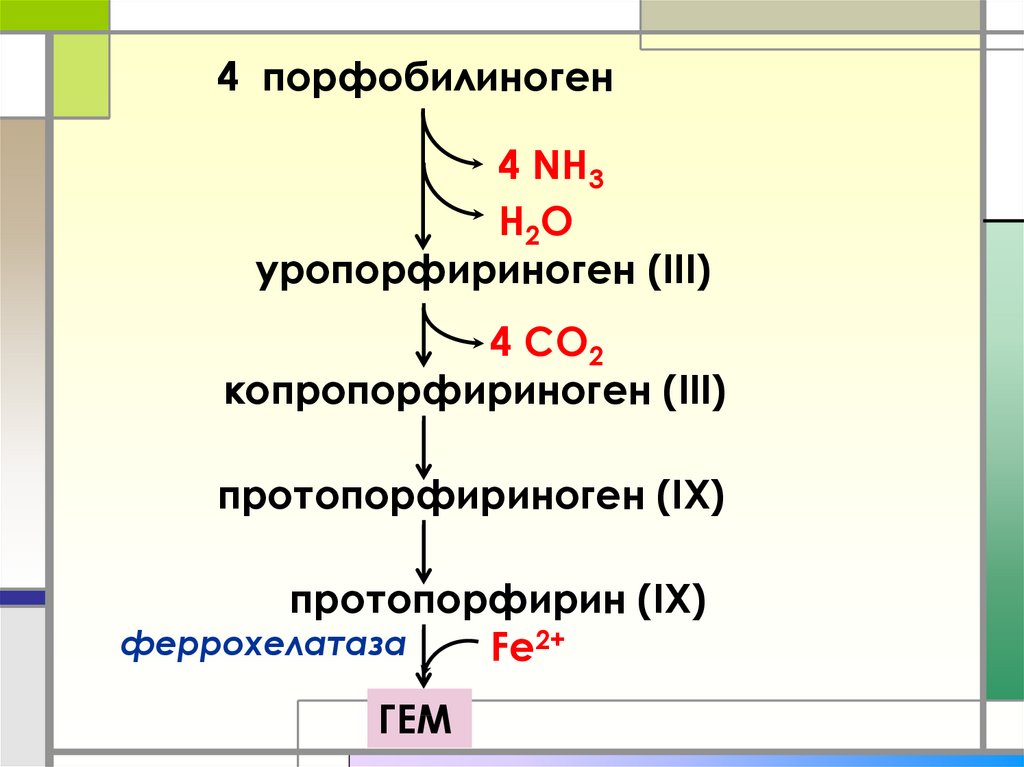
23.
4 порфобилиноген4 NH3
H2O
уропорфириноген (III)
4 СО2
копропорфириноген (III)
протопорфириноген (IХ)
протопорфирин (IХ)
феррохелатаза
Fe2+
ГЕМ
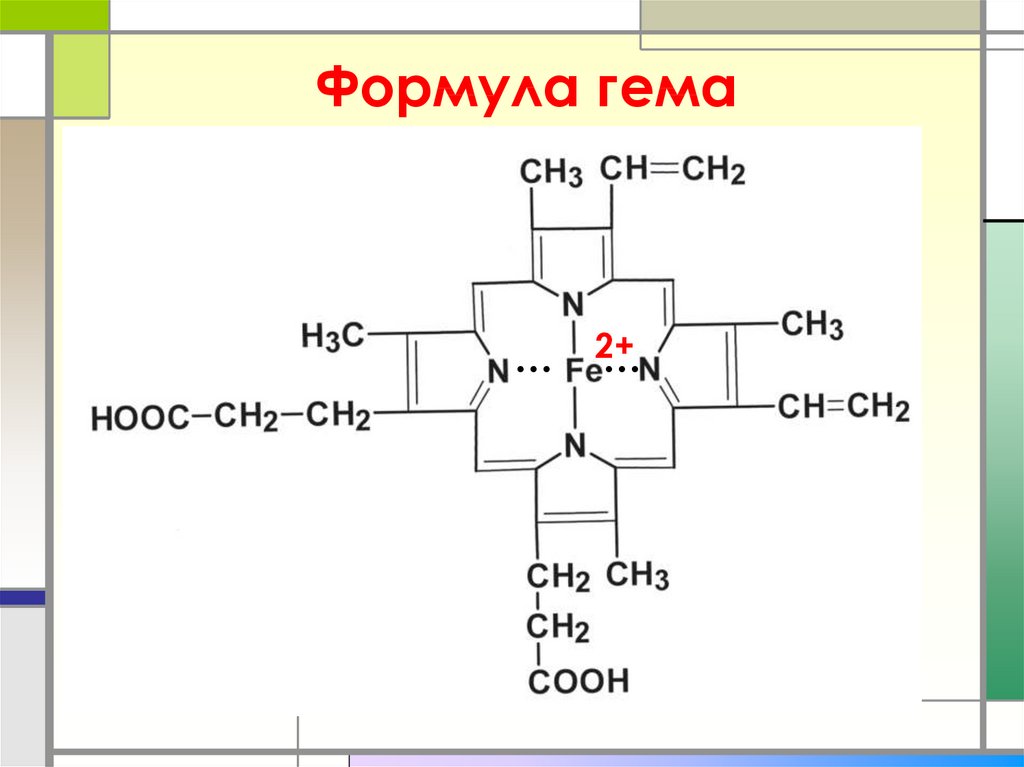
24. Формула гема
…2+
…
25. Использование гема
□ Гемоглобин□ Миоглобин
□ Окислительновосстановительные ферменты
– цитохромы, каталаза,
пероксидаза
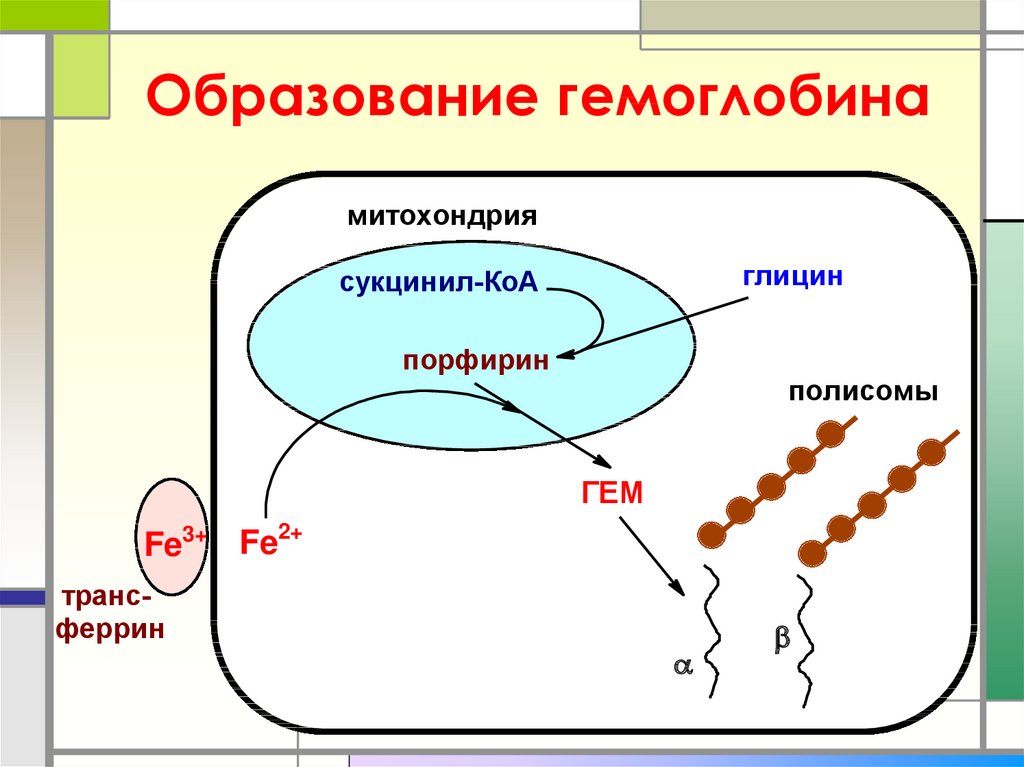
26. Образование гемоглобина
митохондрияглицин
сукцинил-КоА
порфирин
полисомы
ГЕМ
2+
Fe3+ Fe
трансферрин
27. Порфирии
Порфирии – заболевания, обусловленныенарушениями начальных этапов синтеза
гема и сопровождающиеся накопление
порфиринов и их предшественников.
□ Первичные – генетический дефект
ферментов синтеза
□ Вторичные – нарушения регуляции
биосинтеза
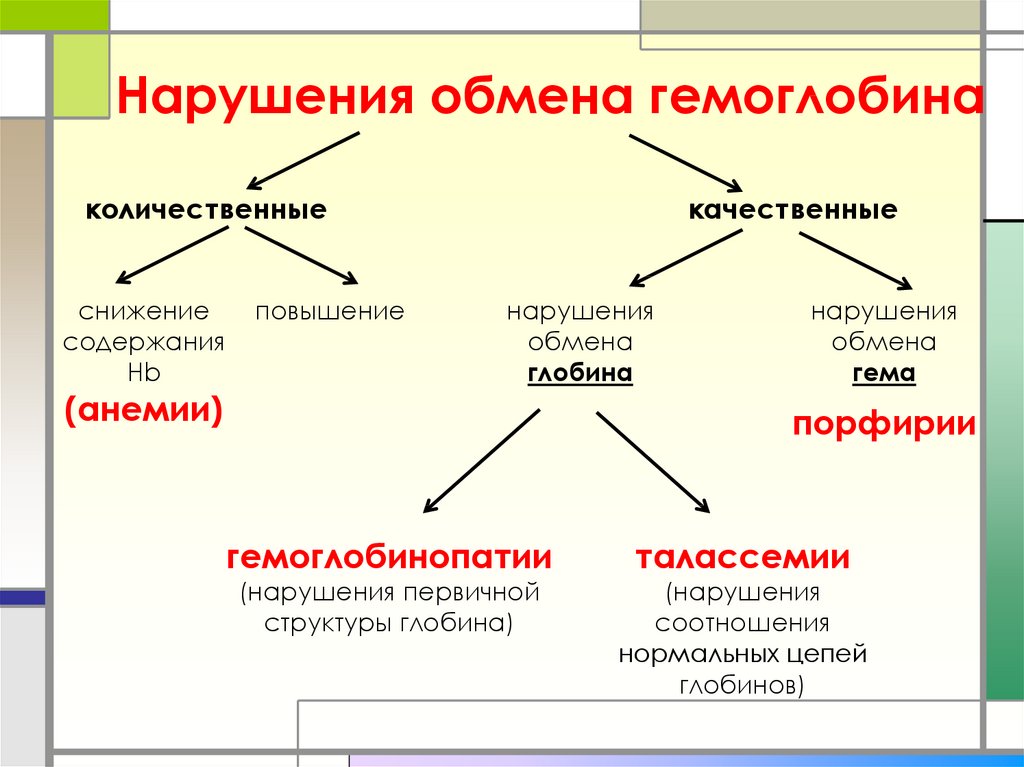
28. Нарушения обмена гемоглобина
количественныеснижение
содержания
Hb
(анемии)
повышение
качественные
нарушения
обмена
глобина
нарушения
обмена
гема
порфирии
гемоглобинопатии
(нарушения первичной
структуры глобина)
талассемии
(нарушения
соотношения
нормальных цепей
глобинов)
29. Формы железа в организме
1. Резервноеферритин (Fe3+)
гемосидерин (Fe3+)
2. Транспортное
трансферрин (Fe3+) (содержание
в крови 9-29 ммоль/л)
3. Функционально активное (гем – Fe2+)
- гемоглобин – транспорт О2 кровью
- миоглобин – резерв О2
- дыхательные ферменты – усвоение О2 на
молекулярном уровне
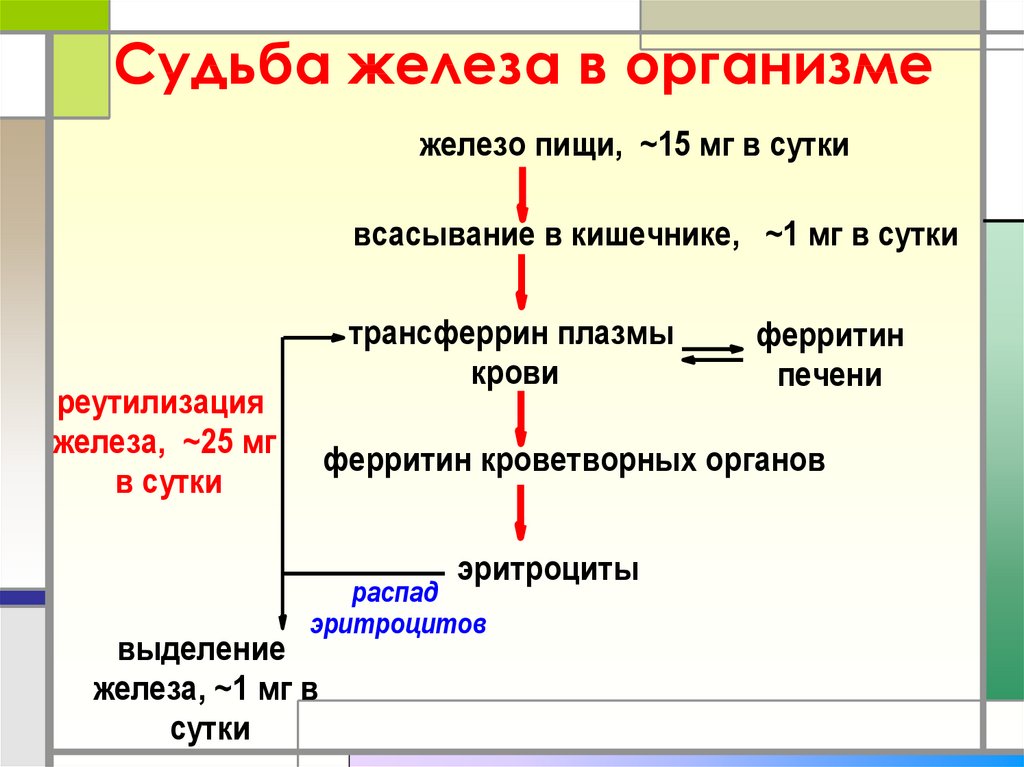
30. Судьба железа в организме
железо пищи, ~15 мг в суткивсасывание в кишечнике, ~1 мг в сутки
трансферрин плазмы
крови
реутилизация
железа, ~25 мг
в сутки
ферритин
печени
ферритин кроветворных органов
эритроциты
распад
эритроцитов
выделение
железа, ~1 мг в
сутки
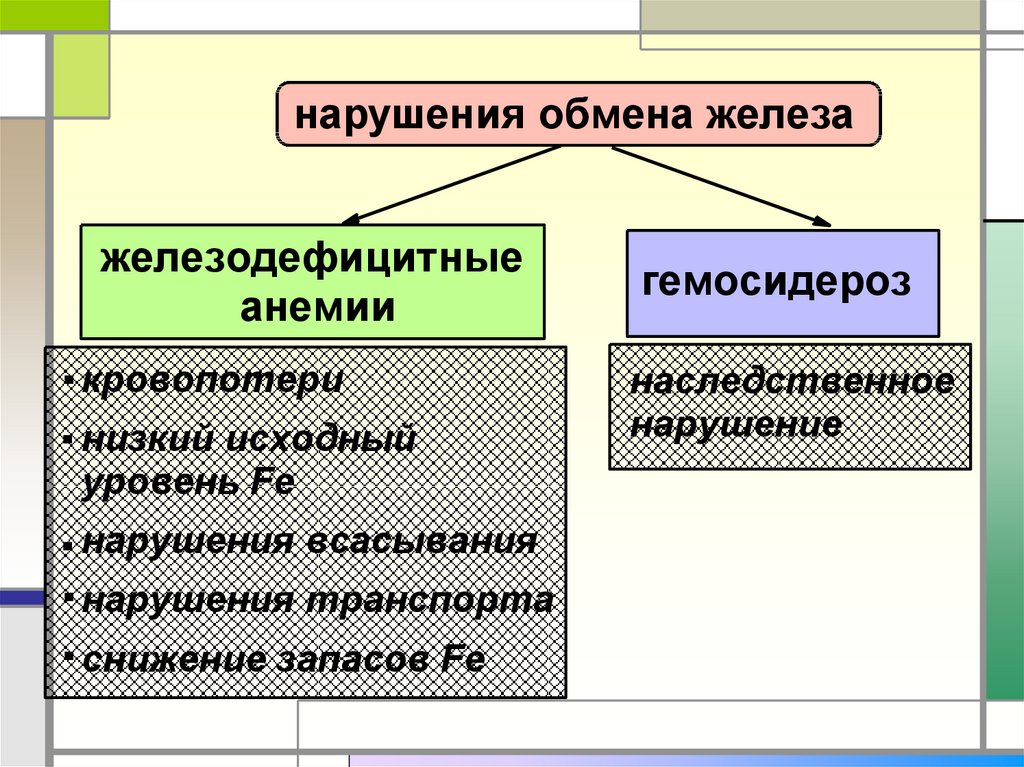
31.
нарушения обмена железажелезодефицитные
анемии
. кровопотери
. низкий исходный
уровень Fe
. нарушения всасывания
. нарушения транспорта
. снижение запасов Fe
гемосидероз
наследственное
нарушение
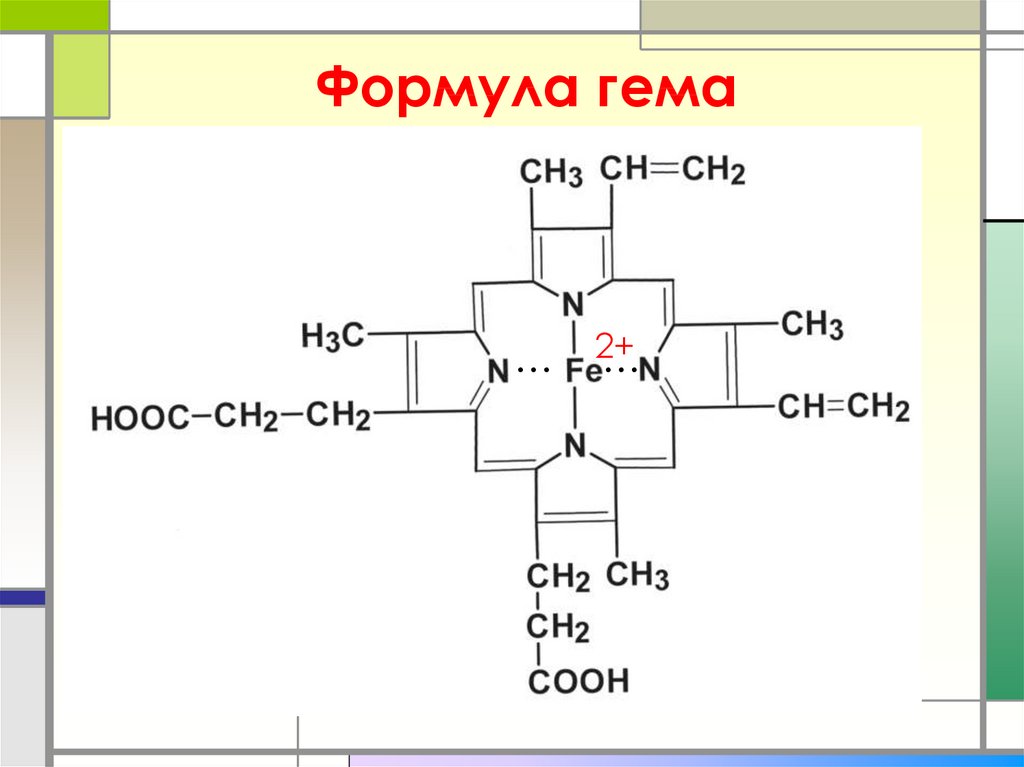
32. Формула гема
…2+
2+
…
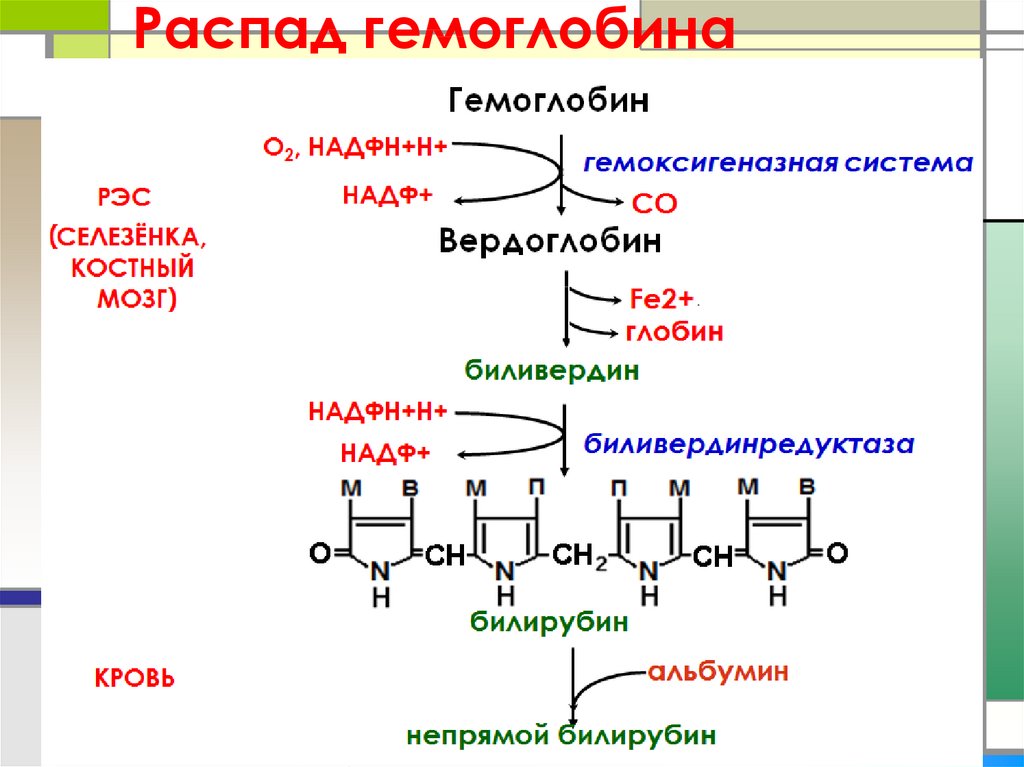
33. Распад гемоглобина
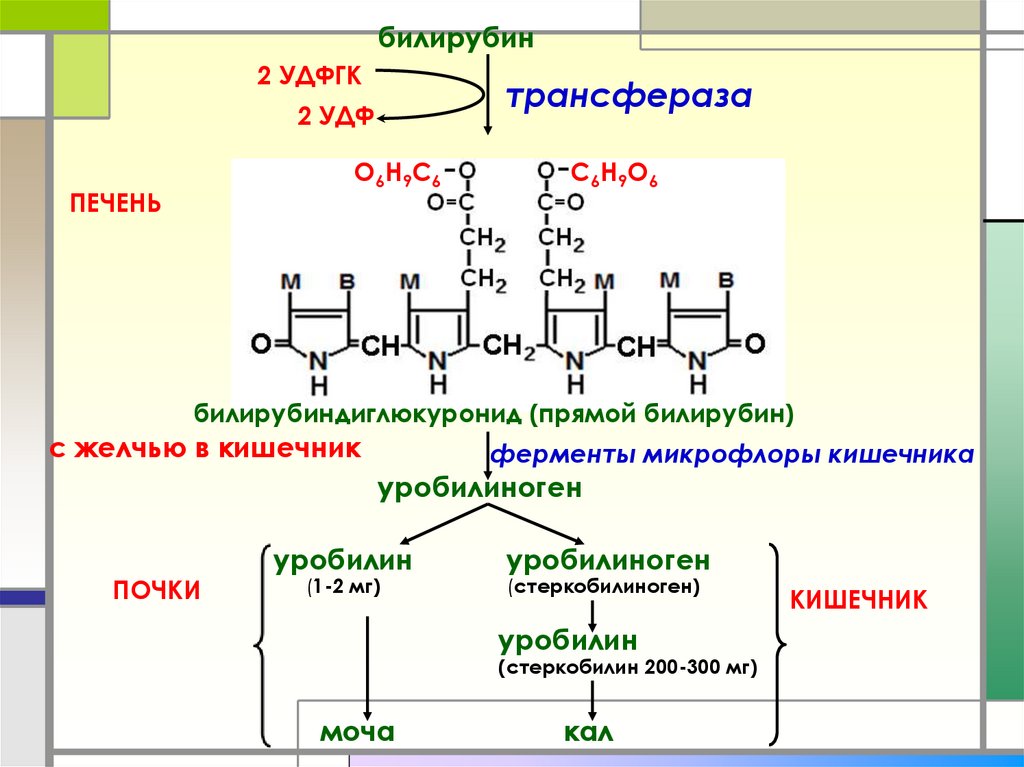
34.
билирубин2 УДФГК
трансфераза
2 УДФ
О6Н9С6
ПЕЧЕНЬ
С6Н9О6
билирубиндиглюкуронид (прямой билирубин)
с желчью в кишечник
ферменты микрофлоры кишечника
уробилиноген
ПОЧКИ
уробилин
(1-2 мг)
уробилиноген
(стеркобилиноген)
уробилин
(стеркобилин 200-300 мг)
моча
кал
КИШЕЧНИК
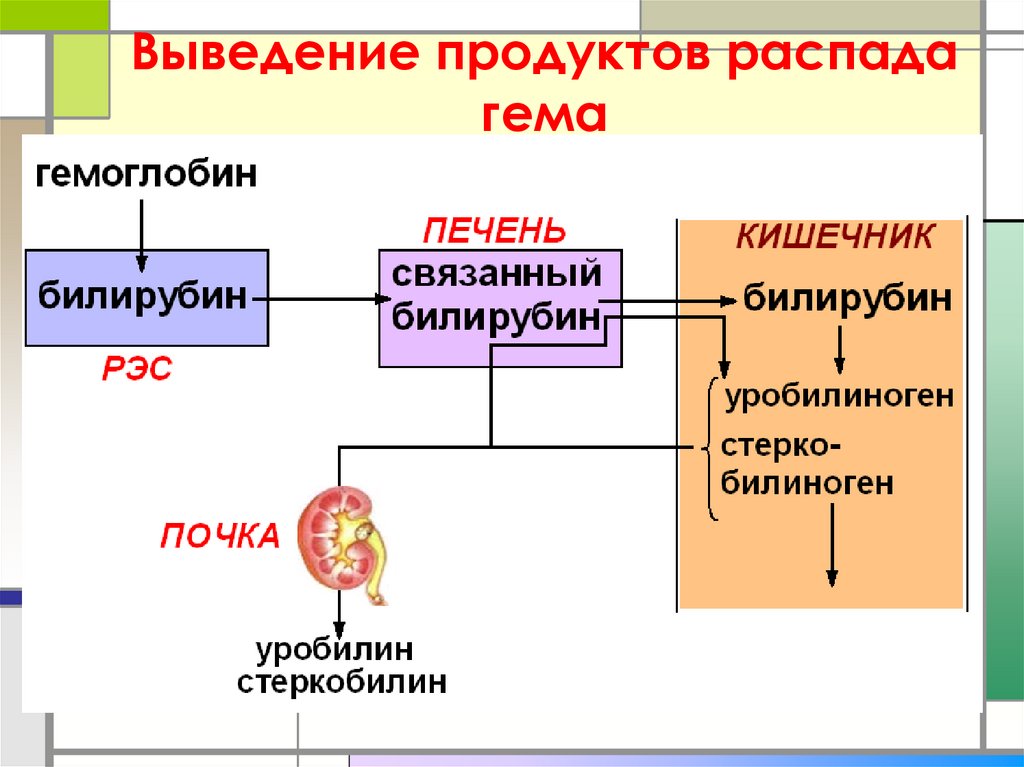
35. Выведение продуктов распада гема
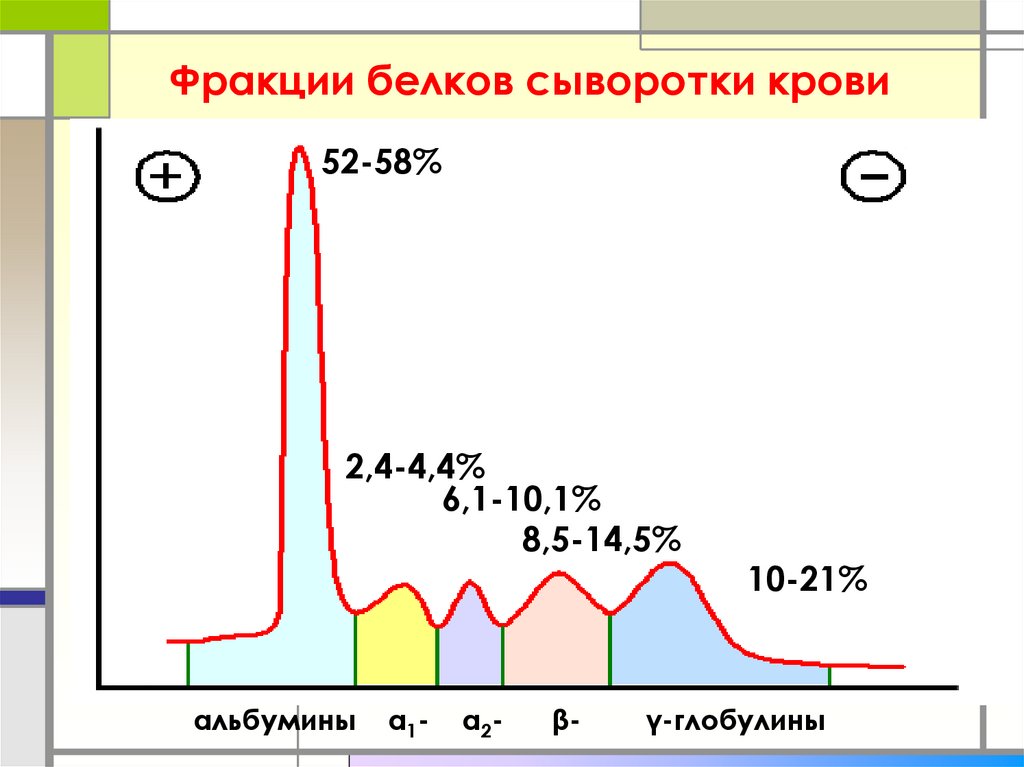
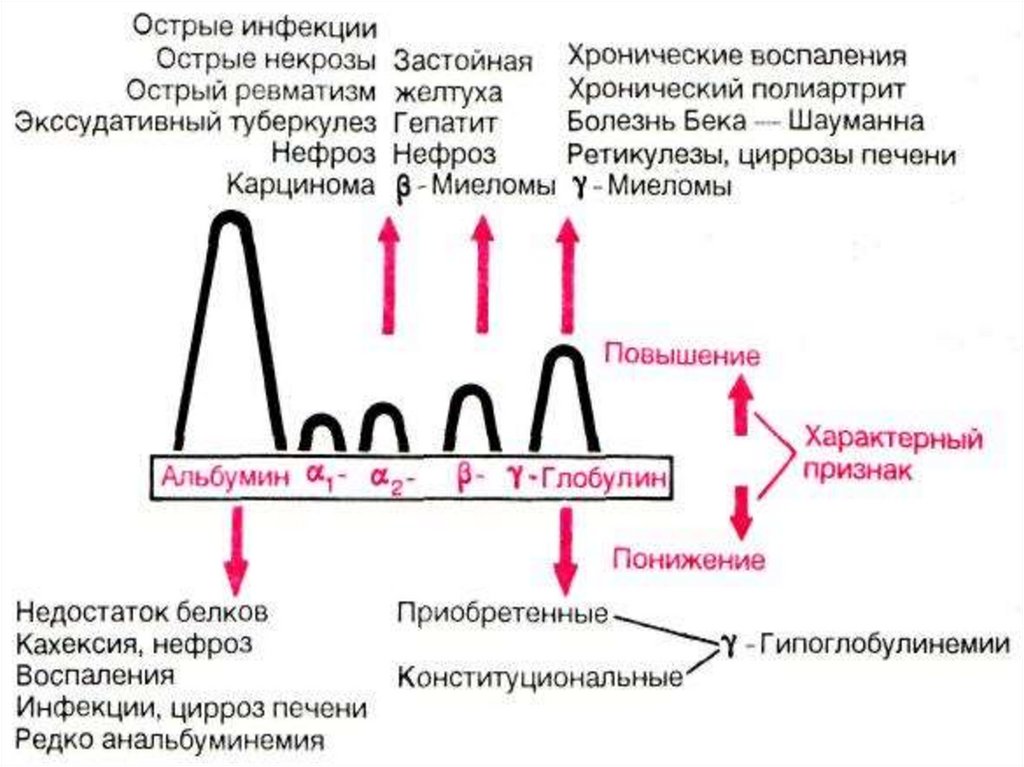
36. Фракции белков сыворотки крови
52-58%2,4-4,4%
6,1-10,1%
8,5-14,5%
альбумины
α1-
α2-
β-
10-21%
γ-глобулины
37.
38. Ферменты плазмы крови:
□ Секреторные;□ Индикаторные
(клеточные);
□ Экскреторные.
39. Энзимодиагностика -
Энзимодиагностика определениеактивности
ферментов с
диагностической
целью
40.
ферментпримеры
использования
Лактатдегидрогеназа
(изофермент ЛДГ1)
Инфаркт миокарда
Аспартатаминотрансфераза
(АСТ)
Инфаркт миокарда
Аланинаминотрансфераза
(АЛТ)
Заболевания печени,
инфаркт миокарда
Креатинкиназа (КК)
Прогрессирующая
(изофермент ММ – мышечный дистрофия
тип, изофермент МВ –
сердечный тип)
Инфаркт миокарда
Кислая фосфатаза
Рак предстательной
железы
41. Нарушения белкового состава крови
□Гипопротеинемия□Гиперпротеинемия
□Диспротеинемия
□Дефектопротеинемия
□Парапротеинемия
42. Белки «острой фазы»
□С-реактивный белок□α2-макроглобулин
□Антитрипсин
□Гаптоглобин
□Криоглобулин
43. Плазменные факторы свёртывания крови
I- фибриноген
II - протромбин
III - тканевой фактор
VI - Са2+
V - проакцелерин
VII - проконвертин
VIII - антигемофильный фактор А
IX - антигемофильный фактор В (Кристмаса)
X - фактор Прауэра-Стьюарта
(препротромбиназа)
XI - плазменный предшественник
тромбопластина
XII - фактор Хагемана
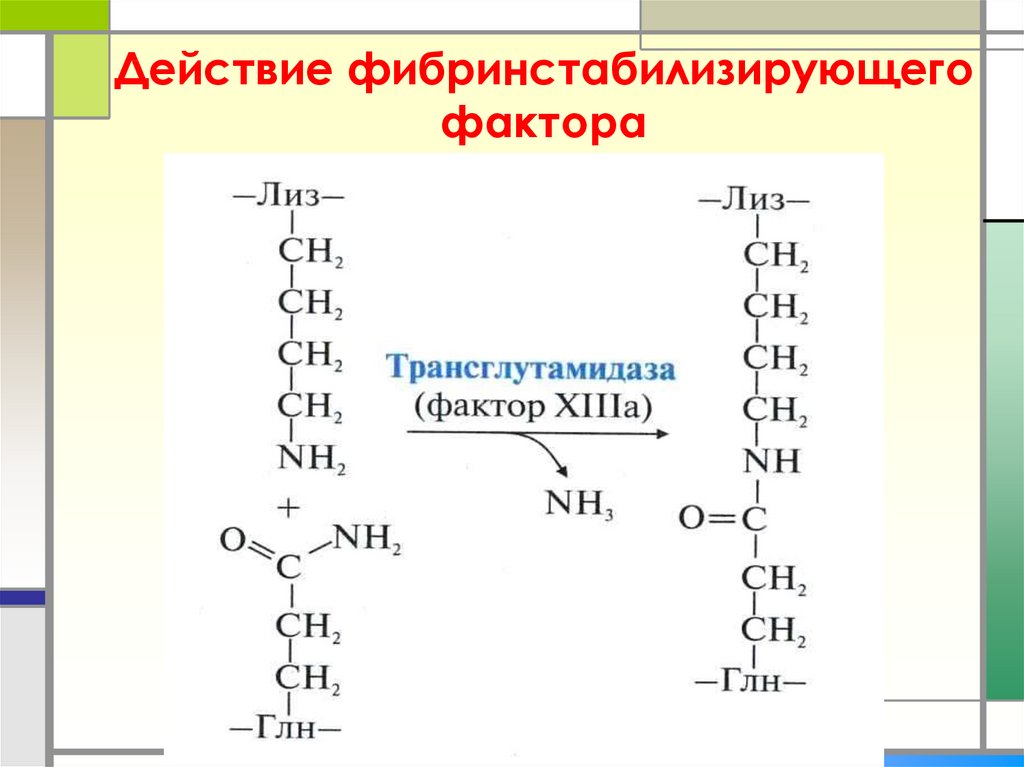
XIII - фибринстабилизирующий фермент
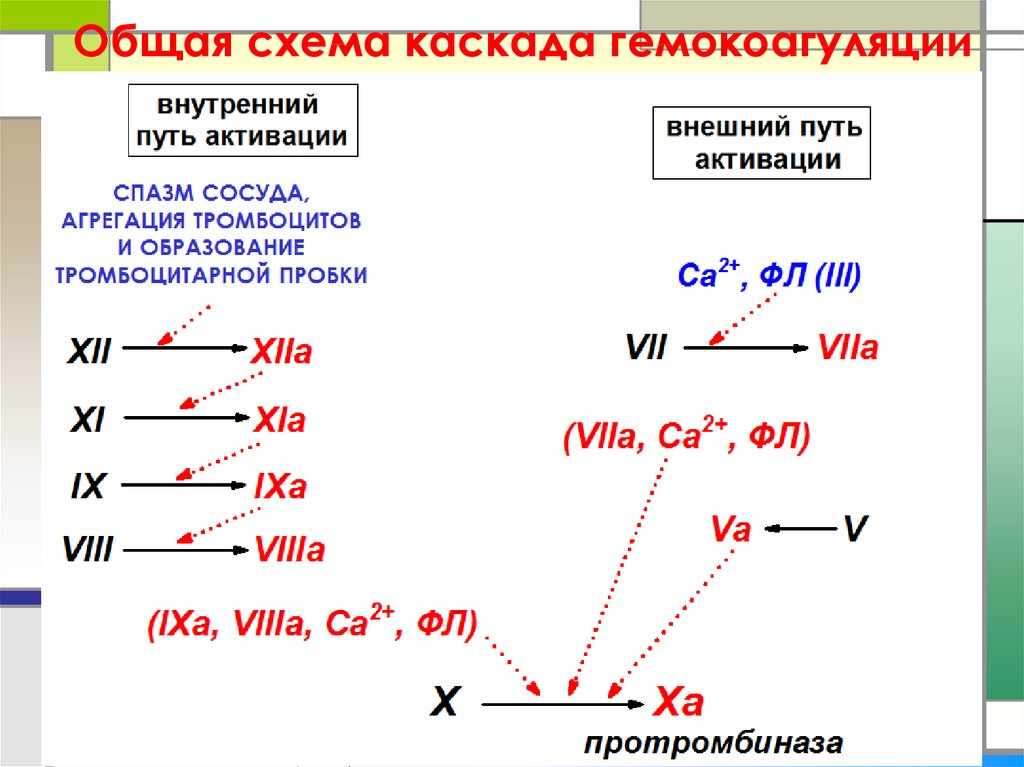
44. Общая схема каскада гемокоагуляции
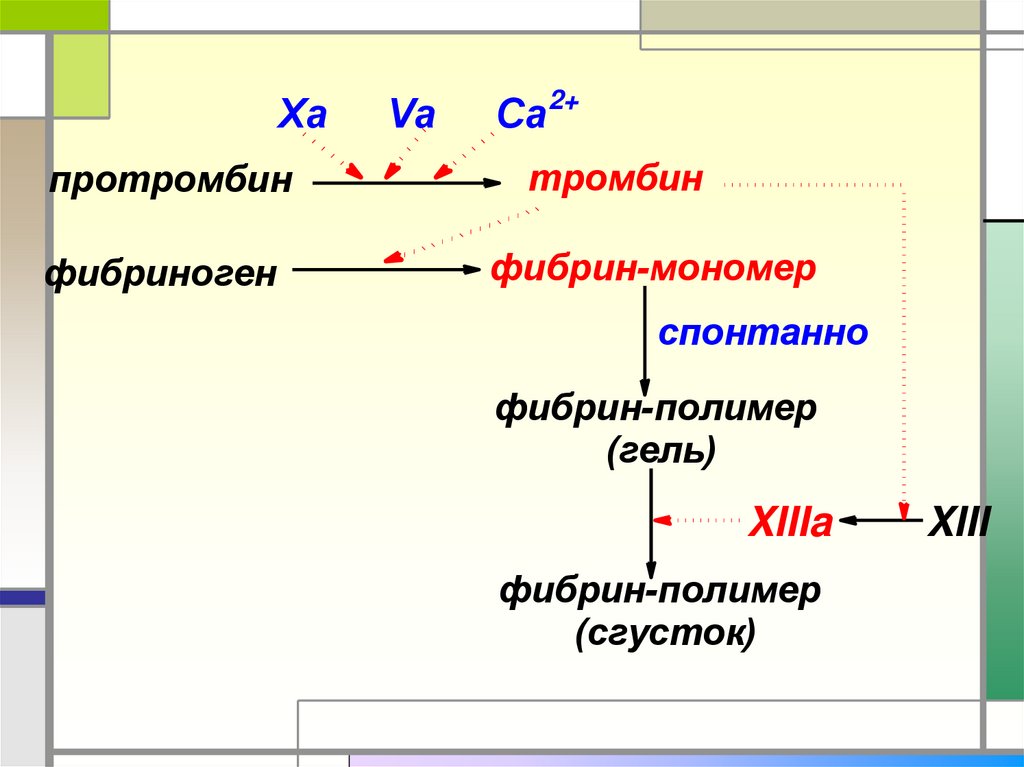
45.
Хапротромбин
фибриноген
Va
Ca2+
тромбин
фибрин-мономер
спонтанно
фибрин-полимер
(гель)
XIIIa
фибрин-полимер
(сгусток)
XIII
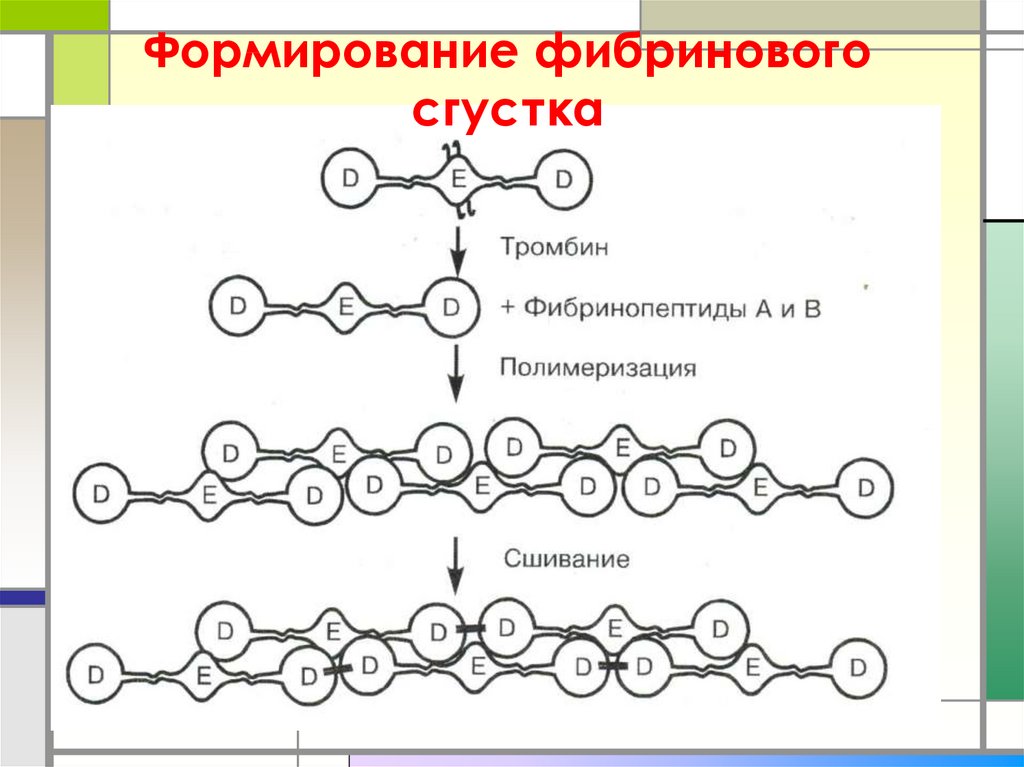
46. Формирование фибринового сгустка
47. Действие фибринстабилизирующего фактора
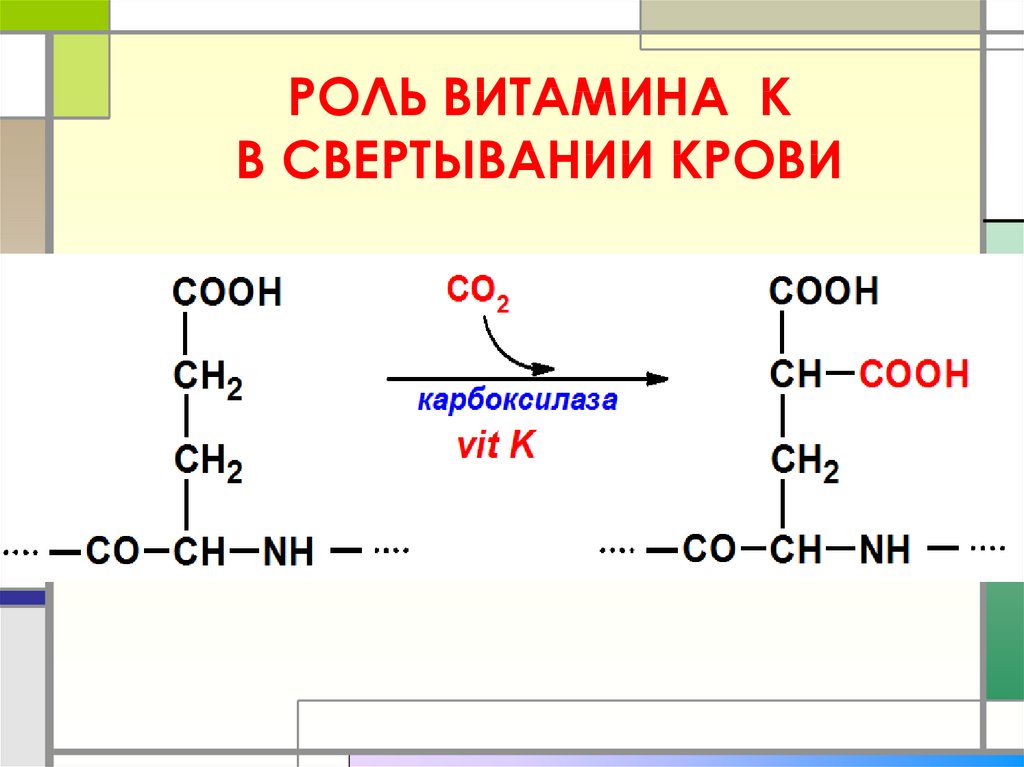
48. РОЛЬ ВИТАМИНА К В СВЕРТЫВАНИИ КРОВИ
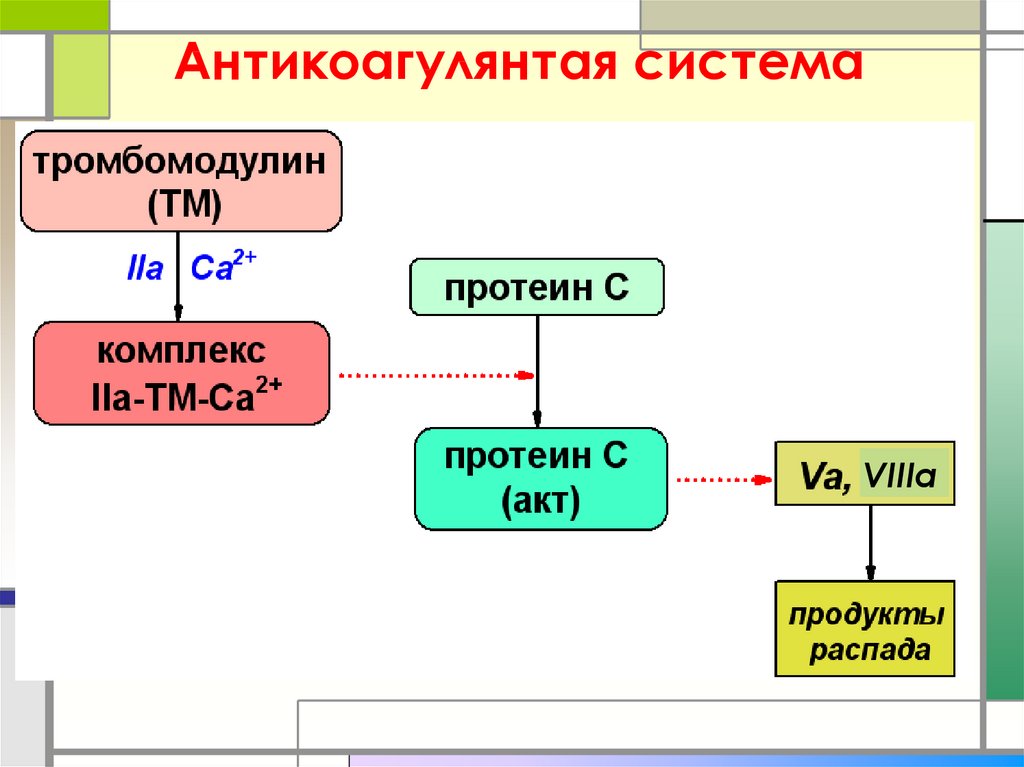
49. Антикоагулянтая система
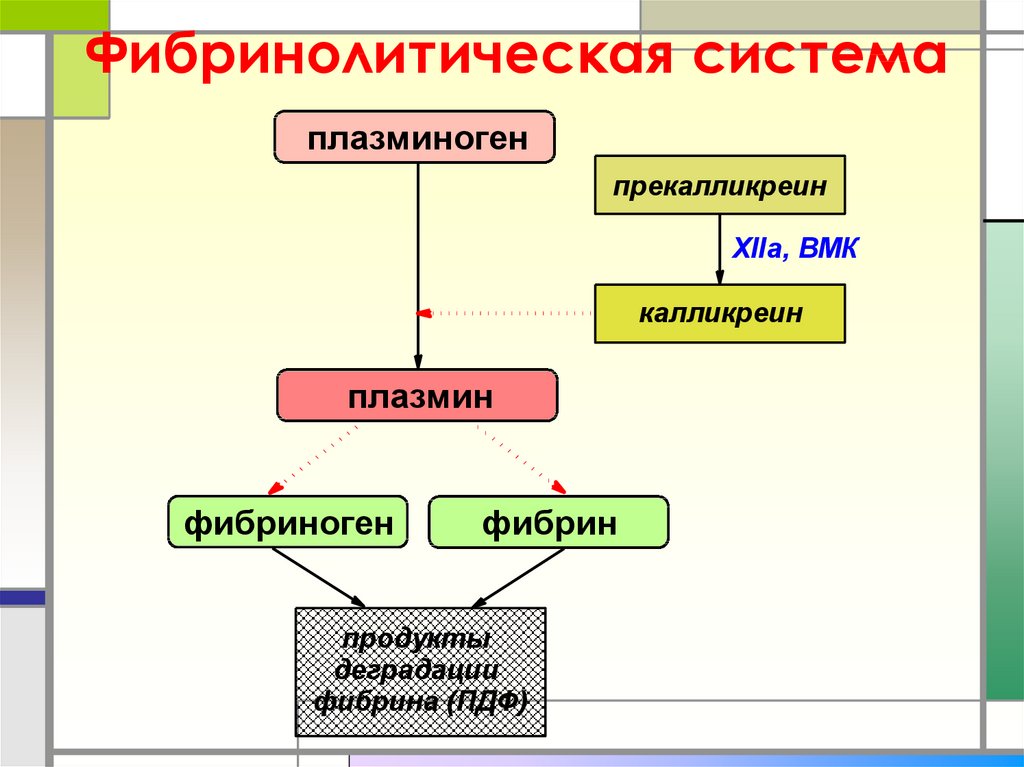
VIIIa50. Фибринолитическая система
плазминогенпрекалликреин
XIIa, ВМК
калликреин
плазмин
фибриноген
фибрин
продукты
деградации
фибрина (ПДФ)
51. Ингибиторы фибринолиза
□α2-антиплазмин□α2-макроглобулин
□Ингибиторы
активаторов
плазминогена
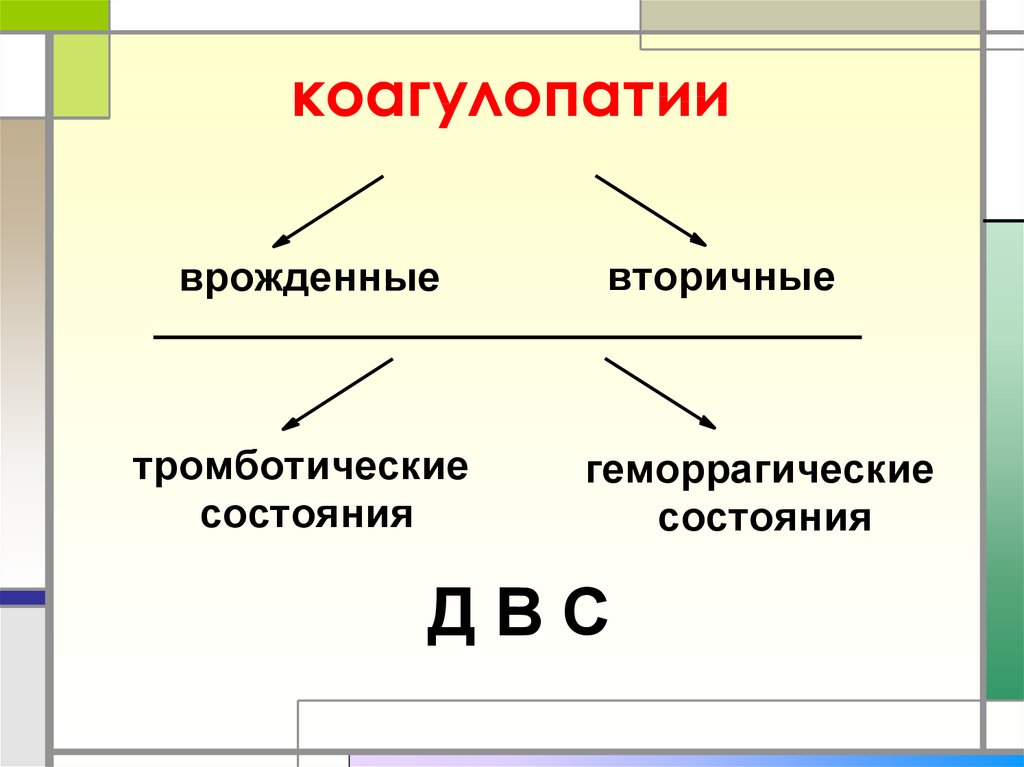
52. коагулопатии
врожденныетромботические
состояния
вторичные
геморрагические
состояния
ДВС
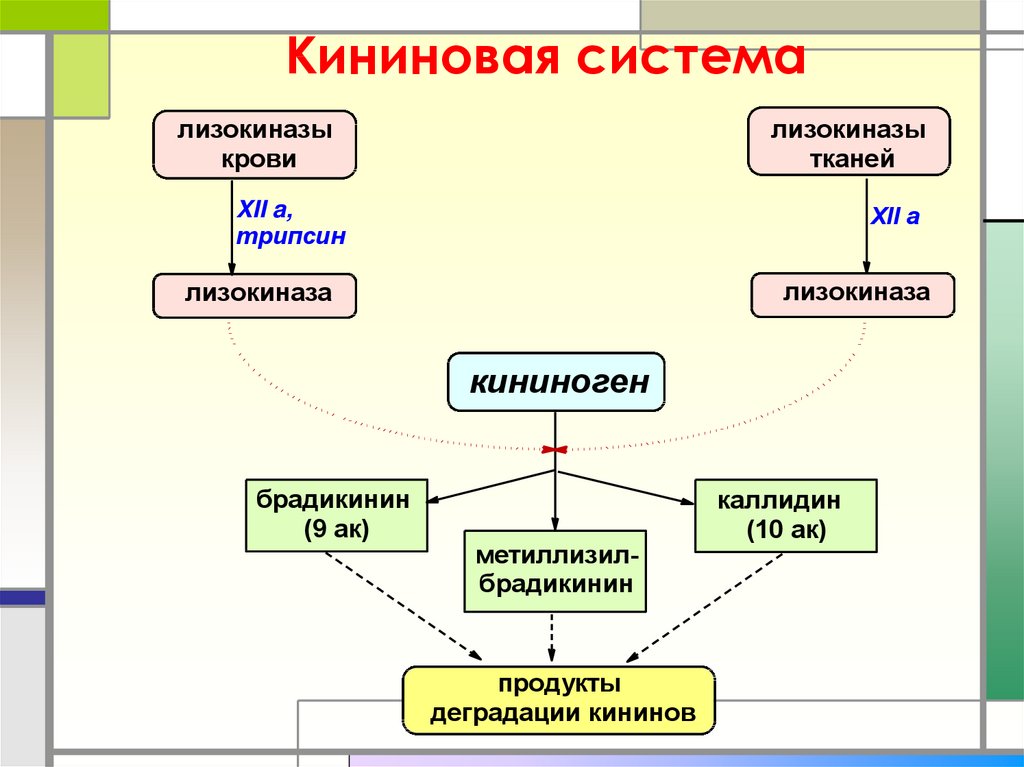
53. Кининовая система
лизокиназытканей
лизокиназы
крови
XII a,
трипсин
XII а
лизокиназа
лизокиназа
кининоген
брадикинин
(9 ак)
метиллизилбрадикинин
продукты
деградации кининов
каллидин
(10 ак)
54. Роль кининов
□ расширяют сосуды (гипотензивное действие,снижают АД),
□ сенсорное,
□ участвуют в воспалительных реакциях,
□ способствуют выходу лейкоцитов (лейкопедез),
□ сокращают гладкую мускулатуру бронхов,
□ регулируют деятельность экзокринных желез,
□ способствуют выработке простагландинов.
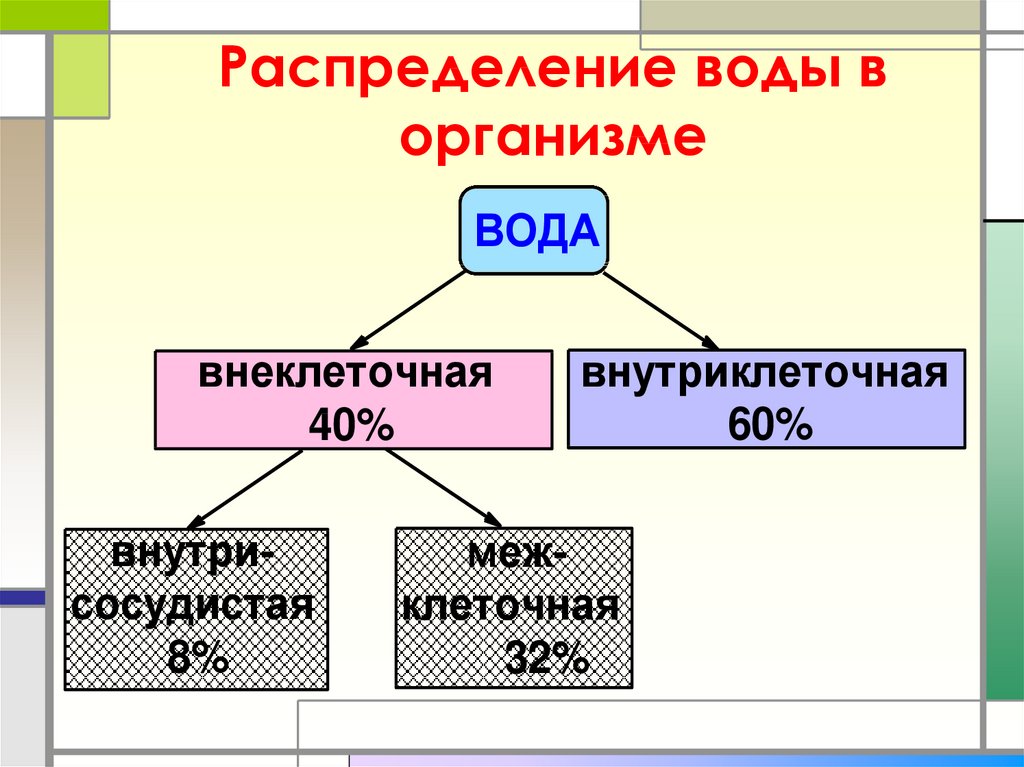
55. Распределение воды в организме
ВОДАвнеклеточная
40%
внутрисосудистая
8%
внутриклеточная
60%
межклеточная
32%
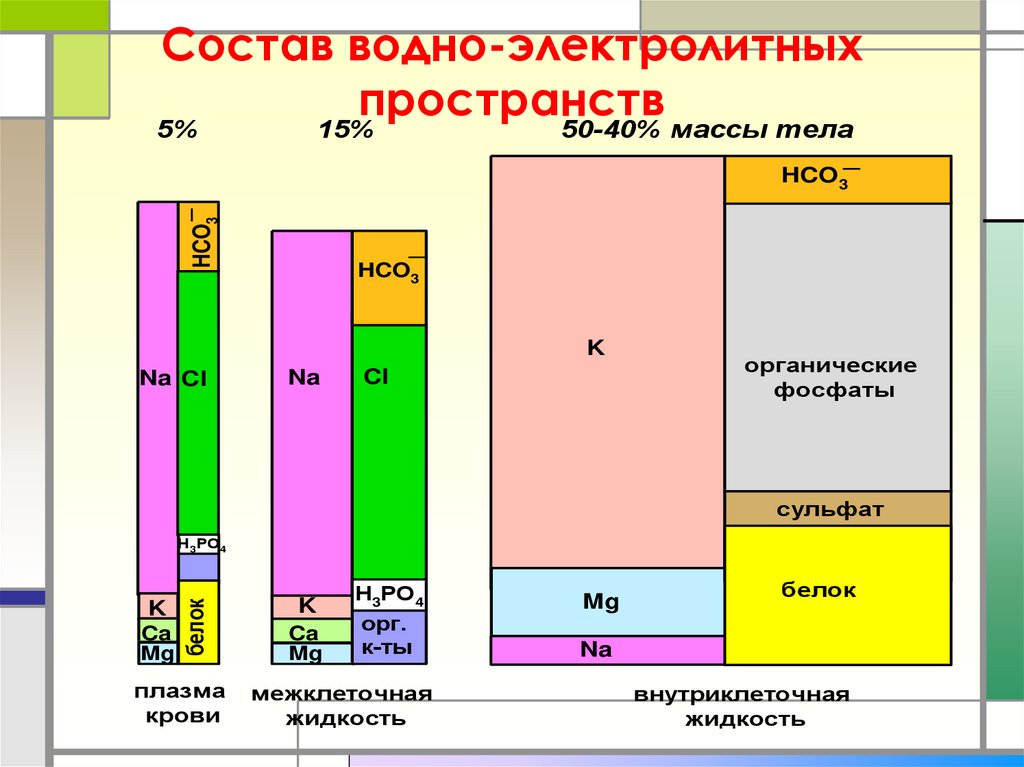
56. Состав водно-электролитных пространств
5%15%
50-40% массы тела
HCO3
HCO3
HCO3
K
Na Cl
Na
Cl
органические
фосфаты
сульфат
K
Ca
Mg
белок
Н3РО4
плазма
крови
K
Ca
Mg
Н3РО4
орг.
к-ты
межклеточная
жидкость
Mg
белок
Na
внутриклеточная
жидкость
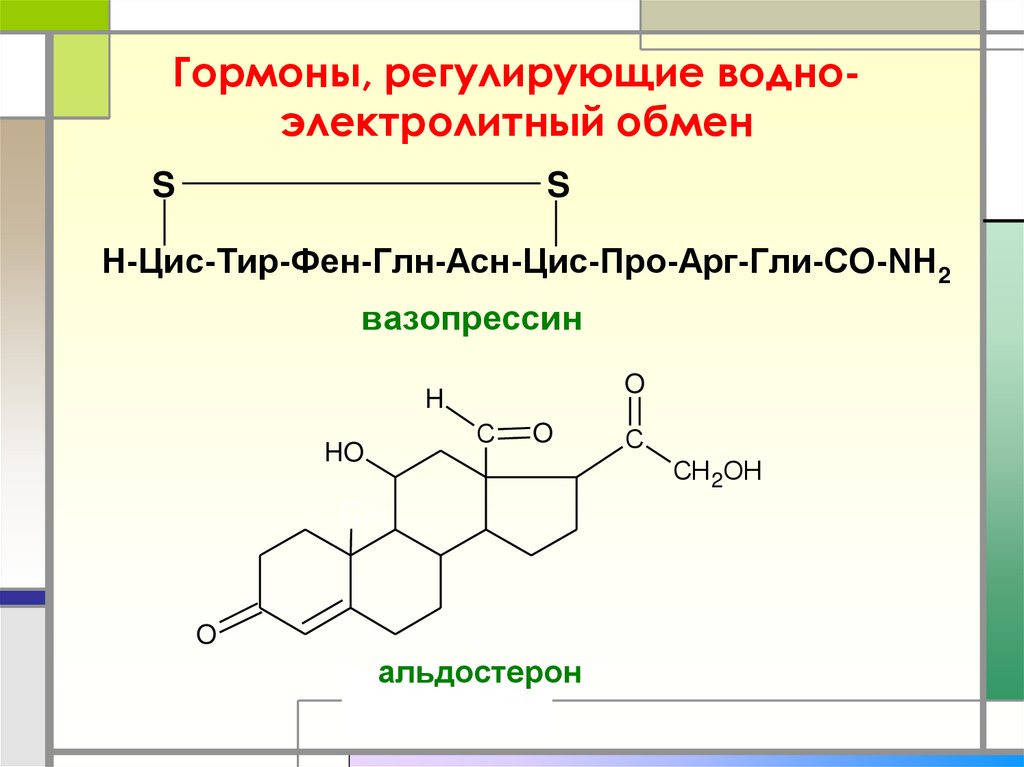
57. Гормоны, регулирующие водно-электролитный обмен
Гормоны, регулирующие водноэлектролитный обменS
S
Н-Цис-Тир-Фен-Глн-Асн-Цис-Про-Арг-Гли-СО-NH2
вазопрессин
O
H
С
HO
O
С
СН 2ОН
CH3
O
альдостерон
альдостерон
58. Ренин-ангеотензиновая система
59. Нарушения водно-электролитного обмена
Нарушения водноэлектролитного обменагипергидратация
(отёки)
дегидратация
(обезвожживание,
эксикоз)
60. Основные показатели КОС крови
□ БО (буферные основания)□ СБО
(сдвиг буферных оснований)
44-54 ммоль/л
± 2,5 ммоль/л
□ СБ (стандартный бикарбонат) 21-25 ммоль/л
□ рН
7,36-7,42
61. Механизмы поддержания КОС
□ Буферные системы□ Лёгочный механизм
□ Почечный механизм
62. Буферные системы
Н2СО31
NaНСО3
20
NaН2PО4
1
Na2НPО4
4
НHb
KHb
НHbO2
KHbO2
гемоглобиновая
бикарбонатная
фосфатная
Pt
COO
NH3+
белковая
63. Почечный механизм поддержания КОС
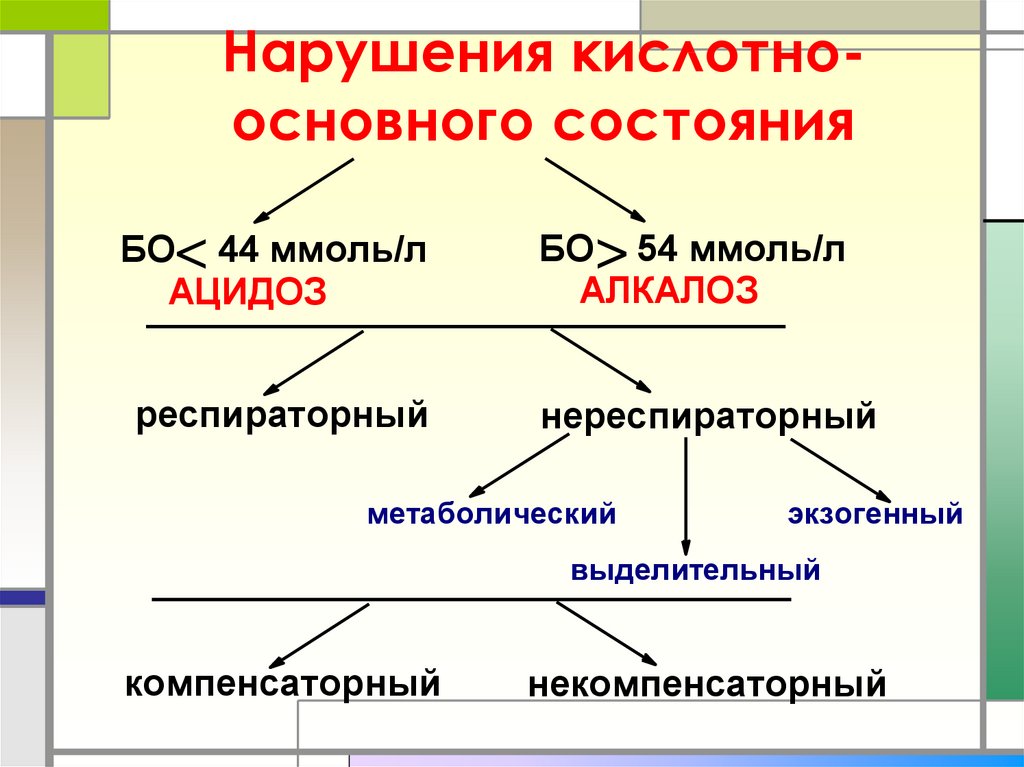
64. Нарушения кислотно-основного состояния
Нарушения кислотноосновного состоянияБО< 44 ммоль/л
АЦИДОЗ
респираторный
БО> 54 ммоль/л
АЛКАЛОЗ
нереспираторный
метаболический
экзогенный
выделительный
компенсаторный
некомпенсаторный
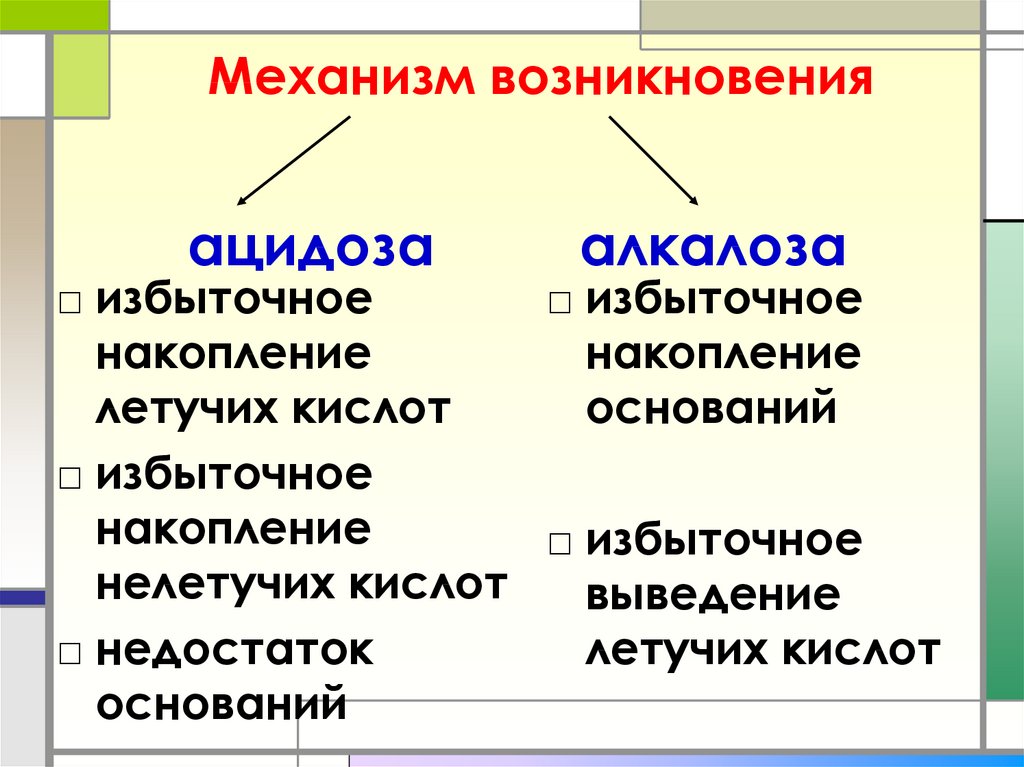
65. Механизм возникновения ацидоза алкалоза
□ избыточное□ избыточное
накопление
накопление
летучих кислот
оснований
□ избыточное
накопление
□ избыточное
нелетучих кислот
выведение
□ недостаток
летучих кислот
оснований
66. Причины нарушений КОС
□ нарушение дыхательнойфункции лёгких
□ нарушение выделительной
функции почек
□ метаболические нарушения в
тканях
□ экзогенные причины
(погрешности питания)




























 Биология
Биология