Похожие презентации:
Галогены
1. Галогены
ГАЛОГЕНЫВыполнили: Конохова Юлия, Цапиенко Анастасия 11а
2.
Период2
3
4
5
Фтор F
Хлор Cl
Бром Br
Иод I
3.
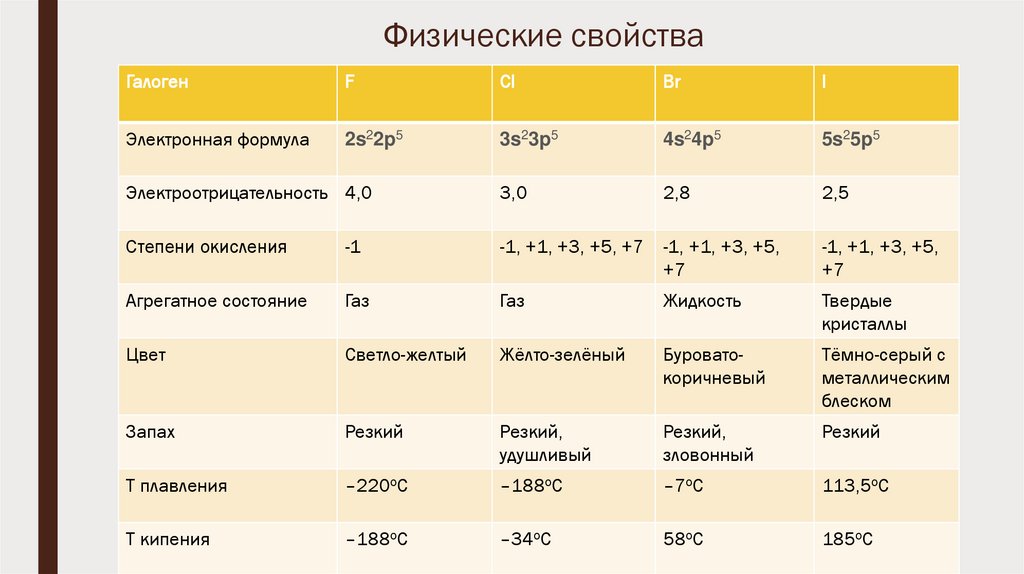
Физические свойстваГалоген
F
Cl
Br
I
Электронная формула
2s22p5
3s23p5
4s24p5
5s25p5
Электроотрицательность 4,0
3,0
2,8
2,5
Степени окисления
-1
-1, +1, +3, +5, +7 -1, +1, +3, +5,
+7
-1, +1, +3, +5,
+7
Агрегатное состояние
Газ
Газ
Жидкость
Твердые
кристаллы
Цвет
Светло-желтый
Жёлто-зелёный
Буроватокоричневый
Тёмно-серый с
металлическим
блеском
Запах
Резкий
Резкий,
удушливый
Резкий,
зловонный
Резкий
T плавления
–220оС
–188оС
–7оС
113,5оС
Т кипения
–188оС
–34оС
58оС
185оС
4. Химические свойства Взаимодействие с ксеноном 2F2 + Xe = XeF4. Взаимодействие с металлами 2М + nHal2 = 2MHaln. Взаимодействие с
водородом.Н2 + Hal2 = 2НHal.
5. Взаимодействие с неметаллами. 2P + 3Cl2 = 2PCl3; Si + 2F2 = SiF4. Взаимодействие с водой F2 + H2O = 2HF + O или 3F2 + 3H2O =
OF2 + 4HF + H2O2;Hal + H2O = HHal + HHalO.
Взаимодействие со щелочами
Cl2 + KOH = KClO + KCl (на холоде);
3Cl2 + 6KOH = KClO3 + 5KCl + 3Н2О (при нагревании).
6. Взаимодействие с сероводородом H2S + Br2 = S + 2HBr. Реакция замещения водорода в предельных углеводородах: CH4 + Cl2 = CH3Cl +
HCl.Реакция присоединения к непредельным углеводородам:
C2H4 + Cl2 = C2H4Cl2.
Взаимное замещение галогенов2KI + Br2 = 2KBr+ I2;
2HBr + Cl2 = 2HCl + Br2.






 Химия
Химия