Похожие презентации:
Кислоты. Определение кислот
1. Тема урока : Кислоты
2. План урока:
1.2.
3.
4.
5.
6.
Определение кислот
Кислоты в природе
Классификация кислот
Химические свойства кислот
Получение кислот
Применение кислот
3. 1. Определение кислот
Кислотами называются сложные вещества,образованные катионами водорода и анионами
кислотных остатков.
4. 2. Кислоты в природе
Кислотные дожди (азотная, серная кислоты)Кислоты
в пище (яблочная, щавелевая,
лимонная, молочная, масляная, кофейная и
другие)
«Химическое оружие» животных и растений.
Муравей
при
укусе
впрыскивает
содержащий
муравьиную
кислоту.
использует и крапива.
яд,
Ее
5.
Паук педипальпида стреляет в своих враговструйкой, состоящей из уксусной кислоты.
Плоские
тысяченожки
используют
яд
пострашнее – пары синильной кислоты.
Мухоморы используют иботеновую
кислоту и ее сложное соединение –
мусцимол.
Разрушение горных пород и образование почвы.
Лишайники могут выделять кислоты,
способные превращать гранит в труху.
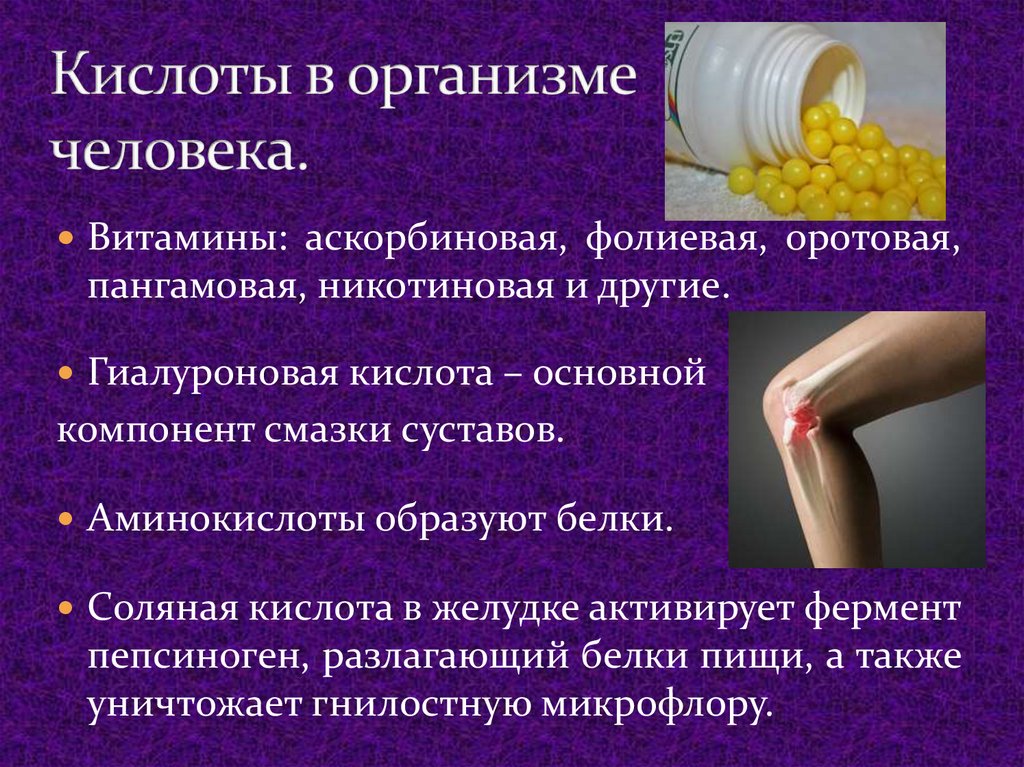
6. Кислоты в организме человека.
Витамины: аскорбиновая, фолиевая, оротовая,пангамовая, никотиновая и другие.
Гиалуроновая кислота – основной
компонент смазки суставов.
Аминокислоты образуют белки.
Соляная кислота в желудке активирует фермент
пепсиноген, разлагающий белки пищи, а также
уничтожает гнилостную микрофлору.
7. 3. Классификация кислот:
По составу:1. Кислородосодержащие: НNO3, H2SO3;
2. Бескислородные: HCl, H2S.
По
основности:
(основность
определяется числом катионов,
образуются при диссоциации).
1. Одноосновные: HBr, HNO2;
2. Двухосновные: H2S, H2SO4;
3. Многоосновные: H3PO4.
кислоты
которые
8. 4. Химические свойства кислот:
I. Взаимодействие с металлами,расположенными в электрохимическом ряду
напряжений металлов до водорода.
2HCI + Zn = ZnCI2 + H2
HCI + Cu = реакция не идет!
9.
II. Взаимодействие с основными оксидами.2 HCl + BaO = BaCI2 + H2O
10.
III. Взаимодействие с растворимыми инерастворимыми основаниями.
Это реакции нейтрализации.
HNO3 + NaOH = NaNO3 + H2O
2HNO3 + Cu(OH)2 = Cu(NO3)2 + 2H2O
11.
IV. Взаимодействие с солямиСильная кислота способна вытеснить слабую
кислоту даже из нерастворимой соли.
2HCI + Na2S = 2NaCI + H2S
12.
13. Получение.
1)Кислородосодержащие получают при
взаимодействии оксидов неметаллов с водой:
SO3 H 2O
H 2 SO4
N 2O5 H 2O 2 HNO3
Na2 SiO3 H 2 SO4 Na2 SO4 H 2 SiO3
2) Бескислородные:
H 2 Cl2 2HCl хлороводород
Затем растворяют в воде и получают соляную
кислоту
14. Применение кислот
Соляная кислотаДля растворения окалины и ржавчины при
никелировании, хромировании, цинковании и т.п.
стальных и чугунных изделий
Для снятия накипи в паровых котлах
Плавиковая кислота HF.
Пропитывают древесину для
предохранения от термитов и других
насекомых.
15.
Серная кислотаДля производства фосфорных и азотных
удобрений
В производстве взрывчатых веществ
Искусственных волокон
Красителей
Пластмасс
Заливка аккумуляторов
16.
Азотная кислотаПроизводство азотных удобрений
Взрывчатых веществ
Лекарственных веществ
Красители
Пластмассы
Искусственные волокна
17. Закрепление
Задание 1.Напишите формулы и дайте характеристику
кислотам на основе их классификации:
кремниевая кислота, плавиковая кислота.
Задание 2.
С какими веществами будет реагировать
фосфорная кислота: К, SO2, Na2SO4, Na2CO3, MgO,
Ag, Ba(OH)2.
Проверьте себя, а потом смотрите ответ!
18. Ответы
Задание 1.H2SiO3 – кислородсодержащая, двухосновная,
нерастворимая, слабая
HF – бескислородная, одноосновная,
растворимая, слабая
Задание 2.
6 K 2 H 3 PO4 2 K 3 PO4 3H 2
3 Na2CO3 2 H 3 PO4 2 Na3 PO4 3CO2 2 H 2O
2 H 3 PO4 3MgО Mg3 ( PO4 ) 2 3H 2O
3Ba(OH ) 2 2 H 3 PO4 Ba3 ( PO4 ) 2 6 H 2O

















 Химия
Химия








