Похожие презентации:
Спирты (карбинолы)
1.
МОДУЛЬ 41
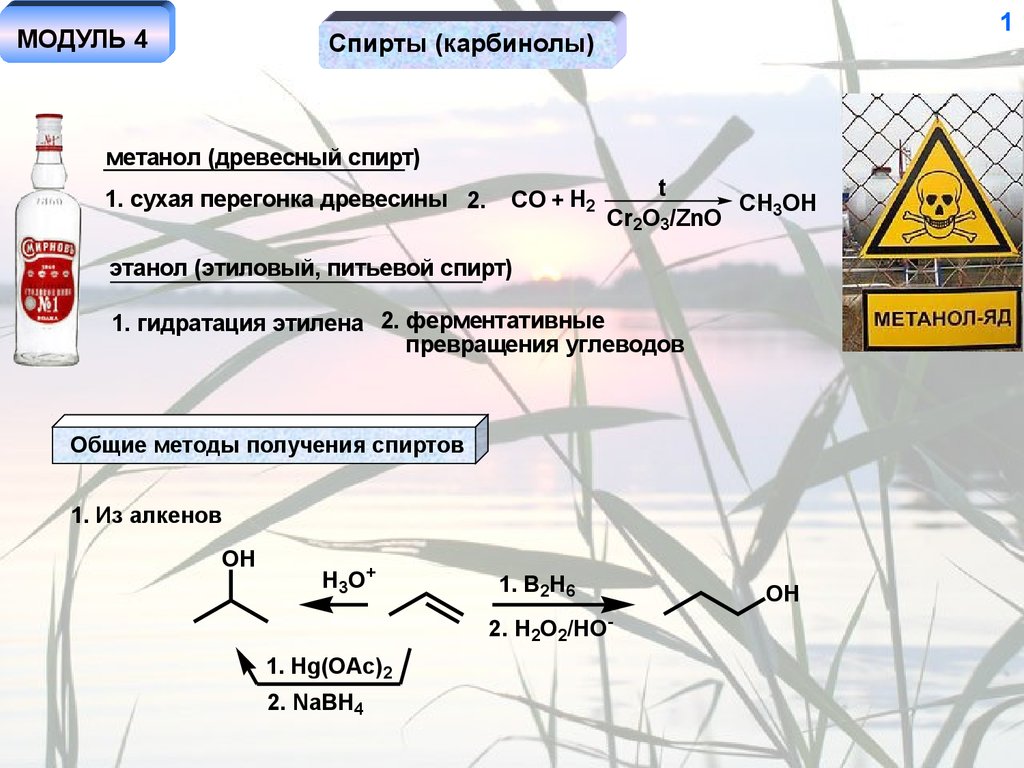
Спирты (карбинолы)
метанол (древесный спирт)
1. сухая перегонка древесины 2.
CO + H2
t
CH3OH
Cr2O3/ZnO
этанол (этиловый, питьевой спирт)
1. гидратация этилена 2. ферментативные
превращения углеводов
Общие методы получения спиртов
1. Из алкенов
OH
H3O+
1. B2H6
2. H2O2/HO-
1. Hg(OAc)2
2. NaBH4
OH
2.
22. Из алкилгалогенидов
RX
HO-
SN1 или SN2
ROH
3. С использованием металлоорганических соединений
ROH
O
R
OH
O2
RMgX
R"
R"
O
R'
R
OH
R'
3.
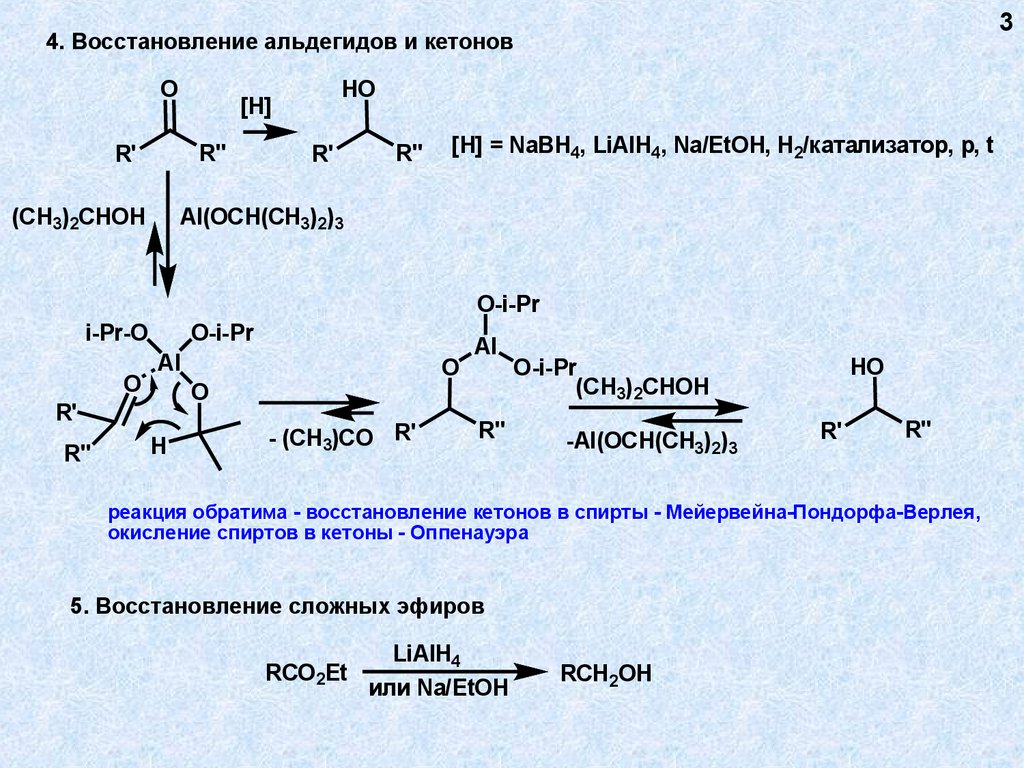
34. Восстановление альдегидов и кетонов
O
R"
R'
(CH3)2CHOH
HO
[H]
R'
R"
[H] = NaBH4, LiAlH4, Na/EtOH, H2/катализатор, p, t
Al(OCH(CH3)2)3
O-i-Pr
i-Pr-O
O
O-i-Pr
Al
O
R'
R"
O
H
- (CH3)CO R'
Al
R"
HO
O-i-Pr
(CH3)2CHOH
-Al(OCH(CH3)2)3
R'
R"
реакция обратима - восстановление кетонов в спирты - Мейервейна-Пондорфа-Верлея,
окисление спиртов в кетоны - Оппенауэра
5. Восстановление сложных эфиров
RCO2Et
LiAlH4
или Na/EtOH
RCH2OH
4.
Свойства спиртов4
1. Наличие подвижного протона – относительно высокая температура кипения,
растворимость в воде, кислотность.
RO- + H2O
Положение равновесия определяется устойчивостью аниона.
Алкил - донор по сравнению с протоном, поэтому гидроксиданион устойчивее алкоксид-аниона. Следовательно, вода более сильная кислота, чем спирты, а алкоксид-анионы более сильные основания, чем гидроксид-анион.
ROH + HO-
Mg
(RO)2Mg
ROH
PX3
Na
RONa
SOCl2
RCl
RX
X = Cl, Br
Образование сложных эфиров
эфиры азотной
кислоты - нитраты RONO2
эфиры азотистой
H2SO4
COCl2
(RO)2CO
эфиры угольной
кислоты - карбонаты
ксантогенаты R
HNO3
RONO кислоты - нитриты
NaNO2
ROH
CS2
HOS
O
-
S
H3O+
R'COCl
R'COOR
сложные эфиры
карбоновых кислот
p-TsCl
ROTs тозилаты
5.
ДегидратацияOH
5
+
H
t
Al2O3
300o
Реакции окисления
а. дегидрирование
CuO, t
RCH2OH
-Cu
RCHO
Cu, t
- H2
RCH2OH
реакции пригодны только для простейших спиртов
б. химическое окисление
OH
R
Cr
R'
R'
R
O
R
R'
альдегиды, кетоны.
для альдегидов возможно переокисление
в кислоты
превращается в Cr3+
O
Cr
HO
H
H+
- HOCrO2-
H
H
O
6+
O
O
сильный
акцептор
элиминирование Е2
относительно связи С-О
6.
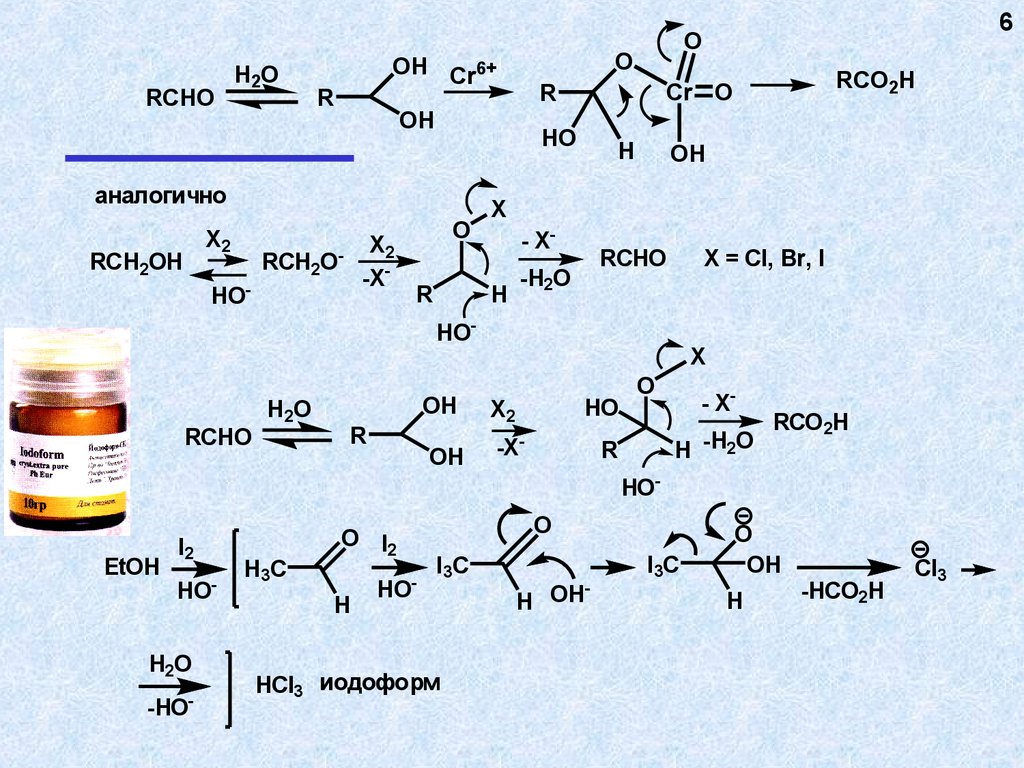
RCHOH2O
R
HO
RCH2OH
X2
-X-
RCH2O-
HO-
O
R
H
OH
X
- XH
RCHO
-H2O
X = Cl, Br, I
HO-
RCHO
H 2O
R
RCO2H
Cr O
R
OH
аналогично
X2
O
OH Cr6+
6
O
X
OH
X2
OH
-X-
HO
O
- XH -H2O
R
RCO2H
HOEtOH
I2
-
HO
H2O
-
-HO
H3C
O I2
H
HO-
O
I3C
HCI3 иодоформ
-
H OH
I3C
O
OH
H
-HCO2H
CI3
7.
Аналогично спирты окисляются в карбонильные соединения:а. KMnO4 / H+
б. CrO3 / H2SO4 (окисление по Джонсу)
в. CrO3 / пиридин / CH2Cl2 (окисление по Саррету, для веществ,
чувствительных к кислотам).
OH
O
MnO2
H2O
PhCH2OH
PhCHO
Качественные реакции на спирты:
спирт
K2Cr2O7
- Cr3+
карбонильные
соединения
наблюдается изменение окраски с оранжевой на зеленую
(реакция неспецифична)
проба Лукаса
спирт
ZnCl2, HCl
алкилгалогениды
H2O
наблюдается расслоение раствора,
механизм SN1 - реакция происходит быстро
в случае образования устойчивого катиона
7
8.
8Многоатомные спирты
OH
OH
OH
OH
OH
OH
этиленгликоль
OH
OH
OH
OH
OH
OH
глицерин
сорбит
Методы синтеза
1. Гидролиз дигалогенидов
Cl
Cl
HO-
OH
OH
HO
OH
HO
пентаэритрит
9.
92. Окисление алкенов
OH
O
Cl
Cl2
OH
OH
3. Пинаконы
O
Cl
-H+
Ca(OH)2
MnO4-
O
O2 / Ag
HOHCO2H
H2O2
(или RCO3H)
O
O
Mg / I2*
H3O+
бензол
*или Al / Hg, Zn / Hg
H3O+
OH
OH
O
H+
OH OH
димеризация
H+
пинакон
в отсутствие
органической
фазы
OH
+e
OH
H+
OH
H
H
H
восстановление по Клеменсену
10.
104. Из ацетилена
Cu+
OH
(CH2)4
OH
H2
CH2O
HO
OH Ni
5. Реакция Принса
H+
O
OCH2+
CH2O
-H+
OH
O
OH
H3O+
-CH2O
OH
Синтез глицерина
Cl2
300
OH
Cl
Cl Cl2
Cl
o
Cl
HO-
HO
OH
11.
OCOR1OCOR2
OCOR3
11
OH
H2O
HO
HO-
+ R1CO2- + R2CO2- + R3CO2-
OH
жиры
мыло
Синтез пентаэритрита
OH
CH3CHO
CH2O
HO
HO-
OH
HO
Свойства многоатомных спиртов
Все реакции, описанные для одноатомных спиртов, характерны и для многоатомных
(высокая растворимость в воде, высокая температура кипения, взаимодействие с
щелочными металлами, образование сложных эфиров, реакции окисления)
ONO2
ONO2
O2NO
ONO2
ONO2
нитроглицерин
ONO2
O2NO
тетранитрат пентаэритрита
12.
12Пинаколиновая перегруппировка
OH OH
OH OH2
+
H
-H2O
HO
O
HO
HO
-H+
более устойчивый катион
пинаколин
OH
Например:
OH2
± H+
OH
-H2O
OH
неустойчивый
катион
± H+
OH2
OH
OH
более устойчивый
катион
-H+
CHO
изомасляный
альдегид
OH
OH
-H2O
устойчивый
катион
13.
13Периодатное окисление
OH
O
HIO4
O
O
I
OH
O
O
OH
-HIO3
OsO4
CHO
H2O2, HIO4
CHO
Образование диоксаланов
OH
O
+
±
OH
H+
O
H2O
O
диоксалан
O
14.
14Методы получения
Простые эфиры
Метод Вильямсона
RONa + R'X
ROR'
SN2 или SN1
конкуренция с реакциями элиминирования!
PhBr
CH3I
CH3ONa
PhONa
жесткие условия, ароматическое нуклеофильное замещение
PhOCH3 происходит в мягких условиях
CH3ONa
OR
Cl
CH3 ONa
RO
NaBH4
HgOAc
Из алкенов
O
CH3I
Hg(OAc)2
ROH
ROH
H+
ONa
OR
HgOAc
меркурониевый
катион - невозможность
перегруппировок
карбокатион возможность
перегруппировок
15.
15Из алкинов
RONa
OR
t
Простые виниловые эфиры не могут
быть получены по методу Вильямсона
OR
ROH
H+, Hg2+
Из спиртов
H+
2 ROH
t
ROR
+
OH H
H
- H+
H
OH2
-H2O
HO
изомеризация!
H
O
O
-H+
образование катиона - изомеризация
+ побочные продукты!
16.
16OH
O
H+
диоксан (1,4-диоксан)
OH
O
Свойства простых эфиров:
Высокая инертность, низкая температура кипения, хорошая растворяющая способность
Гидролиз
ROR'
HX
t
HX - очень сильная кислота, анион - хороший нуклеофил!
X = Br, I
R'OH + RX
H+
H
O
R
X-
+
R' SN1
H
O
R
R'
R'OH + R
SN2 (реже)
X-
RX
R'OH + RX
17.
OHBr
t
Br
-CH3OH
SN1
OH
17
-
Br
è òî ëüêî òàê!
PhOCH3
HBr
t
Ph
H
O
PhOH + CH3Br
CH3 Br S 2
N
HBr
O
HBr
t
O
H
Br- S 2
N
HO
Br
Br
t
Br
Легкость гидролиза виниловых эфиров
(образование очень устойчивых катионов на всех стадиях)
H2O
H+
OR
OR
OR
H+
-H+
H
-ROH
H
OH
OH
-H+
H+
OR
OR
OH
OR
OH
+H2O
O
18.
18Эпоксиды
Синтез
O
RCO3H
HO
Cl2
Ca(OH)2
SN2
O
-H+
Cl
RCO3H
O
O
RCO3H
RCO3H
стереоспецифичность реакции
O
RCO3H
O
O
региоселективность процесса
19.
19Свойства
Эпоксид – циклический простой эфир, содержащий атом кислорода в напряженном
малом цикле. Вследствие этого, легко протекает раскрытие этого цикла при
взаимодействии с нуклеофильными реагентами (с электрофильным катализом и без).
В случае механизма SN2 направление атаки определяется
стерической доступностью.
O
O
Nu
NuOH
OH
OH
-
HO
O
LiAlH4
OH
RO
OR
-
RMgX
S N2
OH
R
20.
NuOH
Пример:
Ýëåêòðî ô èëüí û é êàòàëèç
H
O
OH
SN 1
Nu-
20
OH
Nu-
Nu
SN2
региоселективный синтез моноэфиров гликолей
O
CH3O-
OCH3
CH3OH
OH
OH
OH
H+
OCH3
Изомеризация алкенов через эпоксиды
O
RCO3H
H
H3C
транс-
O
CH3
H
H
H3 C
PPh3
конформация,
необходимая
для протекания
элиминирования
O
H
H3C
PPh3
H
CH3
-OPPh3
цис-
CH3
H
PPh3
21.
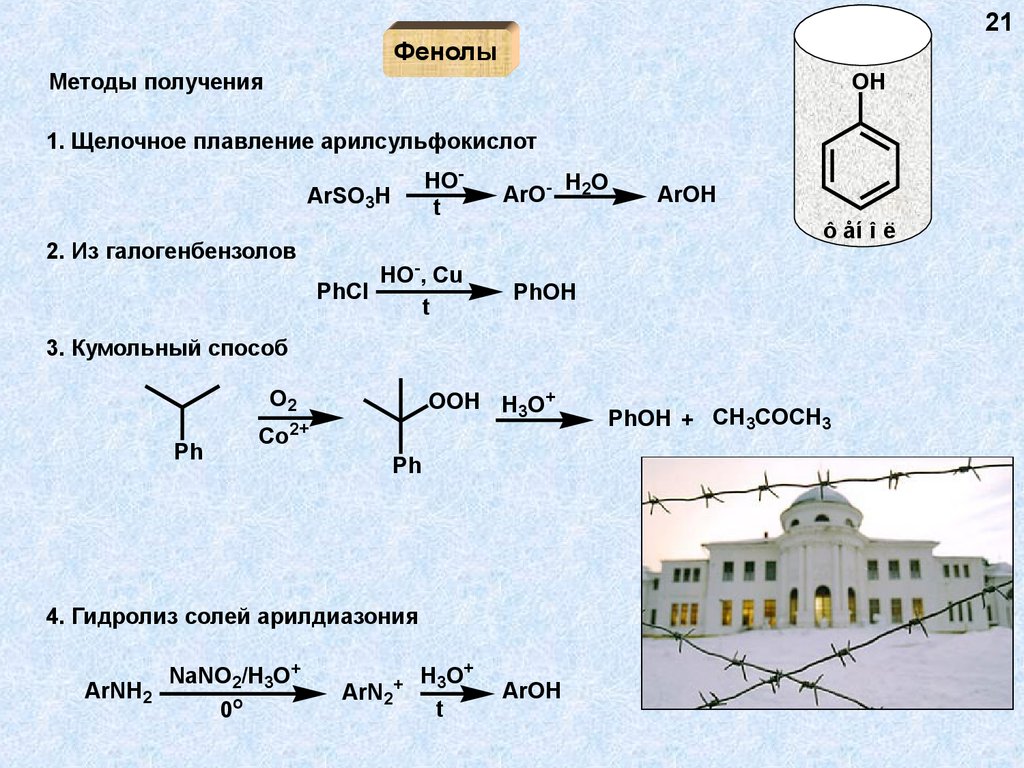
21Фенолы
Методы получения
OH
1. Щелочное плавление арилсульфокислот
HOt
ArSO3H
2. Из галогенбензолов
HO-, Cu
PhCl
t
ArO-
H2O
ArOH
ô åí î ë
PhOH
3. Кумольный способ
O2
OOH H3O+
2+
Co
Ph
Ph
4. Гидролиз солей арилдиазония
ArNH2
NaNO2/H3O+
o
0
ArN2
+
H3O+
t
ArOH
PhOH + CH3COCH3
22.
22Свойства фенолов
1. Повышенная кислотность (фенол - «карболовая кислота»)
OH
O
O
O
O
-H+
делокализация заряда
Акцепторные заместители (особенно в орто- и пара-положениях) повышают
устойчивость фенолят-аниона (кислотность фенола), донорные – понижают.
2. Реакции с электрофильными реагентами
E+
OH
+
E
E+
возможные направления электрофильной атаки - неподеленная
пара электронов атома кислорода (всегда в первую очередь),
орто- и пара-положения кольца (гидроксигруппа - ориентант
первого рода, сильный донор электронов по мезомерному
эффекту)
23.
Реакции по атому кислорода (кинетический контроль)Алкилирование
PhOCH3
(CH3O)2 SO2
PhOH
CH2N2
Ph
O
RX
PhOR
HO-
SN2
R
O
OH
R = CH3 - анизол, R = C2H5 - фенетол
R
200o
перегруппировка Кляйзена
O
R
R
если орто-положения заняты,
идет в пара-положение
синхронный процесс
Прямое алкилирование фенолов в кольцо не происходит ни в каких условиях!
23
24.
24Ацилирование
OH
AlCl3
RCOCl
PhOCOR
PhOH
t
или (RCO)2O
+
ROC
HO
COR
перегруппировка Фриса
OH
O
PhOH +
O
OH
AlCl3
O
O
O
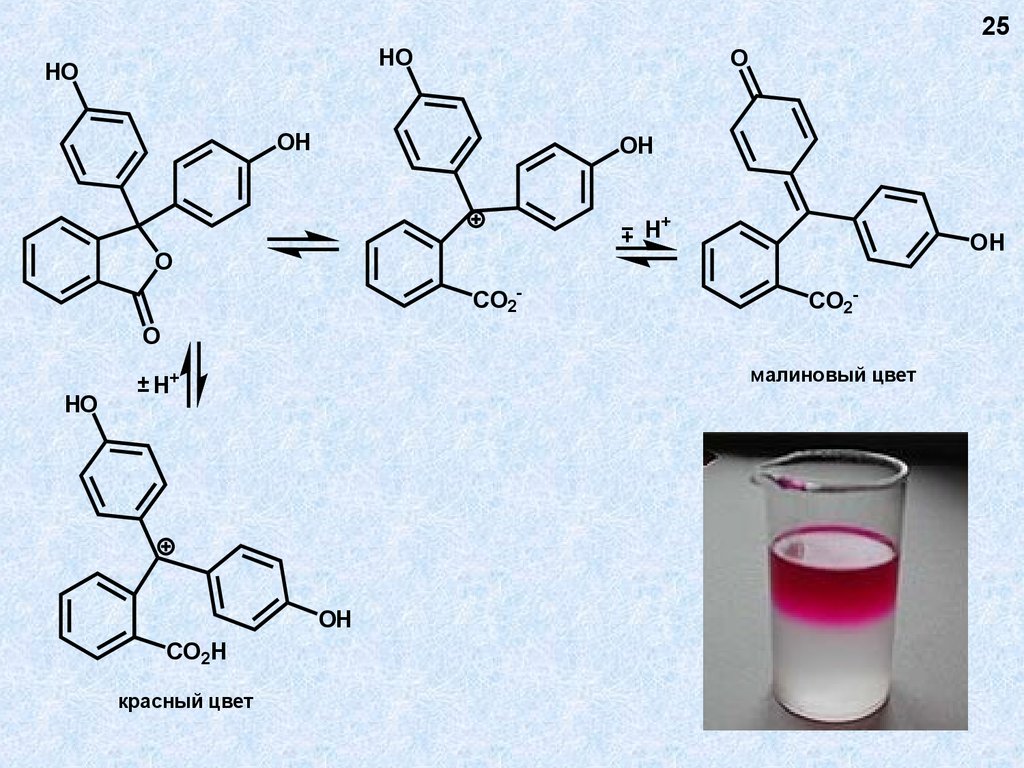
фенолфталеин
(пурген)
Триарилметановые
красители
25.
25HO
HO
O
OH
OH
H+
OH
±
O
CO2-
CO2-
O
HO
малиновый цвет
± H+
OH
CO2H
красный цвет
26.
26Реакции по бензольному кольцу
OH
OH
OH
O2N
HNO3 (разб.)
+
PhOH
Br2
Br
H2O
HNO3 (конц.)
H2SO4
NO2
Br
Br
продукт монозамещения
получить невозможно
OH
O2N
NO2
Cl2
CCl3NO2
хлорикрин
NO2
пикриновая
кислота
27.
27Гидроксигруппа –сильный донор по мезомерному эффекту,
обеспечивающий возможность реакций фенолов со слабыми электрофилами.
нитрозирование
PhOH
O
OH
OH
-H+
NaNO2
H3O+
H
H
NO
O
HON
NO
H
NO
OH
ON
нитрозофенол
Реймер-Тиман
Кольбе-Шмидт
OH
OH
CO2H
салициловая
кислота
CO2
HOt,p
PhOH
CHCl3
HO-
CHO
28.
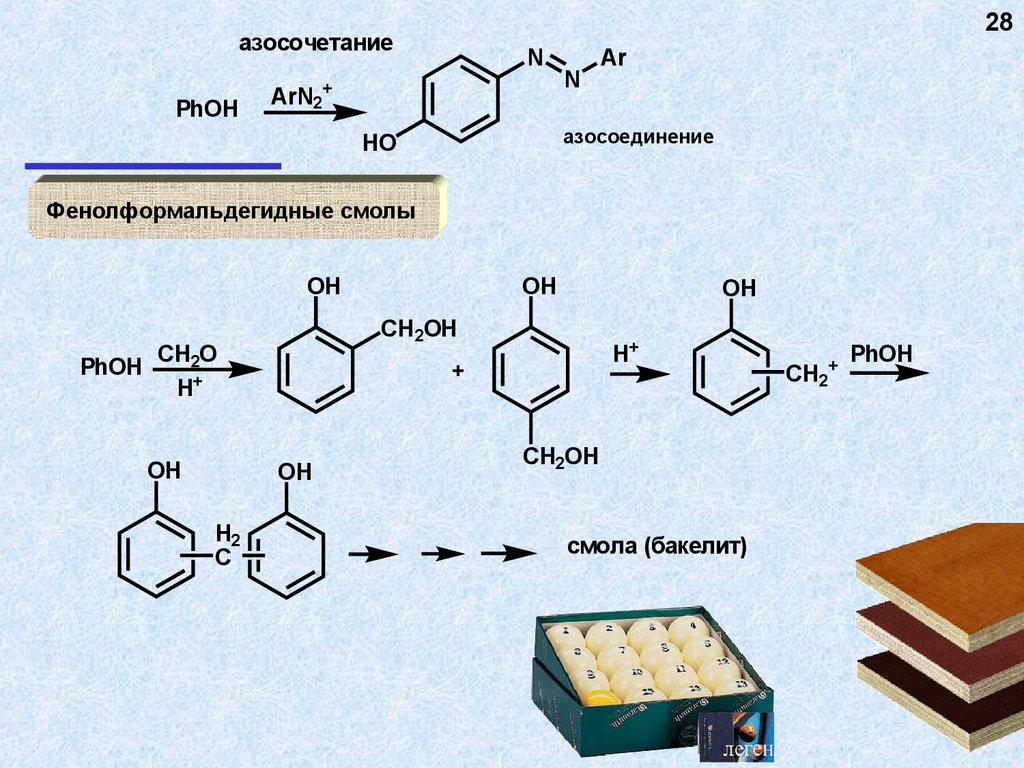
28азосочетание
PhOH
N
ArN2+
N
Ar
азосоединение
HO
Фенолформальдегидные смолы
OH
PhOH
H+
+
OH
H2
C
OH
CH2OH
CH2O
H+
OH
OH
CH2OH
смола (бакелит)
CH2+
PhOH
29.
29O
CrO3
H+
O
PhOH
OH
H2
кат.
бензохинон
Многоатомные фенолы
OH
OH
OH
OH
OH
пирокатехин
резорцин
OH
OH
HO
OH
OH
гидрохинон
пирогаллол
HO
OH
флороглюцин
30.
30Синтез
Cl
OH
-
HO
OH
SO3H
Cu+, t
OH
Cl
OH
OH
HOCu+, t
HOt
SO3H
OH
Cl
OH
Свойства
1. Легкость окисления
OH
HO
O
OH
CrO3
O
OH
+
Ag
O
O
31.
31O
O
O
±e
±H
±e
O
O
O
HO
семихинон
OH
O
O
O
H
+
HO
OH
+
H
O
O
O
хингидрон (КПЗ)
±
пара-бензохинон
e
хингидрон
±e
гидрохинон
32.
32Свойства
Таутомерные равновесия
OH
O
OH
OH
O
O
O
O
O
H+
±
OH
OH
OH
OH
OH
H+
атака по атому углерода
атака по атому кислорода
O
O
OH
OH
OH
O
OH
OH
33.
33Аналогично,
O
OH
HO
OH
O
HO
OH
O
O
OH
O
OH
OH
HO
O
O
NH2
NH3
OH
реакция Бухерера
NaHSO3
OH
NaHSO3
H3O+
34.
34OCH3
OCH3
NH2
+
1. NaNO2 / H3O , 0
OH
o
OH
гваякол
("коптильная жидкость")
OCH3
OCH3
крезолы ("креозот")
OCH3
1. POCl3 / ДМФА
2. H3O+
2. H3O+, t
о-анизидин
OH
вератрол
CHO
ванилин
35.
35Амины
CH3NH2
(CH3)2NH
(CH3)3N
метиламин
(первичный амин)
диметиламин
(вторичный амин)
триметиламин
(третичный амин)
сравни!
C2H5NH2
NH2
NH2
первичные амины
C2H5OH
этанол
(первичный спирт)
OH
пропанол-2
(вторичный спирт)
OH
2,2-диметипропанол
(третичный спирт)
36.
36Алифатические амины
Методы получения
1. Алкилирование аммиака
RNH3 X-
RX + NH3
RNH3 X-
NH3
NH3
R2NH + RX
R3NH XR3N + RX
RNH2 + NH4X
R2NH2 X-
RNH2 + RX
R2NH2 X-
SN2 или SN1 R = алкил,
Х = Cl, Br, I
NH3
R2NH + NH4X
R3NH XR3N + NH4X
R4N X-
По мере накопления алкильных заместителей
у атома азота сила нуклеофила увеличивается.
Поэтому остановить реакцию на стадии
продукта моноалкилирования затруднительно.
37.
372. Синтез Габриэля
O
O
N- K+
RX +
O
O
HO-
RX - алкилгалогенид
HO
OH
N
O
фталимидное
производное
CO2H
H
R
-HO-
O
HO-H2O
N
SN2
+
CO2-
RNH2
или N2H4, t
RX
RNH2
только
первичный амин
HO-
CO2
OH
O
HO-
CO2-
R
HO-, t
NHR
OH
O
H
NHR
±
38.
383. Восстановление нитрилов
H3O
RCHO
H2 Pd/C
H
+
R
RCH2NH2
LiAlH4 (1экв.)*
N-
*обратный порядок прибавления
RCN
1. LiAlH4 (изб.)
2. H2O
RCH2NH2
B2H6
RCH2NH2 не затрагивается NO2, CO2R
4. Восстановительное аминирование
O
O
NH3, H2
NH
Ni
NH3 HCO2H
NH3
NaBH3CN
NH2
реакция Лейкарта
NH2
N
H2
Ni
HN
39.
394а. Восстановительное аминирование в две стадии
O
HO
RNH2
NHR
H+
R
N
H+
-H2O
NaBH4
(LiAlH4)
HN
R
вторичный
амин
имин
R'X
R
N
R'
X-
R
NaBH4
(LiAlH4)
N
R'
третичный
амин
иминиевая соль
5. Восстановление амидов
O
R
RCOCl
NH2
NH3
O
R
NH2
RCOCl
дальнейшая реакция не идет - пара
электронов на атоме азота находится
в сопряжении с карбонильной группой
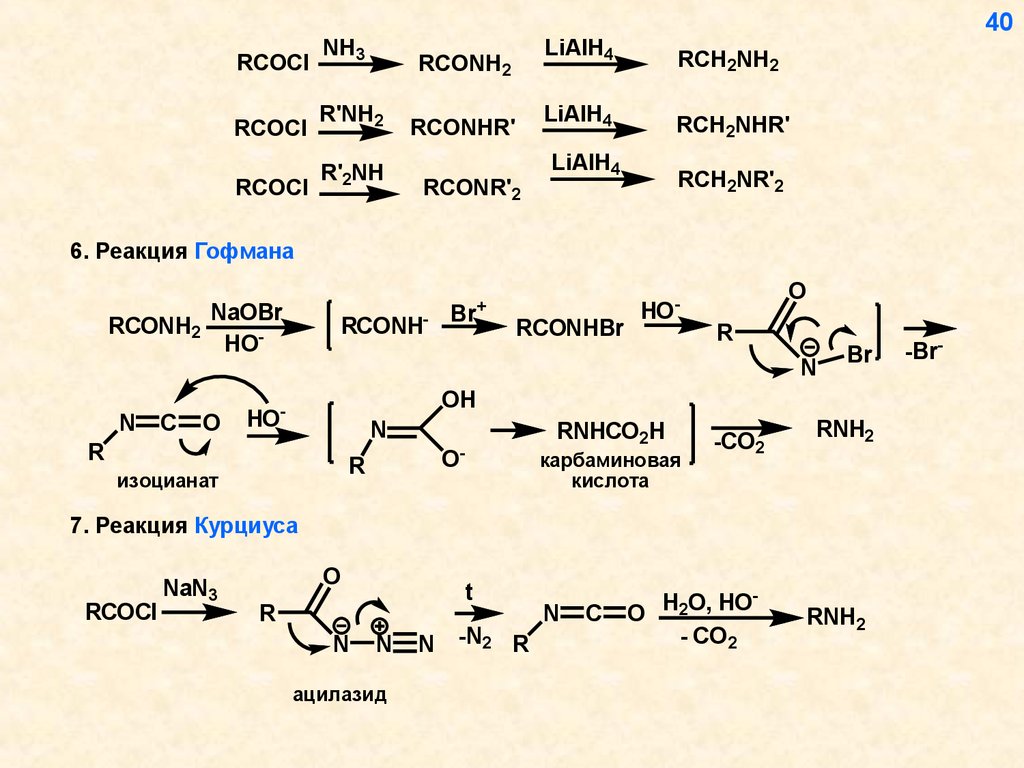
40.
RCOClNH3
RCOCl
R'NH2
RCOCl
R'2NH
RCONH2
RCONHR'
RCONR'2
40
LiAlH4
RCH2NH2
LiAlH4
RCH2NHR'
LiAlH4
RCH2NR'2
6. Реакция Гофмана
RCONH2
N
C
NaOBr
HOO
RCONH-
Br
+
O
-
RCONHBr
HO
R
N
Br
OH
HO-
N
R
O-
R
изоцианат
RNHCO2H
карбаминовая
кислота
-CO2
RNH2
7. Реакция Курциуса
RCOCl
NaN3
O
t
R
N
N
ацилазид
N
-N2 R
N
C
H
O,
HO
2
O
- CO2
RNH2
-Br-
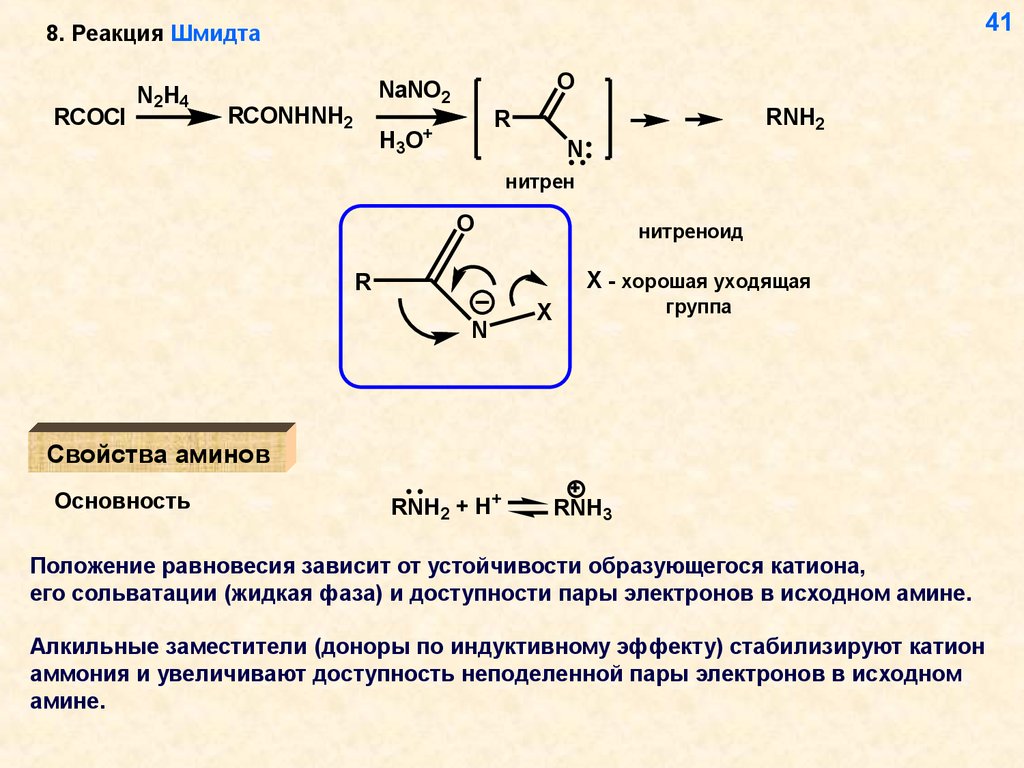
41.
418. Реакция Шмидта
RCOCl
N2H4
O
NaNO2
RCONHNH2
H3
RNH2
R
O+
N
нитрен
O
нитреноид
X - хорошая уходящая
R
N
группа
X
Свойства аминов
Основность
RNH2 + H+
RNH3
Положение равновесия зависит от устойчивости образующегося катиона,
его сольватации (жидкая фаза) и доступности пары электронов в исходном амине.
Алкильные заместители (доноры по индуктивному эффекту) стабилизируют катион
аммония и увеличивают доступность неподеленной пары электронов в исходном
амине.
42.
42Ряд основности
газовая фаза:
NH3 < CH3NH2 < (CH3)2NH < (CH3)3N
жидкая фаза: NH3 < CH3NH2 < (CH3)3N < (CH3)2NH
различный порядок связан с плохой сольватацией объемного
триметиламмонийного катиона
Ароматические амины
NH2
NH2
NH2
NH2
NH2
NH3
+ H+
В ароматическом амине пара электронов находится в сопряжении с фенильной
группой. Протонирование это сопряжение нарушает, что энергетически невыгодно.
Поэтому основность ароматических аминов ниже, чем алифатических.
Донорные заместители, особенно в орто/пара-положениях, повышают основность,
акцепторные – понижают.
43.
43Кислотность аминов
RNH2
-H+
RNH-
Ряд кислотности противоположен ряду основности:
акцепторные заместители стабилизируют анион, донорные – дестабилизируют.
Реакции с электрофильными реагентами
1. Алкилирование
RNH2 + RX
R2NH
RX
RX
R3N
R4N X- реакция неселективная
2. Ацилирование
RNH3 R'CO2t
R'CO2H
RNH2
R'COCl
-HCl
O
HN
R
R'CO2CH3
R'
R'COCl
44.
R2NHR'CONR2
-HCl
R'COCl
R3N
44
R'COCl
O
R'
-
NR3
Cl
H2O
R3NH R'CO2-
молекула содержит очень хорошую уходящую группу и потому неустойчива.
При действии хлорид-аниона она превращается в смесь исходных соединений.
Присутствие следов воды вызывает мгновеный гидролиз
Использование реакции ацилирования (тозилирования) для разделения смеси аминов
устойчивый анион (Ts - сильный акцептор)
RNH2
+
TsCl
RNHTs
TsCl
R2NTs
R2NH
+
TsCl
R3N
RNHTs
обработка разбавленным R NTs
2
раствором кислоты
+ -
R3NH X
-
RNHTs
R2NTs
HO , t
-
-TsO
HO-, t
-TsO-
RNH2
R2NH
HO-
R3N
HO-
RNTs растворим
в воде
HO-
нерастворим
в воде
45.
45Нитрозирование
NaNO2+ H3O+ = HNO2 = NO+ (электрофил)
R = алкил
R3N
R2NH
NaNO2
H3O
смесь продуктов (распад связи С-N)
+
NaNO2
H3O+
N
R2N-NO
R
N
N
R
N
H2
OH2
-H2O
N
NO
-H+
R
N
N
RNHNO
R
затрудненность вращения
вокруг связи N-N
R
N
алифатическая соль
диазония - неустойчива!
N
O
N
N
N-нитрозоамины - канцерогены,
апротонные диполярные растворители
RNH2 NaNO2
H3O+
O
N
-N2
N
R+
OH H+
превращения
карбокатиона
46.
46Превращение аминов в алкены
Cl
N(CH3)3
Ag2O (влаж.)
N(CH3)3
t
>
(CH3)3N
HO-
Cl-
Гофман
H2O2
N
N
O
t
+
~3:2
син-элиминирование, Коуп
Диамины
NH2
(CH2)4
NH2
кадаверин
CN
H2
Ni
NH3 (изб.)
NaCN
CN
NH2
Cl
Cl
H2 N(CH2)5NH2 путресцин ("трупный яд")
NH2
47.
47Ароматические амины
Методы получения
Восстановление нитросоединений
[H]
PhNH2
PhNO2
[H] = Fe/H3O+; Sn/H3O+; H2/катализатор (Pt, Pd, Ni); N2H4/Ni; H2S (Зинин)
NO2
NO2
NaHS
NO2 H O
2
NH2
Из галогенбензолов
PhCl
NaNH2
t
PhNH2
Реакция Гофмана
CONH2
NH2
NaOBr
48.
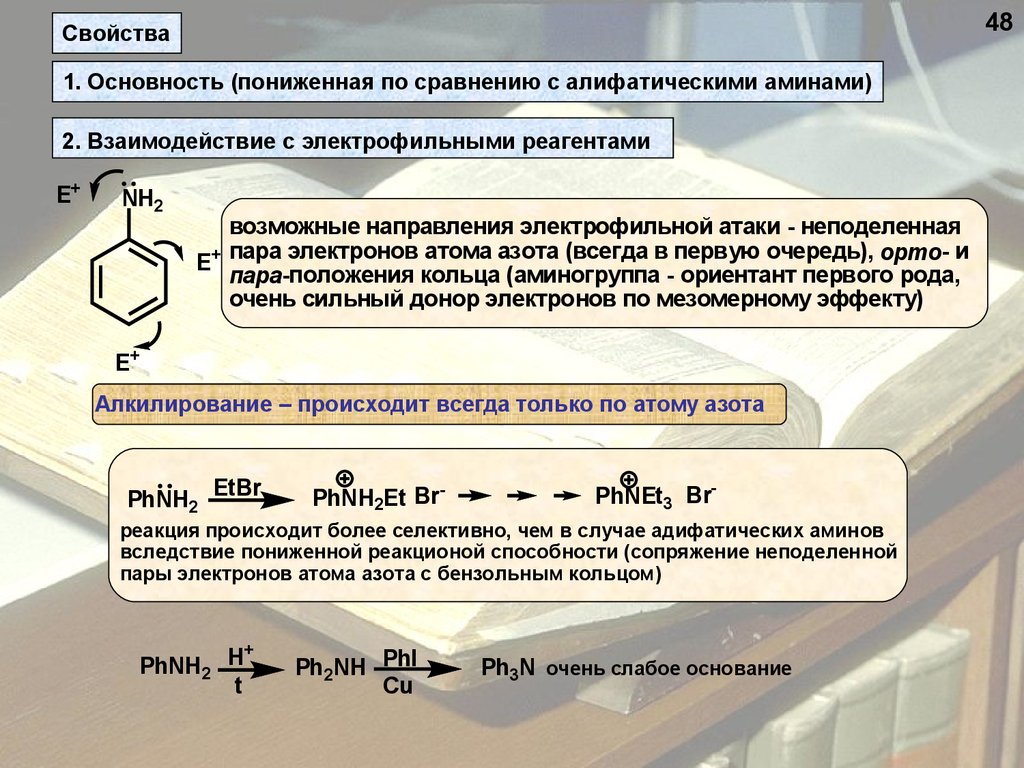
48Свойства
1. Основность (пониженная по сравнению с алифатическими аминами)
2. Взаимодействие с электрофильными реагентами
E+
NH2
возможные направления электрофильной атаки - неподеленная
E+ пара электронов атома азота (всегда в первую очередь), орто- и
пара-положения кольца (аминогруппа - ориентант первого рода,
очень сильный донор электронов по мезомерному эффекту)
E+
Алкилирование – происходит всегда только по атому азота
PhNH2
EtBr
PhNH2Et Br-
PhNEt3 Br-
реакция происходит более селективно, чем в случае адифатических аминов
вследствие пониженной реакционой способности (сопряжение неподеленной
пары электронов атома азота с бензольным кольцом)
+
PhNH2 H
t
Ph2NH PhI
Cu
Ph3N очень слабое основание
49.
49Ацилирование
PhNH2
RCOCl
или (RCO)2O
PhNHCOR
R = CH3 - ацетанилид
R
O
HN
RCOCl
HN
R
R
O
HN
O
ацетамидная группа - донор электронов
по мезомерному эффекту,
но более слабый, чем аминогруппа
Сульфирование
NH3 HSO4-
NH2
SO3H
100o
PhNH3 HSO4спекание
180o
олеум
t
180o
SO3H
SO3 H
метаниловая
кислота
NH2
HO3S
NH2
сульфаниловая
кислота
50.
50NH3
NH2
SO3
SO3H
NHCOCH3
PhNHCOCH3
ClSO3H
NHCOCH3
H3O+
NH3
O
S
Cl
O
O
NH2
H2N
S
O
O
S
O
H2N
белый стрептоцид
первый сульфамидный препарат
(антимикробное действие)
51.
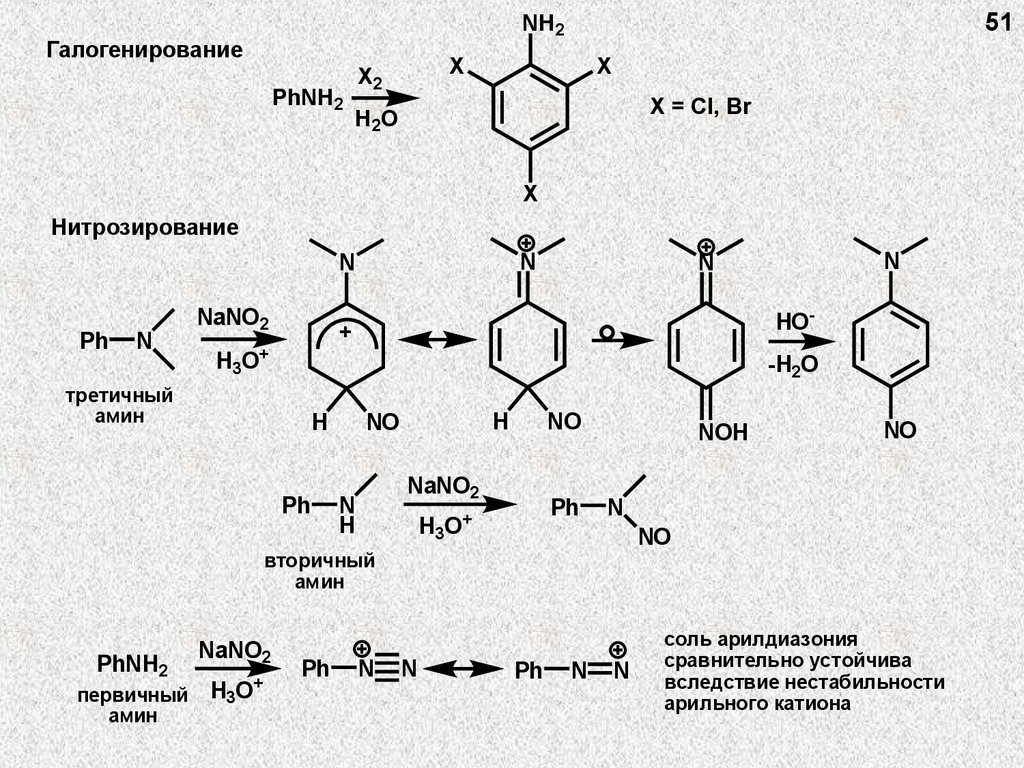
51NH2
Галогенирование
PhNH2
X
X2
X
X = Cl, Br
H2O
X
Нитрозирование
N
N
Ph
N
NaNO2
HO-
+
H3O+
-H2O
третичный
амин
H
Ph
H
NO
NO
NaNO2
N
H
Ph
H3O+
NOH
PhNH2
+
первичный H3O
амин
Ph
N
N
NO
N
NO
вторичный
амин
NaNO2
N
N
Ph
N
N
соль арилдиазония
сравнительно устойчива
вследствие нестабильности
арильного катиона
52.
52Реакции солей диазония
Реакции с выделением азота
ArX
Х = Br, Cl (реакция Зандмейера)
HX CuX
ArNH2
NaNO2
ArN2+
H3O+, 0o
HBF4
NaI
ArN2+BF4-
t
ArF
реакция Больца-Шимана
ArI
ArOH
ArCN
CuCN
ArN3
CuNO2
ArNO2
N3 -
H3O+
ArN2+
HX
Cu
ArX Х = Br, Cl (реакция Гаттермана)
EtOH (или H3PO2)
ArH
53.
53Синтез несимметричных биарилов
HO+
PhN2 X
Ph Ar Гомберг-Бахман-Хей
ArH
t
ArH
-N2 -X
радикальный процесс
-H
активность субстрата: PhNO2 > PhCl >> PhCH3 > PhH
преимущественное направление реакции - пара- и орто-
Ph
Реакции без выделения азота
ArN2+
NaHSO3
ArNHNH2
Азосочетание
SO3H
N2+
Ph
N
N
+
-
азосоставляющая
O3S
диазосоставляющая
N
N
метилоранж (гелиантин) - кислотноосновной индикатор, ранее использовался
для крашения шелка
азосоединение
54.
54В качестве азосоставляющей может быть использовано только ароматическое
соединение, содержащее сильный донорный заместитель – амино, гидрокси, в
некоторых случаях – алкоксигруппу.
Реакция происходит почти исключительно в пара-положение; если оно занято,
то в орто-положение
Метиловый оранжевый – моноазокраситель (одна азогруппа)
H2NO2S
NH2
N
Герхард Домагк – нобелевская премия
по физиологии и медицине, 1939 г
N
пронтозил(красный стрептоцид) моноазокраситель
NH2
NH2
N
SO3Na
N
N
N
NaO3S
конго-красный
бис-азокраситель
H2N
55.
55Окисление ароматических аминов
O
Ph
N
N
Ph
H2O2
PhNH2
RCO3H
PhNO
PhNO2
азоксибензол
CrO42- или MnO4 -
N
Ph
N
H
N
NH2
N n
H
Ph
"анилиновый черный"













































 Химия
Химия








