Похожие презентации:
Удельная теплоемкость газа
1.
Теплоемкости газов.Адиабатный процесс
2.
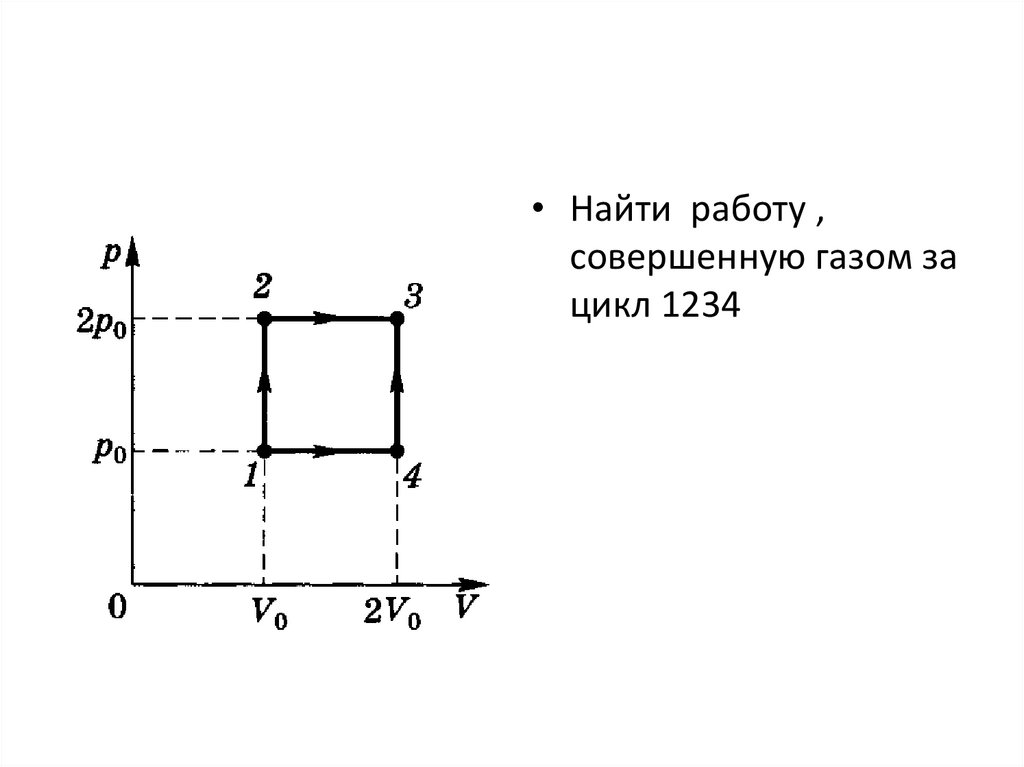
• Найти работу ,совершенную газом за
цикл 1234
3.
• Количество теплоты пропорциональномассе тела и изменению температуры. Но
для газов коэффициент
пропорциональности зависит от способа
изменения состояния газа:
QV cV m T
для изохорного процесса
Q p c p m T
для изобарного процесса
4.
QU
cV
m T m T
3R
cV
2M
5.
Степень свободы• -любое независимое движение, которое
может совершать тело.
• Для одноатомной молекулы i=3
• Для двухатомной молекулы i=5
• Для многоатомной молекулы i=6
6.
Закон равнораспределения• На каждую степень свободы приходится
1/2kT Дж
i
Ek kT
2
iR
cV
2M
7.
QU A
cp
m T
m T
iR
R i 2 R
cp
2M M
2 M
8.
Молярные теплоемкости• -теплоемкости газа в количестве 1 моль
• С=сМ
i
CV R
2
C p CV R
9.
• Адиабатный процесс – это модельтермодинамического процесса,
происходящего в системе без теплообмена с
окружающей средой.
• Линия на термодинамической диаграмме
состояний системы, изображающая
равновесный (обратимый) адиабатический
процесс, называется адиабатой
• Для этого процесса , Q = 0, А=-ΔU
• В случае одноатомного идеального газа
3
3
A R T ( p1V1 p2V2 )
2
2
10.
11.
12.
13.
Уравнение Пуассона• Коэффициент Пуассона
i 2
cV
i
cp
• Уравнение адиабатного процесса
pV const
TV
1
1
const
p
const
T


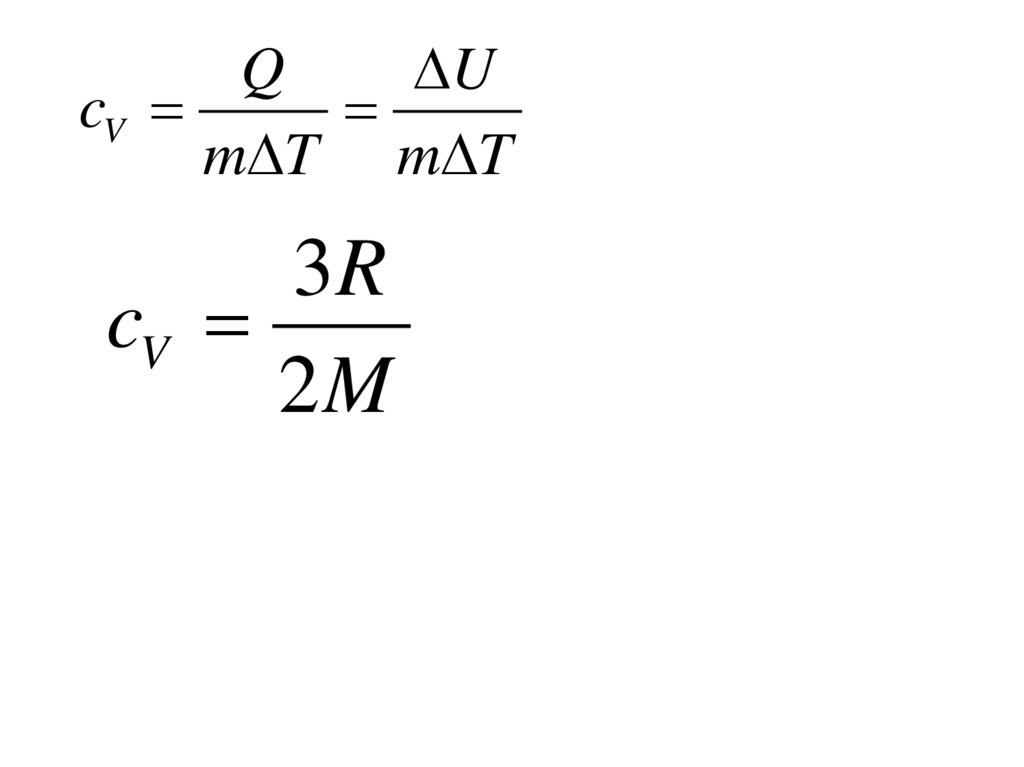








 Физика
Физика