Похожие презентации:
Скорость химической реакции. 9 класс
1.
Скорость химической реакции9 КЛАСС
2.
ТЕМА: ___________?3.
ТЕМА:СКОРОСТЬ ХИМИЧЕСКОЙ
РЕАКЦИИ
ЦЕЛЬ:
Узнать, что такое скорость химической
реакции и от чего она зависит ?
4.
НАШ ПУТЬ.5.
T6.
ИЗМЕНЕНИЕ КОНЦЕНТРАЦИИ ВЕЩЕСТВА ЗАЕДИНИЦУ ВРЕМЕНИ НАЗЫВАЕТСЯ
СКОРОСТЬЮ ХИМИЧЕСКОЙ РЕАКЦИИ
C2 – C1
C
V= ±
= ± t2 –t1
∆t
∆
V - скорость химической реакции
изменение молярной
∆C - концентрации
- временной интервал
∆t
моль/(л · с)
моль / л
с
7.
8.
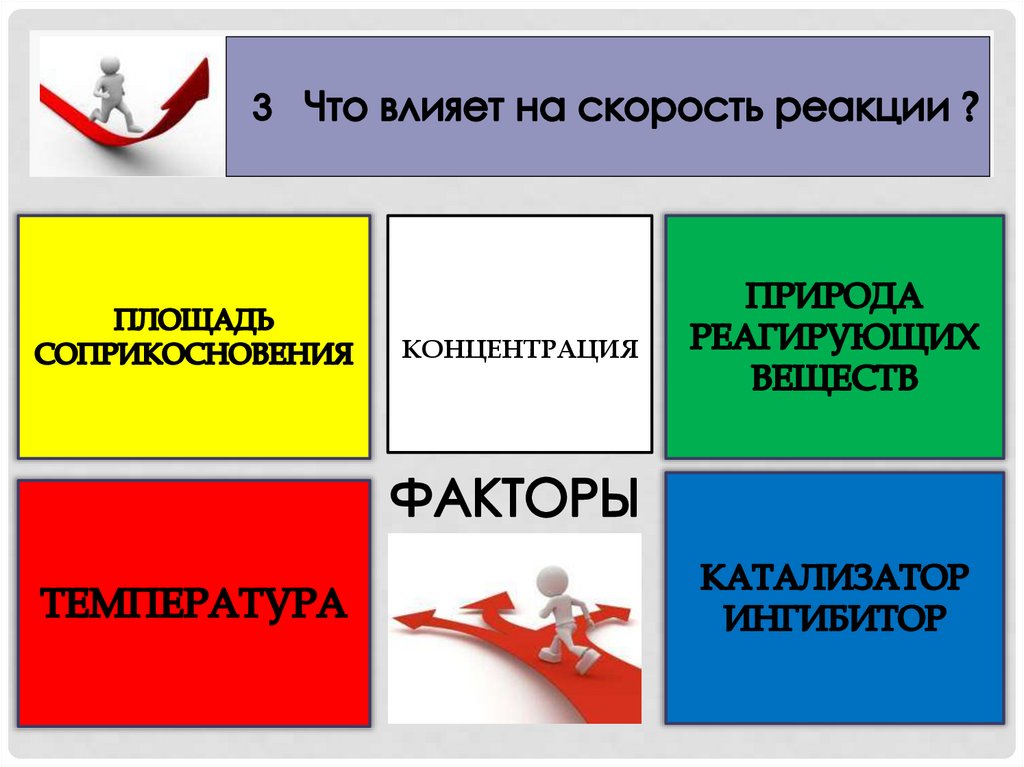
ВЛИЯНИЕ ПРИРОДЫ ВЕЩЕСТВ+ Mg
+ Zn
HCl
Mg + 2HCl = MgCl2 + H2↑
+ Fe
HCl
Zn + 2HCl = ZnCl2 + H2↑
HCl
Fe + 2HCl = FeCl2 + H2↑
9.
ВЛИЯНИЕ ПОВЕРХНОСТИСОПРИКОСНОВЕНИЯ РЕАГЕНТОВ
+ Zn
+ Zn
Гранулированный
Порошок
HCl
HCl
Zn + 2HCl = ZnCl2 + H2↑
10.
ВЛИЯНИЕ ТЕМПЕРАТУРЫ+ CuO
+ CuO
H2SO4
CuO + H2SO4 = CuSO4 + H2O
11.
ВЛИЯНИЕ КАТАЛИЗАТОРА+ MnO2
H2O2
H2O2
2H2O2= 2H2O+O2 ↑
12.
ВЛИЯНИЕ ИНГИБИТОРА+ Fe
HCl
+ Fe
HCl
+ 2-3 капли
формалина
Fe + 2HCl = FeCl2 + H2↑
13.
КОНЦЕНТРАЦИЯ14.
ПРОЧИТАЙТЕ УТВЕРЖДЕНИЯ. ПОСТАВЬТЕЗНАК «V» В СООТВЕТСТВУЮЩЕЙ КОЛОНКЕ.
ПРИМЕР
1.Скорость химической реакции определяется изменением
концентрации одного из реагирующих веществ или одного
из продуктов реакции в единицу времени.
2.Катализатор понижает скорость химической реакции.
3.Скорость
химической
реакции
не
зависит
от
температуры.
4. Порошок цинка взаимодействует с серной кислотой
медленнее, чем гранулы.
5. Оксид меди (II) быстрее взаимодействует с серной
кислотой при 60ºС, а не при 20ºС.
6.В чистом кислороде горение происходит интенсивнее,
чем в воздухе.
7. Для уменьшения скорости химической реакции
необходимо
увеличить
концентрацию
реагирующих
веществ.
ДА
НЕТ












 Химия
Химия








