Похожие презентации:
Хімічні властивості алкенів та алкінів
1.
2.
Найпростіші органічні речовин ̶ вуглеводні,які складаються з атомів тільки двох
елементів: Карбону і Гідрогену
С
H
У молекулах алканів атоми Карбону зв’язані
між собою одинарними зв'язками, а всі інші
валентності насичені атомами Гідрогену
Ненасичені вуглеводні ̶ це органічні сполуки,
в яких не всі валентні електрони атома Карбону
утворюють ковалентні зв'язки з атомами
Гідрогену
3.
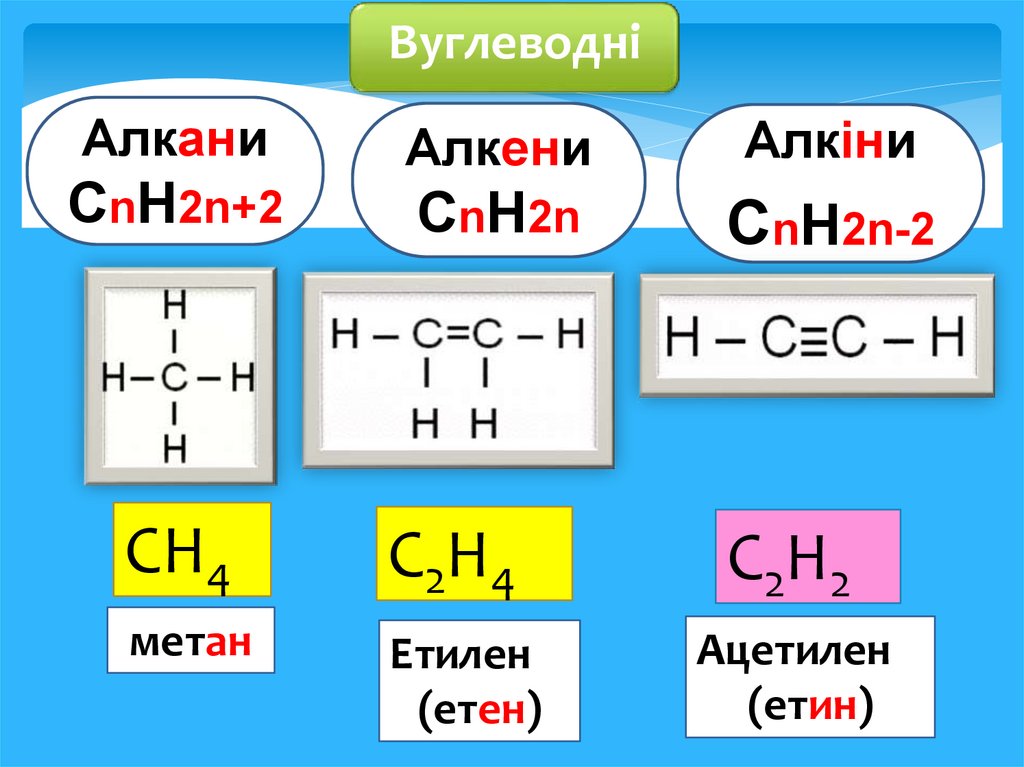
ВуглеводніАлкани
СnН2n+2
Алкени
Алкіни
СnН2n
СnН2n-2
СН4
С2Н4
метан
Етилен
(етен)
С2Н2
Ацетилен
(етин)
4.
Нижчі члени гомологічного рядудо С4Н8 ̶ гази
Середні члени гомологічного ряду
до С18Н36 ̶ рідини
Вищі алкени гомологічного ряду ̶
тверді речовини
Алкени не розчиняються у воді,
але добре розчиняються у
органічних розчинниках
5.
Природний газ на 90% складається з метану та етану, решта припадає напропан та бутан, а от ненасичених вуглеводнів в ньому практично
немає. Чому?
Властивості речовин визначаються будовою речовини. Пригадайте
алкани (насичені в.в.). Який зв’язок між атомами Карбону в молекулах
алканів? (простий) Це були не дуже активні речовини.
Який зв’язок між атомами Карбону у алкенів і алкінів?
6.
7.
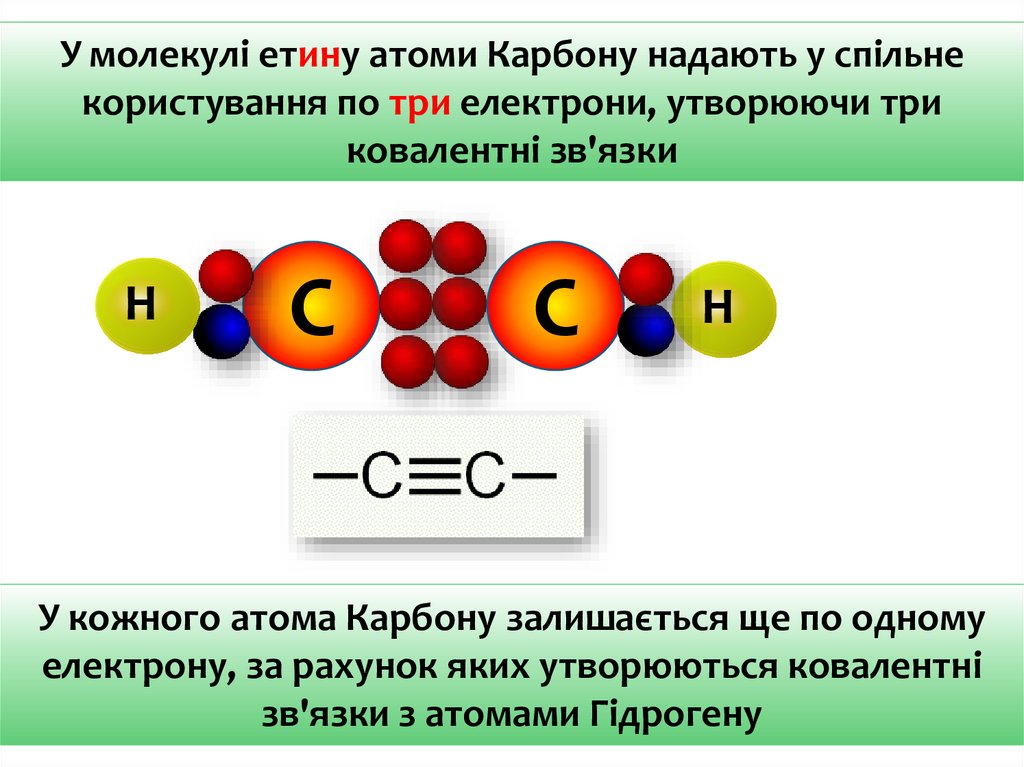
У молекулі етину атоми Карбону надають у спільнекористування по три електрони, утворюючи три
ковалентні зв'язки
Н
С
С
Н
У кожного атома Карбону залишається ще по одному
електрону, за рахунок яких утворюються ковалентні
зв'язки з атомами Гідрогену
8.
У ненасичених вугеводнів між атомами Карбонувиникають подвійні та потрійні зв'язки
СН2= СН2
̶
СН=СН
С2Н4
С2Н2
Етилен
(етен)
Ацетилен
(етин)
9.
За хімічними властивостями алкенивідрізняються від насичених вуглеводнів.
При хімічних реакціях подвійний зв’язок
розривається і переходить в одинарний.
Ni
Н2С=СН2 + Н2 СН3 ̶ СН3
етен
етан
Приєднання Гідрогену (у присутності каталізатора
нікелю, платини при зв. умовах)
Приєднання Гідрогену до молекули речовини
називається реакцією гідрування, або гідрогенізації
10.
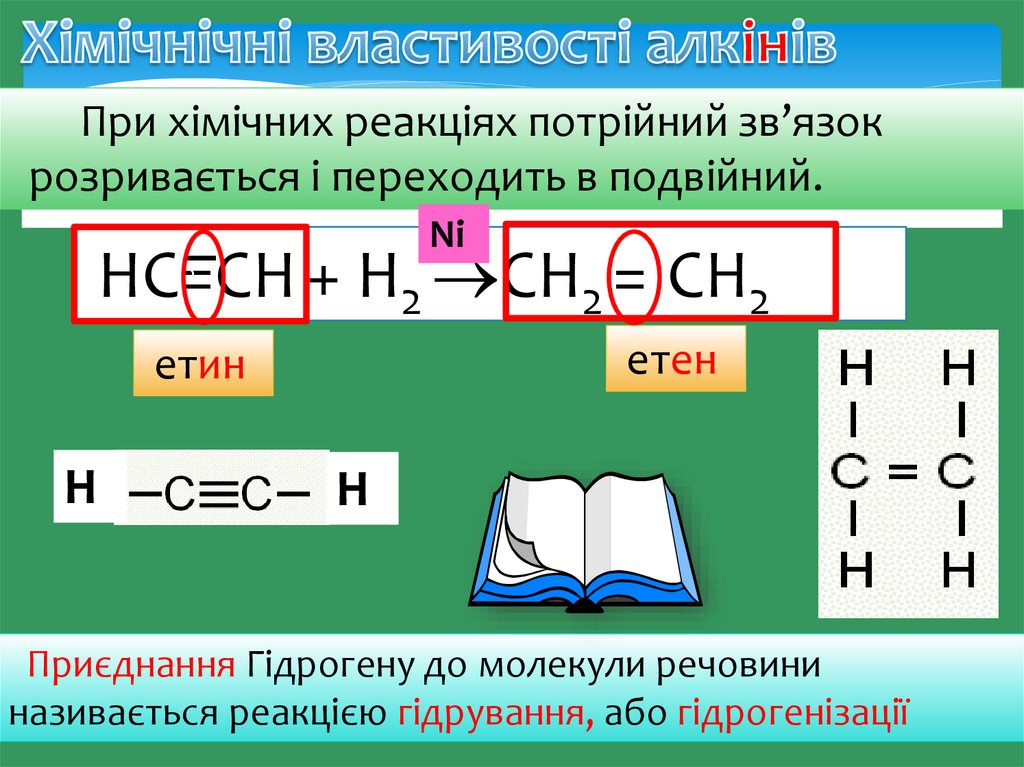
При хімічних реакціях потрійний зв’язокрозривається і переходить в подвійний.
̶
Ni
НС=СН + Н2 СН2 = СН2
2
етен
етин
Н
Н
Приєднання Гідрогену до молекули речовини
називається реакцією гідрування, або гідрогенізації
11.
Приєднання галогенів (Cl2, Br2, I2)2
Н2С=СН2 + Br2 СН2 ̶ СН2
Ι
Ι
етен
Br
Br
1,2- диброметан
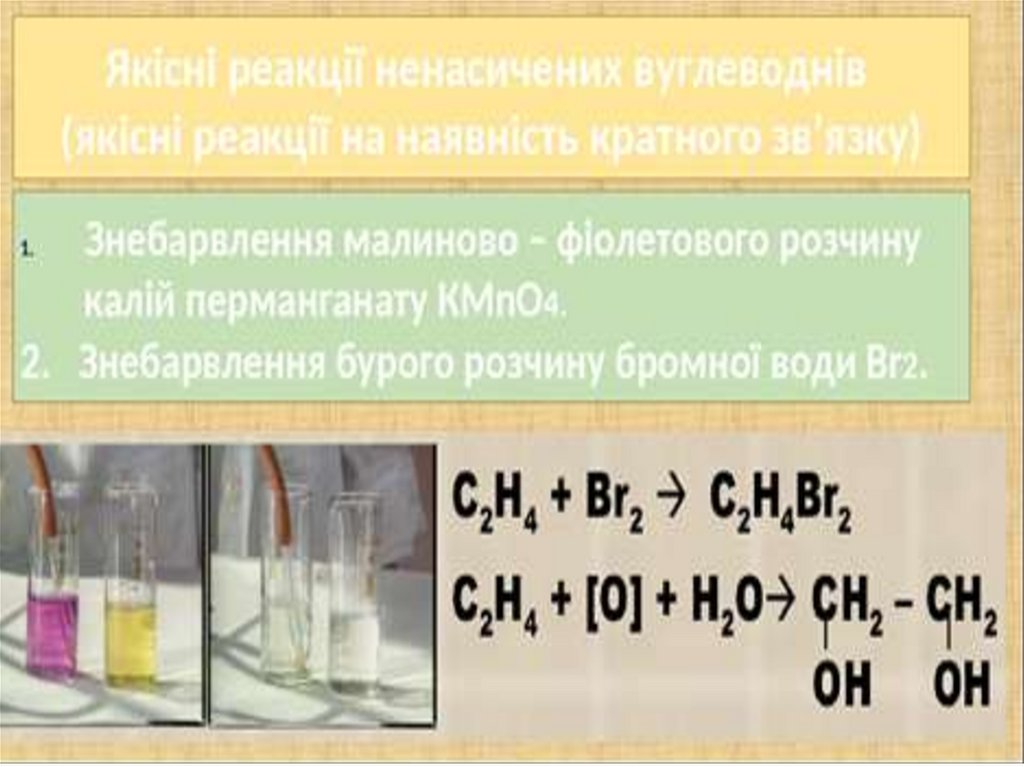
Реакція приєднання Брому є якісною реакцією на
ненасичені вуглеводні
(знебарвлення коричневої бромної води)
Ця якісна реакція дозволяє розпізнати
ненасичені вуглеводні
12.
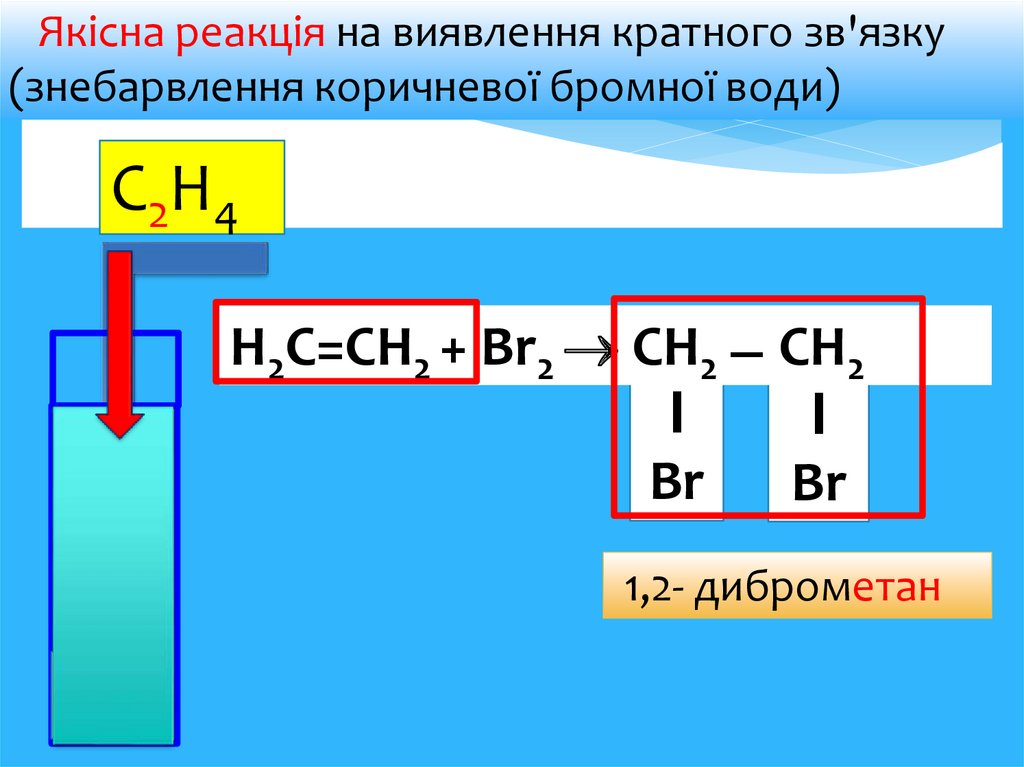
Якісна реакція на виявлення кратного зв'язку(знебарвлення коричневої бромної води)
С2Н4
Н2С=СН2 + Br2 СН2 ̶ СН2
Ι
Ι
Br
Br
1,2- диброметан
Br2
13.
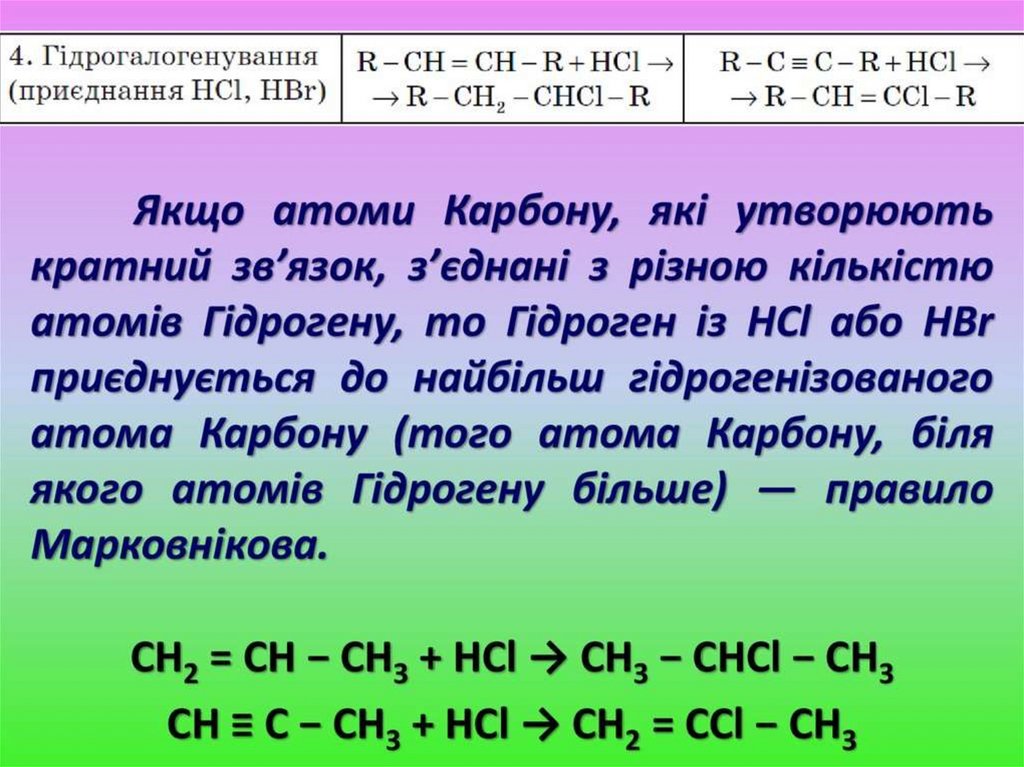
Приєднання галогенів (Cl2, Br2)̶
НС =2 СН + 2 Br
2
етин
СНBr2 ̶ СНBr2
1,1,2, 2- тетрахлоретан
Реакція приєднання Брому є якісною реакцією на
ненасичені вуглеводні
(знебарвлення коричневої бромної води)
Ця якісна реакція дозволяє розпізнати
ненасичені вуглеводні
14.
15.
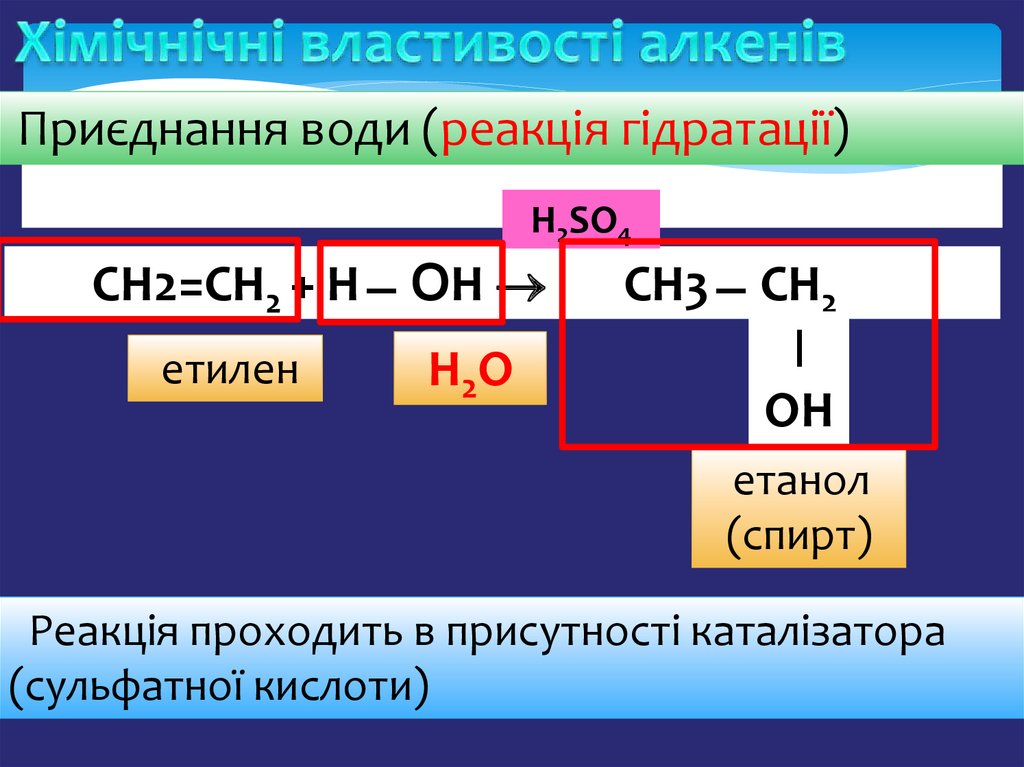
Приєднання води (реакція гідратації)Н2SO4
СH2=СН2 + Н ̶ ОН
етилен
H2O
СН3 ̶ СН2
Ι
ОН
етанол
(спирт)
Реакція проходить в присутності каталізатора
(сульфатної кислоти)
16.
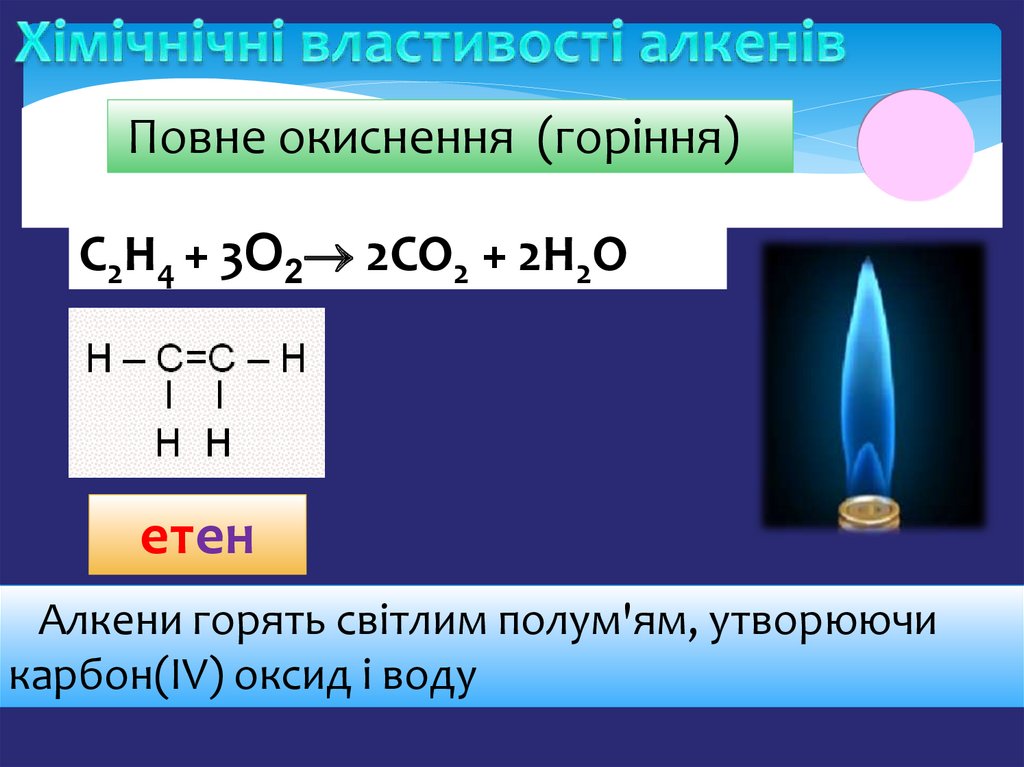
Повне окиснення (горіння)С2Н4 + 3О2 2СО2 + 2Н2О
етен
Aлкени горять світлим полум'ям, утворюючи
карбон(ІV) оксид і воду
17.
Повне окиснення (горіння)С2Н2 + 5О2 4СО2 + 2Н2О
етин
ацетилен
Aлкіни горять світлим киптявим полум'ям,
утворюючи карбон(ІV)оксид і воду
18.
19.
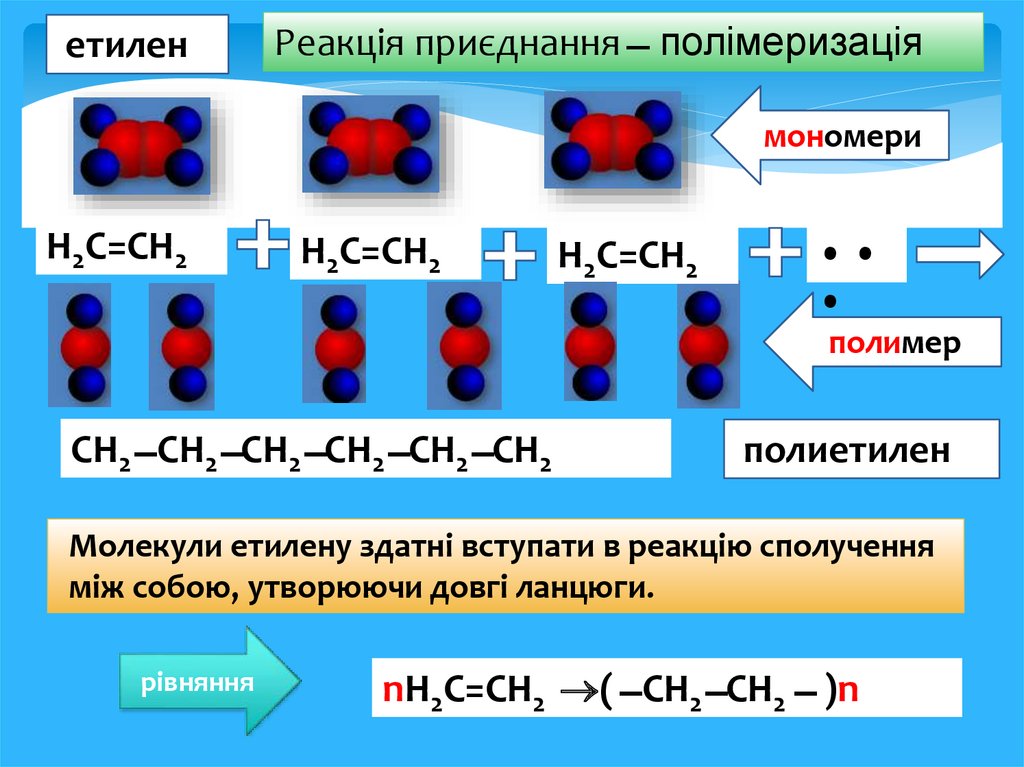
етиленРеакція приєднання ̶ полімеризація
мономери
Н2С=СН2
Н2С=СН2
Н2С=СН2
•
полимер
СН2 ̶ СН2 ̶ СН2 ̶ СН2 ̶ СН2 ̶ СН2
полиетилен
Молекули етилену здатні вступати в реакцію сполучення
між собою, утворюючи довгі ланцюги.
рівняння
nН2С=СН2 ( ̶ СН2 ̶ СН2 ̶ )n
20.
nН2С = СН2 ( ̶ СН2 ̶ СН2 ̶ )nмономер
мономерна
ланка
ступінь
полімеризації
Н2С = СН2 ̶ мономер, вихідна речовина ̶
вуглеводень, з якого синтезується полімер
( ̶ СН2 ̶ СН2 ̶ )n ̶ полімер ̶ речовина, що
утворюється в результаті полімеризації.
̶ СН2 ̶ СН2 ̶ мономерна ланка ̶ повторювана
частина молекули полімеру
Індекс n ̶ ступінь полімеризації, який указує,
скільки мономерних ланок утворюють
молекулу полімеру











 Химия
Химия








