Похожие презентации:
Металлы. Общая характеристика металлов и их свойства
1.
Муниципальное образовательноеучреждение средняя общеобразовательная
школа № 10 г. Павлово
«Металлы.
Общая характеристика
металлов и их свойства»
Выполнила учитель химии
высшей квалификационной категории
Калашникова Ирина Владимировна
11.08.2021
2.
«Мощь и сила науки — во множестве фактов,цель — в обобщении этого множества…»
Дмитрий Иванович
Менделеев
11.08.2021
2
3.
Цель урока:Используя опыт и ранее полученные
знания учащихся, создать «портрет»
металлов как химических элементов и
простых веществ.
4.
Задачи урока:• Обобщить знания учащихся, полученные ранее о
положении металлов в ПСХЭ Д.И. Менделеева
• Актуализировать знания о строении атомов
металлов
• Показать зависимость физических и химических
свойств металлов от наличия в них металлической
связи и особенностей кристаллического строения
• Доказать , что в химических реакциях металлы чаще
всего являются восстановителями
5.
Павлово – город металлистови металлопереработки
Греческое «металлон» обозначало«земляные работы, раскопки», а
позднее «шахты, рудники, руда»
Латинское «металлум» – «руда и
выплавляемый из нее металл»
Французское
«металль»
–
перекочевало к нам в Россию
6.
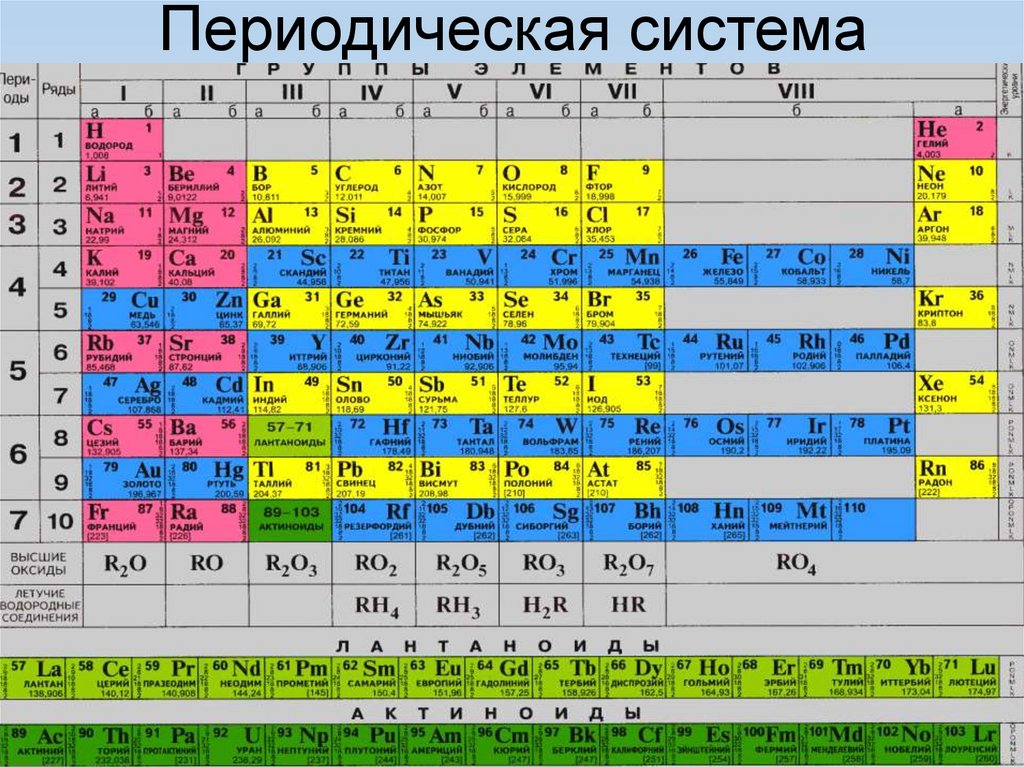
1. Где в ПСХЭ расположены элементы-металлы?2. Является ли деление элементов на металлы и
неметаллы условным? Почему?
3. Какими физическими свойствами обладают
простые вещества металлы?
4. Какими особенностями в строении обладают
атомы металлов?
5. Выполни тест!
11.08.2021
6
7.
Периодическая система11.08.2021
.
7
8.
Строение атомов главныхподгрупп:
• строение атома
калия
• 19 К + 19
11.08.2021
• строение атома
кальция
• 20 Са + 20
.
8
9.
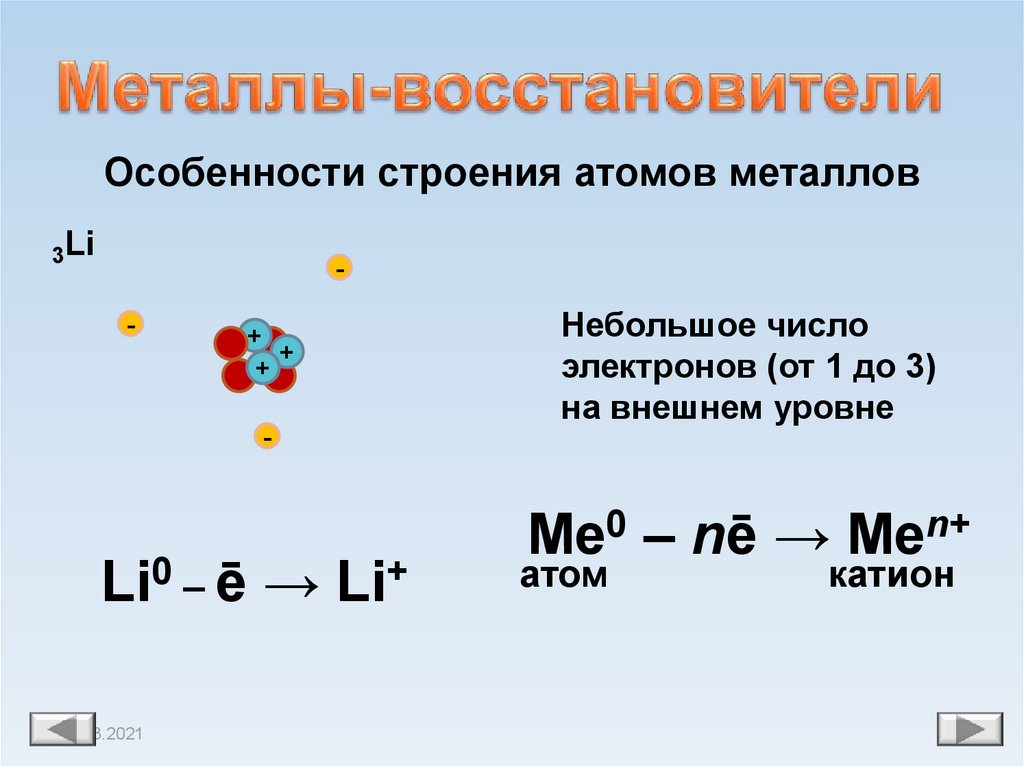
Особенности строения атомов металлов3Li
-
+
+
+
Небольшое число
электронов (от 1 до 3)
на внешнем уровне
-
Li0 _ ē → Li+
11.08.2021
Мe0 – nē → Men+
атом
катион
9
10.
Металлы - простые вещества• Металлы соединены между собой
металлической связью
(она не обладает направленностью и
насыщаемостью)
• Металлы могут иметь металлическую,
ионную или атомную кристаллические
решетки
• Особое строение кристаллической
решетки – наличие «электронного газа»
11.08.2021
10
11.
Физические свойства металлов –простых веществ
Пластичность
Металлический блеск
Электропроводность
Теплопроводность
Твердость
Плотность
Температуры плавления и кипения
11.08.2021
11
12.
H 2OКислоты
Соли
11.08.2021
12
13.
Ме11.08.2021
+ кислород
оксиды
+ водород
гидриды
+ сера
сульфиды
+ азот
нитриды
13
14.
Допишите уравнения возможных реакций,расставьте степень окисления и составьте
уравнение электронного баланса
• Mg + O 2 =
• Ca + H 2 =
• Hg + S =
11.08.2021
14
15.
Лабораторный опыт № 1 : Прокаливание медной пластинкиt
2 Cu + O2 → 2CuO
Соблюдай правила техники
безопасности!
Внимание!
11.08.2021
Au + O2 → не реагирует
Pt + O2 → не реагирует
15
16.
Li K Ba Sr Ca NaMg Al Mn Zn Cr Fe Cd Co Ni Sn Pb
(H2) Cu Hg Ag Pt Au
Активные металлы
(Li – Na)
H 2O
гидроксид + H2↑
Металлы средней
активности
(Mg - Pb)
H 2O
оксид + H2↑
Неактивные
металлы (Bi – Au)
H 2O
Не реагируют
11.08.2021
17
17.
Допишите уравнения возможных реакций:Al + H2O →
Zn + H2O →
Ag + H2O →
11.08.2021
Губарева В.А.
18
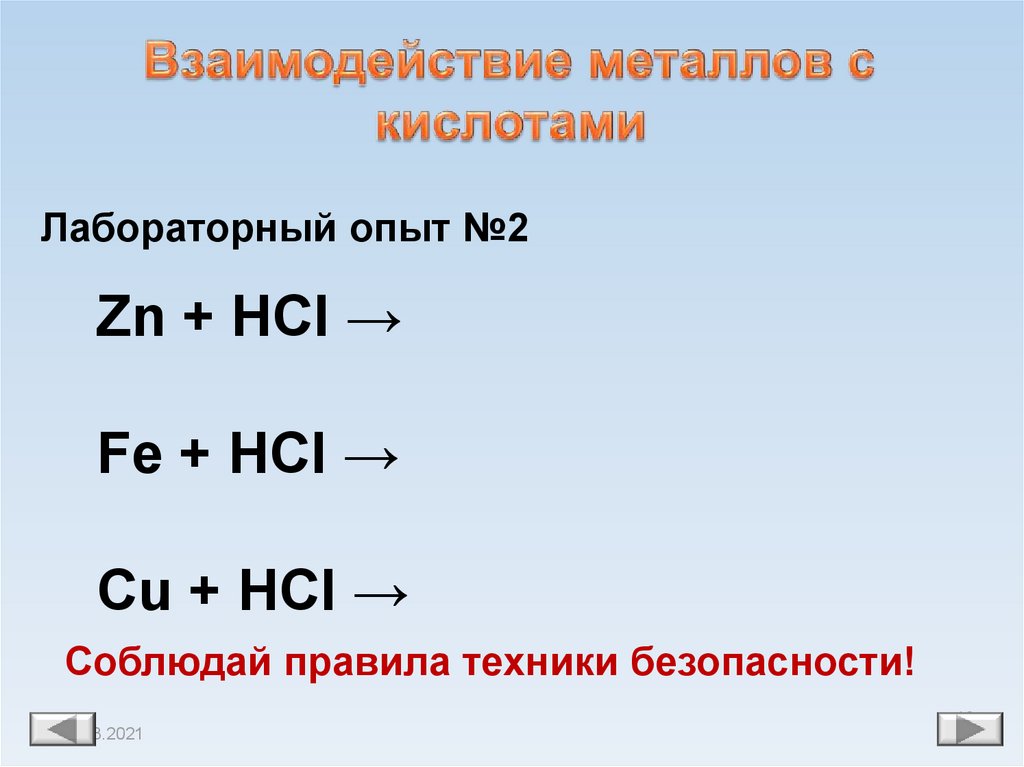
18.
Лабораторный опыт №2Zn + HCl →
Fe + HCl →
Cu + HCl →
Соблюдай правила техники безопасности!
19
11.08.2021
19.
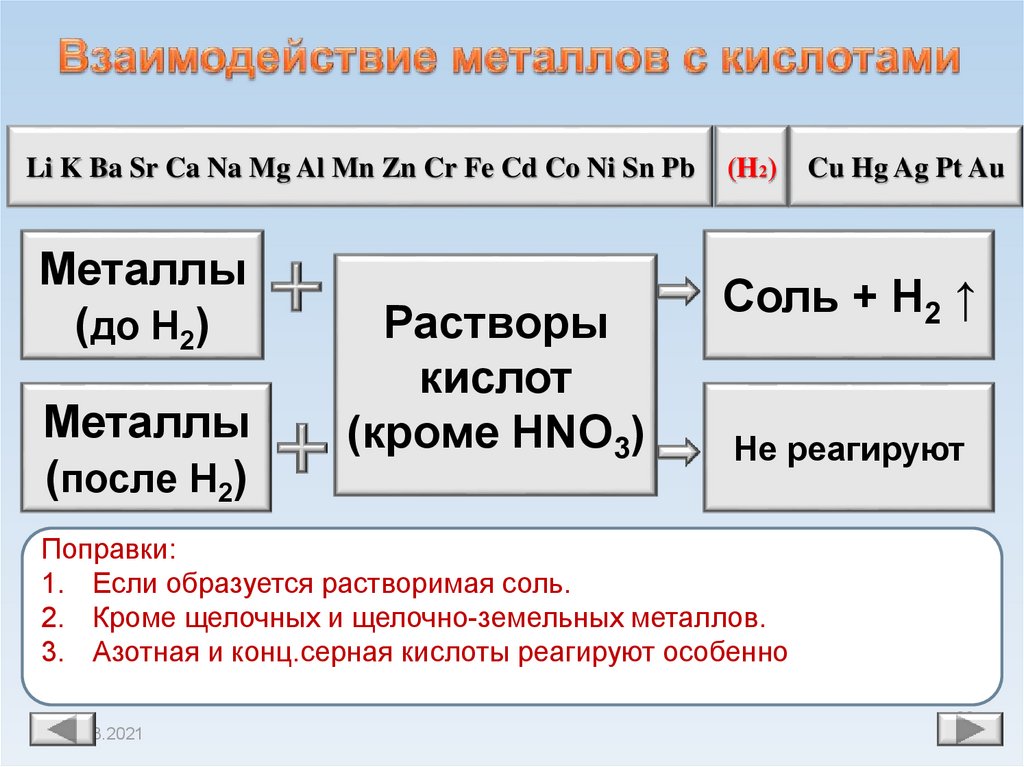
Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn PbМеталлы
(до Н2)
Металлы
(после Н2)
Растворы
кислот
(кроме HNO3)
(H2)
Cu Hg Ag Pt Au
Соль + Н2 ↑
Не реагируют
Поправки:
1. Если образуется растворимая соль.
2. Кроме щелочных и щелочно-земельных металлов.
3. Азотная и конц.серная кислоты реагируют особенно
20
11.08.2021
20.
Лабораторный опыт №3Fe
Cu
Fe + CuCl2 →
CuCl
FeCl
Cu + FeCl2 →
Соблюдай правила техники
Поправки:
безопасности!
1. Если образуется
растворимая соль.
2
2
Более
активный
металл вытесняет
2. Кроме
щелочных
и щелочно-земельных
металлов.
Вывод:
11.08.2021
менее активный из раствора его соли.
21
21.
Допишите уравнения возможных реакций:Ag + CuCl2 →
Zn + FeCl3 →
Fe + AgNO3 →
11.08.2021
22.
С какими из веществ будут реагировать предложенныеметаллы при нормальных условиях?
Na
K2SO4(р-р)
O2
H2O
NaCl (р-р)
Li2O
SO2
Mg
Na2SO4
FeSO4(р-р)
SO3
H2SO4 (р-р)
Ca
NaOH (р-р)
Zn
FeCl2 (р-р)
HCl
Al2(SO4)3
Al2S3
H2O
SO2
Cu
Fe
HCl
CaO
O2
P2O5
AgNO3 (р-р)
23.
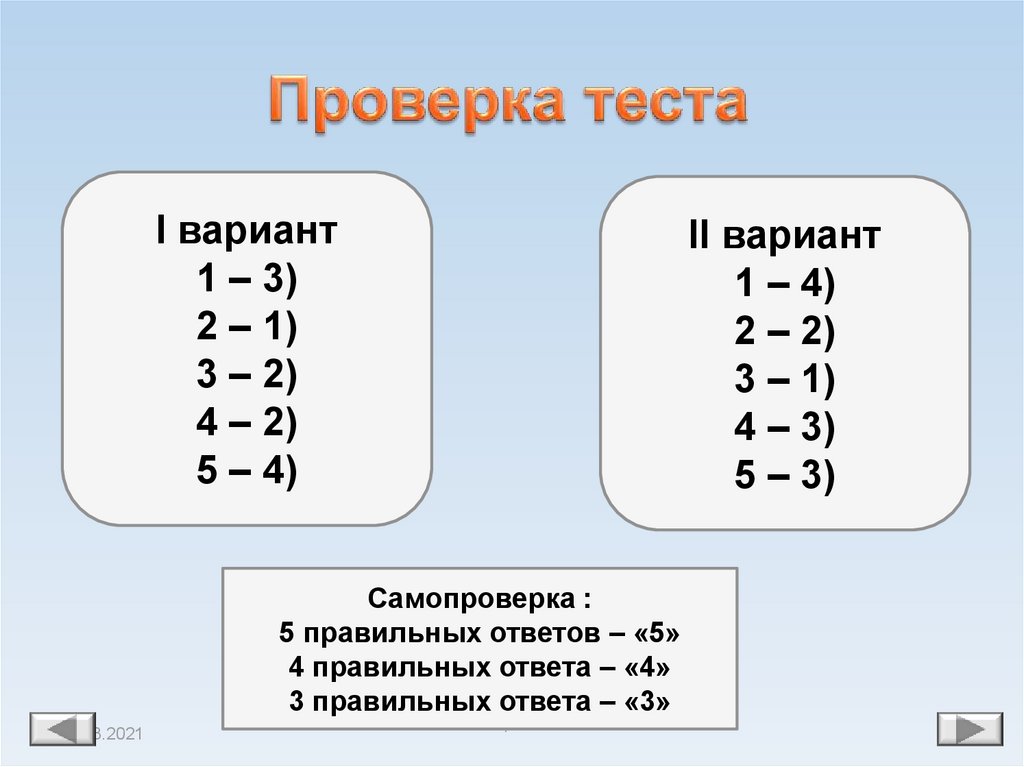
I вариант1 – 3)
2 – 1)
3 – 2)
4 – 2)
5 – 4)
II вариант
1 – 4)
2 – 2)
3 – 1)
4 – 3)
5 – 3)
Самопроверка :
5 правильных ответов – «5»
4 правильных ответа – «4»
3 правильных ответа – «3»
11.08.2021
.
24
24.
•С какими веществами реагируют металлы?•Чем являются металлы в реакциях –
окислителями или восстановителями?
•Какие поправки вводятся для реакций
металлов с водой, кислотами, солями?
•Для чего нужно изучать химические свойства
металлов? Где их можно использовать?
•Где применить полученные знания?
11.08.2021
25
25.
«Мыслящий ум не чувствует себя счастливым, пока емуне удается связать воедино разрозненные факты».
Д. Хевелси
Сегодня мы попытались создать портрет металлов из тех
фактов, которые нам известны и из новых сведений.
Предлагаю вам продолжить предложения:
Сегодня я узнал…
Я удивился…
Я хотел бы…
26
26.
1. § 18 , упр. 12,13 (письменно)2. Найти интересный материал по теме:
«Металлы»
.
27




















 Химия
Химия








