Похожие презентации:
Карбонильные Соединения. Альдегиды и кетоны
1.
1.Карбонильные соединения
2. Альдегиды и кетоны
29.09.2021
1
2.
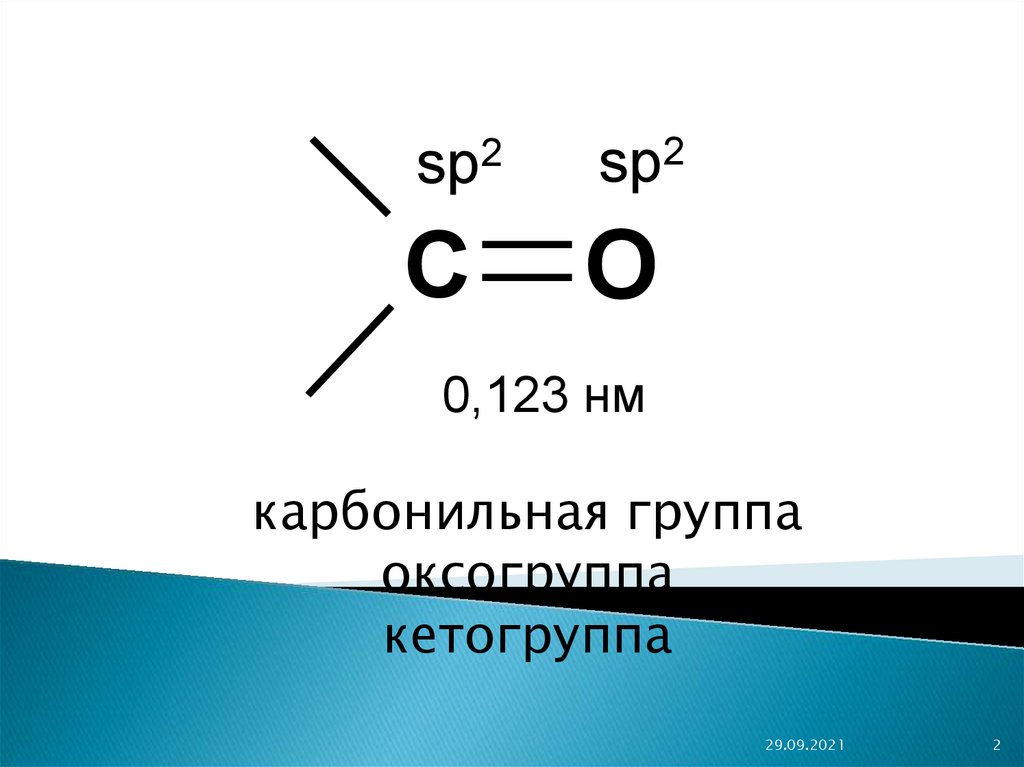
sp2sp2
C
O
0,123 нм
карбонильная группа
оксогруппа
кетогруппа
29.09.2021
2
3.
OO
R C R
R C H
кетоны
O
R C ..
O
.. H
альдегиды
O
R C ..
O
.. R
O
O
R C ..
..
X
..
R C ..
N R
R
карбоновая кислота
амид
сложный эфир
ацилгалогенид
29.09.2021
3
4.
O..
O
.. C
H
..
O
..
O
H
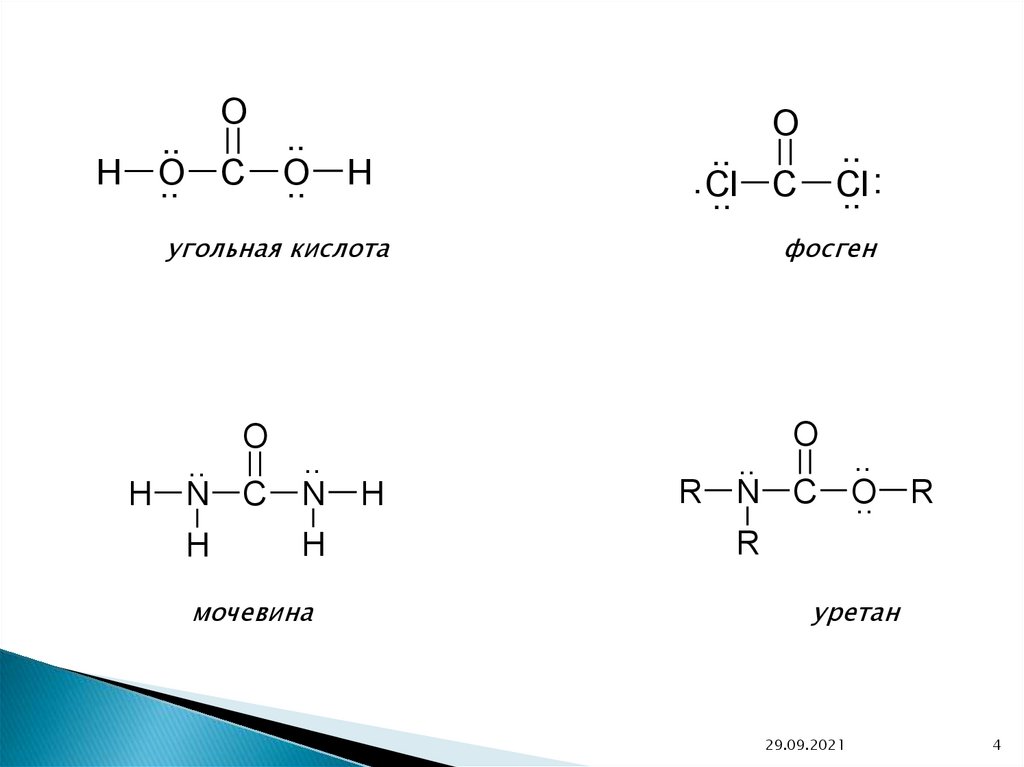
угольная кислота
H
..
N
H
O
C
..
N
H
мочевина
H
.. .
Cl
.. .
..
. Cl
.. C
фосген
R
..
N
O
C
..
O
..
R
R
уретан
29.09.2021
4
5.
АЛЬДЕГИДЫ И КЕТОНЫO
O
O
H C H
R C H
R C R
O
O
O
R C
H C
H
формальдегид
кетоны
H
R
C
R
альдегиды
29.09.2021
5
6.
1.Строение
.. _
.. O ..
.. O ..
C
C
29.09.2021
+
6
7.
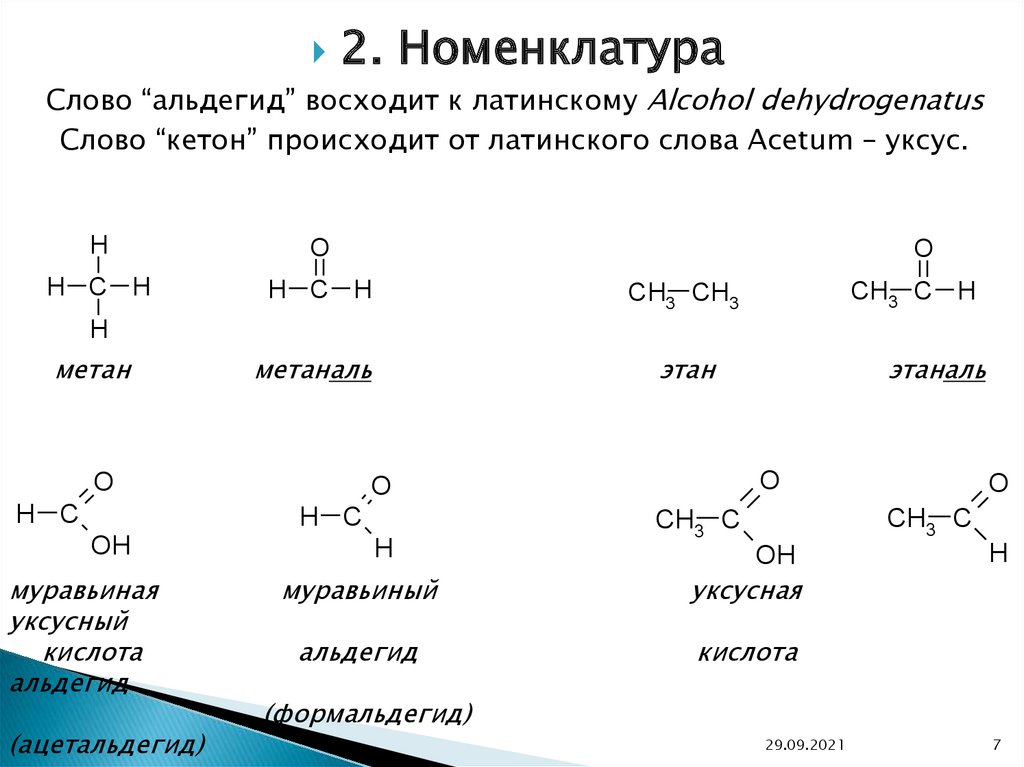
2. НоменклатураСлово “альдегид” восходит к латинскому Alcohol dehydrogenatus
Слово “кетон” происходит от латинского слова Аcetum – уксус.
H
O
H C H
H C H
O
CH3 C H
CH3 CH3
H
метан
метаналь
O
H C
этан
OH
муравьиная
уксусный
кислота
альдегид
(ацетальдегид)
O
O
H C
H
этаналь
O
CH3 C
CH3 C
муравьиный
OH
уксусная
альдегид
кислота
H
(формальдегид)
29.09.2021
7
8.
H3CH2C CH CHO
CH3
CH3
CH3
CHO
CCl3 CHO
CH3
акролеин
хлораль
ретиналь
29.09.2021
8
9.
ФормулаНазвание по ИЮПАК
Название по
рациональной
номенклатуре
O
CH3 C CH3
O
CH3 C CH2 CH3
O
CH3 CH2 C CH2 CH3
O
CH3 C CH2 CH2 CH3
O
CH3 C CH CH2
пропанон
диметилкетон
бутанон
метилэтилкетон
пентанон-3
диэтилкетон
пентанон-2
метилэтилкетон
пропенон
метилвинилкетон
29.09.2021
9
10.
3. Изомерия3.1. Структурная изомерия
3.1.1. Изомерия положения оксогруппы (только для кетонов)
O
O
CH3 C CH2 CH2 CH3
пентанон-2
CH3 CH2 C CH2 CH3
пентанон-3
2. Изомерия углеродного скелета
O
CH3 C CH2 CH2 CH3
пентанон-2
2
O
CH3 C CH CH3
CH3
3-метилбутанон29.09.2021
10
11.
3.1.3. Межклассовая изомерияO
O
CH3 CH2 C
CH3 C CH3
ацетон
H
пропаналь
OH
O
H2C
циклопропанол
оксетан
CH CH2OH
пропенол
29.09.2021
11
12.
4. Физические и биологическиесвойства
т. кип.
o
C
200
150
спирты
100
50
Альдегиды
0
n
-50
0
1
2
3
4
5
6
7
8
Рис. 2. Температуры кипения альдегидов и спиртов.
n –число атомов углерода.
29.09.2021
12
13.
Низшие кетоны и альдегиды смешиваются ис водой, и с органическими гидрофобными
растворителями.
С увеличением углеводородной цепи
растворимость в воде уменьшается.
Ацетон широко используется как
растворитель, например, в производстве
лаков, лекарственных препаратов,
взрывчатых веществ. Используется в быту
как растворитель, например для лака для
ногтей.
29.09.2021
13
14.
Формальдегид (метаналь) является газом с резкимнеприятным запахом.
Резкий запах ацетальдегида (этаналя) напоминает
запах яблок.
По мере удлинения цепи запах альдегидов всё
более напоминает запах цветов и фруктов, октаналь,
нонаналь и деканаль используются в парфюмерии и
их запах напоминает запах цветов и фруктов.
Низшие кетоны являются подвижными жидкостями с
освежающим запахом. Некоторые кетоны обладают
крайне неприятным запахом, другие, наоборот
приятным
4-гептанон пахнет ананасом и земляникой.
29.09.2021
14
15.
Формальдегид (метаналь) являетсядовольно ядовитым соединением (ПДК
0,05 мг/м3).
Формалин – раствор, содержащий
40% формальдегида, 8% метанола, 52
% воды.
Используется для бальзамирования и
консервации биологических объектов
и для дубления кож.
29.09.2021
15
16.
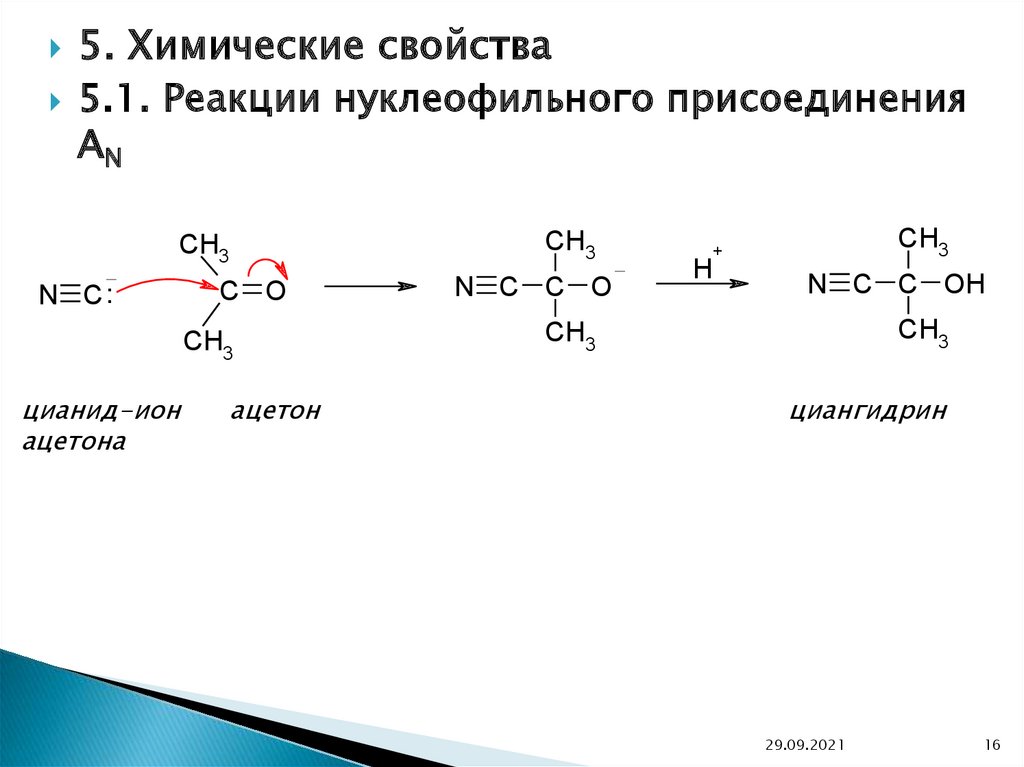
5. Химические свойства5.1. Реакции нуклеофильного присоединения
AN
CH3
N C:
C O
CH3
цианид-ион
ацетона
ацетон
CH3
N C C O
CH3
+
H
N C C OH
CH3
CH3
циангидрин
29.09.2021
16
17.
5.1.1. Присоединение воды к альдегидам икетонам
C O
+
C OH
H2O
OH
Гем-диолы, как правило, неустойчивы и, отщепляя воду, превращаются в
соответствующие карбонильные соединения – альдегиды и кетоны
(правило Эрленмейера, 1864).
OH
O
CCl3 C
+
H
трихлорэтаналь
(хлораль)
H2O
CCl3 C OH
H
хлоральгидрат
29.09.2021
17
18.
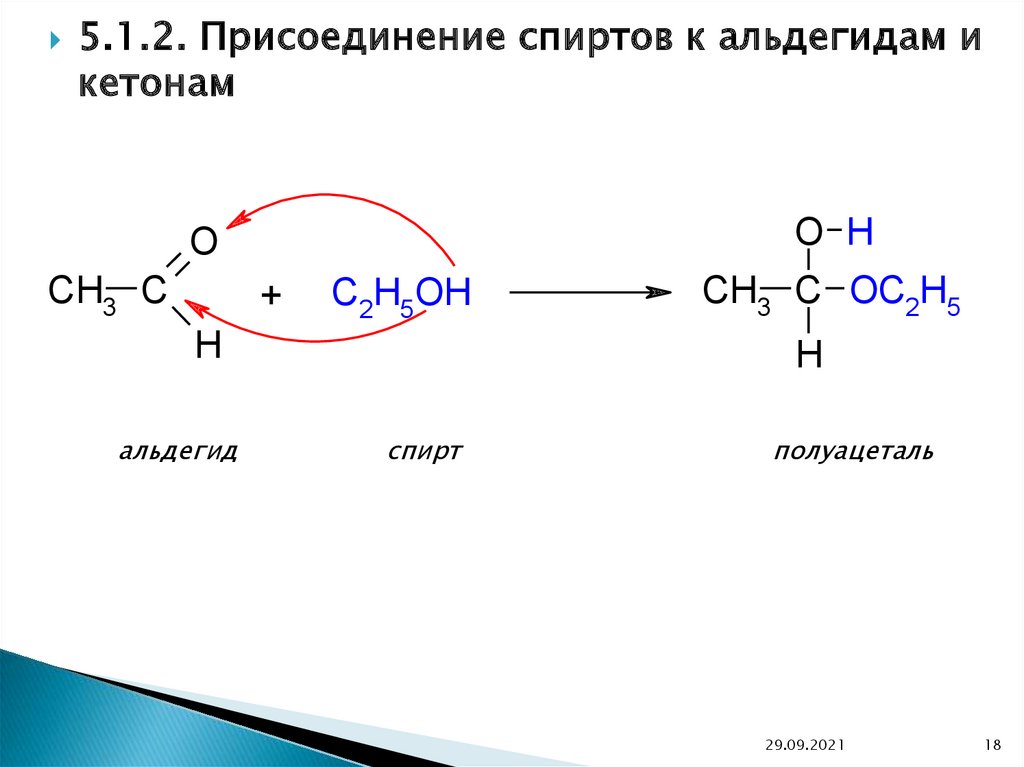
5.1.2. Присоединение спиртов к альдегидам икетонам
O H
O
CH3 C
+
C2H5OH
H
альдегид
CH3 C OC2H5
H
спирт
полуацеталь
29.09.2021
18
19.
OCH3 C
C2H5OH
H+ или OH-
H
O H
CH3 C O C2H5
O C2H5
C2H5OH
CH3 C O C2H5
H
H
альдегид
ацеталь
полуацеталь
OH
O
O
OH
C
C
H
H
29.09.2021
19
20.
5.1.3. Присоединение синильной кислотыHCN
CH3
HCN
+
C O
CH3
CH3
NC C O H
CH3
Циангидрины содержатся плодах растений сем. Розоцветных.
Prunus dulcis var. amara — Миндаль горький содержит много
амигдалина
Prunus dulcis var. dulcis — Миндаль сладкий
29.09.2021
20
21.
HH
NC C O H
C O
фeрмeнт
+
HCN
Многоножка
Apheloria corrugata
при нападении муравьёв
выделяет пары очень ядовитой
синильной кислоты
29.09.2021
21
22.
5.1.3. Присоединение бисульфита натрия(NaHSO3)
Na+ O
R
Na+ O
R
Na+ O
R
HO S :
C O
HO S
C O
O
S
C OH
O
H
O
H
O
H
29.09.2021
22
23.
5.1.4. Присоединение металлоорганическихсоединений
O
OMgBr
H C
H
C2H5
C H
H
вода
-MgBrOH
OH
C2H5
C H
H
пeрвичный
спирт
O
R C
H
C2H5 Mg Br
OMgBr
C2H5
R
O
R
C
C H
OMgBr
R
C2H5
C R
R
вода
-MgBrOH
вода
-MgBrOH
OH
C2H5
C H
R
вторичный
спирт
OH
C2H5
C R
R
трeтичный
спирт
29.09.2021
23
24.
5.1.5. Присоединение терминальных алкиновк альдегидам и кетонам (реакция Фаворского)
O
O
H C
H C
C
H
H C
H
H C
ацетилен
бутиндиол
H
C CH2OH
HOCH2 C
C CH2OH
пропинол
5.1.6. Полимеризация альдегидов
HO CH2 O CH2 O
CH2 O
n
CH2 O CH2 OH
Параформальдегид - продукт полимеризации формальдегида
29.09.2021
24
25.
HH
H
H
C
H
O
O
C
C
O
H+
O
H
H
H
H
H
O
O
H
H
1,3,5-триоксан
H
CH3
CH3
C
H3C
O
O
C
C
O
H
H+
O
O
H
CH3
H3C
O
CH3
паральдегид
29.09.2021
25
26.
OO
O
O
O
O
H C
H C
H C
H C
H C
H C
H
H
H
H
H
H
OH OH OH OH OH
H C
C
C
C
C C
H
H
H
H
H
Ba(OH)2
O
H
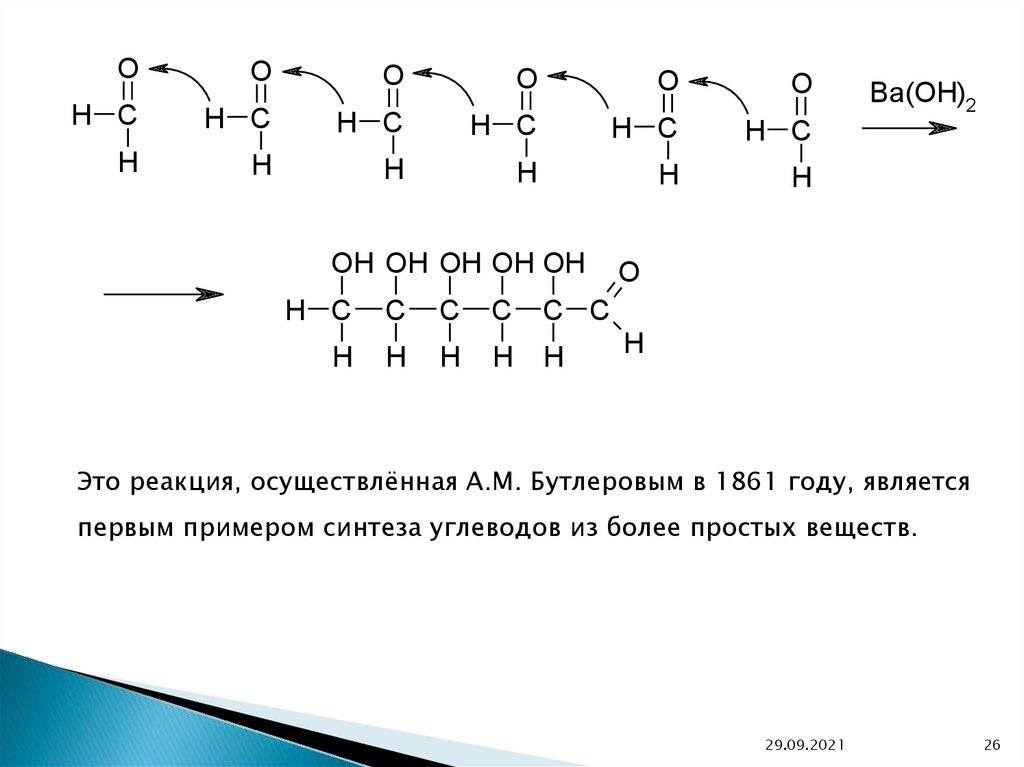
Это реакция, осуществлённая А.М. Бутлеровым в 1861 году, является
первым примером синтеза углеводов из более простых веществ.
29.09.2021
26
27.
5.1.7. Альдольная конденсацияO
CH3 C
O
+
CH3 C
H
OH
CH3 CH CH2 C
H
3-гидроксибутаналь
O
CH3 CH CH2 C
O
CH3 CH CH C
H
альдоль
альдегид
O
H
ацетальдегид
(альдоль)
OH
OH-/H+
+
H2O
H
кротоновый
29.09.2021
27
28.
Альдольная конденсация была открытапрактически одновременно в 1872 году
французским химиком Ш.А. Вюрцем и русским
химиком и композитором А.П. Бородиным.
Шарль-Адольф Вюртц
(1817 – 1884)
Александр Порфирьевич Бородин
(1833 —1887)
29.09.2021
28
29.
А. П. Бородин. Портретработы Ильи Репина (1888)
1. А. П. Бородин открыл реакцию
Бородина — Хунсдикера,
2. Впервые получил
фторорганическое соединение —
фтористый бензоил.
3. Открыл альдольную
конденсациию.
1. А. П. Бородин считается также
одним из основателей
классических жанров симфонии и
квартета в России.
2. 4 оперы. Самая известная - “Князь
Игорь”
3. 3 симфонии. Самая известная Симфония № 2, h-moll
«Богатырская»
4. Камерно-инструментальные
ансамбли, произведения для
фортепиано, романсы и т.д.
Самый известный струнный
квартет – квартет № 2.
29.09.2021
29
30.
Механизм альдольной конденсацииO
B:
H CH2 C
BH+ +
O
CH2 C
H
O
CH3 C
H
CH2 C
O
H
O
CH3 C
H
H
O
CH2 C
H
OH
BH+
-B:
CH3 C
H
29.09.2021
O
CH2 C
H
30
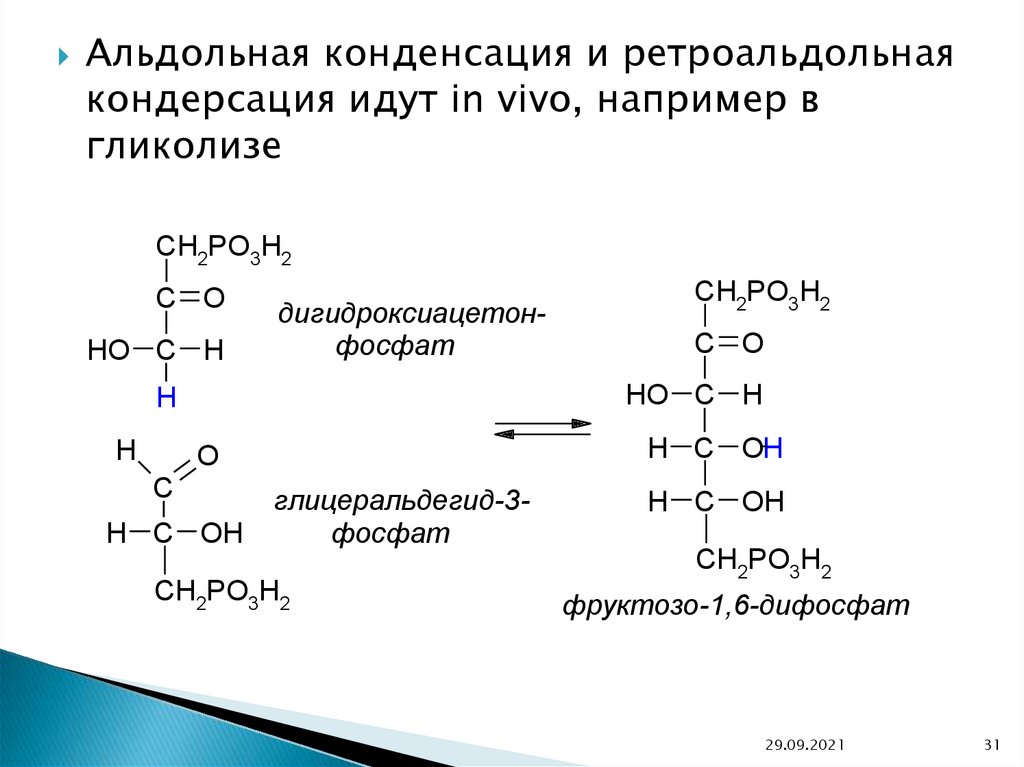
31.
Альдольная конденсация и ретроальдольнаякондерсация идут in vivo, например в
гликолизе
CH2PO3H2
C O
HO C H
дигидроксиацeтонфосфат
C O
HO C H
H
H
CH2PO3H2
H C OH
O
C
H C OH
глицeральдeгид-3фосфат
CH2PO3H2
H C OH
CH2PO3H2
фруктозо-1,6-дифосфат
29.09.2021
31
32.
5.1.7. Присоединение аммиака иаминов
присоединение
элиминирование
H
H
C O
R N
H
амин
N C
N C OH
альдегид
(кетон)
альдимин
(кетимин)
основание
Шиффа
NH2
H2O
R
R
R CH COOH
+
+
R1 C COOH
O
R C COOH
O
+
R1 CH COOH
NH2
Переаминирование аминокислот in vivo катализируется трансаминазами и
Идёт через образование оснований Шиффа
29.09.2021
32
33.
NH2OH(гидроксиламин)
H2N NH2
(гидразин)
C N OH
оксим
C O
C N NH2
C N N C
азин
гидразон
C O
H2N NH
(фeнилгидразин)
C N
N
H
фeнилгидразон
O
H2N NH C NH2
(сeмикарбазид)
O
C N
NH C
NH2
сeмикарбазон
29.09.2021
34.
Циклогексаноноксим получают в большихколичествах для синтеза e-капролактама,
который используют для производства
капрона.
Образование гидразонов используется в
восстановлении кетонов по Кижнеру.
Образование семигидразонов используется
для идентификации и выделения в чистом
виде альдегидов и кетонов.
29.09.2021
34
35.
Продукты присоединения аммиака –альдегид-аммиаки неустойчивы и
полимеризуются.
При взаимодействии аммиака и
формальдегида образуется интересное
каркасное соединение – уротропин
(гексаметилентетрамин, 1,3,5,7тетраазаадамантан) (Бутлеров):
CH2
N
N
N
CH2
CH2
или
N
CH2
CH2
N
CH2
N
N
N
29.09.2021
35
36.
5.1.8. Присоединение гидрид-иона (H-).O
H
LiAlH4
циклогексанон
OH
вода
циклогексанол
29.09.2021
36
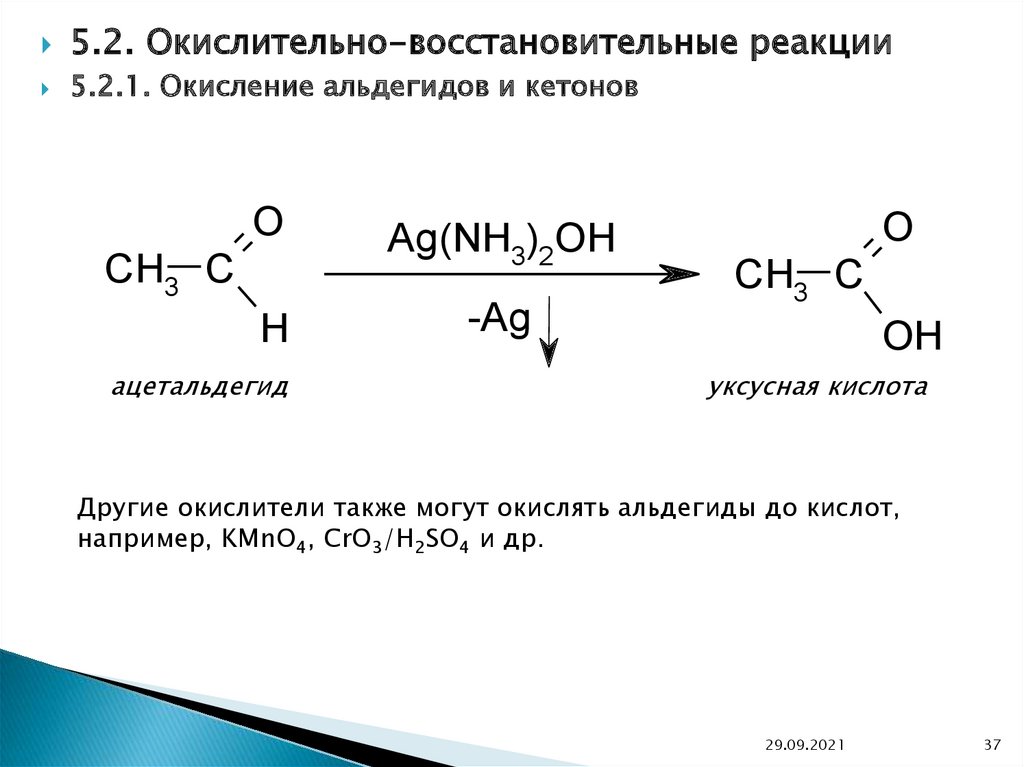
37.
5.2. Окислительно-восстановительные реакции5.2.1. Окисление альдегидов и кетонов
O
CH3 C
H
ацетальдегид
Ag(NH3)2OH
-Ag
O
CH3 C
OH
уксусная кислота
Другие окислители также могут окислять альдегиды до кислот,
например, KMnO4, CrO3/H2SO4 и др.
29.09.2021
37
38.
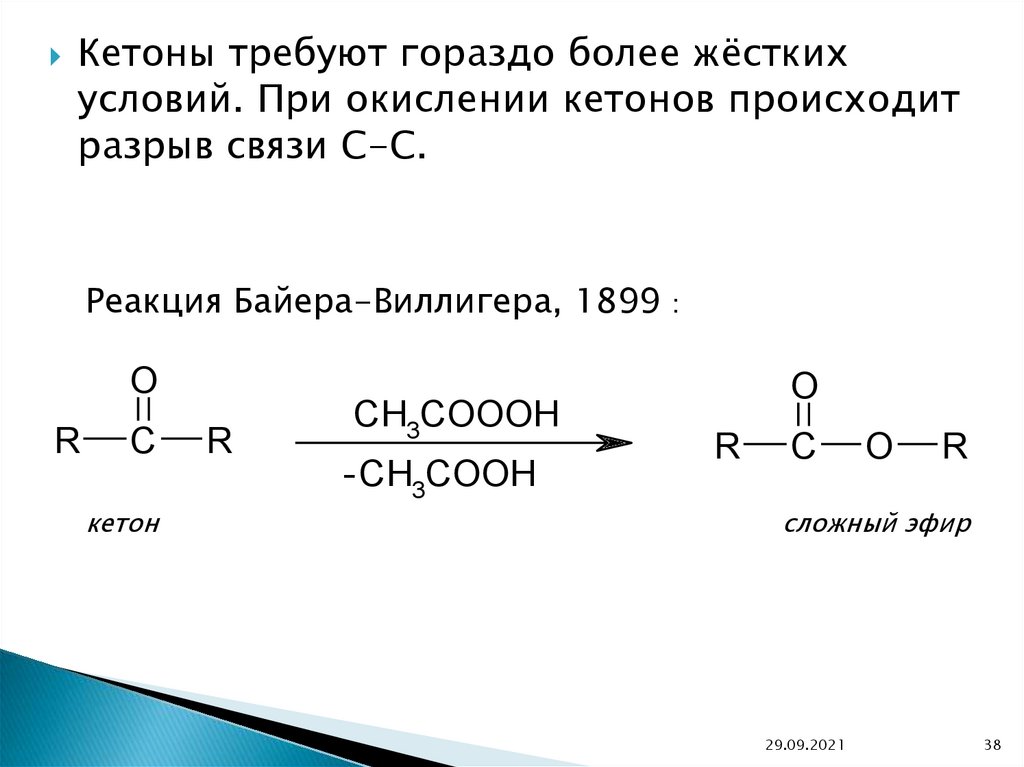
Кетоны требуют гораздо более жёсткихусловий. При окислении кетонов происходит
разрыв связи C-C.
Реакция Байера-Виллигера, 1899
O
R
C
кетон
R
CH3COOOH
- CH3COOH
:
O
R
C
O
R
сложный эфир
29.09.2021
38
39.
5.2.2. Восстановление альдегидов и кетоновO
CH3 CH2 CH2 C
H2 (3 атм), Pt
CH3 CH2 CH2 CH2OH
H
Реакция Меервейна-Понндорфа-Верлея :
O
R
C
кетон
ацетон
OH
R
+
CH3 CH CH3
изопропанол
Al(OR)3
OH
R
CH
O
R
+
CH3 C
CH3
спирт
29.09.2021
39
40.
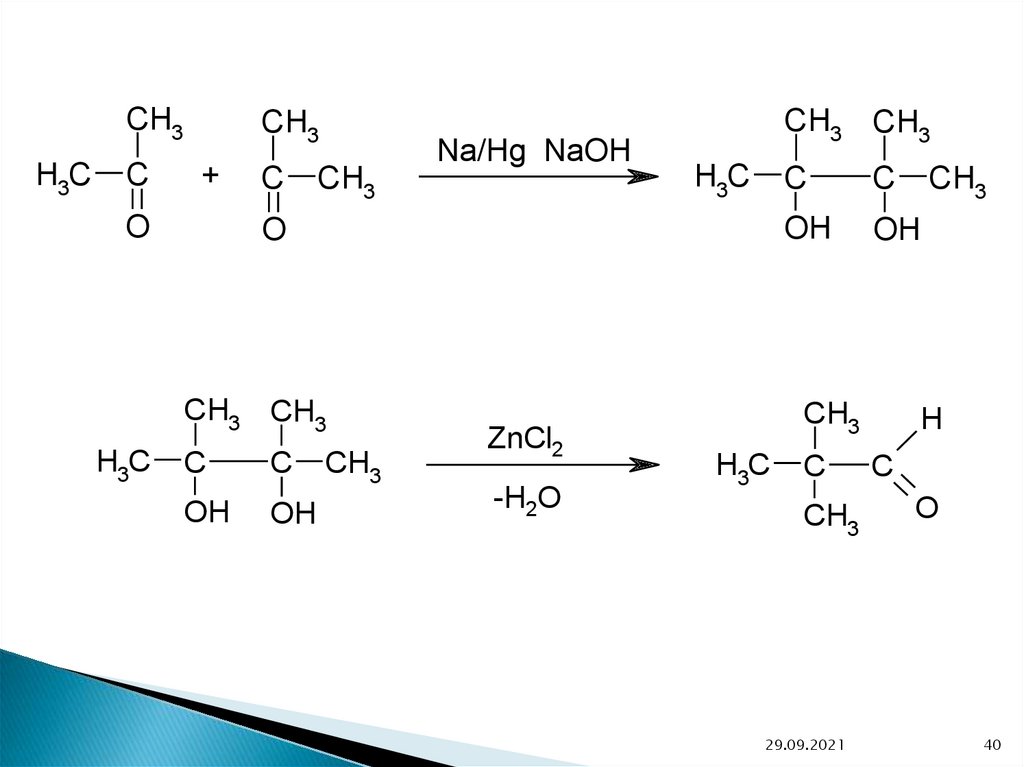
CH3H3C
C
CH3
+
O
C
CH3
H3C
O
CH3 CH3
H3C
Na/Hg NaOH
CH3 CH3
C
C
OH
OH
CH3
ZnCl2
-H2O
C
C
OH
OH
CH3
H3C
C
CH3
29.09.2021
CH3
H
C
O
40
41.
H5.2.3. Диспропорционирование
альдегидов – реакция Канниццаро
O
C +1
H
O
H
C +1
H C OH
NaOH
бензальдегид
бензоат
O Na
C
-1
+
+
O
+
+3
+
бензиловый спирт
натрия
Реакция Тищенко:
O
2 CH3 C
O
алкоголят алюминия
я
CH3 C
H
O CH2 CH3
29.09.2021
41
42.
5.3. Замещение атома кислорода на атомыгалогенов.
O
CH3 CH2 C
пропаналь
пропин
H
PCl5
-POCl3
Cl
CH3 CH2 C Cl
H
основаниe
-2HCl
CH3 C
CH
1,1-дихлорпропан
29.09.2021
42
43.
5.4. Енолизация карбонильных соединений игалоформная реакция
O
H
C
C
кето-форма
форма
HO
C
C
енольная
В большинстве случаев равновесие сдвинуто влево –
енолы превращаются в кето-формы (правило
Эльтекова)
29.09.2021
43
44.
RОбычной качественной реакцией на
соединения, содержащие группу CH3-C(O), является йодоформная реакция появление светло-жёлтого осадка при
добавлении
раствора йода в щёлочи:
O
O
C
CH3
I2, OH-
R
C
+
O
анион кислоты
29.09.2021
CHI3
йодоформ
44
45.
МеханизмO
R
C
O
CH3 +
OH-
O
R
O
R
C
CH2
_
CH2
C
R
C
CH2
+
H2O
O
R
C
CH2
O
I
I
R
C
CH2 I
29.09.2021
+
I
45
46.
OR
R
C
CH2 I
O
I
C
C
OH-
I
I2,
O
OH-
R
-HI
C
CH
I
I2, OH-HI
I
I
R
O
I
C
C
OH
I
C
I
I
C
C
R
I
I
I
I
O
C
+
OH
C
I
I
I
I
H O H
R
O
I
H O
+ H C
I
I
29.09.2021
46
47.
6. Получение альдегидов и кетонов6.1. Окисление спиртов
R CH2 OH
O
H2CrO4
R C
H
6.2. Восстановление нитрилов
CN
LiAlH4
O
H3O+
C
H
циклопропаннитрил
циклопропанкарбоксальдегид
CN
LiAlH4
CH2NH2
47
29.09.2021
48.
6.3. Восстановление хлорангидридовкарбоновых кислот – реакция Розенмунда
O
O
R
+
C
H2
R
Cl
+
C
HCl
H
Реакция была открыта в 1872 году А.М. Зайцевым и подробно
исследована К.В. Розенмундом в 1918 году
29.09.2021
48
49.
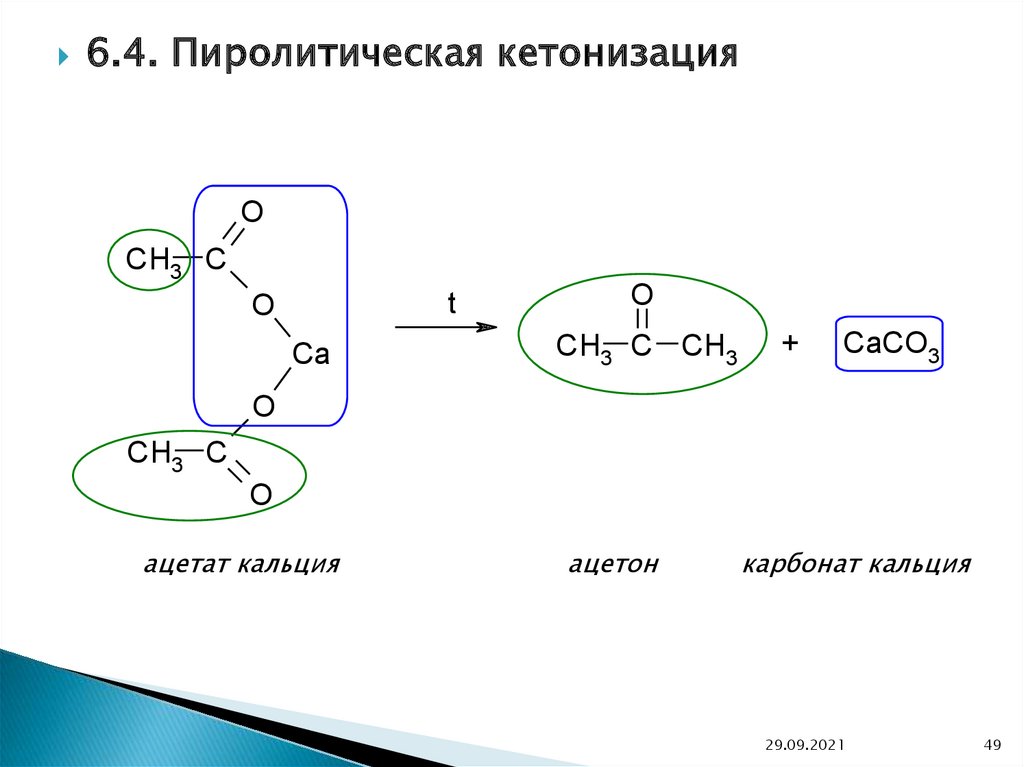
6.4. Пиролитическая кетонизацияO
CH3 C
t
O
Ca
O
CH3 C CH3
+
CaCO3
O
CH3 C
O
ацетат кальция
ацетон
карбонат кальция
29.09.2021
49
50.
6.4. Оксосинтез (гидроформилирование)Присоединение угарного газа и водорода к
алкенам в присутствии кобальтовых
катализаторов при нагревании 140-180oC и
давлении 3-8 МПа:
H3C CH2 C
H2C CH2 + CO + H2
H
O
H
6.5. Реакция Кучерова
C
C
H + H2O
HgSO4
O
H2C
C
H
H3C
C
H
OH
виниловый спирт
этаналь
29.09.2021
50
51.
6.6. Реакция Вакера-Хёхста2 H2C CH2 + O2
PdCl2, CuCl2
O
2 CH3 C
H
Эта реакция в настоящее время в основном используется для
промышленного синтеза ацетальдегида.
Ацетальдегид (этаналь, уксусный альдегид), СН3СНО, бесцветная
жидкость с резким запахом, tкип = 20,2 °С.
Сырье в производстве уксусной кислоты, уксусного ангидрида и
других продуктов. Уксусный ангидрид, в свою очередь, используется
для получения ацетатного волокна.
29.09.2021
51
52.
6.7. Другие синтезыR
R
R
O
O3
2R
R
R
R C
R
R
C R
O
HIO4
2R
C R
C
R
OH OH
R C
C
BH3
H2O2
O
R CH2 C
R
Br
R C
C H
+
2 HBr
R C
CH3
KOH, H2O
O
R C
CH3
Br
29.09.2021
52
53.
29.09.202153










































 Химия
Химия








