Похожие презентации:
Общая характеристика металлов
1.
Общая характеристикаметаллов
Учитель химии МБОУ «Тулатинская средняя
общеобразовательная школа»
Тарасенко Т.В.
2.
Положение металлов впериодической системе
1. Определите местоположение
металлов в периодической системе
2. Назовите самые
распространённые на ваш взгляд
металлы, ответ обоснуйте.
3.
ВI-III группа (кроме Н и В)
IV-VIII группа ( в конце группы)
Побочные подгруппы
Fr
At
4.
Строение атомаМе
Внешний слой от 1 до 3 е
Исключение Ме IV –VII А групп
Rа Ме R а неМе
5.
Окислительно-восстановительные свойства0
А)Ме - ne
+n
Ме (окисление)
восстановитель
Б) Возможные степени окисления МЕ
Низшая 0,+1,+2,+3
Высшая +4,+5,+6,+7,+8
Приведите пример соединений
металлов с указанными степенями
окисления металлов
6.
В) Изменение восстановительных свойствметаллов в периодической системе
в периоде
уменьшаются
увеличиваются
7.
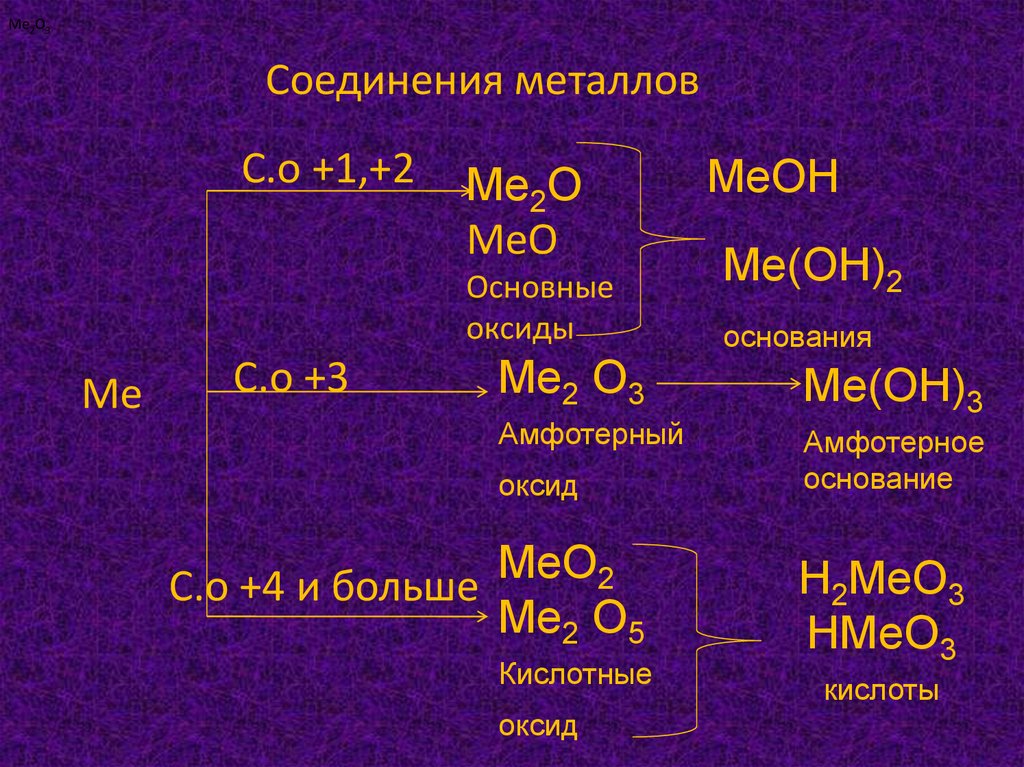
Ме2О3Соединения металлов
С.о +1,+2
Ме2О
МеО
Основные
оксиды
Ме
С.о +3
Ме2 О3
Амфотерный
оксид
МеО
2
С.о +4 и больше
Ме2 О5
Кислотные
оксид
МеОН
Ме(ОН)2
основания
Ме(ОН)3
Амфотерное
основание
Н2МеО3
НМеО3
кислоты
8.
Летучие водородные соединения необразуют, но с водородом образуют
твёрдые вещества гидриды
МеН IА группа
МеН2 II А группа и т.д
9.
Нахождение в природеАктивные Ме – только в виде
соединений NaCl, Ca3(PO4)2
Менее активные Ме – в
виде соединений и в
свободном виде (Sn,Pb, Cu)
Неактивные Ме –в
свободном виде (Pt,Au)
10.
Характеристика простых веществ металлов1.Строение молекулы
А)Молекулы Ме - одноатомны
Металлическая связь
Металлическая
кристаллическая
решётка
Твёрдые (кроме ртути),
пластичные, тепло- и
электропроводные, имеют
металлический блеск
11.
Б) Изменение физических свойствв периодической таблице
В периоде
Твёрдость, температура плавления и кипения –
уменьшаются( причина: увеличение числа электронов
на внешнем слое, увеличивается порядковый номер,
частично уменьшается радиус атома)
В группе главной подгруппе эти
свойства увеличиваются
12.
Самый лёгкий металл P˂5 г/см3Li p=0,53 г/см3
Самый тяжёлый металл Р ˃ 5 г/см3
Os p=22,6 г/см3
13.
Мелёгкие
тяжёлые
Ме
мягкие
твёрдые
14.
Ме0С
Тугоплавкие
t
пл˃1000
легкоплавкие
Hg t пл= -38,9 0С
W t пл= 33900С
15.
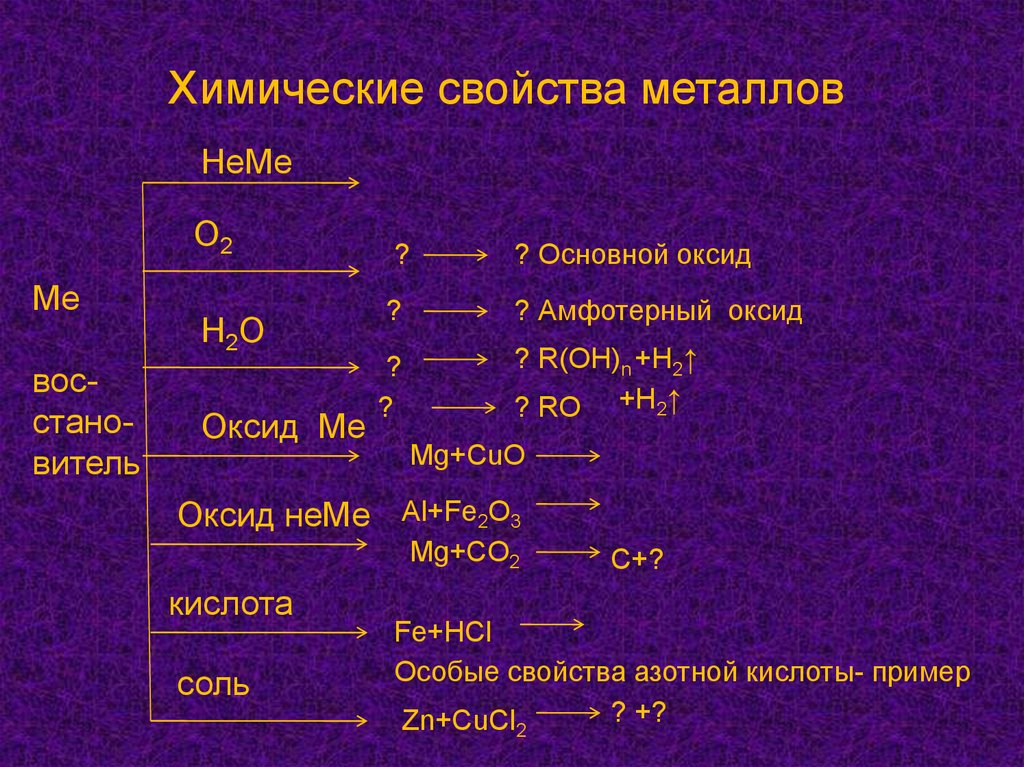
Химические свойства металловНеМе
О2
Ме
восстановитель
Н2О
Оксид Ме
?
? Основной оксид
?
? Амфотерный оксид
?
?
? R(OH)n +H2↑
? RO +H2↑
Mg+CuO
Оксид неМе Al+Fe2O3
Mg+CO2
кислота
соль
C+?
Fe+HCl
Особые свойства азотной кислоты- пример
? +?
Zn+CuCl
2
16.
Домашнее заданиеП..20, записать уравнения
химических реакций
характеризующих схему
химические свойства металлов,
з.1 стр 89













 Химия
Химия








