Похожие презентации:
Окислительно-восстановительные процессы
1.
Тема: Окислительновосстановительные процессы2.
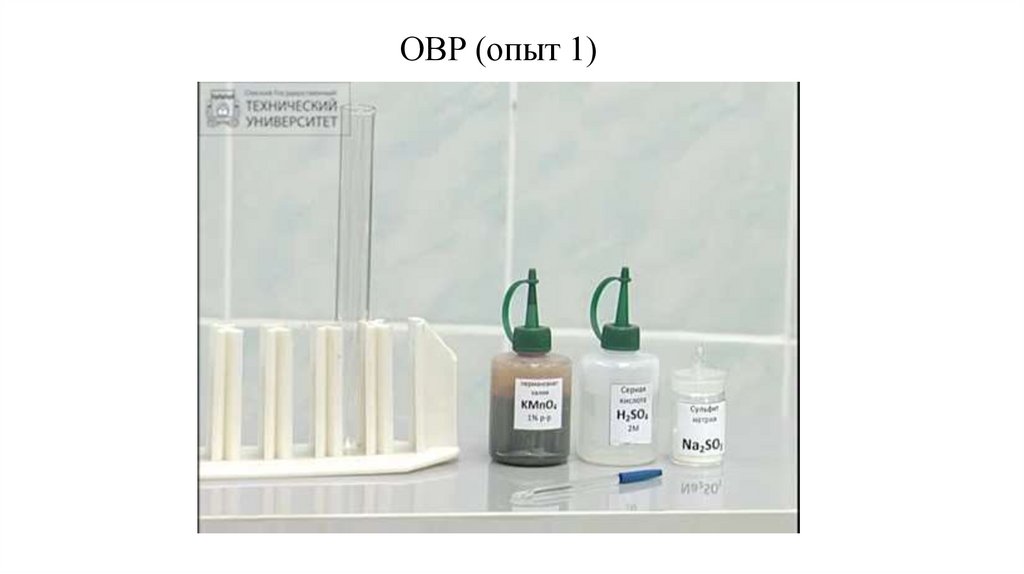
ОВР (опыт 1)3.
ОВР (опыт 2)4.
ОВР (опыт 3)5.
Рассмотрим метод электронного баланса дляуравнения реакции Р + О2 → Р2О5
Р0 - 5е- → Р+5
О20 +4е- →2О-2
Р0 - 5е- → Р+5 окисление
восстановитель
О20 +4е- →2О-2 восстановление
окислитель
Далее необходимо перенести коэффициенты в исходную схему, преобразуя
её в уравнение реакции.
4Р + 5О2 → 2Р2О5
6.
Рассмотрим метод электронного баланса для уравненияреакции
KMnO4 +HCl → KCl + MnCl2 +Cl2 +H2O
2
Mn+7 + 5е- → Mn+2
5
2Cl-1 - 2е- → Cl20
10
Перенести коэффициенты в исходную схему, преобразуя её в уравнение
реакции:
2KMnO4 +HCl → KCl +2MnCl2 +5Cl2 +H2O
7.
Перед формулой HCl коэффициент пока не поставлен, т.к невсе
ионы
Cl-1
участвовали
в
окислительновосстановительном процессе, часть из них принимала
участие в образовании солей. Поэтому требуется уравнять
число атомов элементов, не участвующих в окислительновосстановительном процессе (К, Н, частично Cl). Получаем
уравнение:
2KMnO4 +16HCl →2KCl +2MnCl2 +5Cl2 +8H2O
8.
Формативное оцениваниеЗадание: закончить уравнения реакций, расставить коэффициенты методом электронного баланса в
реакциях которых вы увидели в опытах в начале урока
KMnO4 + Na2SO3 + H2SO4 →
KMnO4 + Na2SO3 + H2O →
KMnO4 + Na2SO3 + NaOH →
9.
Подведение итогов урока«True» or «False»
- окислитель – элемент, который отдает электроны;
- восстановление – процесс отдачи электронов;
- восстановитель – элемент, который принимает электроны;
- окисление – процесс принятия электронов;
- сера в реакции горения с кислородом проявляет свойства
окислителя;
- степень окисления хрома в хромате калия равна +6.
- степень окисления кислорода в пероксиде водорода равна -2.








 Химия
Химия








