Похожие презентации:
Пиридин. Строение пиридина
1. Химия гетероциклических соединений
Лекция 5Пиридин
2.
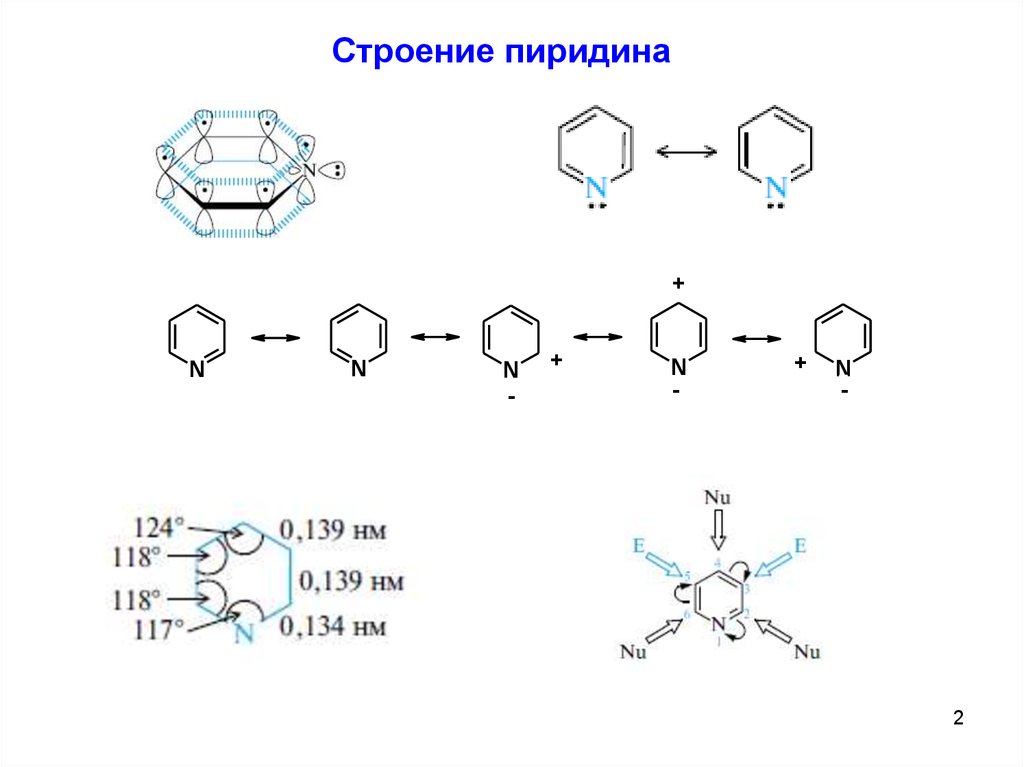
Строение пиридина+
N
N
N
-
+
N
-
+
N
-
2
3.
Синтез ГанчаПолучение пиридинов циклоконденсацией b-кетоэфиров с альдегидами и NH3
через стадию окисления первоначально образующихся дигидропиридинов.
O
O
2
R
O
O
+
1
R
OR
+
2
H
R
2
O
OR
RO
NH3
R
1
N
R
1
Механизм реакции
O
образование енамина
образование
непредельного
кетона
NH3
CO2Et
H3C
O
H3C
CO2Et
NH2
CO2Et
- HOH H C
3
O
CH2O
- HOH
H3C
CO2Et
CH2
присоединение по Михаэлю енамина к непредельному кетону
EtOOC
H2C
H3C
NH2 O
CH2OEt
CH3
EtOOC
H3C
COOEt
EtOOC
COOEt
-
O
NH2 CH3
+
H3C
O
NH2 CH3
3
4.
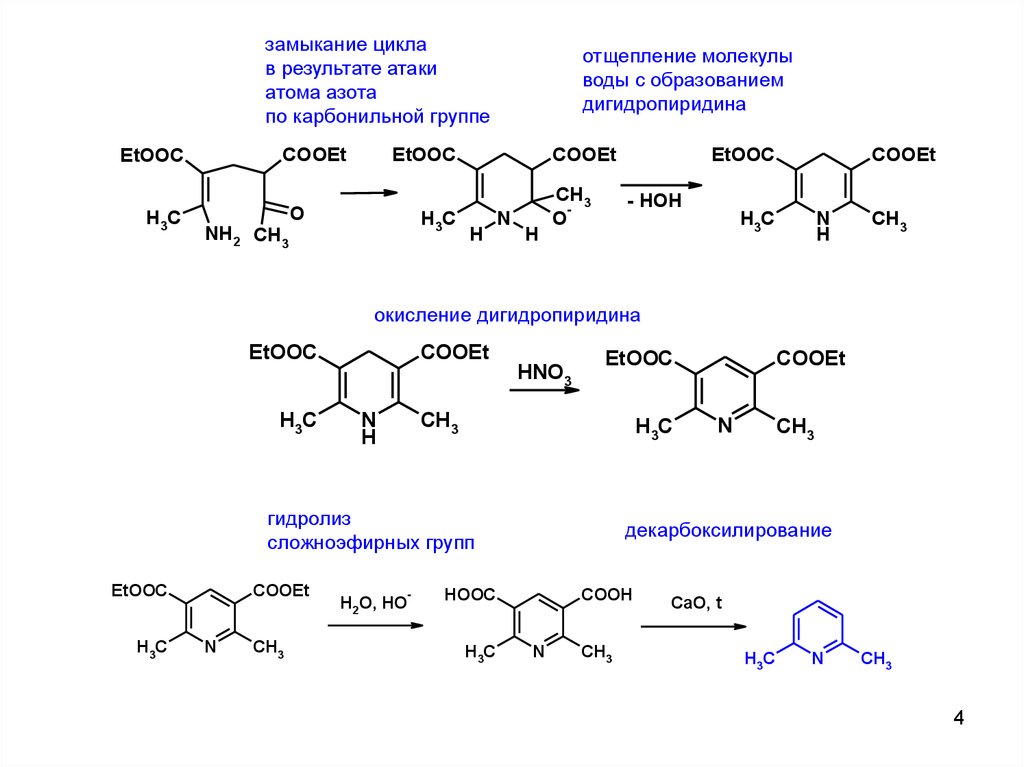
замыкание циклав результате атаки
атома азота
по карбонильной группе
COOEt
EtOOC
H3C
отщепление молекулы
воды с образованием
дигидропиридина
COOEt
EtOOC
O
H3C
NH2 CH3
H
N
H
CH3
O
EtOOC
COOEt
- HOH
N
H
H3C
CH3
окисление дигидропиридина
EtOOC
COOEt
HNO3
H3C
N
H
EtOOC
CH3
H3C
гидролиз
сложноэфирных групп
EtOOC
H3C
COOEt
N
CH3
-
H2O, HO
N
CH3
декарбоксилирование
HOOC
H3C
COOEt
COOH
N
CH3
CaO, t
H3C
N
CH3
4
5.
Подбор синтонов для построения2,4,6-тризамещенных пиридинов
Ph
CHO
EtOOC
Ph
COOEt
EtOOC
COOEt
+
Ph
O
Ph
O
Ph
Ph
N
H
HNO3
Ph
Ph
EtOOC
COOEt
1) H2O, HO
Ph
2) H
3) Cu, t
-
+
Ph
N
Ph
N
Ph
Пропускание смеси ацетилена и синильной кислоты через раскаленную трубку
2
HC CH
HCN, t
N
Реакция Дильса-Альдера взаимодействием бутадиена с нитрилами
при высокой (400 °С) температуре
R
N
N
R
5
6.
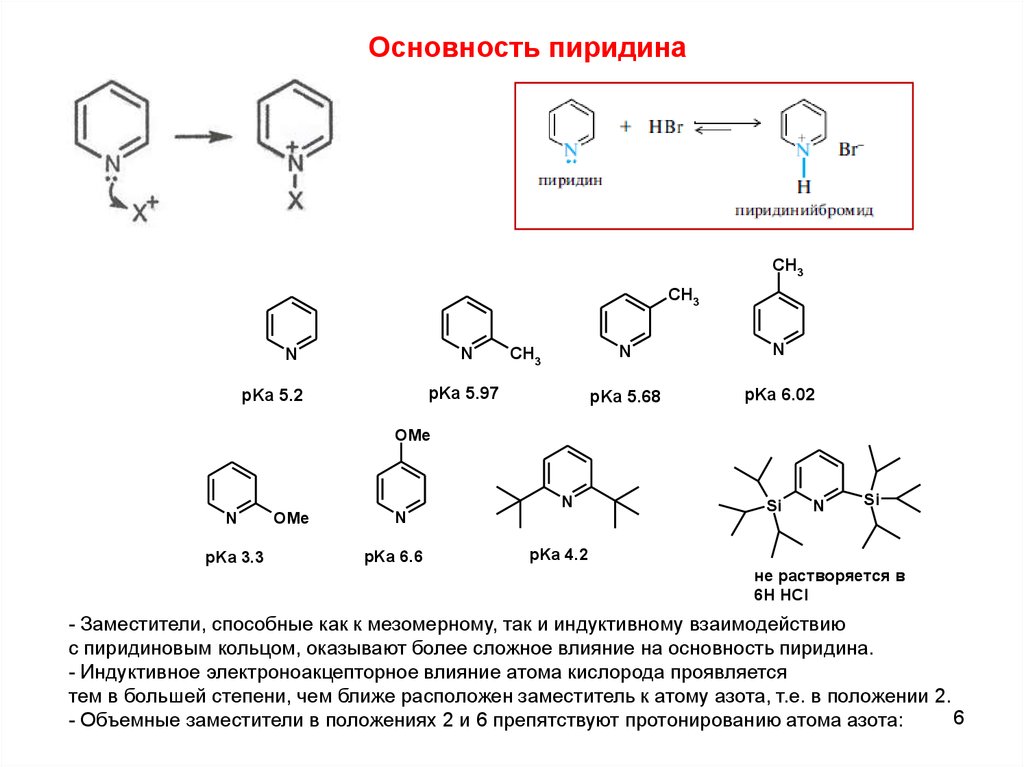
Основность пиридинаCH3
CH3
N
N
CH3
pKa 5.97
pKa 5.2
N
N
pKa 5.68
pKa 6.02
OMe
N
N
pKa 3.3
OMe
N
pKa 6.6
Si
N
Si
pKa 4.2
не растворяется в
6Н HCl
- Заместители, способные как к мезомерному, так и индуктивному взаимодействию
с пиридиновым кольцом, оказывают более сложное влияние на основность пиридина.
- Индуктивное электроноакцепторное влияние атома кислорода проявляется
тем в большей степени, чем ближе расположен заместитель к атому азота, т.е. в положении 2.
6
- Объемные заместители в положениях 2 и 6 препятствуют протонированию атома азота:
7.
Реакции электрофильного замещения+
N
+
E
H
N
E
H
N
+
E
H
крайне
невыгодная
структура
E H
E H
E H
+
+
N
N
+ крайне
N
невыгодная
структура
H
H
N
E
+
H
+
E
E
+
N
N
Атака электрофила идет в положение 3. По реакционной способности в реакциях
электрофильного замещения пиридин напоминает нитробензол.
7
8.
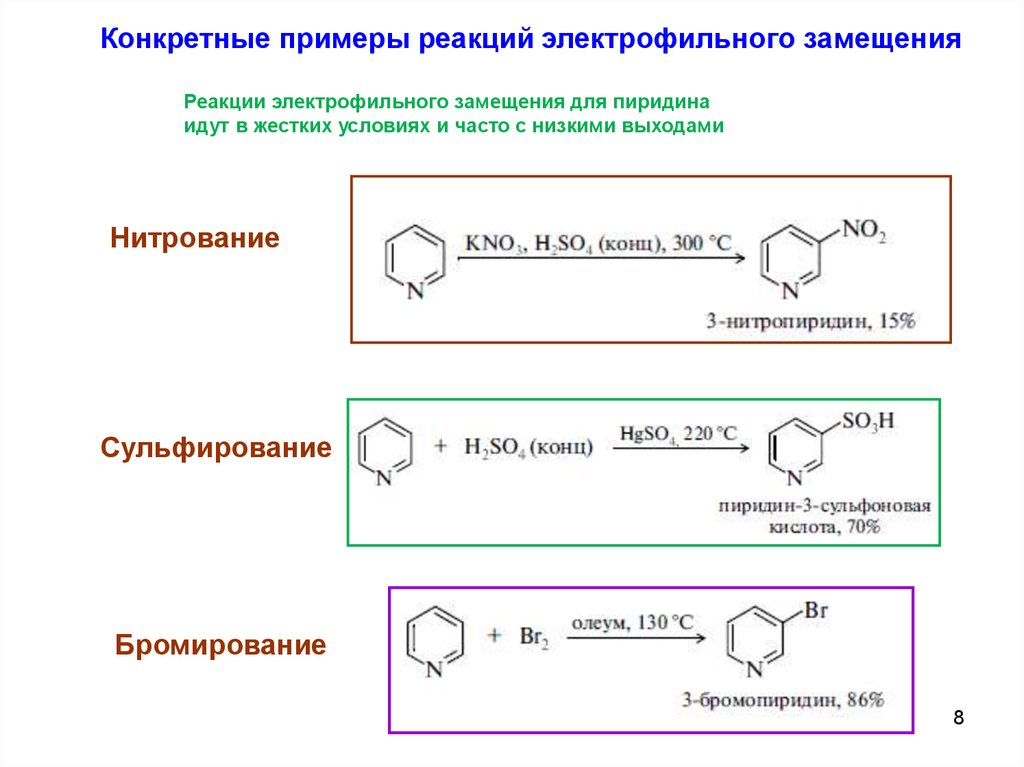
Конкретные примеры реакций электрофильного замещенияРеакции электрофильного замещения для пиридина
идут в жестких условиях и часто с низкими выходами
Нитрование
Сульфирование
Бромирование
8
9.
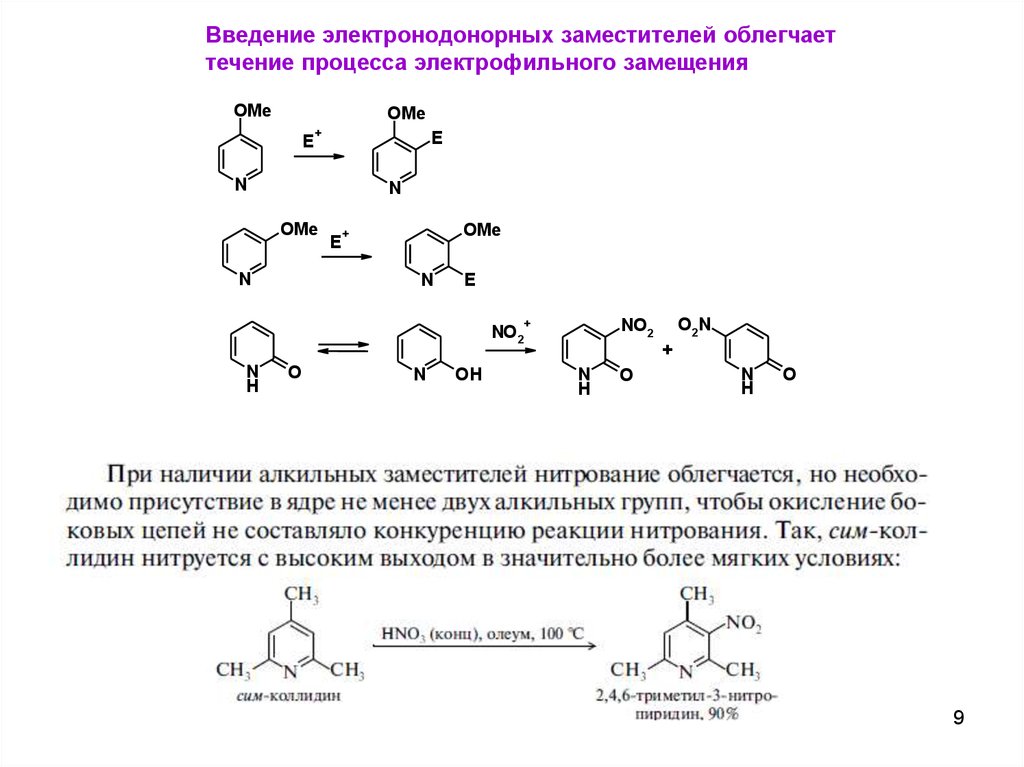
Введение электронодонорных заместителей облегчаеттечение процесса электрофильного замещения
OMe
OMe
E
+
E
N
N
OMe
N
E
OMe
+
N
E
NO2
N
H
O
N
OH
O2 N
NO2
+
+
N
H
O
N
H
O
9
10.
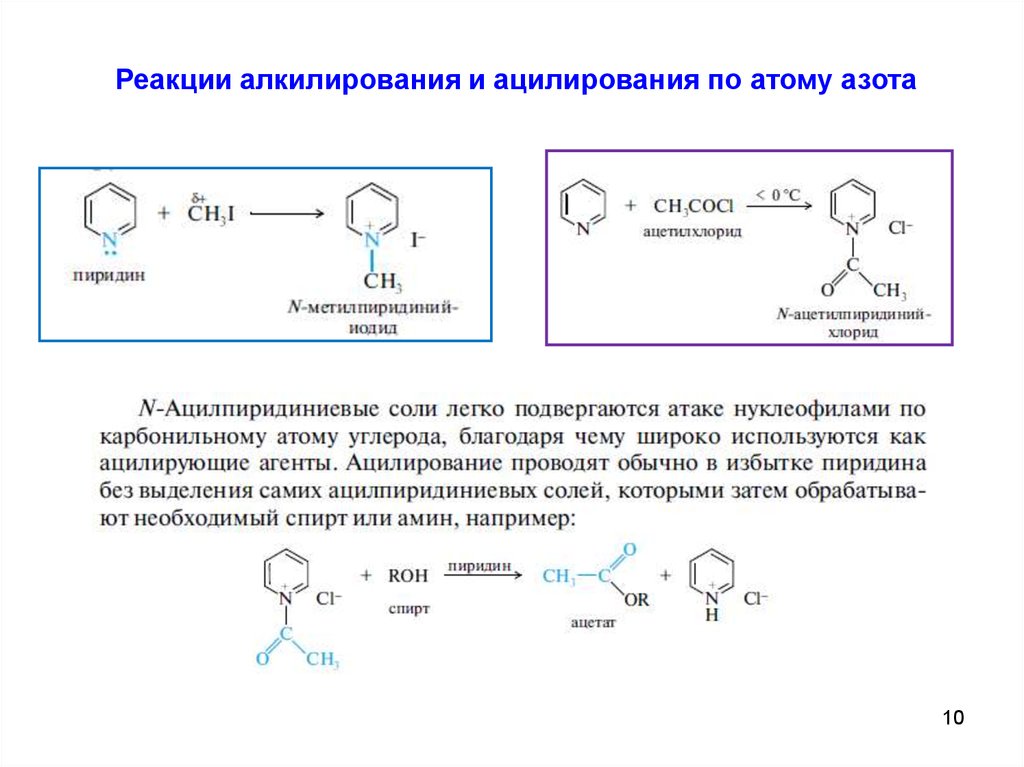
Реакции алкилирования и ацилирования по атому азота10
11.
Реакции нуклеофильного замещения в пиридинеАминирование по Чичибабину
При аминировании пиридина
по Чичибабину получаются
главным образом пиридины
с аминогруппой в a-положении
Механизм
- NH2
N
+ Na
H
N
- Na +
H
промежуточный
циклический комплекс
11
12.
При пропускании паров пиридина над твердой КОН при 300-320 0Сс небольшим выходом образуется 2-пиридон
KOH, t
N
N
H
OH
N
OH
N
H
O
12
13.
Избирательное замещениев 3,4-дигалогенопроизводных пиридина
13
14.
Восстановление пиридинаH2, Ni
N
H
LiAlH4
N
H
N
H
H
1,2-дигидропиридин
пиперидин
Na, EtOH
H H
N
H
1,4-дигидропиридин
14
15.
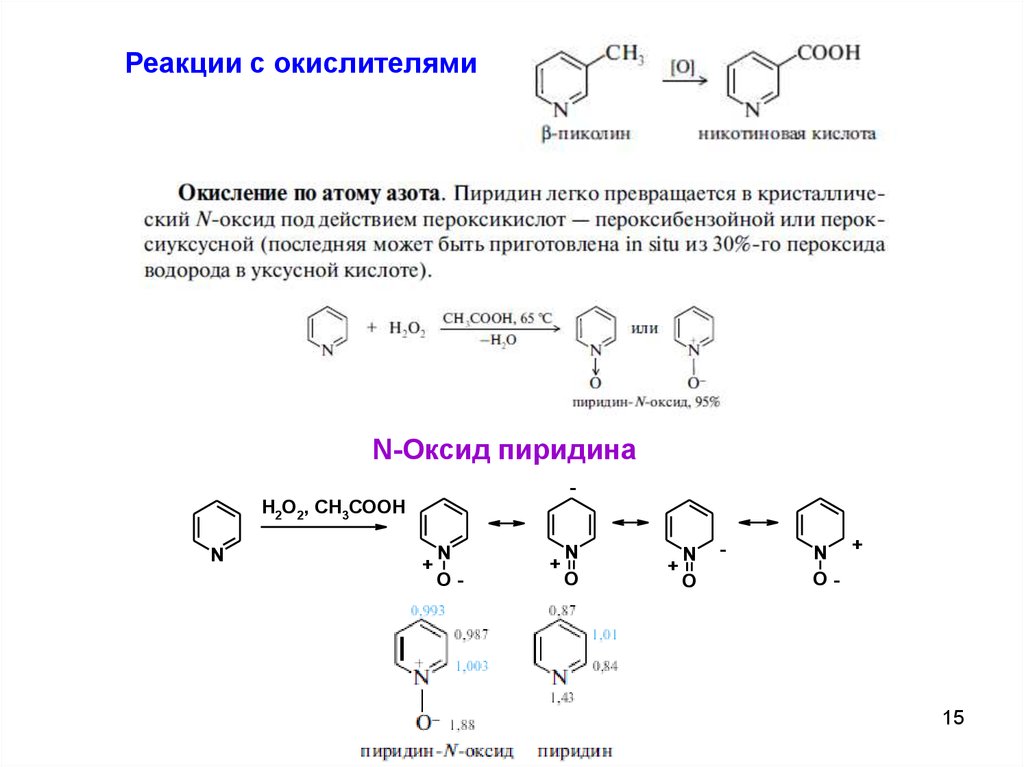
Реакции с окислителямиN-Оксид пиридина
H2O2, CH3COOH
N
N
+
O-
N
+
O
N
+
O
-
N +
O-
15
16.
Электрофильное замещение в N-оксиде пиридина протекает в положения 2 и 4NO2
Cl
Cl
HCl
[H]
+
N
O-
- HNO2
+
N
N
O-
SO3H
SO3H
H2SO4
+
N
O-
[H]
+
N
O-
SO3H
N
SO3H
16
17.
Конденсации с участием 2-метилпиридина и 4-метилпиридна17
18.
Таутомерные превращения гидроксипиридинов18
19.
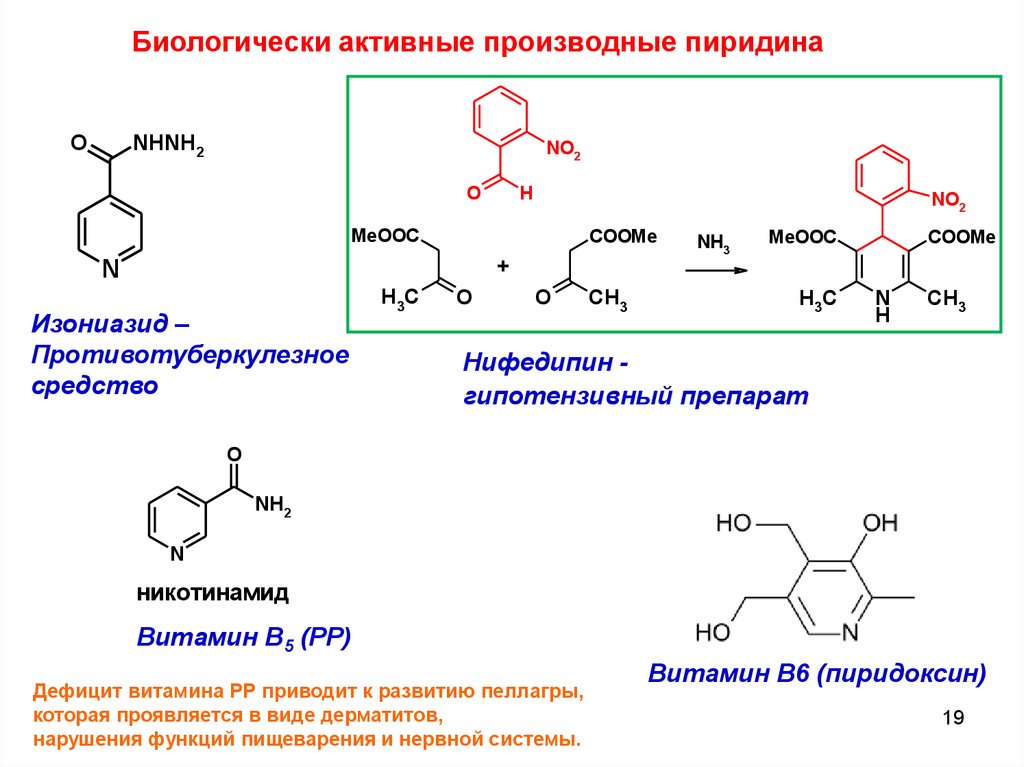
Биологически активные производные пиридинаNHNH2
O
NO2
O
H
NO2
MeOOC
COOMe
N
NH3
MeOOC
COOMe
+
Изониазид –
Противотуберкулезное
средство
H3C
O
O
CH3
H3C
N
H
CH3
Нифедипин гипотензивный препарат
O
NH2
N
никотинамид
Витамин В5 (РР)
Дефицит витамина РР приводит к развитию пеллагры,
которая проявляется в виде дерматитов,
нарушения функций пищеварения и нервной системы.
Витамин В6 (пиридоксин)
19
20.
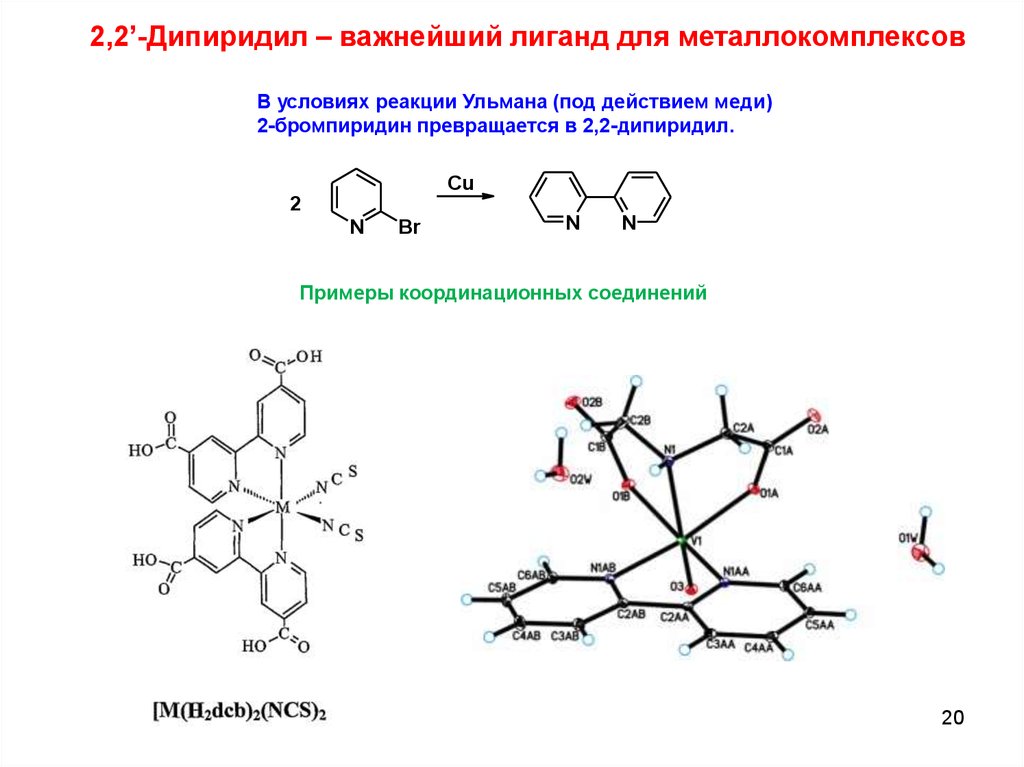
2,2’-Дипиридил – важнейший лиганд для металлокомплексовВ условиях реакции Ульмана (под действием меди)
2-бромпиридин превращается в 2,2-дипиридил.
Cu
2
N
Br
N
N
Примеры координационных соединений
20
21.
Курс лекций является частью учебно-методического комплекса«Химия гетероциклических соединений»
автор:
Носова Эмилия Владимировна, д.х.н., доцент кафедры органической химии УГТУ-УПИ
Учебно-методический комплекс подготовлен на кафедре органической и
биомолекулярной химии химико-технологического института УрФУ
Никакая часть презентации не может быть воспроизведена в
какой бы то ни было форме без письменного разрешения авторов
21 12












 Химия
Химия








