Похожие презентации:
Химические свойства фурана, пиррола, тиофена. Биологически активные производные ряда фурана, пиррола, тиофена. (Лекция 3)
1. Химия биологически активных веществ
Лекция 31. Другие химические свойства
фурана, пиррола, тиофена
2. Биологически активные производные
ряда фурана, пиррола, тиофена
2.
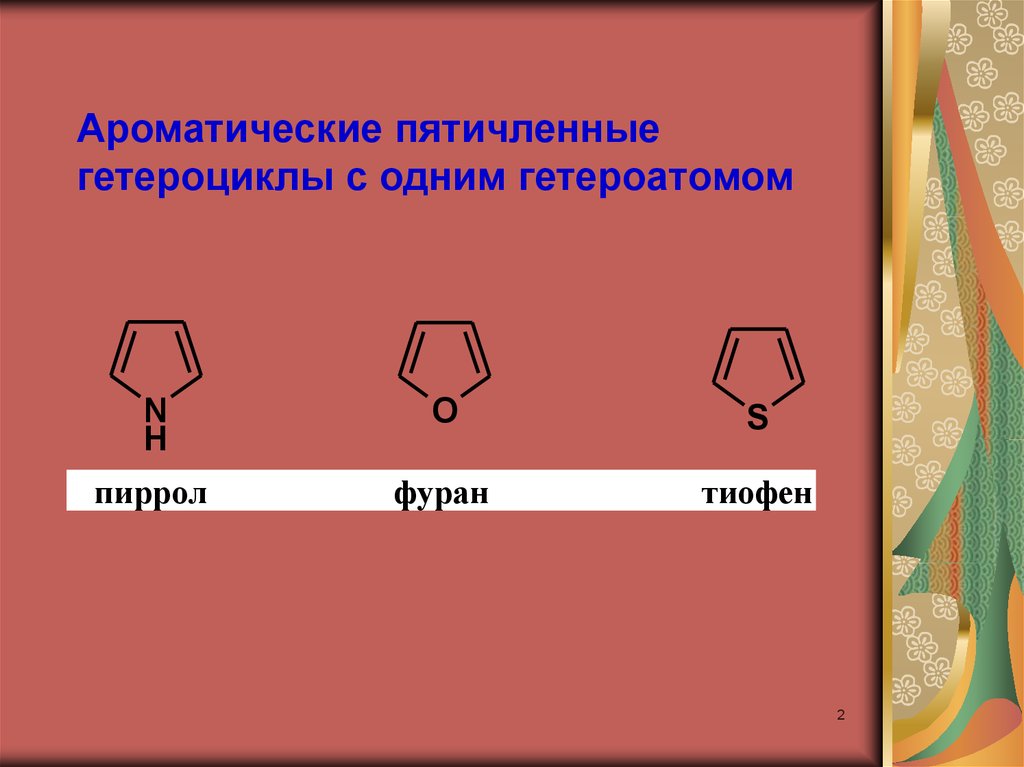
Ароматические пятичленныегетероциклы с одним гетероатомом
N
H
O
S
пиррол
фуран
тиофен
2
3.
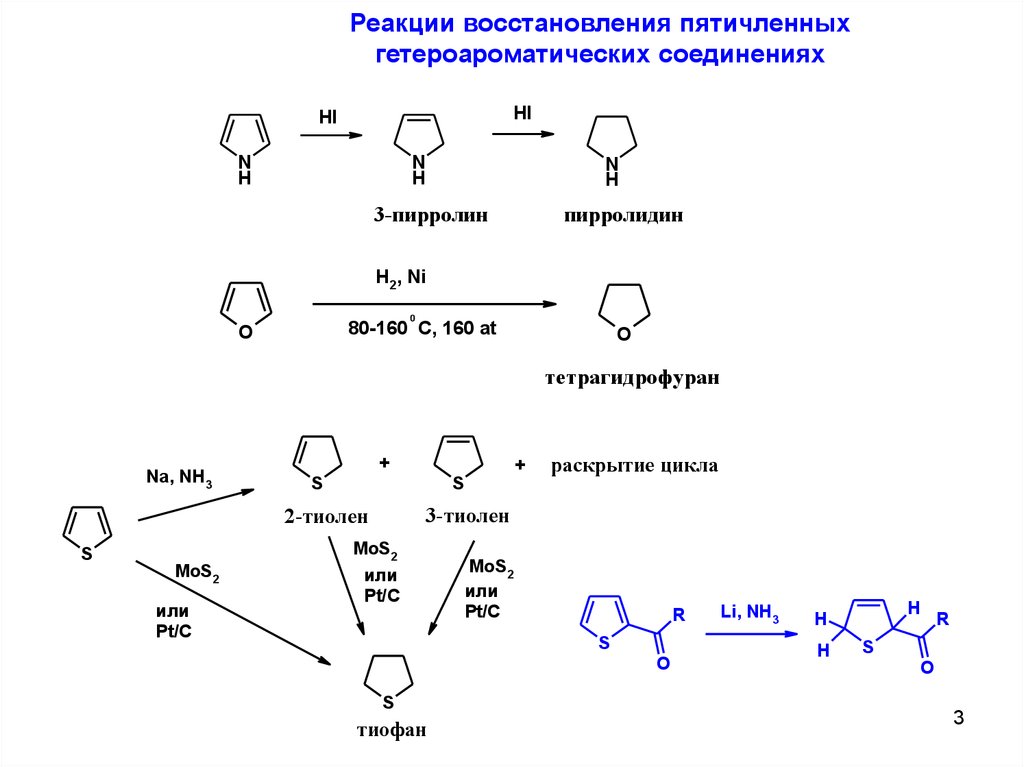
Реакции восстановления пятичленныхгетероароматических соединениях
HI
HI
N
H
N
H
N
H
3-пирролин
пирролидин
H2, Ni
0
80-160 C, 160 at
O
O
тетрагидрофуран
Na, NH3
MoS2
или
Pt/C
раскрытие цикла
S
S
3-тиолен
2-тиолен
S
+
+
MoS2
или
Pt/C
MoS2
или
Pt/C
R
S
O
S
тиофан
Li, NH3
H
H
H
R
S
O
3
13
4.
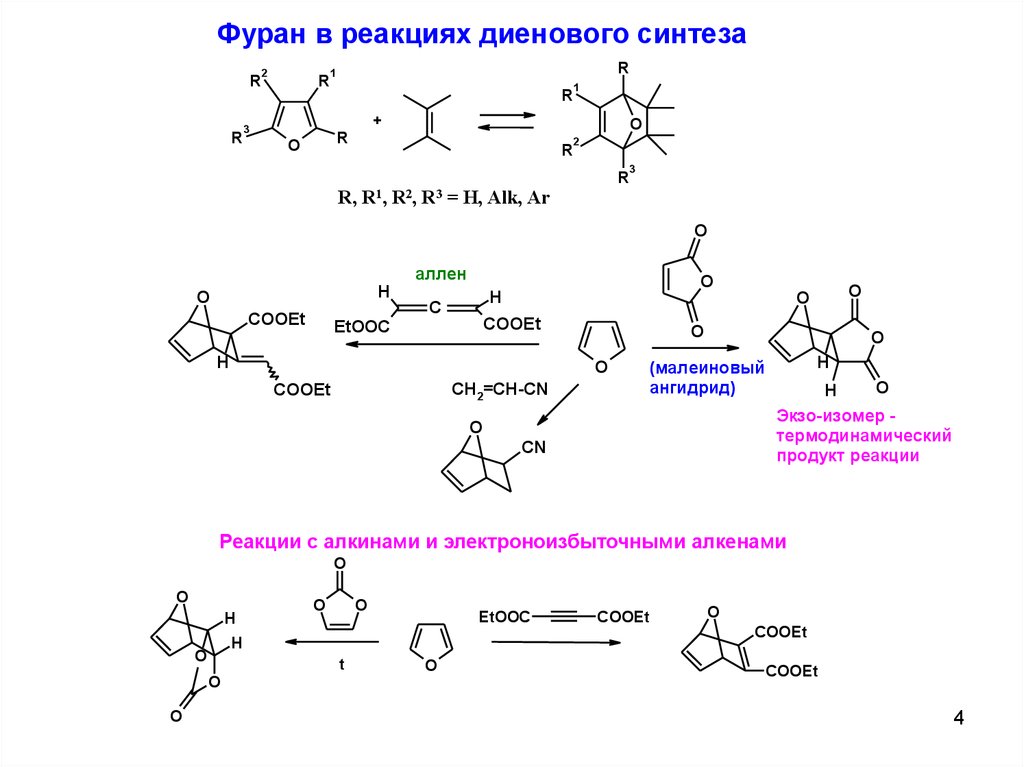
Фуран в реакциях диенового синтезаR
R
2
R
R
1
R
1
+
3
O
R
O
R
2
R
R, R1, R2, R3 = H, Alk, Ar
3
O
аллен
H
O
C
COOEt
O
H
COOEt
EtOOC
H
O
O
CH2=CH-CN
COOEt
O
O
O
(малеиновый
ангидрид)
O
CN
H
O
H
Экзо-изомер термодинамический
продукт реакции
Реакции с алкинами и электроноизбыточными алкенами
O
O
H
O
EtOOC
t
O
COOEt
O
COOEt
H
O
O
O
O
COOEt
4
5.
Особенности реакции Дильса–Альдерав ряду производных пиррола
O
O
O
O
H
N
H
N
H
+
O
H
H
MeOOC
N
H
N
H
O
COOMe
COOMe
N
H
N
H
COOMe
C(O)CH3
MeOOC
COOMe
N
N
C(O)CH3
Высокое давление
и присутствие AlCl3
ускоряют реакцию
COOEt
COOEt
N
SiMe3
+
N
SiMe3
Реакции на основе
N-трет-бутилоксикарбонилпиррола
NBoc
CH2
Br
CH2=C=CHSO2Ph
COOMe
NBoc
Br
N
SO2Ph
Boc
COOMe
5
6.
Особенности реакции Дильса–Альдерав ряду производных тиофена
O
O
S
O
O
H
S
15 кбар
O
H O
Экструзия атома серы из первоначально
образующихся продуктов
S
MeS
OMe
S
MeOOC
COOMe
MeO
COOMe
COOMe
MeS
MeO
COOMe
MeS
COOMe
фталаты
6
7.
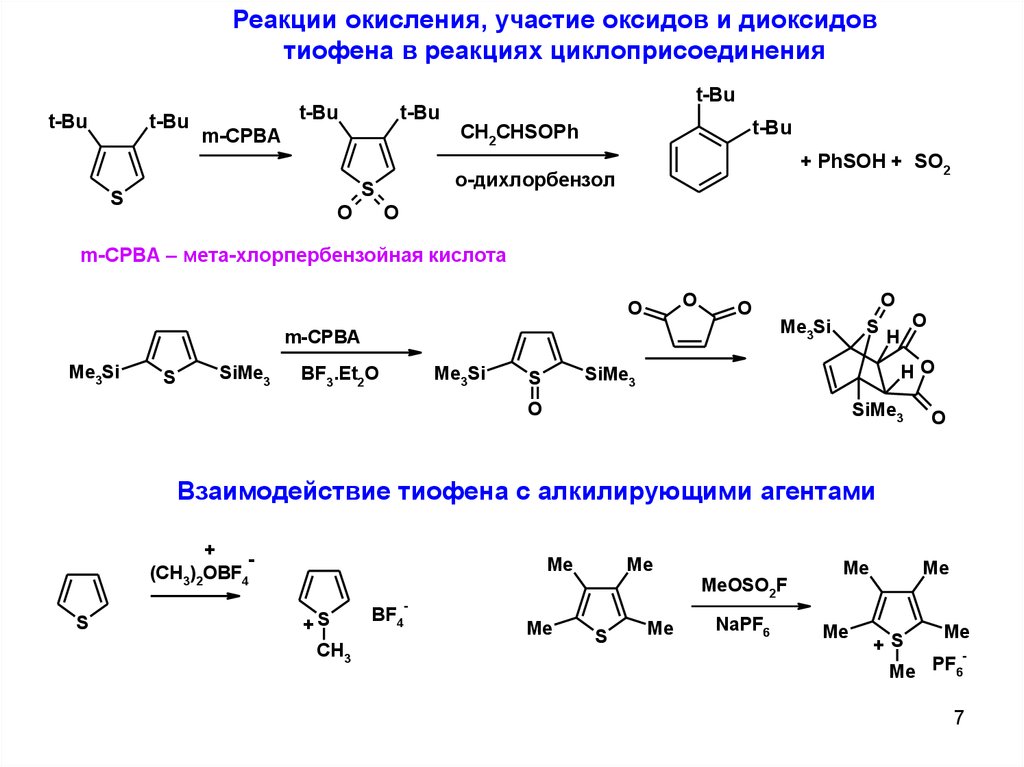
Реакции окисления, участие оксидов и диоксидовтиофена в реакциях циклоприсоединения
t-Bu
t-Bu
t-Bu
t-Bu
CH2CHSOPh
m-CPBA
O
+ PhSOH + SO2
о-дихлорбензол
S
S
t-Bu
t-Bu
O
m-CPBA – мета-хлорпербензойная кислота
O
O
Me3Si
m-CPBA
Me3Si
S
SiMe3
O
O
Me3Si
BF3.Et2O
S
HO
SiMe3
S
O
H
O
SiMe3
O
Взаимодействие тиофена с алкилирующими агентами
+
(CH3)2OBF4
S
Me
Me
MeOSO2F
+S
CH3
Me
Me
-
BF4
Me
S
Me
NaPF6
Me
Me
+S
Me PF6
7
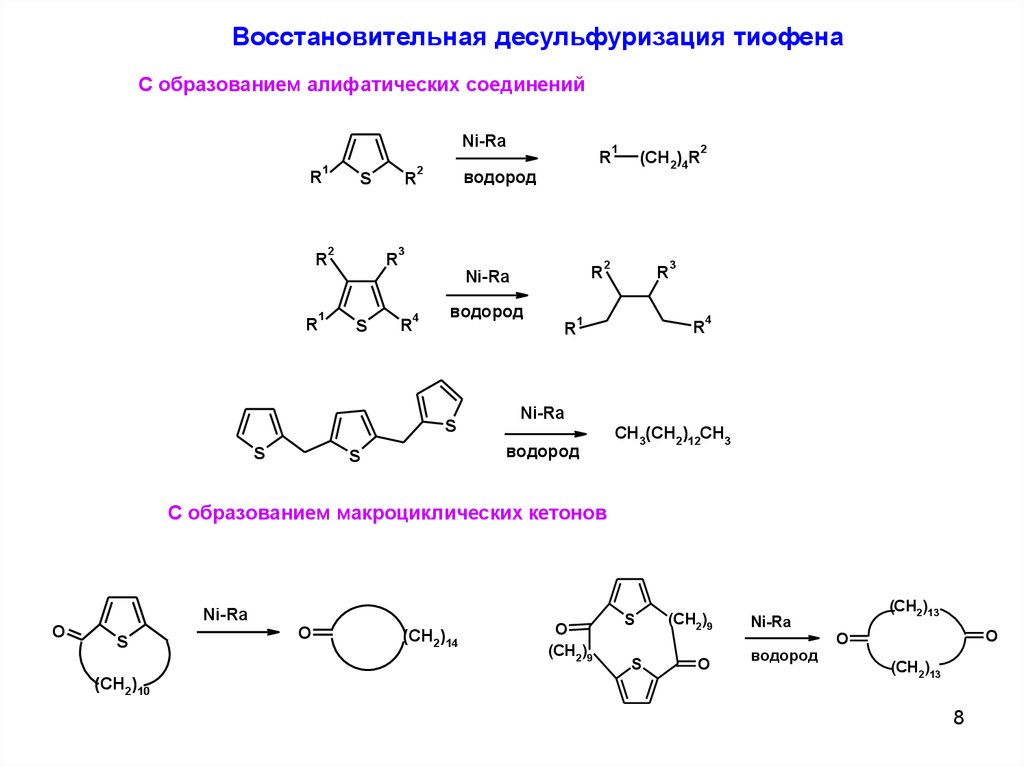
8.
Восстановительная десульфуризация тиофенаС образованием алифатических соединений
Ni-Ra
R
1
R
S
2
R
R
R
2
1
S
2
3
R
4
R
водород
R
S
S
(CH2)4R
водород
Ni-Ra
R
1
2
1
3
R
4
Ni-Ra
водород
S
R
CH3(CH2)12CH3
С образованием макроциклических кетонов
Ni-Ra
O
S
(CH2)10
O
(CH2)14
O
(CH2)9
S
S
(CH2)9
O
(CH2)13
Ni-Ra
водород
O
O
(CH2)13
8
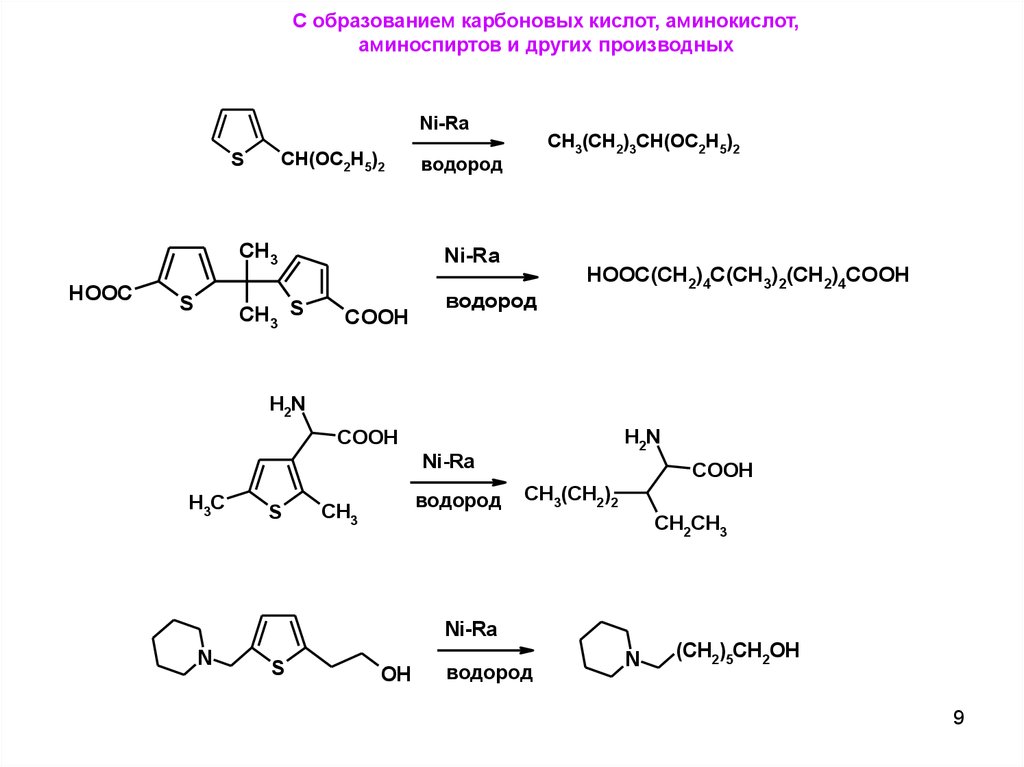
9.
С образованием карбоновых кислот, аминокислот,аминоспиртов и других производных
Ni-Ra
S
CH(OC2H5)2
CH3
HOOC
S
CH3 S
CH3(CH2)3CH(OC2H5)2
водород
Ni-Ra
COOH
водород
HOOC(CH2)4C(CH3)2(CH2)4COOH
H2N
H2N
COOH
Ni-Ra
H3C
S
водород
CH3
COOH
CH3(CH2)2
CH2CH3
Ni-Ra
N
S
OH
водород
N
(CH2)5CH2OH
9
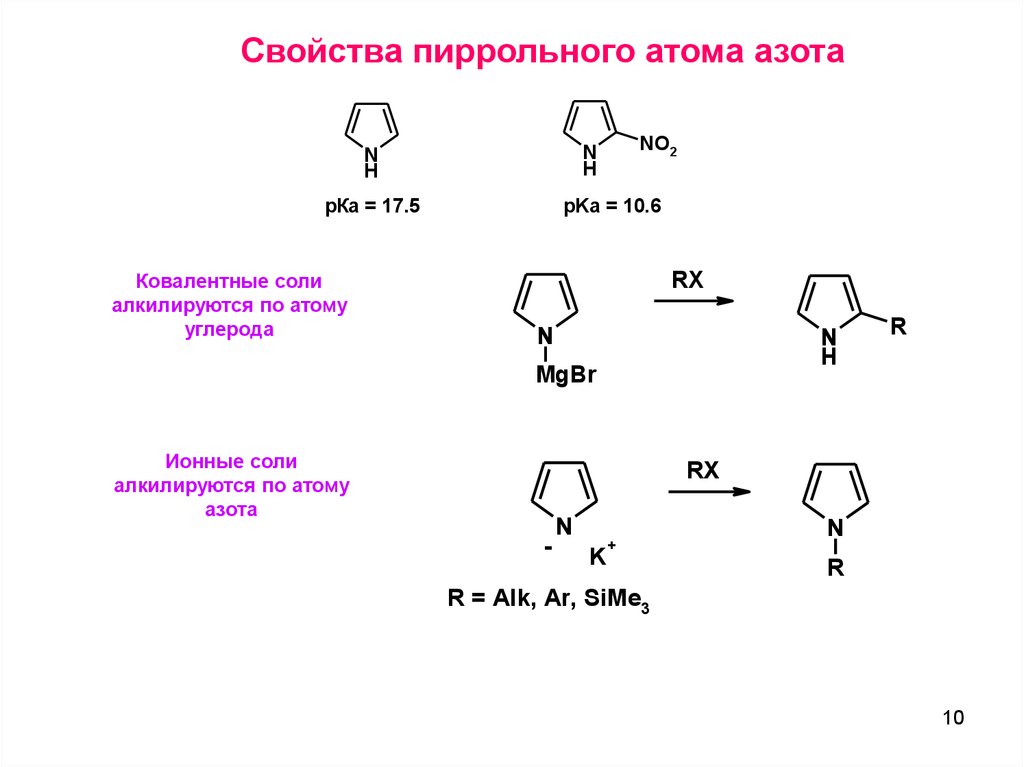
10.
Свойства пиррольного атома азотарКа = 17.5
Ковалентные соли
алкилируются по атому
углерода
NO2
N
H
N
H
pKa = 10.6
RX
N
N
H
MgBr
Ионные соли
алкилируются по атому
азота
R
RX
-
N
K
+
N
R
R = Alk, Ar, SiMe3
10
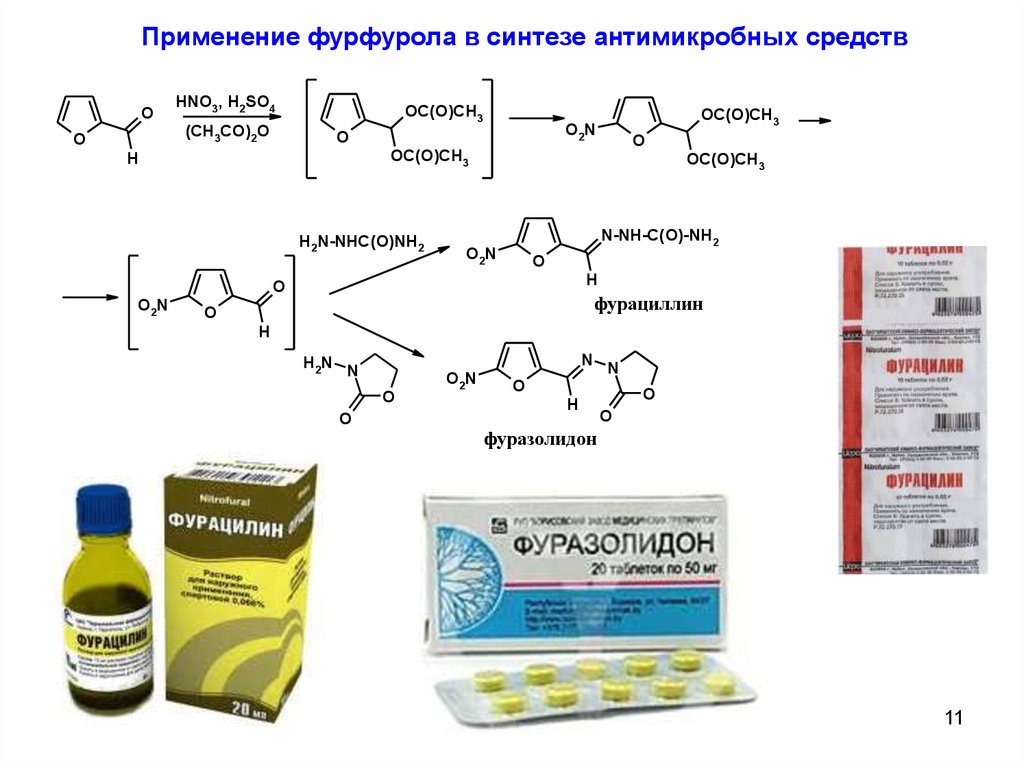
11.
Применение фурфурола в синтезе антимикробных средствO
HNO3, H2SO4
OC(O)CH3
(CH3CO)2O
O
O
O
OC(O)CH3
H
H2N-NHC(O)NH2
OC(O)CH3
N-NH-C(O)-NH2
O2N
O
H
O
O2N
OC(O)CH3
O2N
фурациллин
O
H
H2N
N
N
O
O
O2N
O
H
N
O
O
фуразолидон
11
12.
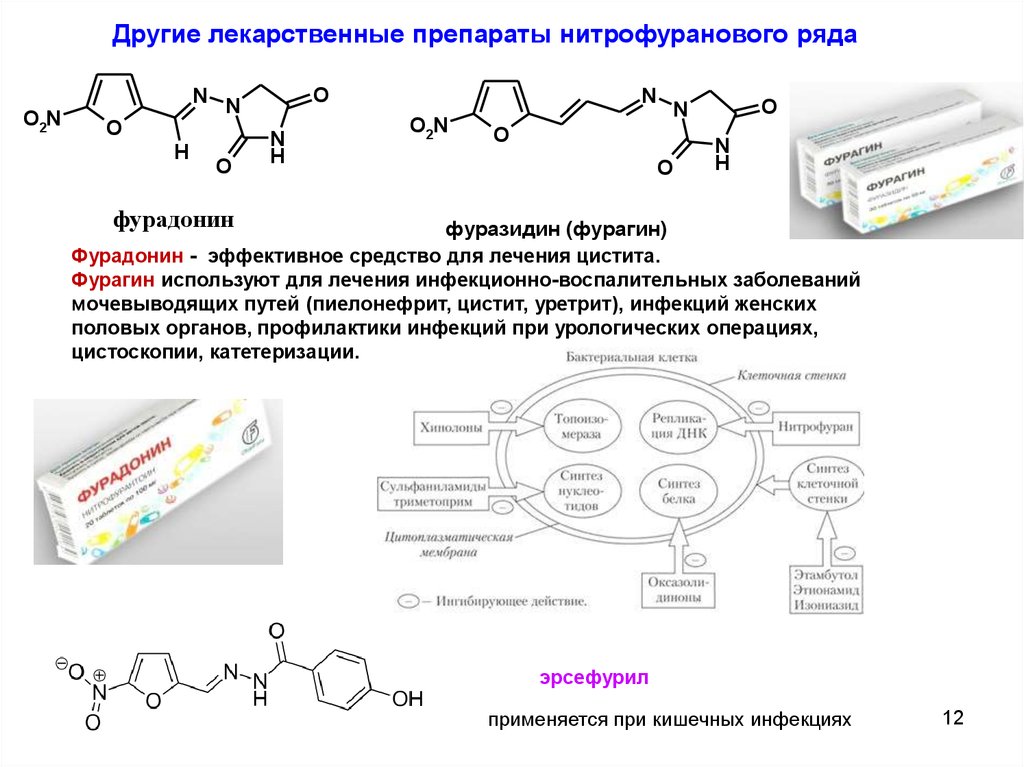
Другие лекарственные препараты нитрофуранового рядаN
O2N
O
H
O
N
O
N
N
H
O2N
O
N
O
O
N
H
фурадонин
фуразидин (фурагин)
Фурадонин - эффективное средство для лечения цистита.
Фурагин используют для лечения инфекционно-воспалительных заболеваний
мочевыводящих путей (пиелонефрит, цистит, уретрит), инфекций женских
половых органов, профилактики инфекций при урологических операциях,
цистоскопии, катетеризации.
эрсефурил
применяется при кишечных инфекциях
12
13.
NO2N
O
N N
N
N
O2N
N
H
N
N
O
фуракрилин
фуразонал
Фуразонал применяют для лечения бактериальной дизентерии.
Фуракрилин используют в хирургической практике при лечении
некротической стадии ран. Фуракрилин превосходит по антимикробной
активности близкий к нему по химическому строению фуразонал в 5—25 раз.
O
Синтез
фуракрилина
H3C
H
O
O2N
O
-
O2N
HO
H
O
5-нитрофурфурол
H2N N
O
H
5-нитрофуралакролеин
N
N
1-амино-1,3,4-триазол
N N
O2N
N
N
O
фуракрилин
13
14.
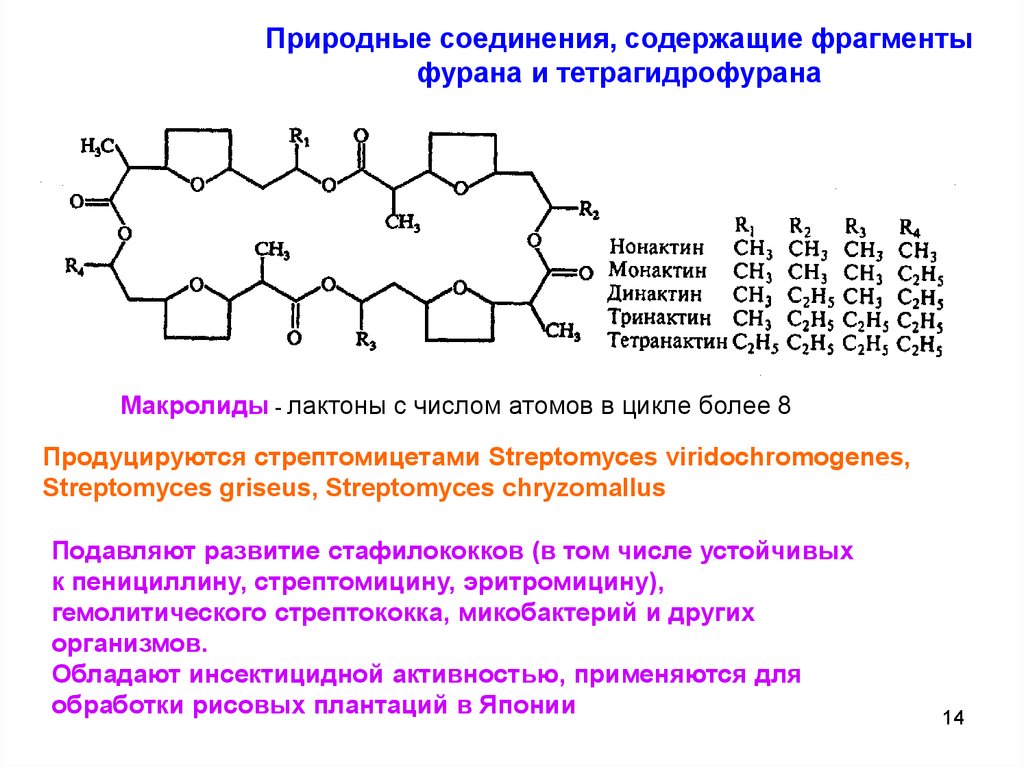
Природные соединения, содержащие фрагментыфурана и тетрагидрофурана
Макролиды - лактоны с числом атомов в цикле более 8
Продуцируются стрептомицетами Streptomyces viridochromogenes,
Streptomyces griseus, Streptomyces chryzomallus
Подавляют развитие стафилококков (в том числе устойчивых
к пенициллину, стрептомицину, эритромицину),
гемолитического стрептококка, микобактерий и других
организмов.
Обладают инсектицидной активностью, применяются для
обработки рисовых плантаций в Японии
14
9
15.
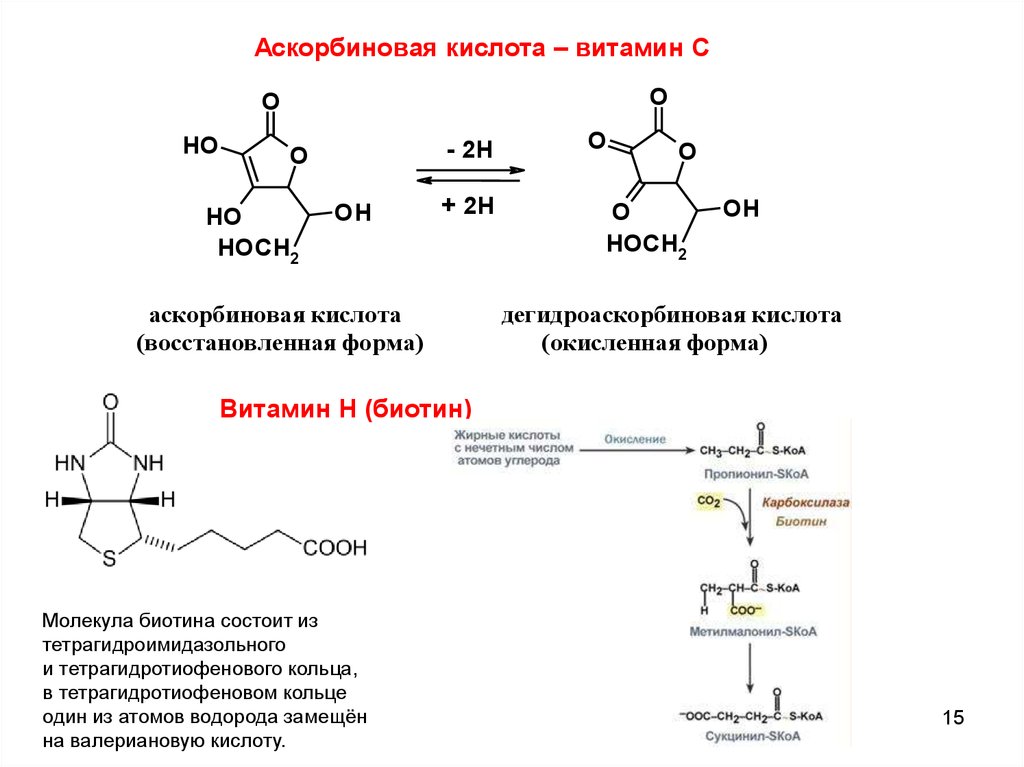
Аскорбиновая кислота – витамин СO
O
HO
- 2H
O
HO
HOCH2
OH
+ 2H
аскорбиновая кислота
(восстановленная форма)
O
O
O
HOCH2
OH
дегидроаскорбиновая кислота
(окисленная форма)
Витамин Н (биотин)
Молекула биотина состоит из
тетрагидроимидазольного
и тетрагидротиофенового кольца,
в тетрагидротиофеновом кольце
один из атомов водорода замещён
на валериановую кислоту.
15
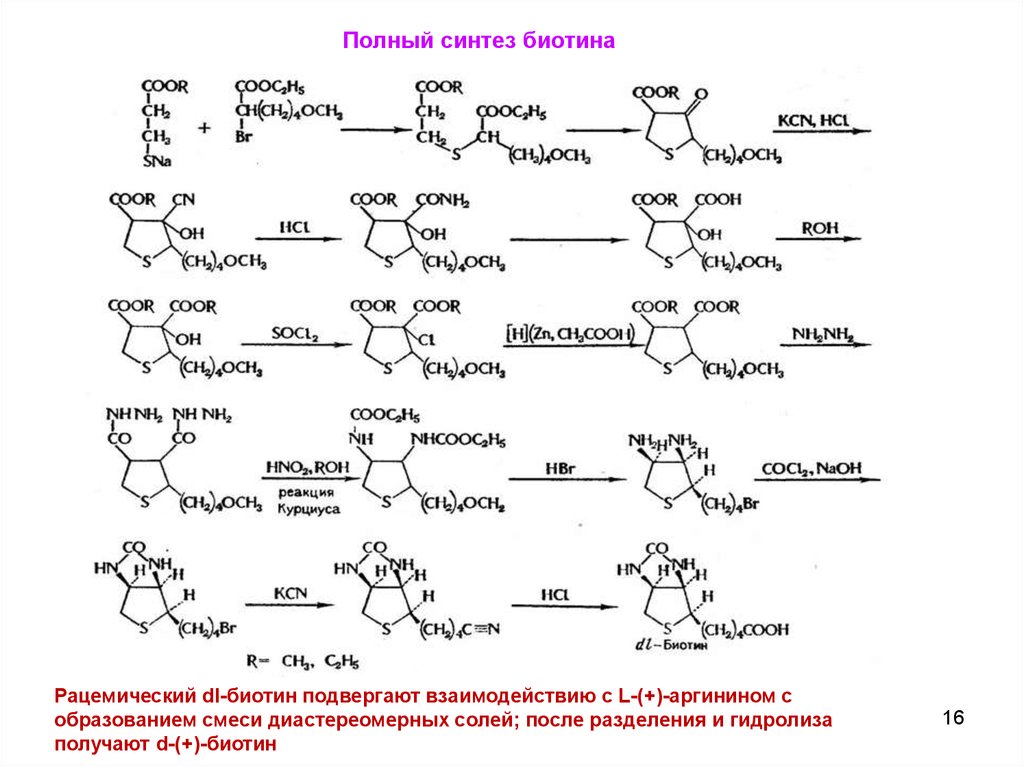
16.
Полный синтез биотинаРацемический dl-биотин подвергают взаимодействию с L-(+)-аргинином с
образованием смеси диастереомерных солей; после разделения и гидролиза
получают d-(+)-биотин
16
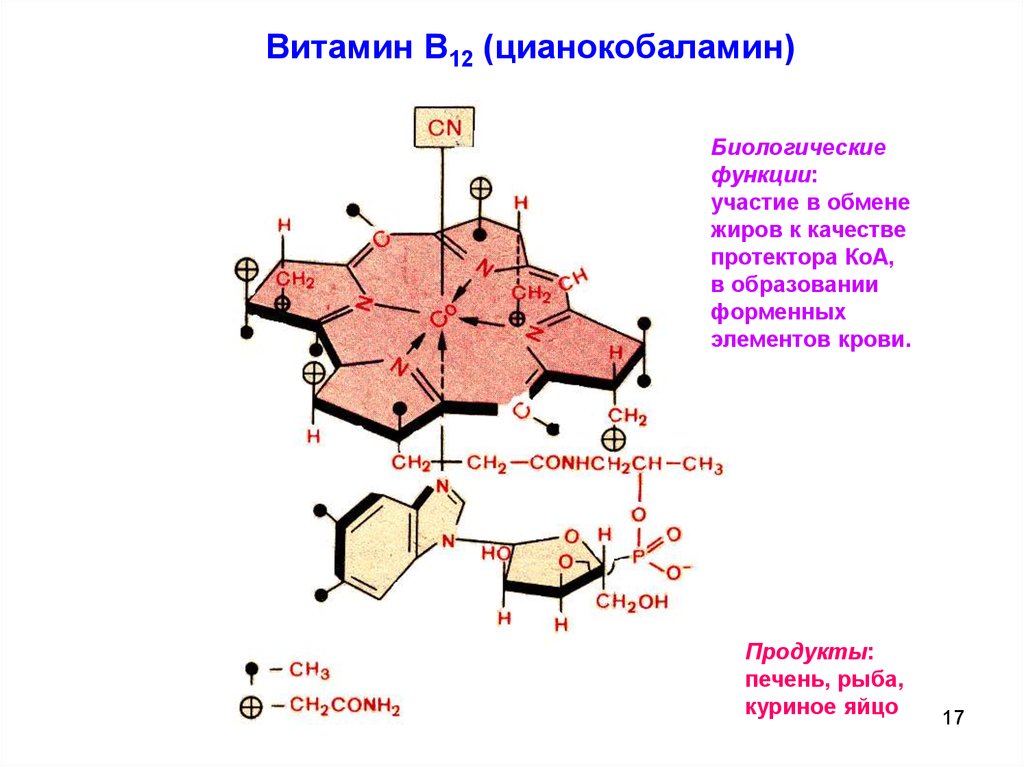
17.
Витамин В12 (цианокобаламин)Биологические
функции:
участие в обмене
жиров к качестве
протектора КоА,
в образовании
форменных
элементов крови.
Продукты:
печень, рыба,
куриное яйцо
17
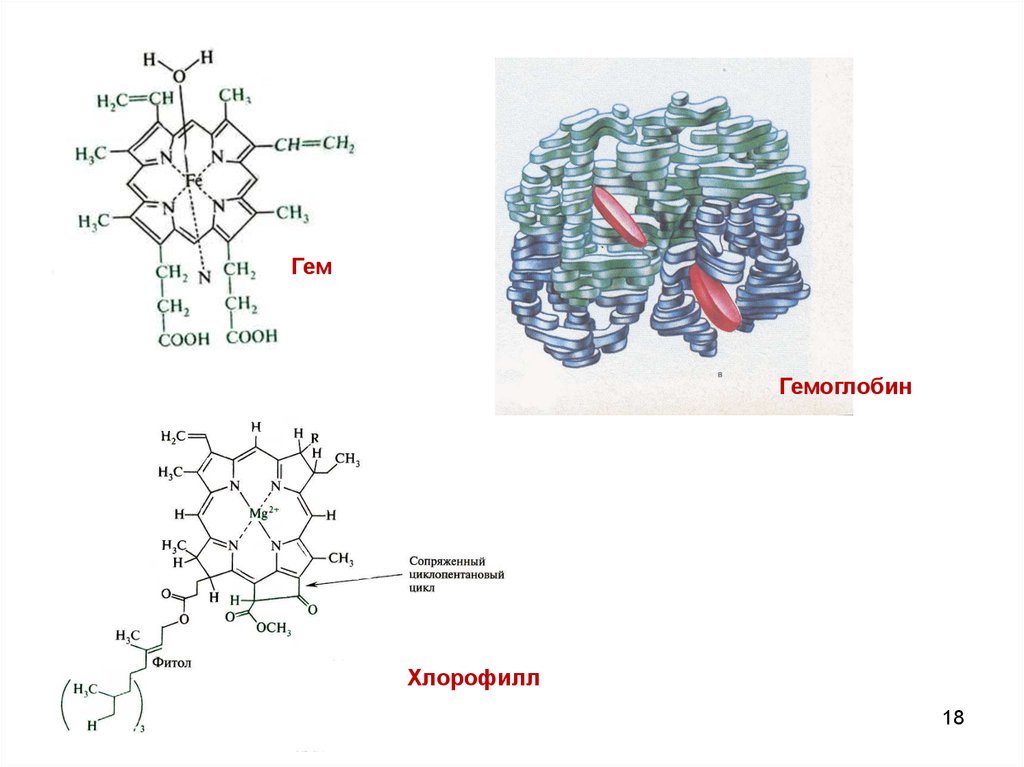
18.
ГемГемоглобин
Хлорофилл
18
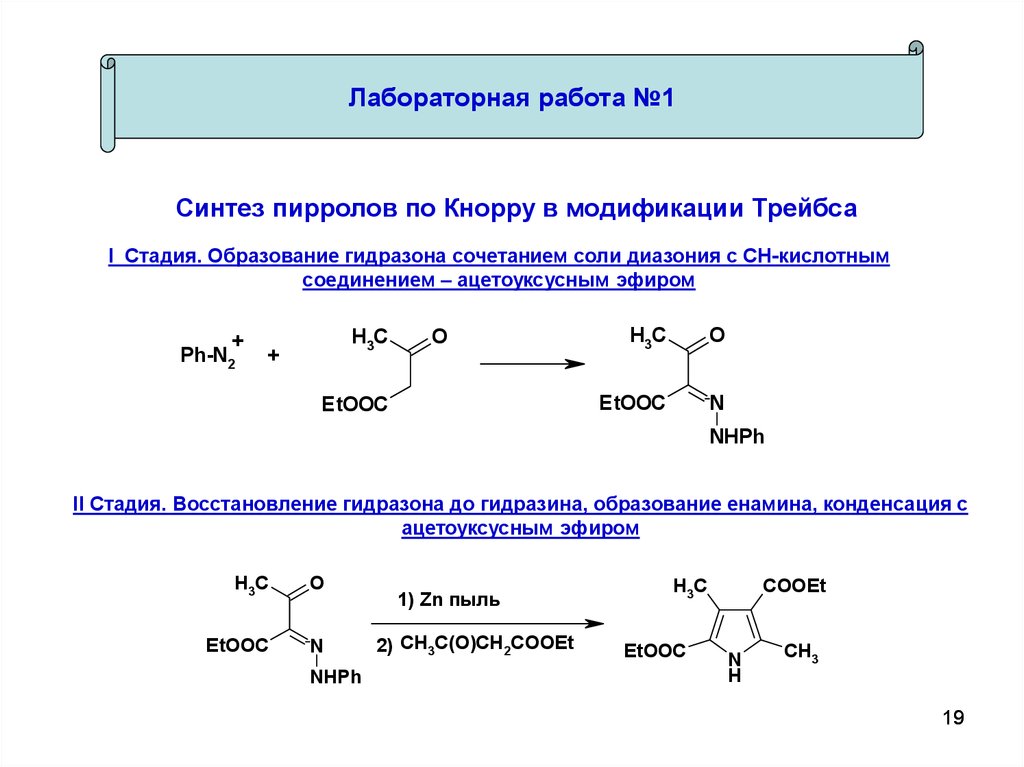
19.
Лабораторная работа №1Синтез пирролов по Кнорру в модификации Трейбса
I Стадия. Образование гидразона сочетанием соли диазония с СН-кислотным
соединением – ацетоуксусным эфиром
+
Ph-N2
H3C
+
O
EtOOC
H3C
O
EtOOC
N
NHPh
II Стадия. Восстановление гидразона до гидразина, образование енамина, конденсация с
ацетоуксусным эфиром
H3C
O
EtOOC
N
NHPh
1) Zn пыль
2) CH3C(O)CH2COOEt
H3C
EtOOC
COOEt
N
H
CH3
19
20.
Курс лекций является частью учебно-методического комплекса«Химия биологически активных веществ»
автор:
Носова Эмилия Владимировна, д.х.н., доцент кафедры органической химии УГТУ-УПИ –
лектор
Учебно-методический комплекс подготовлен на кафедре органической химии
химико-технологического факультета ГОУ ВПО УГТУ-УПИ
Никакая часть презентации не может быть воспроизведена в
какой бы то ни было форме без письменного разрешения авторов
20 20





 Биология
Биология Химия
Химия








