Похожие презентации:
Соли аммония
1.
Соли аммония2.
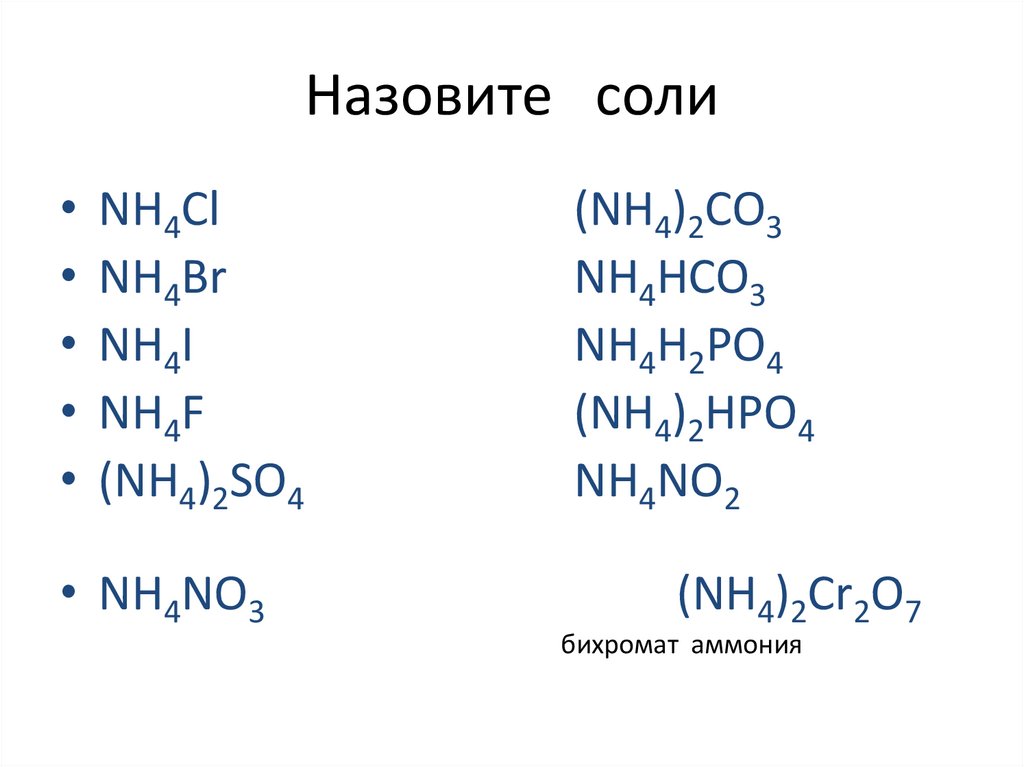
Назовите соли• NH4Cl
• NH4Br
• NH4I
• NH4F
• (NH4)2SO4
• NH4NO3
(NH4)2CO3
NH4HCO3
NH4H2PO4
(NH4)2HPO4
NH4NO2
(NH4)2Cr2O7
бихромат аммония
3.
NH4Cl(NH4)2Cr2O7
4.
Химические свойства:• 1) Соль + Соль
NH4Cl + AgNO3 →
• 2) Cоль + кислота
(NH4)2CO3 + HCl →
• 3) Cоль + щелочь
(NH4)2SO4 + КОН →
Допишите уравнения, составьте полные и сокращенные
ионные уравнения
5.
Особенные свойства солей аммония• Возгонка (соли летучих кислот) :
• NH4Cl → NH3↑ + HCl↑
• (NH4)2CO3→ 2 NH3↑ + CO2↑ + H2O
• (NH4)2SO3 →
• (NH4)2S →
6.
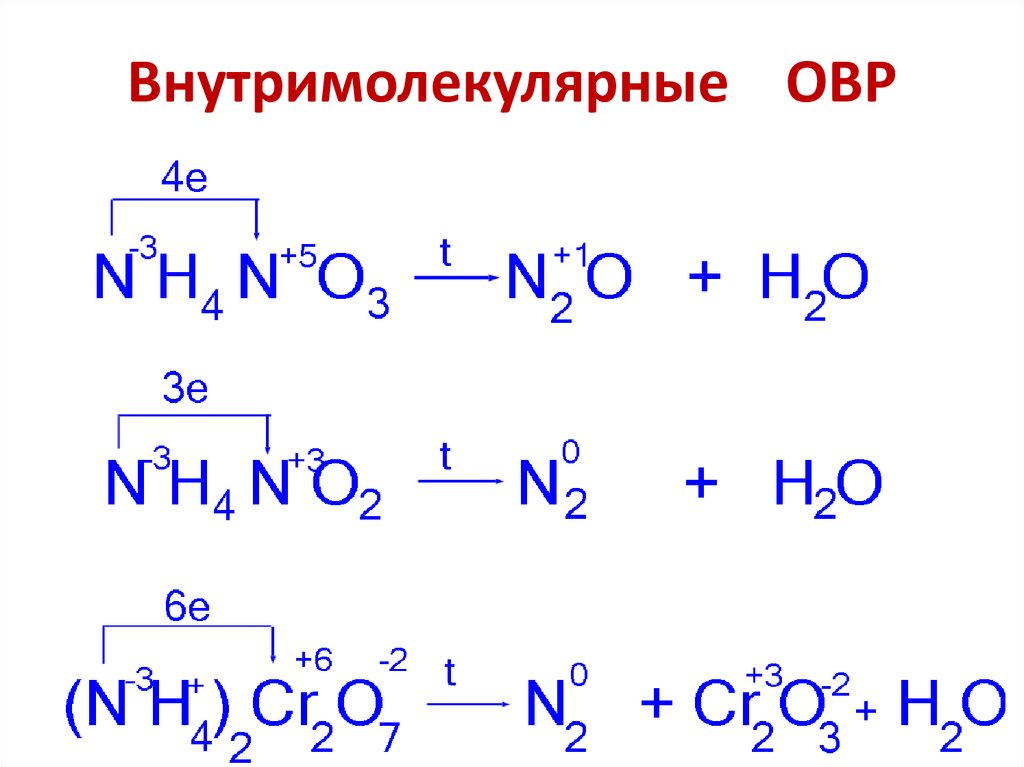
Внутримолекулярные ОВР7.
Дана схема превращений:(NH4)2СО3 → NH4Br → X → N2
• Напишите молекулярные уравнения
реакций, для первого превращения
составьте сокращенное ионное уравнение.
8.
Дан раствор сульфата аммония,а так же набор следующих реактивов:
цинк, растворы хлорида натрия, соляной
кислоты, гидроксида калия, нитрата бария..
Используя реактивы только из данного
списка, проведите две реакции,
характеризующие свойства сульфата
аммония. Приведите ионные уравнения,
укажите признаки реакций
9.
Задача.
• После пропускания 67,2 л аммиака через
избыток раствора бромоводородной
кислоты было получено 440 г раствора
соли. Вычислите массовую долю соли в
полученном растворе.







 Химия
Химия








