Похожие презентации:
Оксиды углерода
1.
2.
Входной тестСтроение молекул
Физические свойства
Физиологическое воздействие
Получение
Химические свойства
Применение
Закрепление знаний
.
3.
Оксид углерода (II)1.Укажите
4.Агрегатное
8.Характер
7.
6.
3.Химическая
тривиальное
2.
Относительная
Относительная
состояние
свойств
связь
Молекулярная
(исторически
5.Цвет,
запах
молекулярная
при
плотность
обычных
этого
вформула
молекуле
сложившееся)
по
условиязх
оксида
масса
воздуху
название
09.04.2023
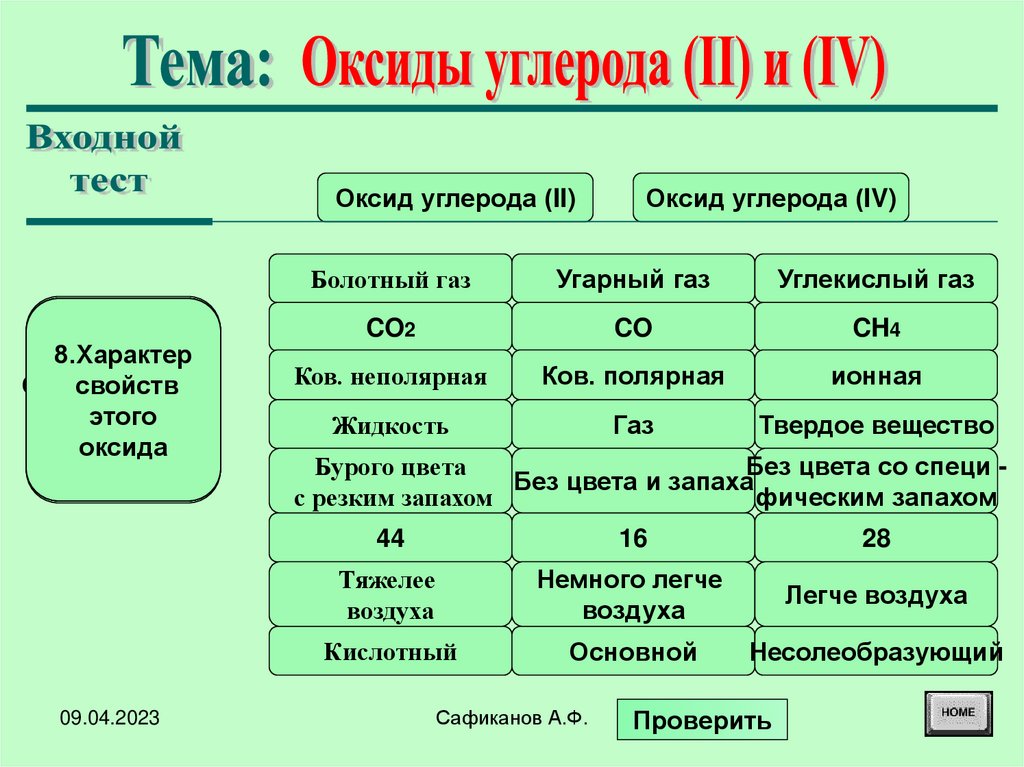
Оксид углерода (IV)
Болотный газ
Угарный газ
Углекислый газ
CO2
CO
CH4
Ков. неполярная
Ков. полярная
ионная
Жидкость
Газ
Твердое вещество
Бурого цвета
Без цвета со специ Без цвета и запаха
с резким запахом
фическим запахом
44
16
28
Тяжелее
воздуха
Немного легче
воздуха
Легче воздуха
Кислотный
Основной
Несолеобразующий
Сафиканов А.Ф.
Проверить
4.
Оксид углерода (II)2
С О
2
Оксид углерода (IV)
4
С О
2
2
:С :::О:
С О
:О ::С ::О:
( акцептор)( донор)
( м ол екул а л инейная)
C О
С О
О С О
IV
2
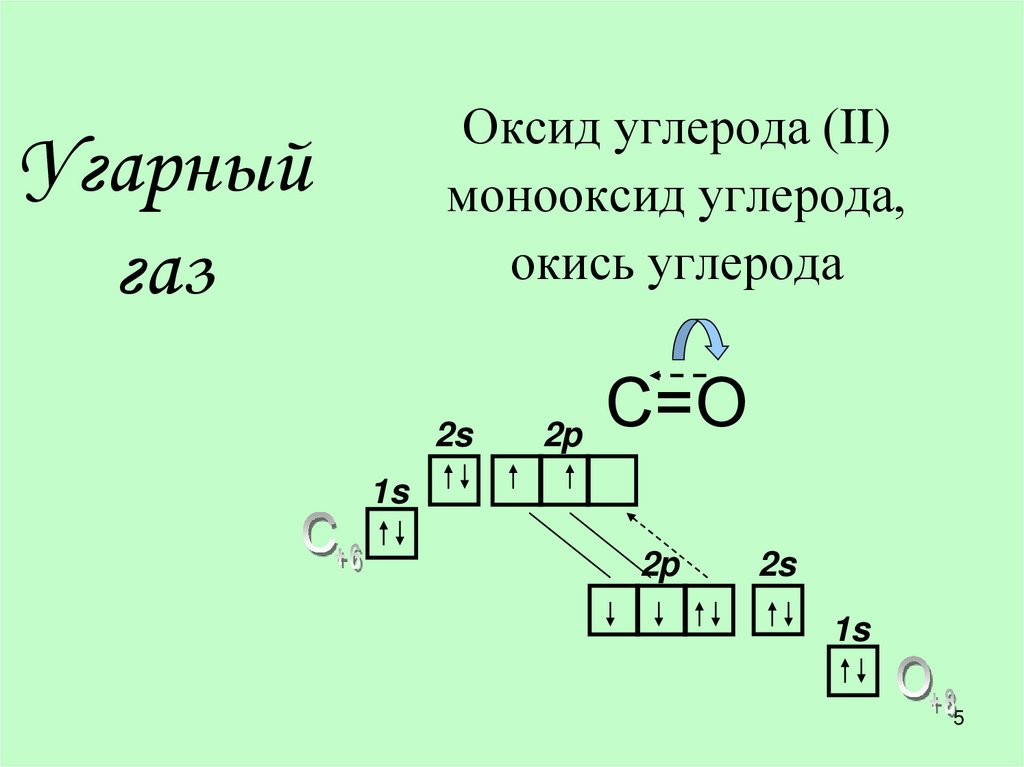
5. Угарный газ
Оксид углерода (II)монооксид углерода,
окись углерода
Угарный
газ
2s
С=О
2p
1s
2p
2s
1s
5
6.
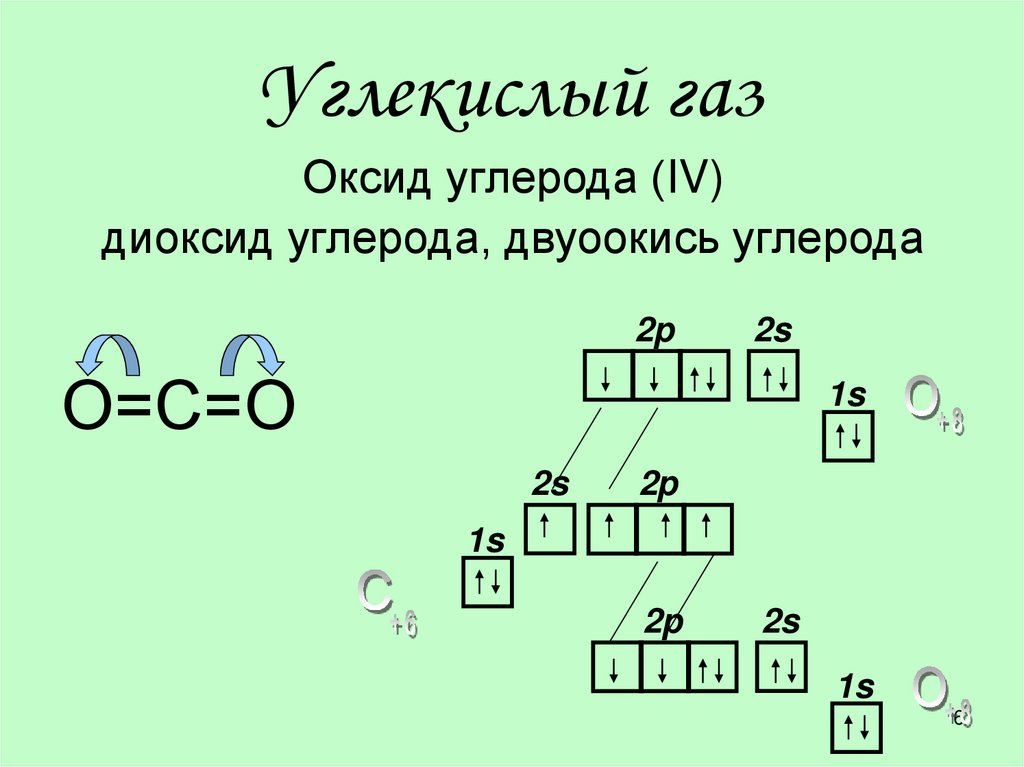
Углекислый газОксид углерода (IV)
диоксид углерода, двуоокись углерода
2p
2s
О=С=О
1s
2s
2p
1s
2p
2s
1s
6
7.
Оксид углерода (II)Г,
Ц, З,
Оксид углерода (IV)
Г,
ЯД!
100v H2O - 2,3 V CO
100v H2O - 88 V CO2
0
37
С , р 5атм
t пл
0
t 20,5 С ,
t 191,5 С.
0
0
пл
0
Ц, З
при обычном давлении
переходит в газ;
0
кип
0
20
С , р 60атм
t
0
Хранят СО в баллонах
красного цвета
переходит в бесцв. жидкость.
.
8.
Оксид углерода (II)ЯД! Он соединяется с
гемоглобином, нарушая тканевое
дыхание и вызывая кислородное
голодание тканей.
Оксид углерода (IV)
Не токсичен, но не поддерживает
дыхание.
Физиологическое воздействие на
человека:
Физиологическое воздействие на до 2% - до 480 мин. - учащается
.
дыхание;
человека:
2 - 5% - до 30 мин. -появляется шум .
0,01 - до 480 мин. - слабая
.
в ушах, учащается пульс;
.
головная боль;
.
0,05 - до 60 мин. - тошнота, . . . . . 5 - 8 % - 5 - 10 мин. - сильные .
.
головные боли, недомогание;
усиленное сердцебиение;
0,1 - до 60 мин. - рвота, потеря
. Свыше 10% - 1-2 мин. - потеря
..
.
сознания, смерть.
.
сознания;
0,5 - до 20-30 мин. - смертельное . .
.
отравление.
.
9.
Оксид углерода (II)1) С + О2 = 2СО +Q
( недостаток О2)
2) В промышленности:
С + СО2 → 2СО - 175 kДж
3) В лаборатории:
t, Н2SО4
НСООН
Н2О + СО
Муравьиная кислота
Н2С2О4 →
СО + СО2 +Н2О
Щавелевая кислота
Оксид углерода (IV)
1) В природе (дыхание)
С6Н12О6+ 6О2 = 6СО2 + 6Н2О +Q
1) В быту
СН4+ 2О2 = СО2 + 2Н2О+ Q
(избыток О2)
2) В промышленности:
t
СаСО3 → СаО + СО2
3) В лаборатории:
СаСО3 +2НСl → СаСl2 +Н2О + СО2 ۟
10.
Оксид углерода (II)СО – несолеобразующий оксид
1) Горит синим пламенем
2СО + О2 → 2СО2 +572кДж
2) С галогенами
СО + Сl2 → СОCl2
(
фосген –ЯД!
3) Сильный восстановитель
СО +СuO →Cu + CO2
4) С расплавом щелочи
СО +NaOH (конц) →НСООNa
формиат
натрия
Оксид углерода (IV)
СО2 – кислотный оксид
1 )Взаимодействует с водой
СО2 + Н2О
Н2СО3
2) Взаимодействие со
щелочами
СО2 +2 NaОН→ Na2СО3 + Н2О
СО2 + NaОН→ NaНСО3
изб
Качественная реакция:
СО2 +Сa(ОН)2→ СаСО3 ↓ + Н2О
3) Взаимодействие с оксидами
СО2 + ВaО→ ВaСО3
4) СО2 –окислитель
2Мg + CO2 →2 MgO + C
11.
Оксид углерода (II)• В смеси с H2 и другими горючими
газами в качестве топлива;
• При получении спиртов, альдегидов, карбоновых кислот и др.;
• Восстановитель в металлургии
(напр., при выплавке чугуна и
стали);
•Для обработки мяса животных и
рыбы, придает им ярко красный
цвет и вид свежести, не изменяя
вкуса.
09.04.2023
Оксид углерода (IV)
• В пищевой промышленности
используется как консервант;
• В качестве разрыхлителя теста;
• Сухой лёд используется в
качестве хладагента в ледниках и
морозильных установках;
• Баллоны с жидкой углекислотой
широко применяются в качестве
огнетушителей;
•Для производства газированной
воды и лимонада;
• В качестве инертной среды при
сварке проволокой.
Сафиканов А.Ф.
12.
Укажите свойства, характерныедля углекислого газа:
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
09.04.2023
Газ без цвета, запаха, вкуса.
Ядовитый газ.
Тяжелее воздуха.
Горит.
Немного легче воздуха.
Проявляет свойства кислотного оксида.
Не горит, не поддерживает горение.
Взаимодействует со щелочами.
Не вызывает отравления человека.
Образует соли.
В окислительно-восстановительных реакциях является
восстановителем.
В воде растворяется плохо.
Сафиканов А.Ф.
Проверить
13. Домашнее задание
• П. 33, упр. 1,2, тесты на стр.120• П. 34, упр. 1,2, 3*, тесты на стр.120
09.04.2023
Сафиканов А.Ф.










 Химия
Химия








