Похожие презентации:
Диазониевые соли
1.
ДИАЗОНИЕВЫЕ СОЛИ2.
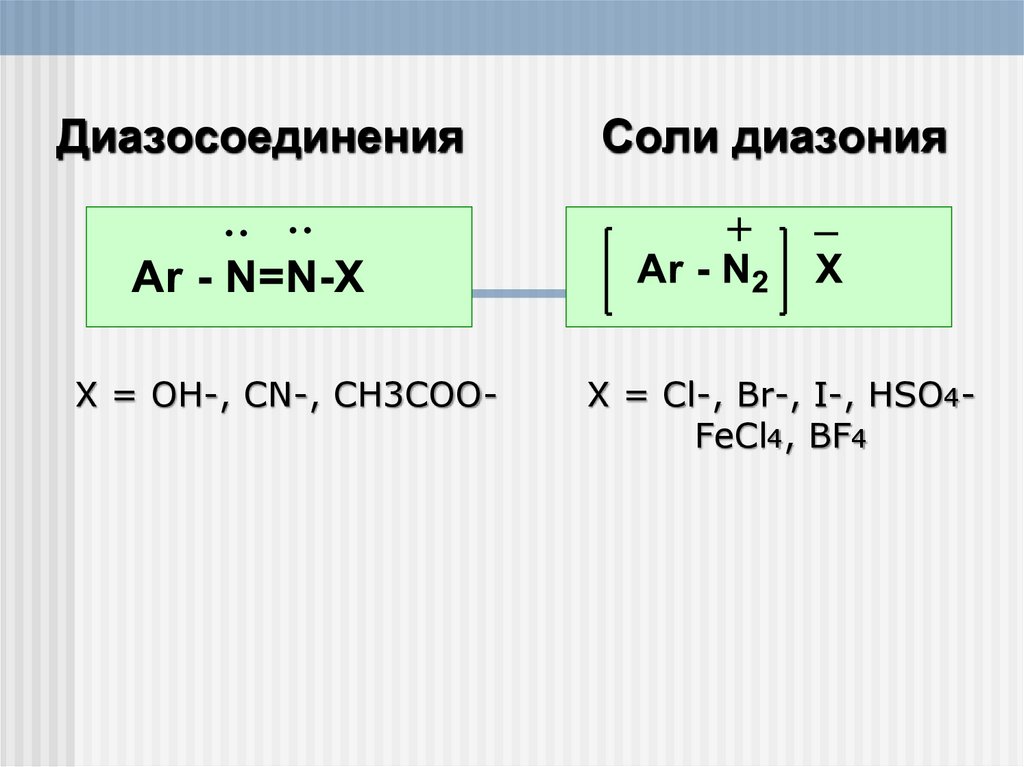
ДиазосоединенияСоли диазония
X = OH-, CN-, CH3COO-
X = Cl-, Br-, I-, HSO4FeCl4, BF4
3.
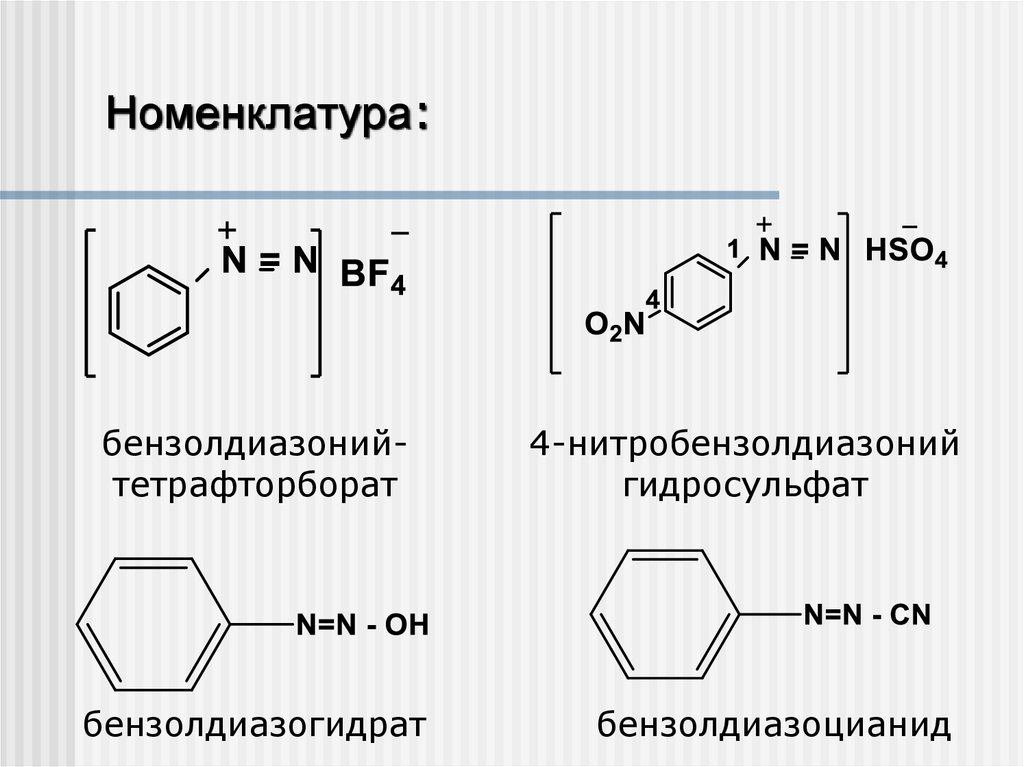
Номенклатура:бензолдиазонийтетрафторборат
4-нитробензолдиазоний
гидросульфат
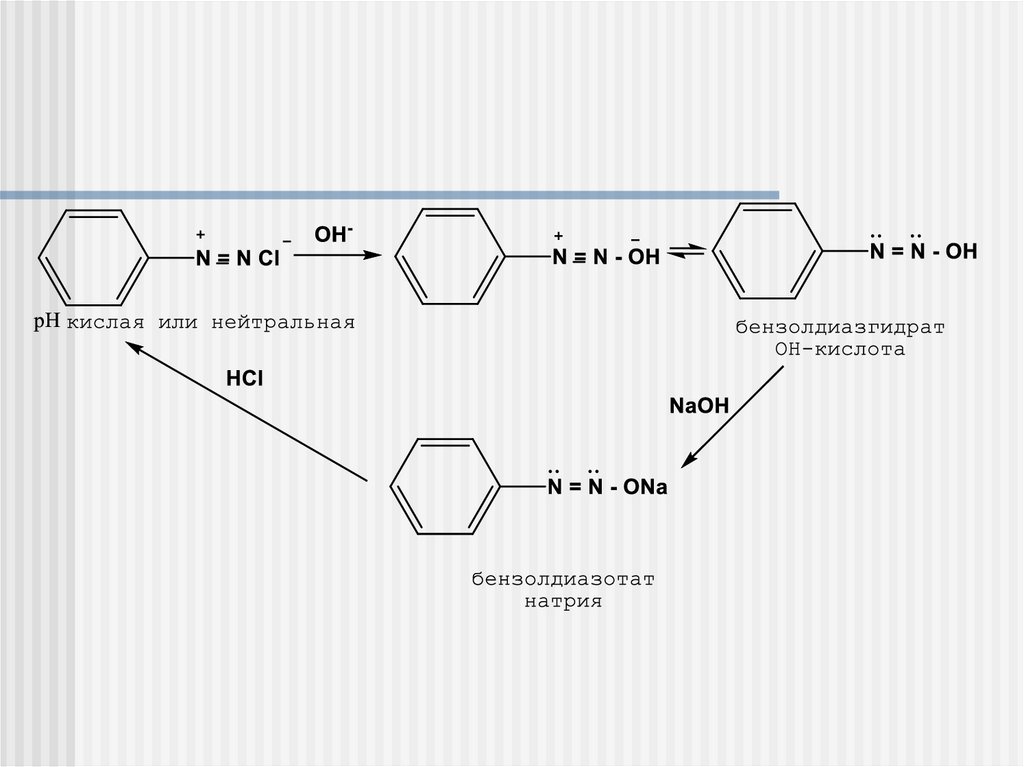
бензолдиазогидрат
бензолдиазоцианид
4.
Получение:Условия соблюдающиеся при проведении реакции
диазотирования:
1.Реакцию проводят при пониженных температурах, для
предотвращения разложения азотистой кислоты и соли
диазония.
2.Применяют избыток минеральной кислоты.
3.Окончание реакции определяется по наличию избытка HNO2.
5.
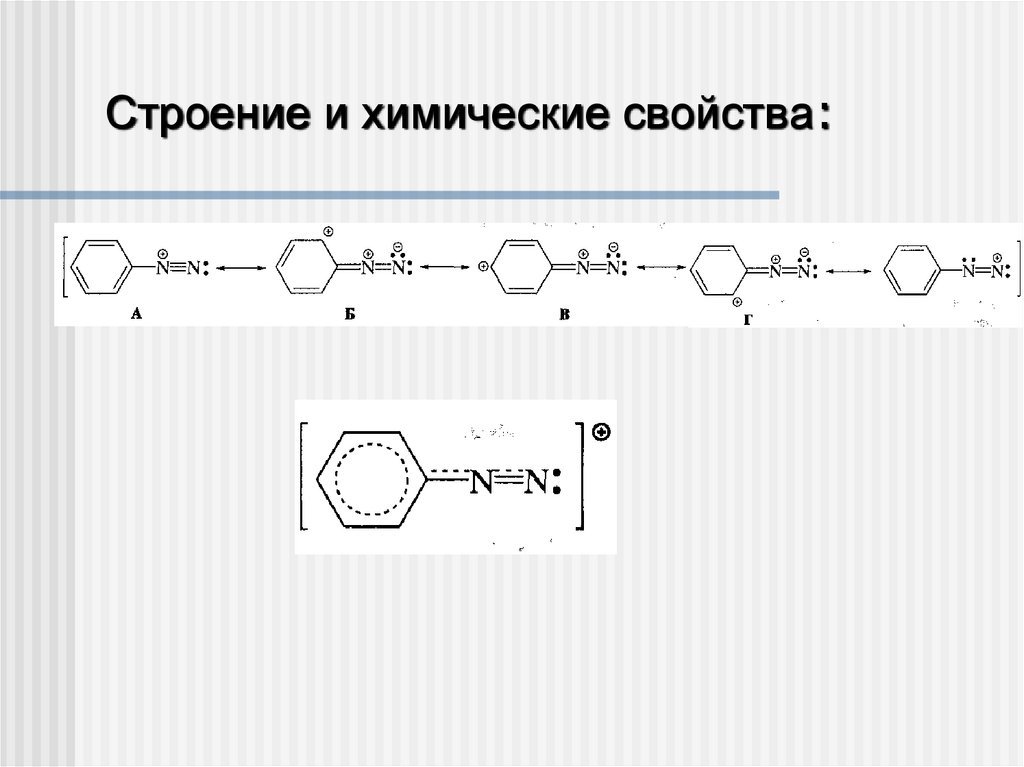
Строение и химические свойства:6.
7.
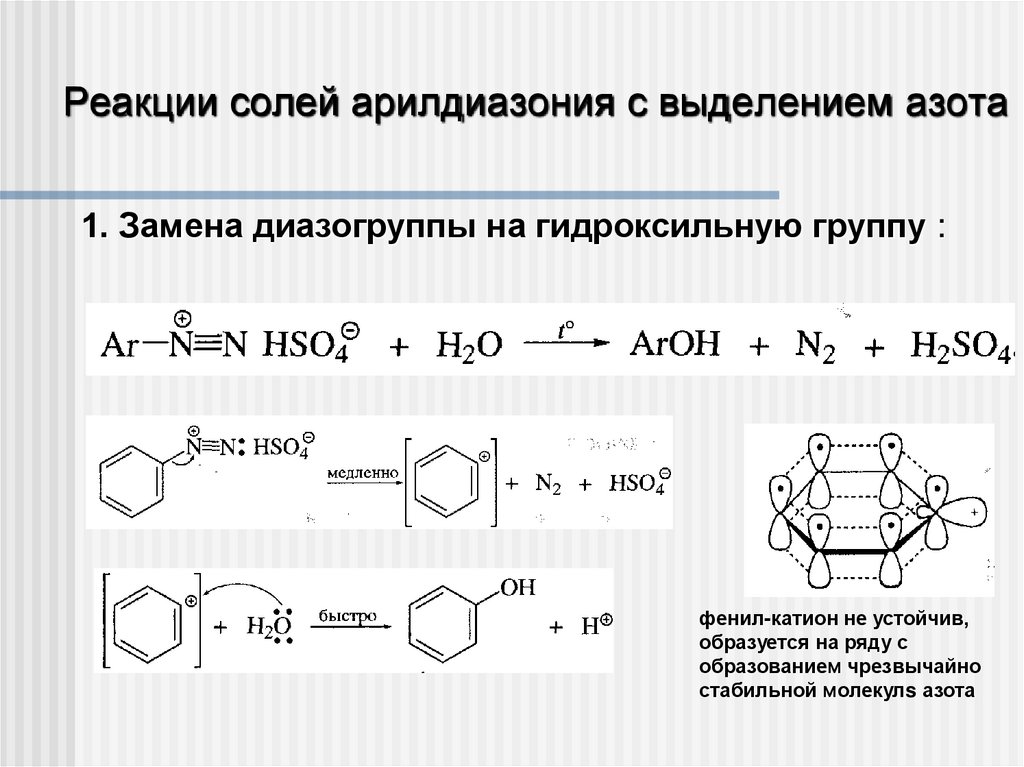
Реакции солей арилдиазония с выделением азота1. Замена диазогруппы на гидроксильную группу :
фенил-катион не устойчив,
образуется на ряду с
образованием чрезвычайно
стабильной молекулs азота
8.
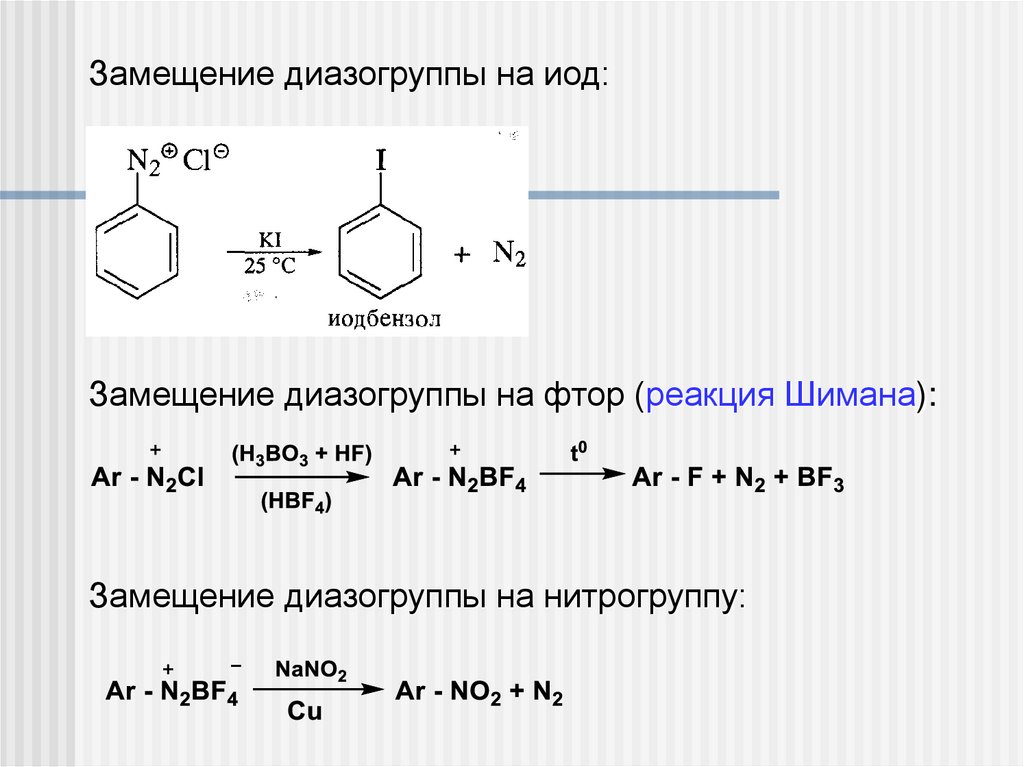
Замещение диазогруппы на иод:Замещение диазогруппы на фтор (реакция Шимана):
Замещение диазогруппы на нитрогруппу:
9.
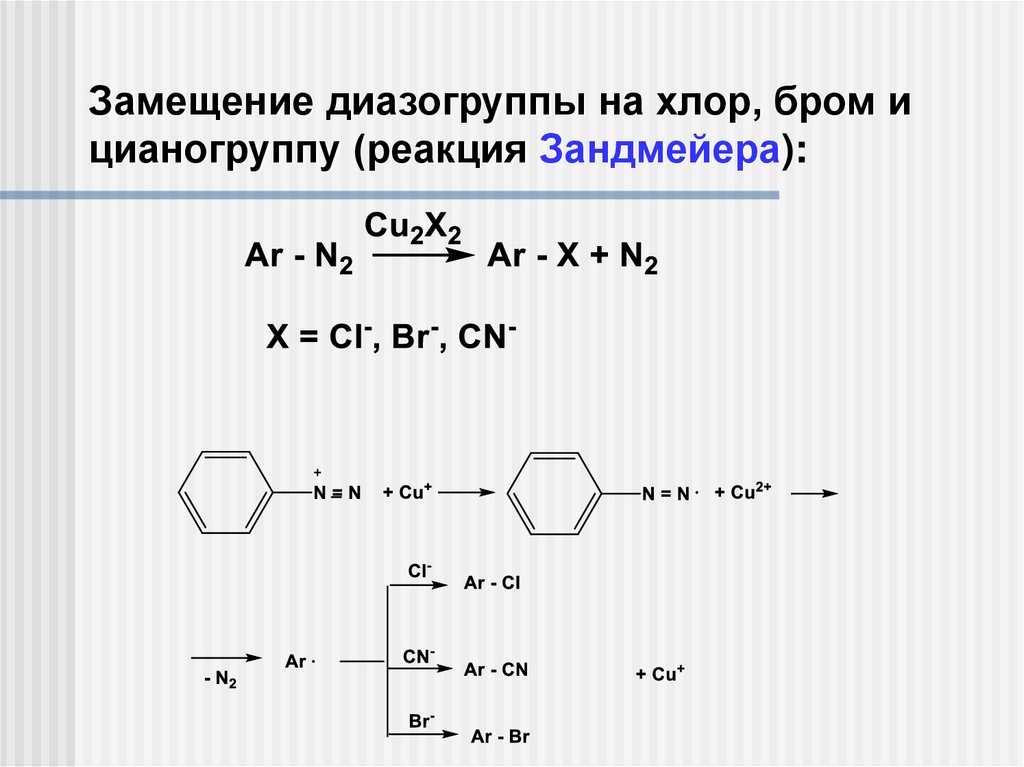
Замещение диазогруппы на хлор, бром ицианогруппу (реакция Зандмейера):
10.
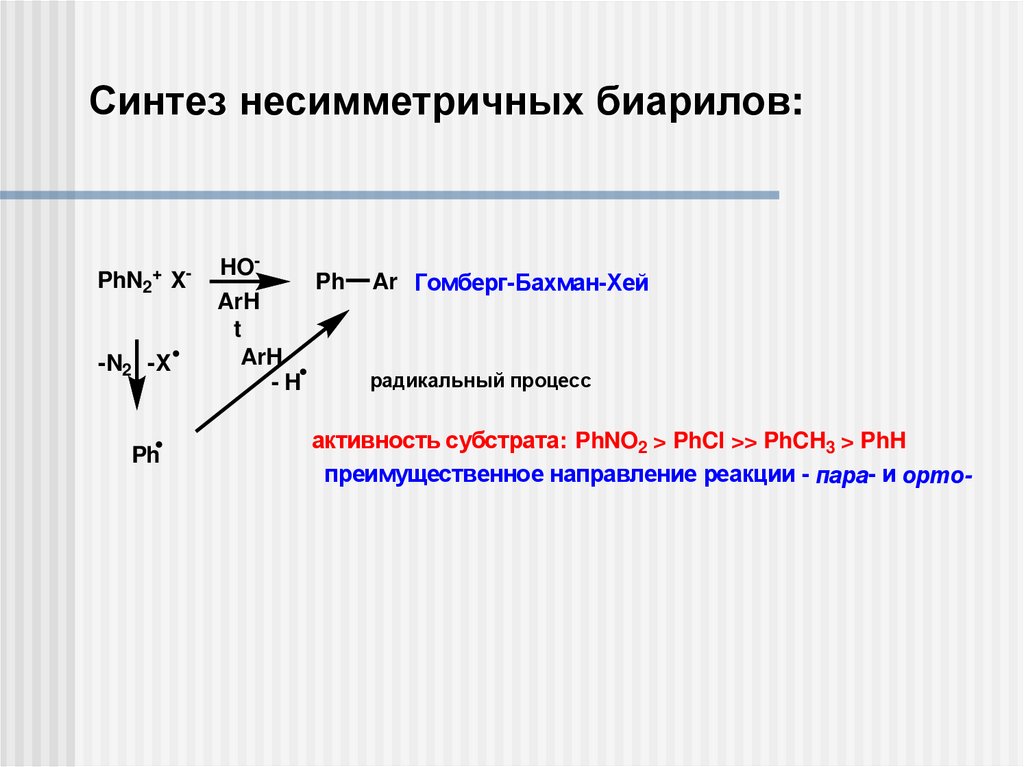
Синтез несимметричных биарилов:PhN2+ X-
-N2 -X
Ph
HOPh
ArH
t
ArH
-H
Ar Гомберг-Бахман-Хей
радикальный процесс
активность субстрата: PhNO2 > PhCl >> PhCH3 > PhH
преимущественное направление реакции - пара- и орто-
11.
Замещение диазогруппы на водород(дезаминирование):
ROH/t SN
ROH/AcONa SR
H3PO2
12.
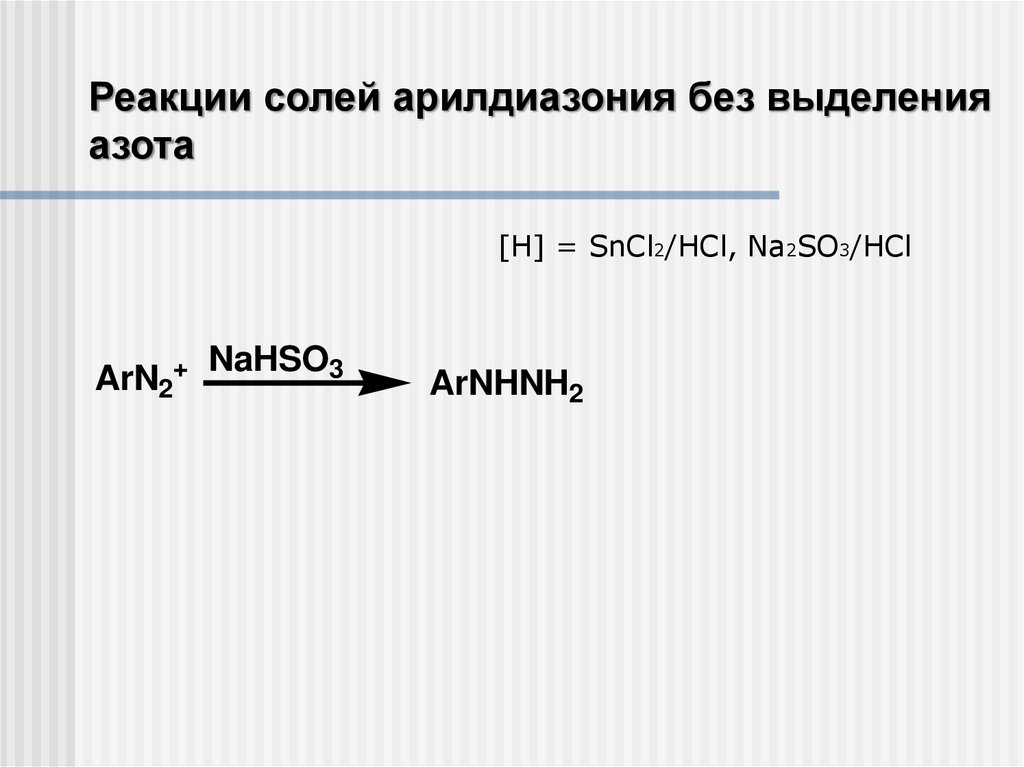
Реакции солей арилдиазония без выделенияазота
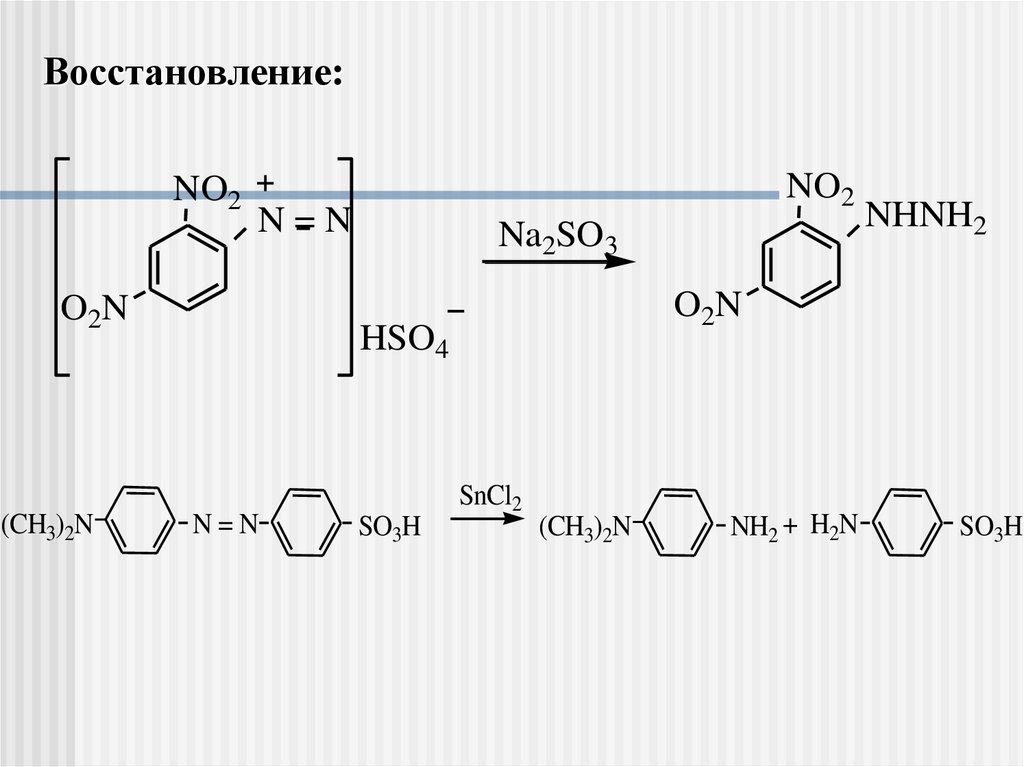
[H] = SnCl2/HCl, Na2SO3/HCl
ArN2+
NaHSO3
ArNHNH2
13.
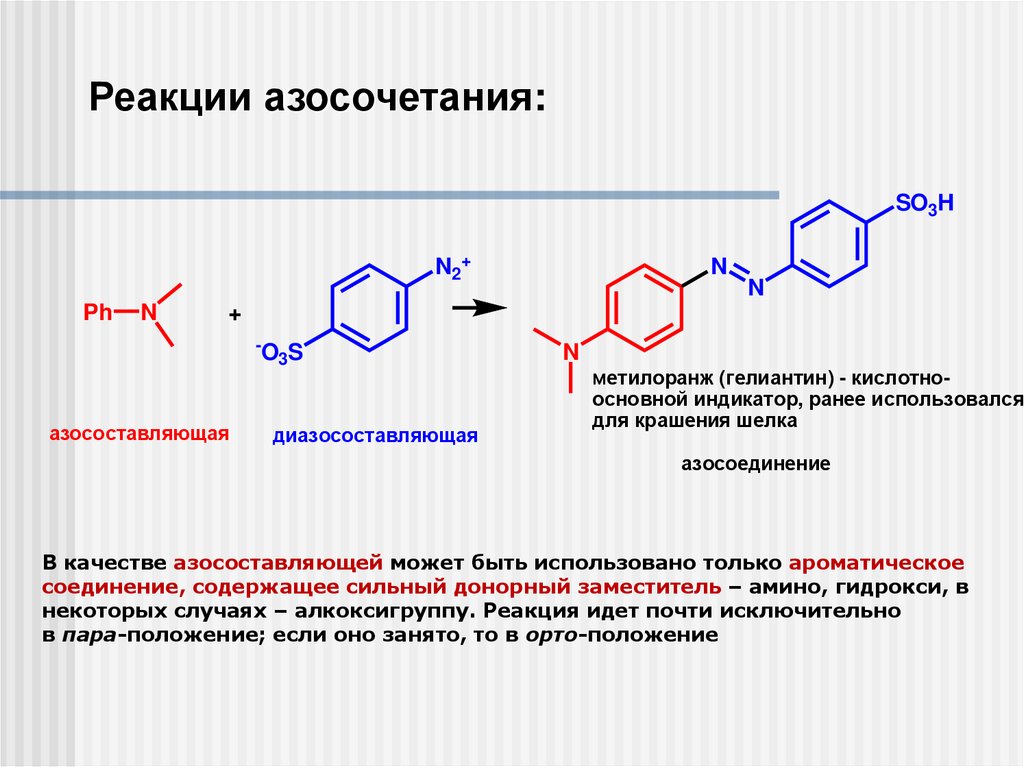
Реакции азосочетания:SO3H
N2+
Ph
N
N
N
+
-
азосоставляющая
O3S
диазосоставляющая
N
метилоранж (гелиантин) - кислотноосновной индикатор, ранее использовался
для крашения шелка
азосоединение
В качестве азосоставляющей может быть использовано только ароматическое
соединение, содержащее сильный донорный заместитель – амино, гидрокси, в
некоторых случаях – алкоксигруппу. Реакция идет почти исключительно
в пара-положение; если оно занято, то в орто-положение
14.
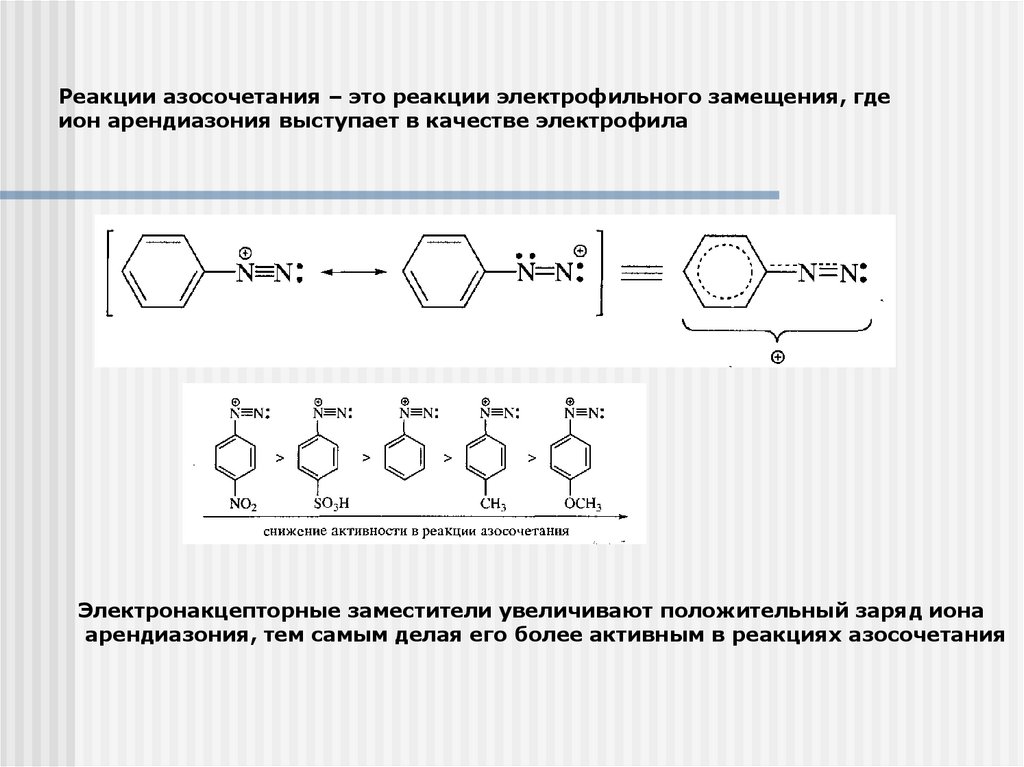
Реакции азосочетания – это реакции электрофильного замещения, гдеион арендиазония выступает в качестве электрофила
Электронакцепторные заместители увеличивают положительный заряд иона
арендиазония, тем самым делая его более активным в реакциях азосочетания
15.
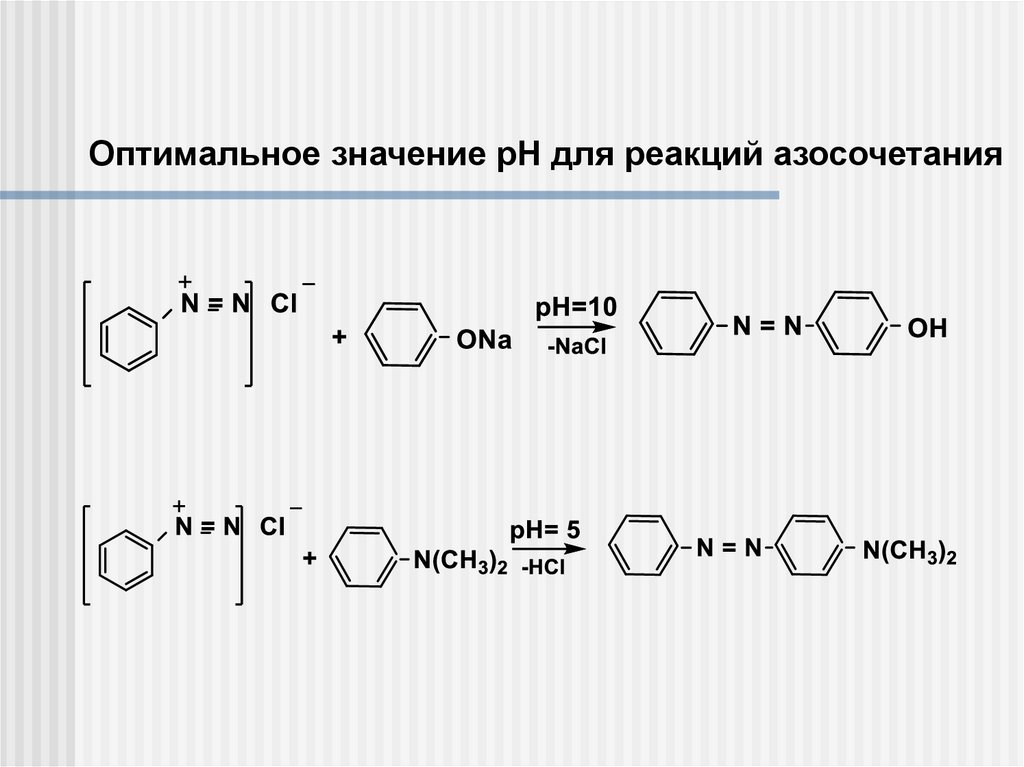
Оптимальное значение рН для реакций азосочетания16.
Восстановление:NO2
N=N
O2N
(CH3)2N
NO2
Na2SO3
O2N
HSO4
N=N
SnCl2
SO3H
NHNH2
(CH3)2N
NH2 + H2N
SO3H
17.
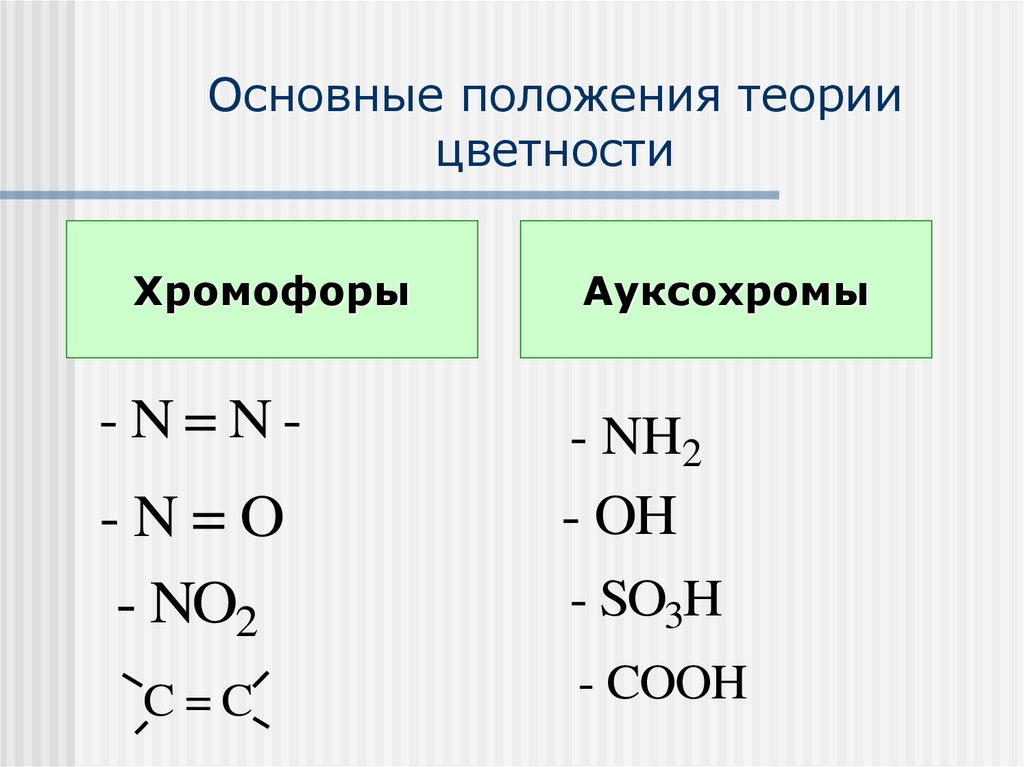
Основные положения теориицветности
Хромофоры
-N=N-
Ауксохромы
-N=O
- NO2
- NH2
- OH
- SO3H
C=C
- COOH
18.
(CH3)2NN=N
SO3Na
ауксохром
хромоген
ауксохром
19.
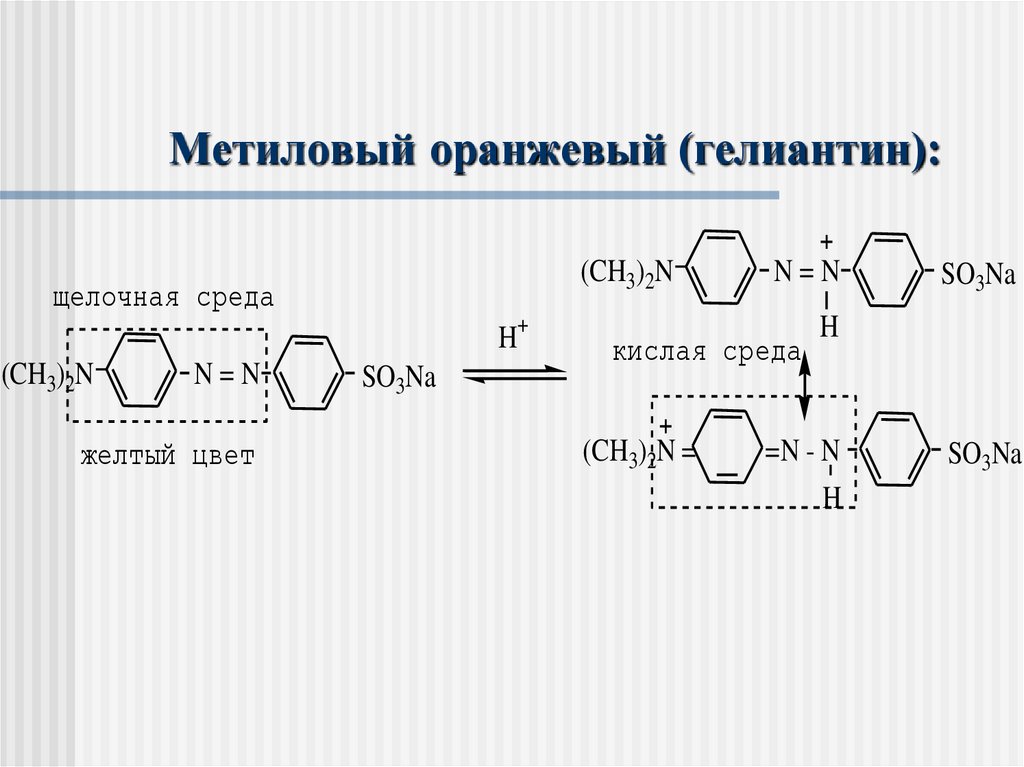
Метиловый оранжевый (гелиантин):(CH3)2N
щелочная среда
H+
(CH3)2N
N=N
желтый цвет
SO3Na
N=N
кислая среда
(CH3)2N =
SO3Na
H
=N - N
H
SO3Na
20.
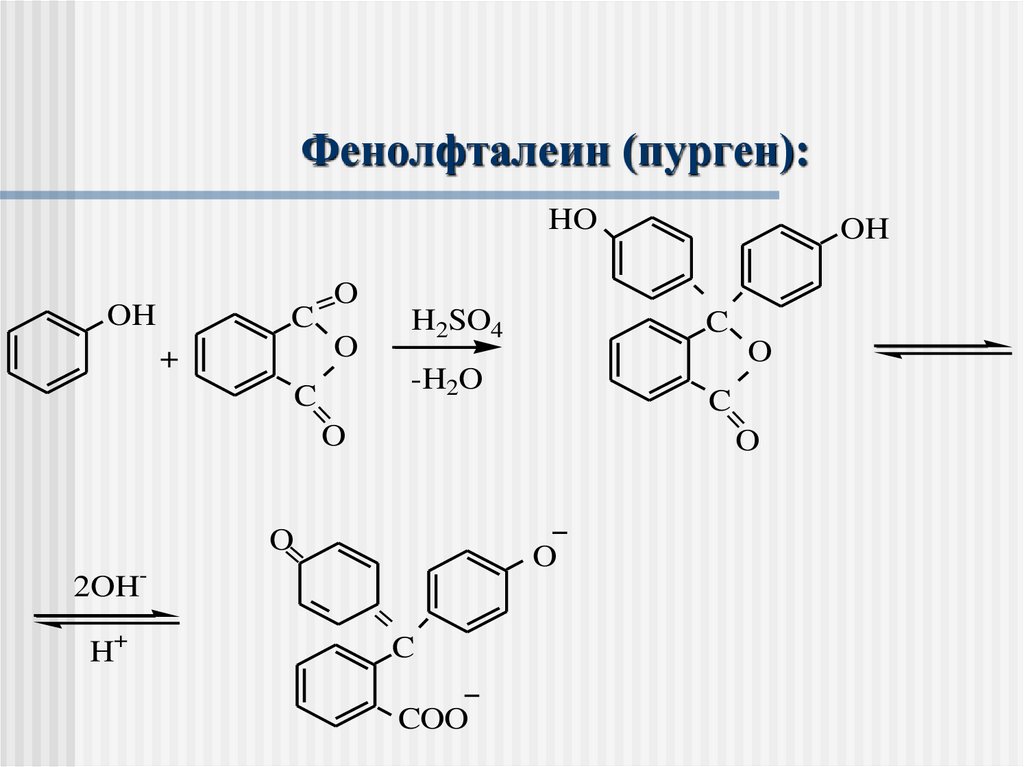
Фенолфталеин (пурген):HO
OH
+
O
=
C
O
H2SO4
C
-H2O
C
O
=
=
C
O
O
O=
O
-
2OH
H+
OH
=
C
COO




 Химия
Химия