Похожие презентации:
Азо-, диазосоединения
1. Азо-,диазосоединения
128.03.2019
2.
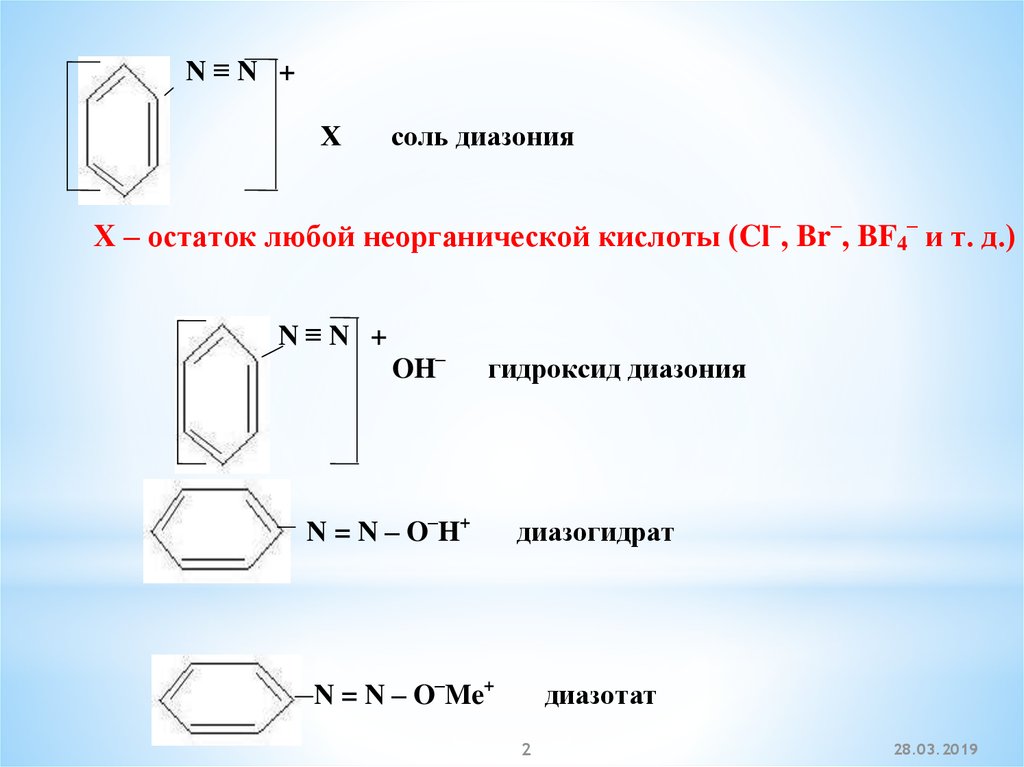
N≡N +Х
соль диазония
Х – остаток любой неорганической кислоты (Cl–, Br–, BF4– и т. д.)
N≡N +
OH–
гидроксид диазония
N = N – O–H+
диазогидрат
N = N – O–Me+
диазотат
2
28.03.2019
3.
I. Номенклатура солей диазония+
N≡N
Х–
N≡N +
Cl–
хлористый фенил диазоний
N≡N +
CH3
Cl
–
орто-метилфенилдиазонийхлорид
орто-толилдиазонийхлорид
N≡N +
NO2
SO3H
BF4 –
2-нитро – 3 – сульфофенилдиазонийборфторид
3
28.03.2019
4.
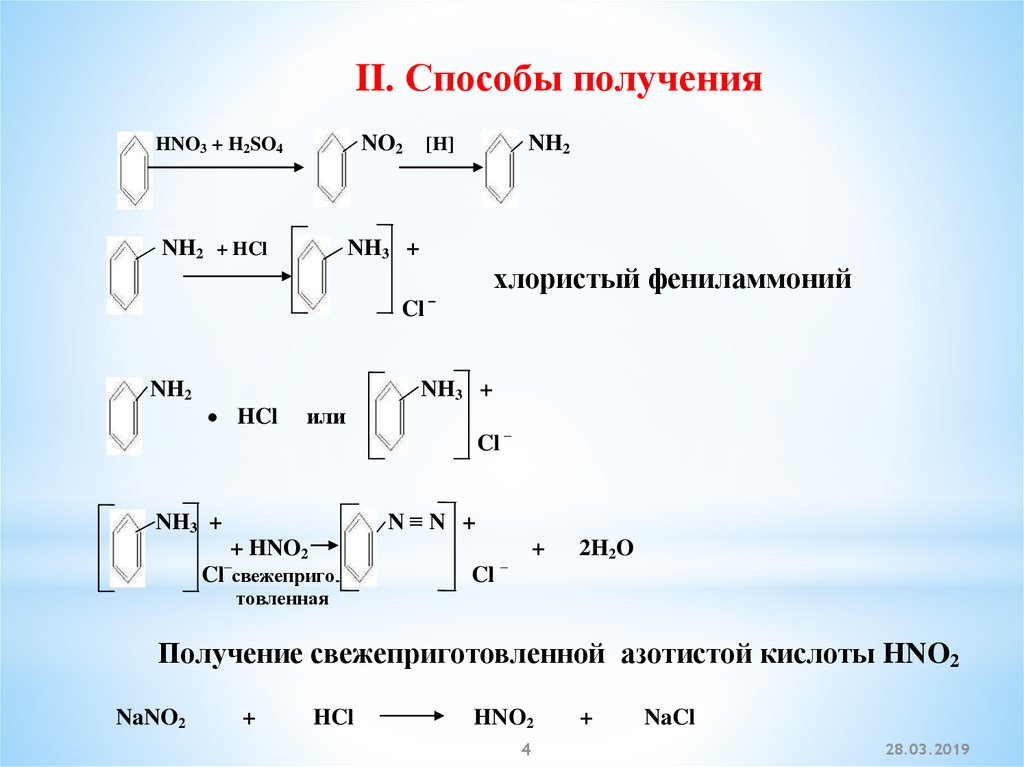
II. Способы полученияNO2 [H]
HNO3 + H2SO4
NH2 + HCl
NH3 +
хлористый фениламмоний
Cl
NH2
HCl
NH2
–
NH3 +
или
Cl –
N≡N +
NH3 +
+ HNO2
–
Cl свежеприго-
Cl
+
–
2H2O
товленная
Получение свежеприготовленной азотистой кислоты HNO2
NaNO2
+
HCl
HNO2
4
+
NaCl
28.03.2019
5.
Ароматические катионыдиазония стабилизируюся
сопряжением с ароматической
системой и являются вполне
устойчивыми и выделяемыми
5
28.03.2019
6.
III. Химические свойстваРеакции, идущие
с выделением азота
Реакции, идущие
без выделения азота
6
28.03.2019
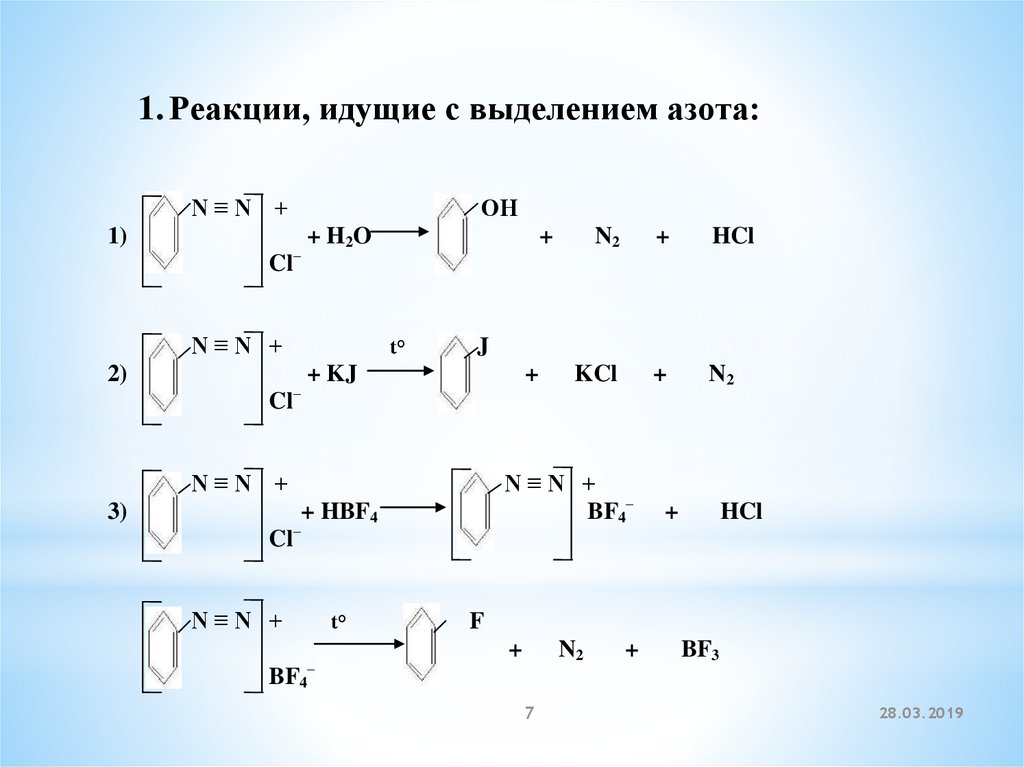
7.
1. Реакции, идущие с выделением азота:N≡N +
1)
Cl
OH
–
+ H2O
N≡N +
2)
Cl
+
t°
–
Cl
–
+ KJ
+
BF4
t°
–
HCl
KCl
+
N2
N≡N +
BF4–
+ HBF4
N≡N +
+
J
N≡N +
3)
N2
+
HCl
F
+
N2
7
+
BF3
28.03.2019
8.
N≡N +4)
Cl
H
–
+ H2PO3 + H2O
N≡N +
5)
+
H3PO4
+
HCl
+
N2
H
+ CH3OH
Cl–
+
N2
+
H–C=O
|
H
+
HCl
ОСН3
+
НCl
+
N2
28.03.2019
8
9.
6) Реакции Зандмейераа)
N≡N +
CuCl
Cl
б)
в)
CuBr
г)
CuNO2
+
Cl
CuCN
–
+
CuCl
N2
+
CuCl
NO2
–
N≡N +
N2
Br
–
N≡N +
Cl
+
–
N≡N +
Cl
Cl
+
N2
+
CuCl
+
CuCl
CN
9
+
N2
28.03.2019
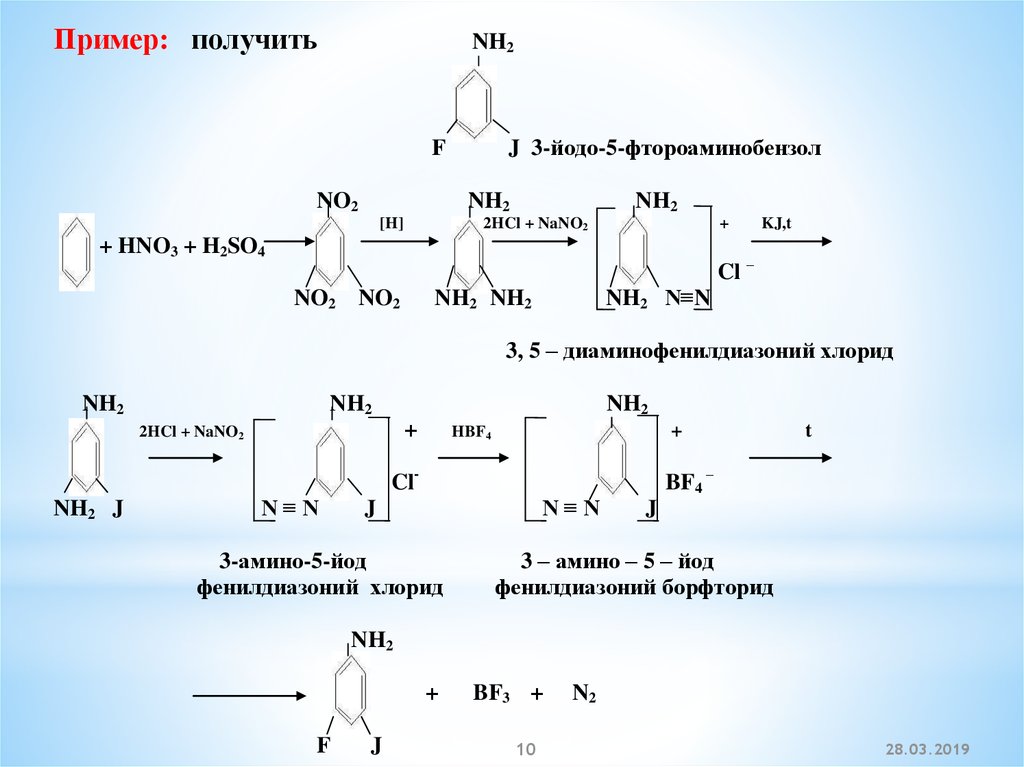
10.
Пример: получитьNH2
|
F
NO2
J 3-йодо-5-фтороаминобензол
NH2
[H]
NH2
2HCl + NaNO2
+
+ HNO3 + H2SO4
KJ,t
Cl –
NO2 NO2
NH2 N≡N
NH2 NH2
3, 5 – диаминофенилдиазоний хлорид
NH2
NH2
NH2
+
2HCl + NaNO2
+
HBF4
BF4 –
ClNH2 J
N≡N
N≡N
J
3-амино-5-йод
фенилдиазоний хлорид
t
J
3 – амино – 5 – йод
фенилдиазоний борфторид
NH2
+
F
J
BF3 +
10
N2
28.03.2019
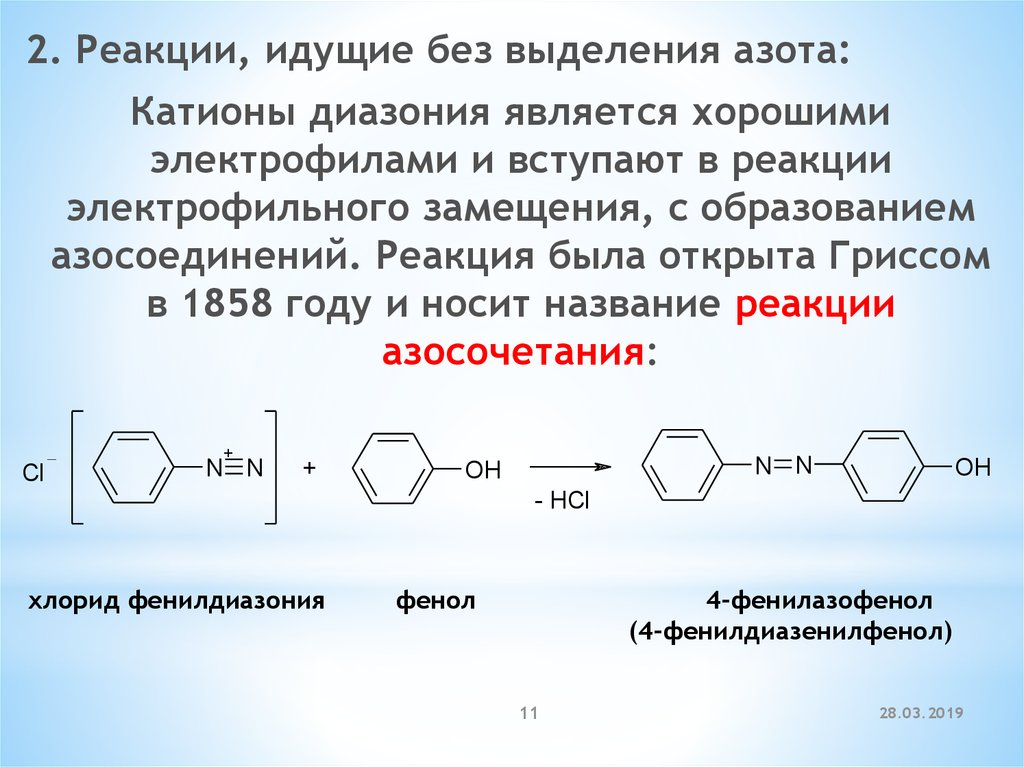
11.
2. Реакции, идущие без выделения азота:Катионы диазония является хорошими
электрофилами и вступают в реакции
электрофильного замещения, с образованием
азосоединений. Реакция была открыта Гриссом
в 1858 году и носит название реакции
азосочетания:
+
Cl
N N
+
N N
OH
OH
- HCl
хлорид фенилдиазония
фенол
4-фенилазофенол
(4-фенилдиазенилфенол)
11
28.03.2019
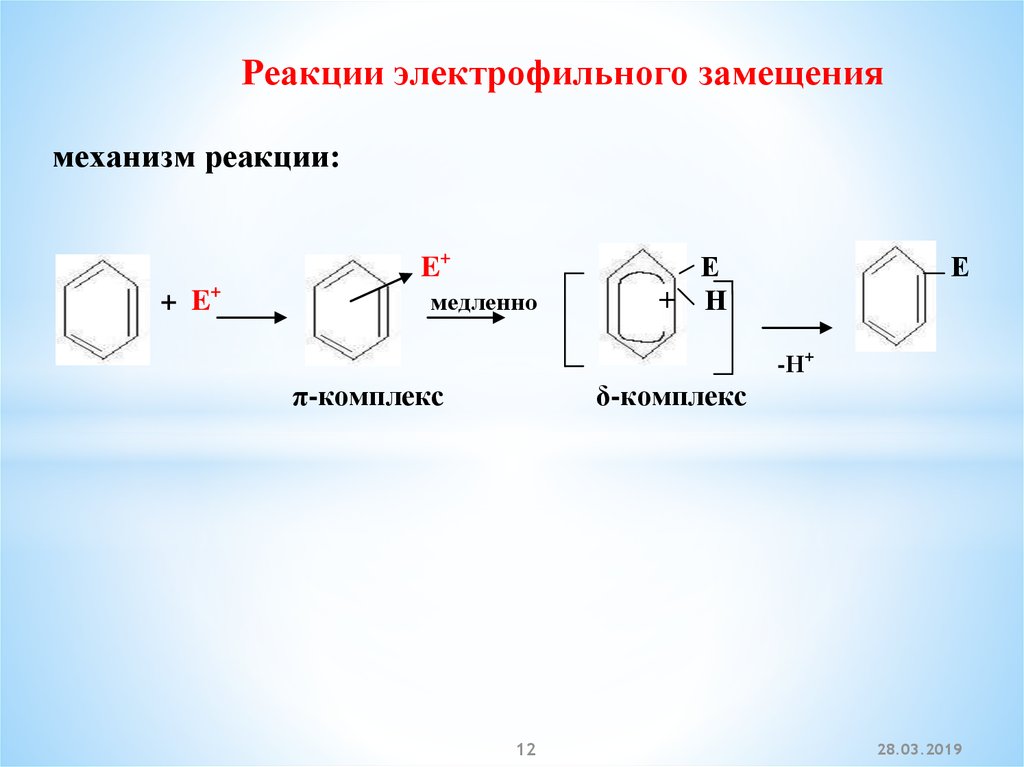
12.
Реакции электрофильного замещениямеханизм реакции:
E+
+ E+
медленно
Е
+ Н
Е
-Н+
π-комплекс
δ-комплекс
12
28.03.2019
13.
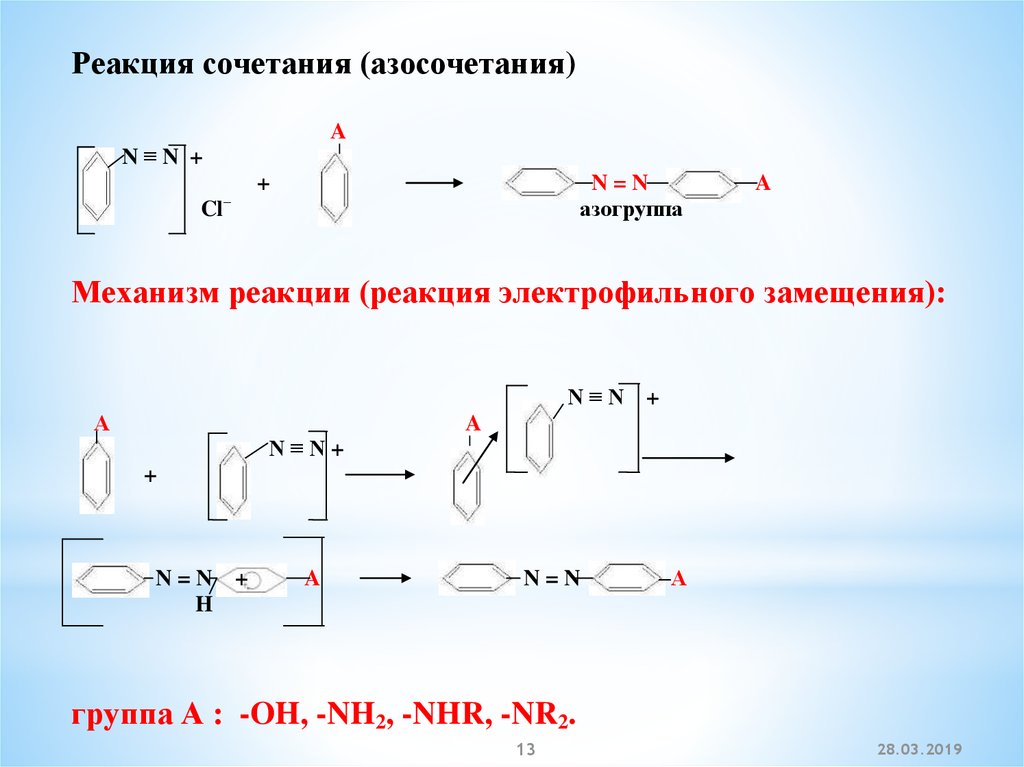
Реакция сочетания (азосочетания)A
|
N≡N +
Cl
–
+
N=N
азогруппа
A
Механизм реакции (реакция электрофильного замещения):
N≡N +
А
A
N≡N+
|
+
N=N +
H
A
N=N
–А
группа А : -OH, -NH2, -NHR, -NR2.
13
28.03.2019
14.
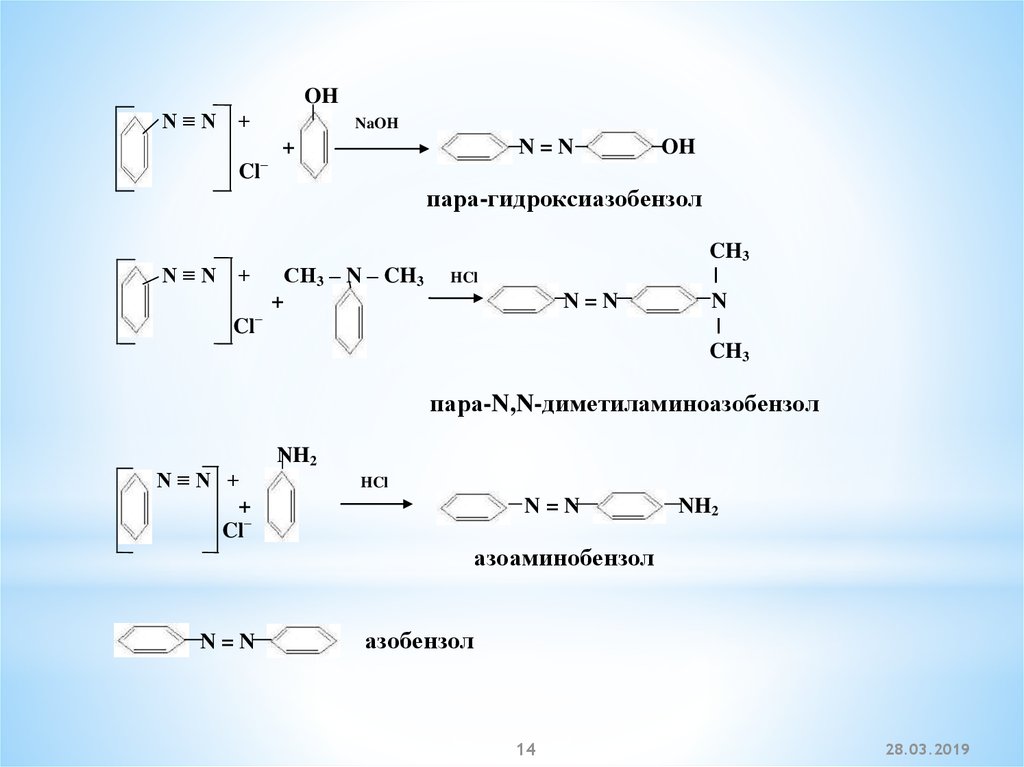
OHN≡N +
NaOH
Cl
–
+
N=N
OH
пара-гидроксиазобензол
N≡N +
Cl
CH3 – N – CH3
–
HCl
+
N=N
CH3
|
N
|
CH3
пара-N,N-диметиламиноазобензол
N≡N +
+
Cl–
NH2
HCl
N=N
NH2
азоаминобензол
N=N
азобензол
14
28.03.2019
15.
Существуют 2 категории групп1. Хромофорные группы (данные группы
соединению):
1) простые группы
С=С
С=О ;
;
двойная
связь
оксо-
–N=O;
O
нитро-
дают окраску химическому
–N=O ;
–N=N–
нитрозо-
азо-
2) сложные (хиноидные) группы
=
=;
//
\\
2. Ауксохромные группы
окрашиванию):
(сообщающие
материалу
способность
-NH2, -OH, -SO3H
15
28.03.2019
к
16.
Пример: азокраситель метиловый оранжевый в зависимости от рНсреды имеет разную окраску
O
||
NaO – S –
||
O
-N=Nжелтый цвет
O
||
NaO-S||
O
-N–N=
|
H
CH3
|
-N
|
CH3
H+
OH-
CH3
|
= N+
|
CH3
красный цвет
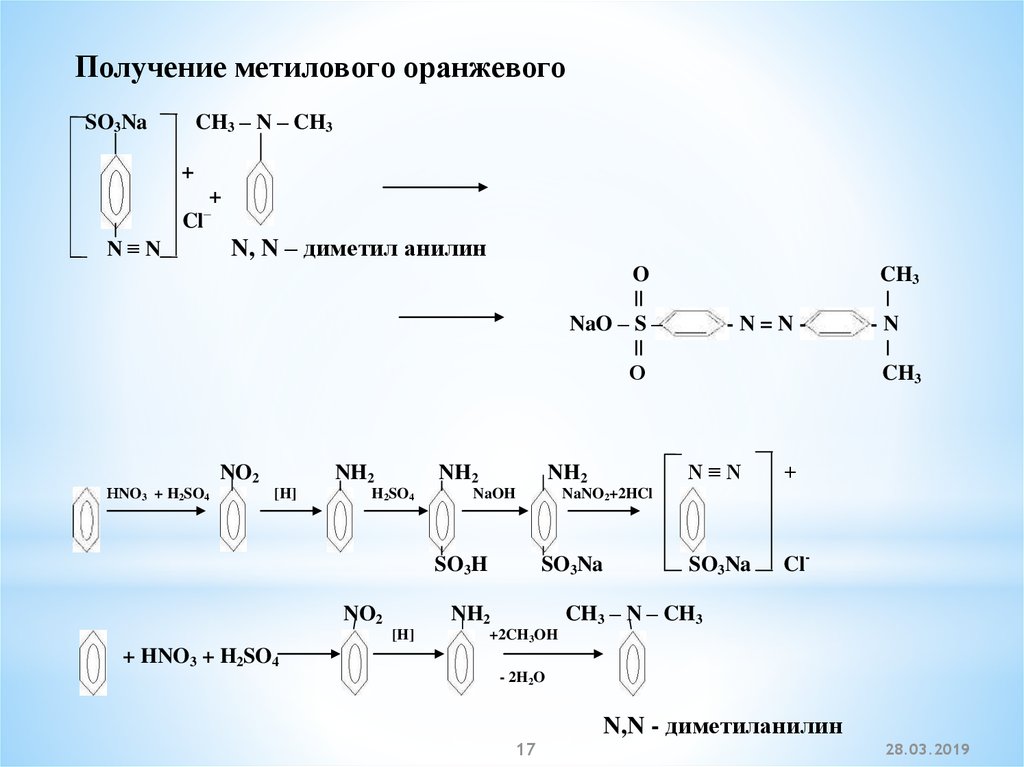
Получение метилового оранжевого
SO3Na
CH3 – N – CH3
+
Cl
Группа А
–
+
метилоранж
N≡N
N, N – диметил анилин
16
28.03.2019
17.
Получение метилового оранжевогоCH3 – N – CH3
SO3Na
+
+
Cl
–
N≡N
N, N – диметил анилин
O
||
NaO – S –
||
О
НNO3 + H2SO4
NO2
NH2
[H]
NH2
H2SO4
NH2
NaOH
SO3H
NO2
N≡N
+
SO3Na
Cl-
NaNO2+2HCl
SO3Na
CH3 – N – CH3
NH2
[H]
-N=N-
CH3
|
-N
|
CH3
+2CH3OH
+ HNO3 + H2SO4
- 2H2O
N,N - диметиланилин
17
28.03.2019
18.
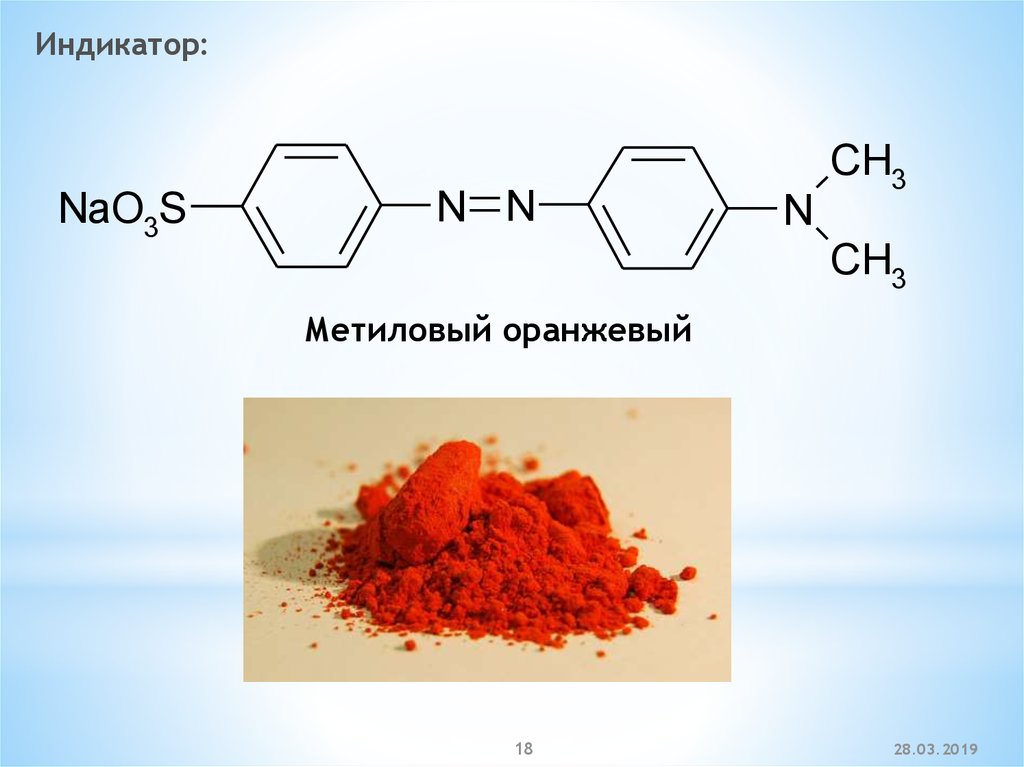
Индикатор:NaO3S
N N
N
CH3
CH3
Метиловый оранжевый
18
28.03.2019
19.
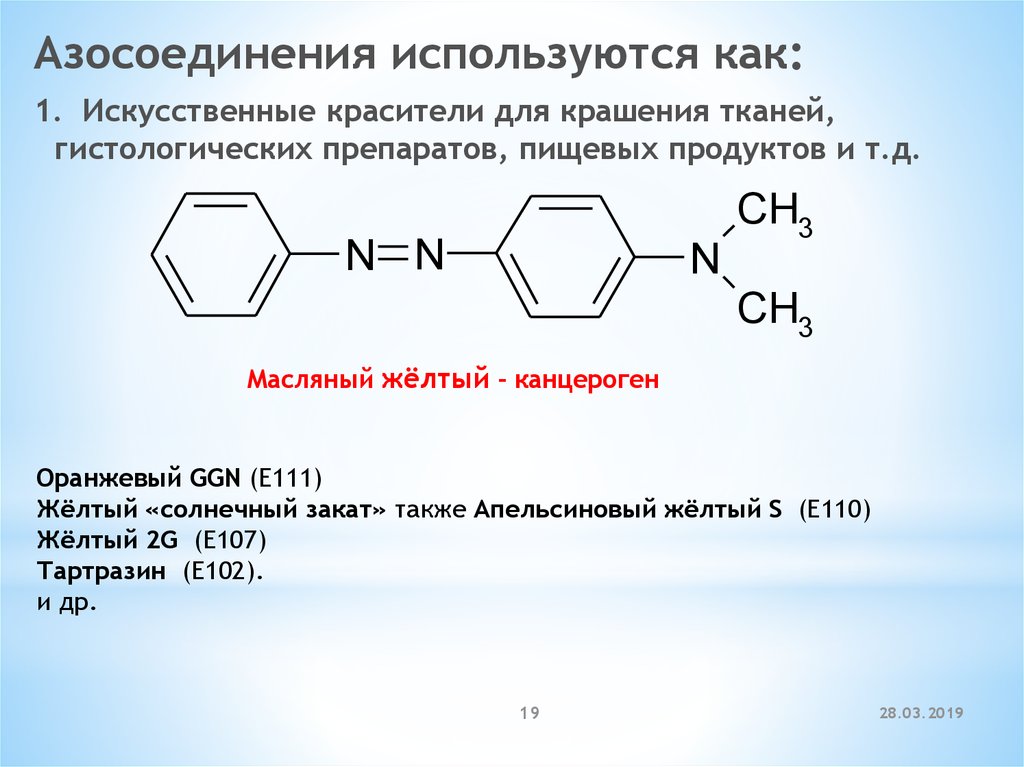
Азосоединения используются как:1. Искусственные красители для крашения тканей,
гистологических препаратов, пищевых продуктов и т.д.
N N
N
CH3
CH3
Масляный жёлтый - канцероген
Оранжевый GGN (E111)
Жёлтый «солнечный закат» также Апельсиновый жёлтый S (E110)
Жёлтый 2G (E107)
Тартразин (E102).
и др.
19
28.03.2019
20.
Е110 - вызывают аллергическиереакции, заложенность носа,
насморк, тошноту, боли в
животе, гиперактивность.
Е111 - (солнечный закат)
запрещён к использованию по
причине токсичности. Е111
способен вызывать аллергию,
которая выражается в виде
кожных высыпаний,
подташнивания и возможных
головных болях.
E107 - применяется для окрашивания
безалкогольных напитков в желтый
цвет.
Воздействие на человека: опасен для
людей страдающих астмой, может
стать причиной аллергической
Е102 - может приводить к разнообразным
реакции.
негативным последствиям от головной
боли до раковых опухолей. Тартразин
усиливает канцерогенные качества
бензоата натрия (Бензоат натрия Е-211).
Бензоат натрия обладает свойствами антибиотика и усилителя
цвета. Встречается в соусах для барбекью, прессервах, соевых
соусах, "фруктовых" драже, леденцах и пр. Вызывает
аллергические реакции. Вредные свойства усиливаются в
сочетании с Е-102 (тартразином).
28.03.2019










 Химия
Химия