Похожие презентации:
Антибиотики. Действие антибиотиков
1.
2.
Антибиотики.1
Антибиотики
– природные вещества микробного (позднее – растительного и
животного) происхождения и продукты их химической модификации, способные
в низких концентрациях (10–3–10–2 мкг/мл) подавлять развитие бактерий, низших
грибов, простейших, вирусов или клеток злокачественных опухолей.
Известно несколько тысяч природных антибиотиков, среди которых наиболее
представительными группами и часто применяемыми в медицине являются 4
основных структурных типа: b-лактамы, тетрациклины, неполиеновые
макролиды и аминогликозиды (практически все – гетероциклические
соединения). Значительно больше существует синтетических и полусинтетических аналогов и производных, обладающих большей активностью и
устойчивостью, чем природные прототипы. Лишь 3% находят применение в
медицине. Пенициллины и цефалоспорины – более половины всех
производимых антибиотиков.
По механизму действия антибиотики можно разделить на 4 основных типа:
1)
2)
3)
4)
ингибиторы синтеза бактериальной клеточной стенки;
ингибиторы матричного (рибосомального) синтеза белка;
ингибиторы синтеза нуклеиновых кислот;
ингибиторы функционирования цитоплазматической мембраны.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
3.
Пенициллины.2
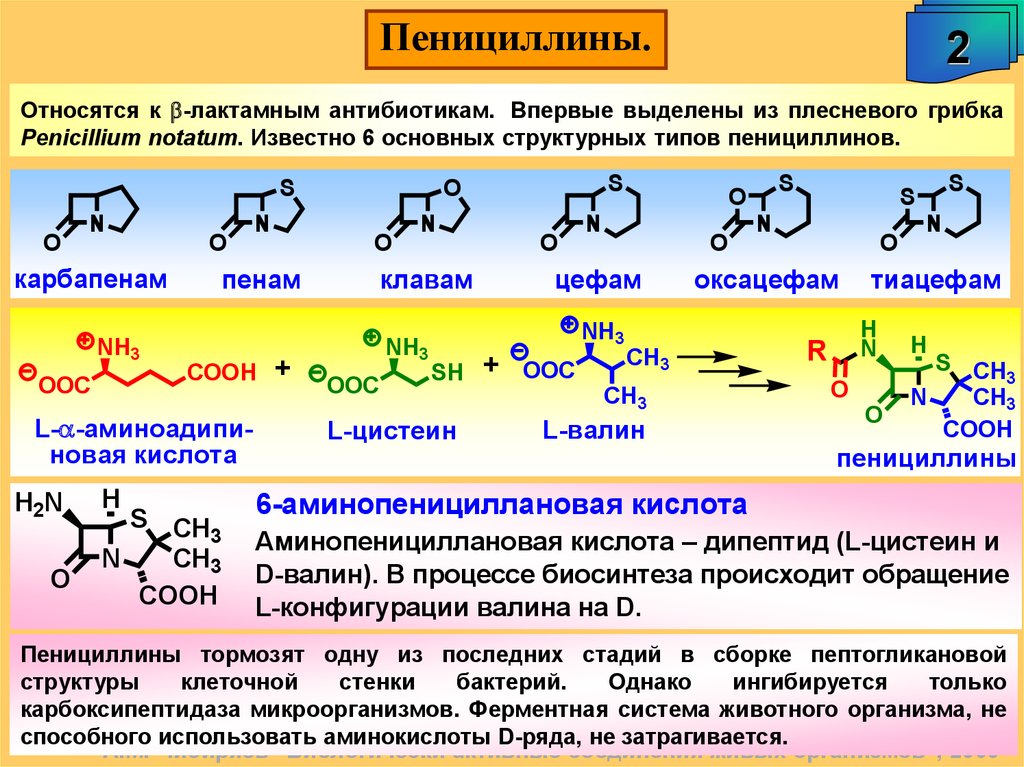
Относятся к b-лактамным антибиотикам. Впервые выделены из плесневого грибка
Penicillium notatum. Известно 6 основных структурных типов пенициллинов.
S
O
N
карбапенам
O
N
NH3
COOH
OOC
L- -аминоадипиновая кислота
H2N
O
H
O
пенам
S CH
3
N
CH3
COOH
+
S
O
N
клавам
NH3
OOC
O
N
O
цефам
L-цистеин
CH3
CH3
L-валин
S
S
N
O
оксацефам
NH3
SH + OOC
S
O
тиацефам
H
N
R
N
O
O
H
S CH
3
N
CH3
COOH
пенициллины
6-аминопенициллановая кислота
Аминопенициллановая кислота – дипептид (L-цистеин и
D-валин). В процессе биосинтеза происходит обращение
L-конфигурации валина на D.
Пенициллины тормозят одну из последних стадий в сборке пептогликановой
структуры
клеточной
стенки
бактерий.
Однако
ингибируется
только
карбоксипептидаза микроорганизмов. Ферментная система животного организма, не
способного использовать аминокислоты D-ряда, не затрагивается.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
4.
Практически важные пенициллины.R1
H
N
O
3
тиазолидин
S CH
3
N
CH3
COOR2
H
Довольно нестабильные вещества, в щелочной среде и при
нагревании легко раскрывается
лактамный цикл с образованием
биологически не активных пенициллоиновых кислот. Аналогично
действуют
b-лактамазы
–
ферменты устойчивых к пенициллинам штаммов микроорганизмов. Через усиление активности этого фермента развива-
ется резистентность организма.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
5.
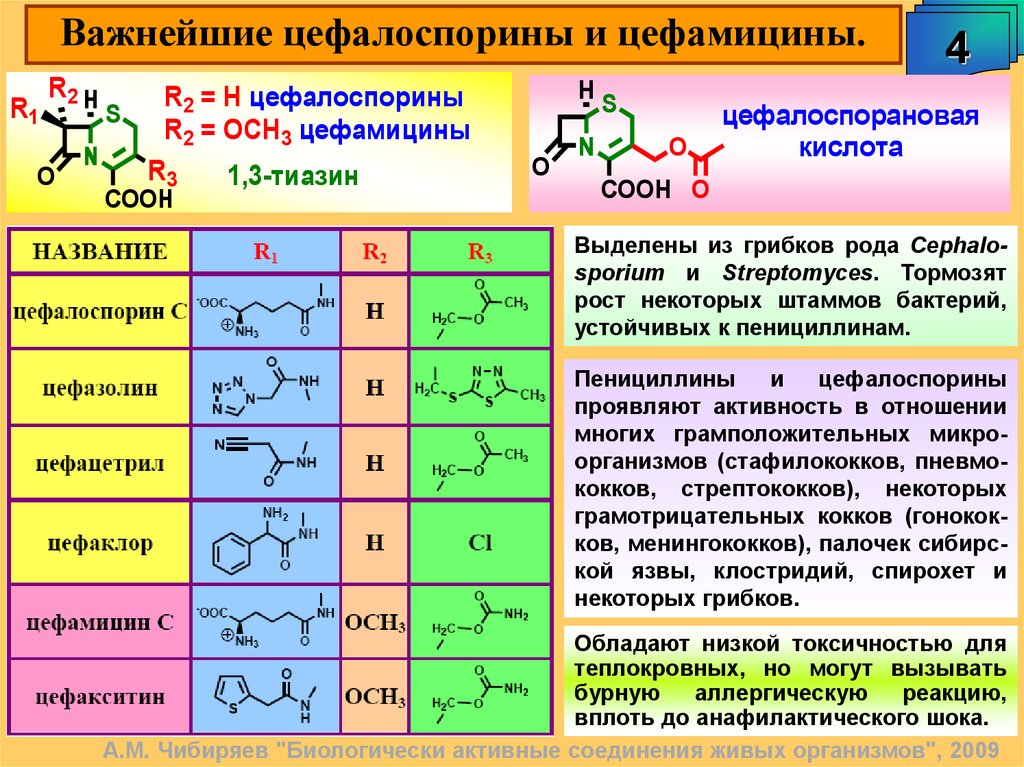
Важнейшие цефалоспорины и цефамицины.R2 H
R2 = H цефалоспорины
R1
S
R2 = OCH3 цефамицины
N
R3
O
1,3-тиазин
COOH
H
O
N
S
O
4
цефалоспорановая
кислота
COOH O
Выделены из грибков рода Cephalosporium и Streptomyces. Тормозят
рост некоторых штаммов бактерий,
устойчивых к пенициллинам.
Пенициллины
и
цефалоспорины
проявляют активность в отношении
многих грамположительных микроорганизмов (стафилококков, пневмококков, стрептококков), некоторых
грамотрицательных кокков (гонококков, менингококков), палочек сибирской язвы, клостридий, спирохет и
некоторых грибков.
Обладают низкой токсичностью для
теплокровных, но могут вызывать
бурную
аллергическую
реакцию,
вплоть до анафилактического шока.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
6.
Важнейшие тетрациклины.N
HO
5
R3 R2 R1X
H
A B C D
R4
O
OH
O
OH O
OH
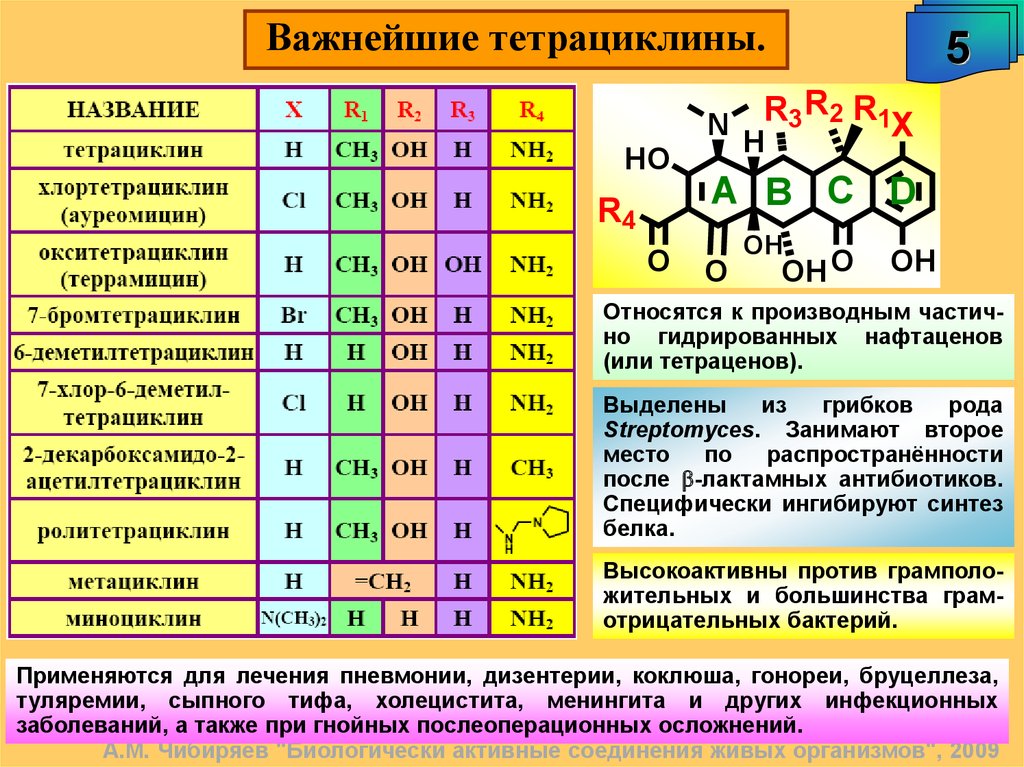
Относятся к производным частично гидрированных нафтаценов
(или тетраценов).
Выделены
из
грибков
рода
Streptomyces. Занимают второе
место
по
распространённости
после b-лактамных антибиотиков.
Специфически ингибируют синтез
белка.
Высокоактивны против грамположительных и большинства грамотрицательных бактерий.
Применяются для лечения пневмонии, дизентерии, коклюша, гонореи, бруцеллеза,
туляремии, сыпного тифа, холецистита, менингита и других инфекционных
заболеваний, а также при гнойных послеоперационных осложнений.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
7.
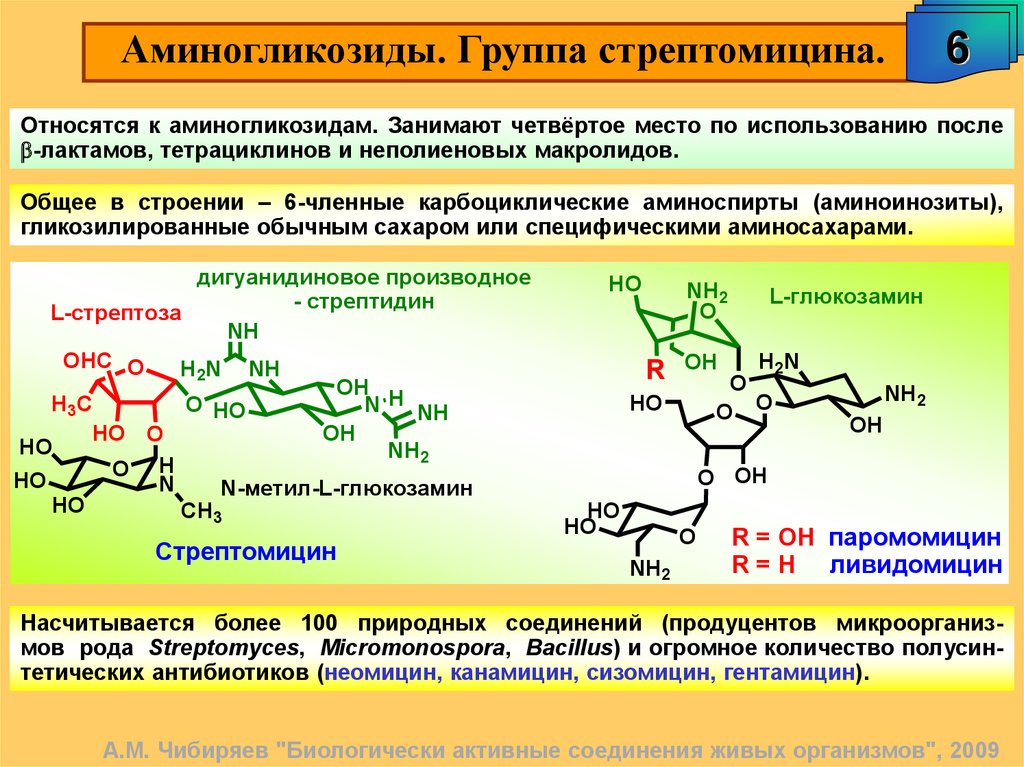
Аминогликозиды. Группа стрептомицина.6
Относятся к аминогликозидам. Занимают четвёртое место по использованию после
b-лактамов, тетрациклинов и неполиеновых макролидов.
Общее в строении – 6-членные карбоциклические аминоспирты (аминоинозиты),
гликозилированные обычным сахаром или специфическими аминосахарами.
дигуанидиновое производное
- стрептидин
L-стрептоза
NH
OHC O
H2N NH
OH
H3C
O HO
N H NH
HO O
OH
HO
NH2
O H
HO
N
N-метил-L-глюкозамин
HO
CH3
Стрептомицин
HO
NH2
O
L-глюкозамин
R OH O H2N
HO
O
NH2
O
OH
O OH
HO
HO
O
NH2
R = OH паромомицин
R = H ливидомицин
Насчитывается более 100 природных соединений (продуцентов микроорганизмов рода Streptomyces, Micromonospora, Bacillus) и огромное количество полусинтетических антибиотиков (неомицин, канамицин, сизомицин, гентамицин).
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
8.
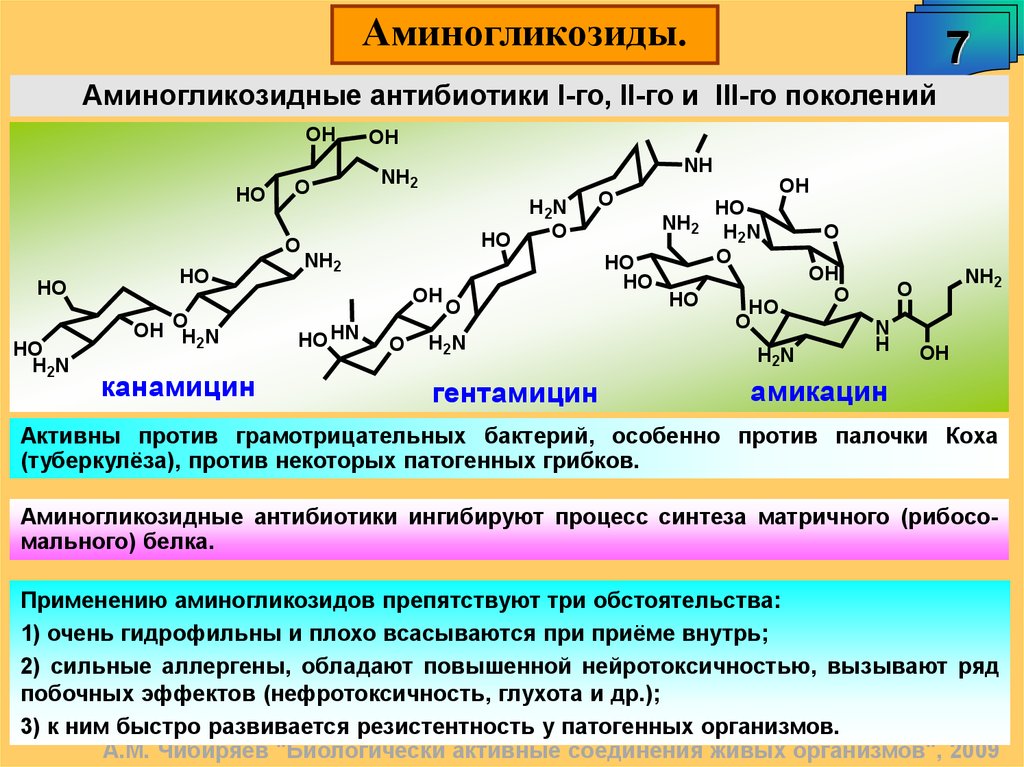
Аминогликозиды.7
Аминогликозидные антибиотики I-го, II-го и III-го поколений
OH
HO
O
O
HO
HO
H2N
HO
OH
NH
NH2
H2N
O
HO
NH2
OH
OH OH N
2
канамицин
HO HN
O
NH2
HO
HO
O
H2N
гентамицин
OH
O
HO
HO
H2N
O
HO
O
H2N
O
OH
O
NH2
O
N
H
OH
амикацин
Активны против грамотрицательных бактерий, особенно против палочки Коха
(туберкулёза), против некоторых патогенных грибков.
Аминогликозидные антибиотики ингибируют процесс синтеза матричного (рибосомального) белка.
Применению аминогликозидов препятствуют три обстоятельства:
1) очень гидрофильны и плохо всасываются при приёме внутрь;
2) сильные аллергены, обладают повышенной нейротоксичностью, вызывают ряд
побочных эффектов (нефротоксичность, глухота и др.);
3) к ним быстро развивается резистентность у патогенных организмов.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
9.
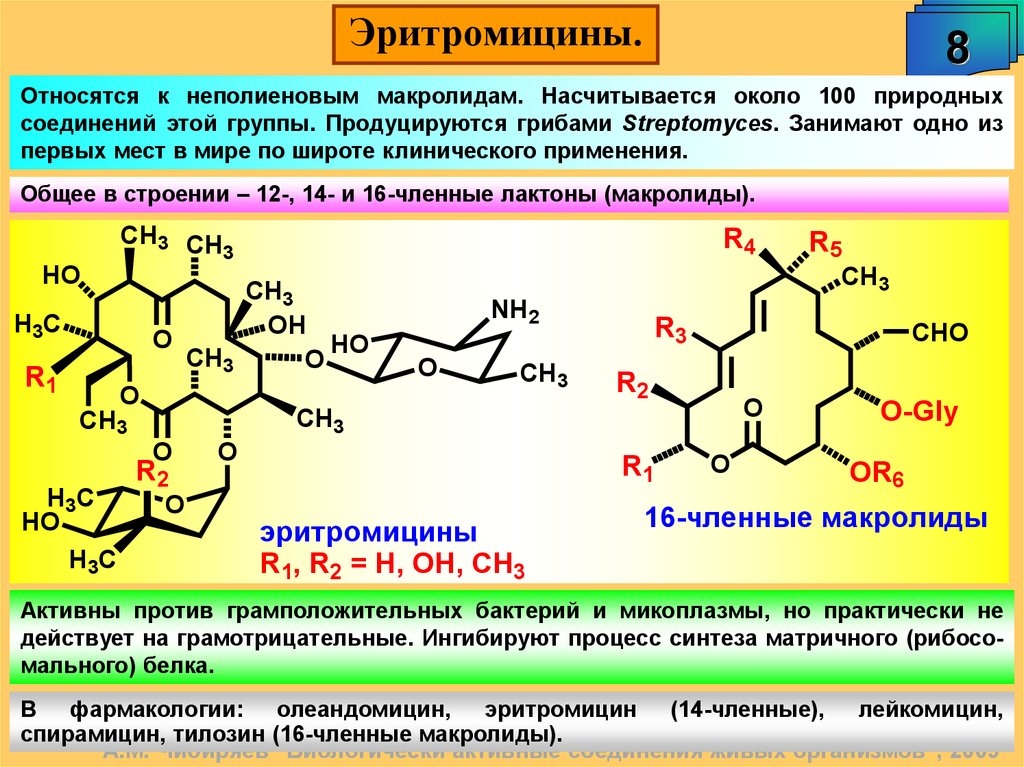
Эритромицины.8
Относятся к неполиеновым макролидам. Насчитывается около 100 природных
соединений этой группы. Продуцируются грибами Streptomyces. Занимают одно из
первых мест в мире по широте клинического применения.
Общее в строении – 12-, 14- и 16-членные лактоны (макролиды).
CH3 CH
3
HO
CH3
OH
O
HO
CH3
O
H3C
R1
O
O
R2
O
R5
CH3
NH2
O
CH3
R3
CHO
R2
O
CH3
CH3
H3C
HO
H3C
R4
O
R1
эритромицины
R1, R2 = H, OH, CH3
O
O-Gly
OR6
16-членные макролиды
Активны против грамположительных бактерий и микоплазмы, но практически не
действует на грамотрицательные. Ингибируют процесс синтеза матричного (рибосомального) белка.
В фармакологии: олеандомицин, эритромицин (14-членные), лейкомицин,
спирамицин, тилозин (16-членные макролиды).
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
10.
Неполиеновые макролиды (антибиотики).N
HO
O
HO
HO
O
Et
O
O
O
O
метимицин
(12-членный макролид)
O
H3CO
O
H3C
HO
H3C
O
Et
эритромицин
(14-членный макролид)
OH
OH
OH
O
O
HO
O
Et O
N
HO
CHO
HO
O
O
O
O
OH
HO
CH3
OH OH OH
OH O
COOH
9
O
O
O
OH
N
розарамицин
(16-членный макролид)
нистатин
(38-членный полиеновый
макролид)
O
O
OH
NH2
OH
А.М. Чибиряев "Биологически активные
соединения живых организмов", 2009
11.
Грамицидин А.O
10
( 15 аминокислотных остатков ) NH OH
H
Относится к группе олигопептидных антибиотиков, которые являются
одновременно каналообразователями в биологических мембранах. В
частности, две молекулы грамицидина А образуют спираль, полую
внутри (диаметр – 0.3 нм), которая встраивается в липидный бислой
мембран. По этому каналу осуществляется транспорт ионов K+, Na+, H+.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009




 Химия
Химия








