Похожие презентации:
Химические свойства кислот (8 класс)
1.
Химические свойствакислот.
2.
Она жжётся и кусается,Если к нам на руки проливается.
Дырки в брюках оставляет
И бумагу прожигает.
Вот такая вот она –
Эта наша …!
3.
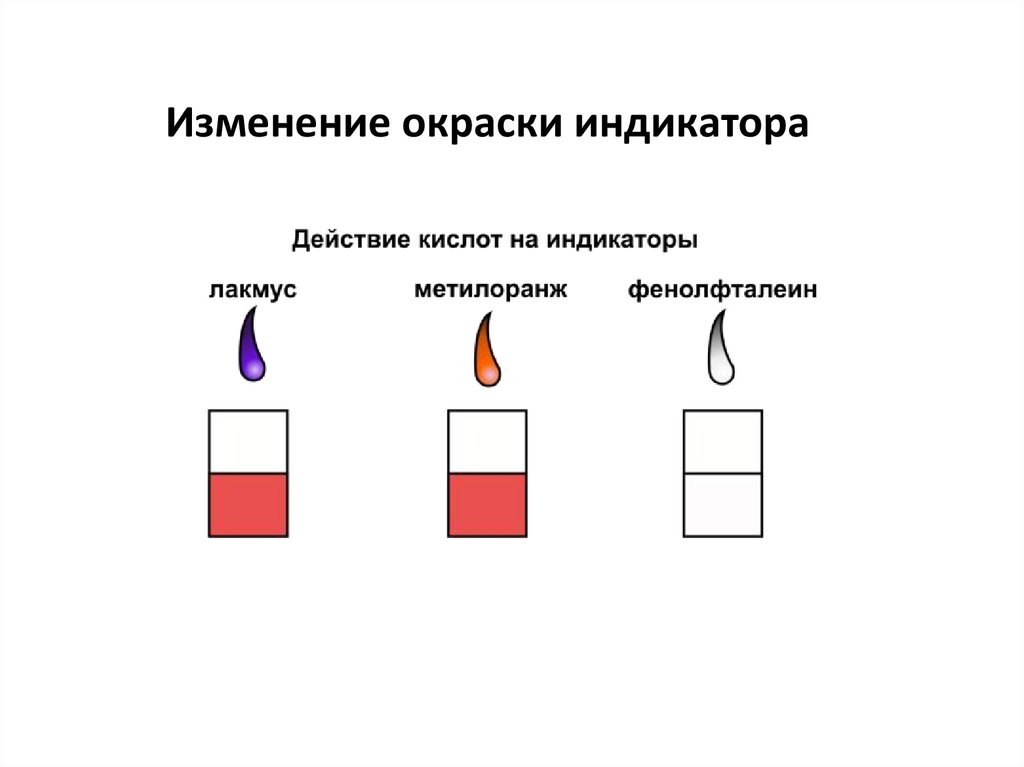
Изменение окраски индикатора4.
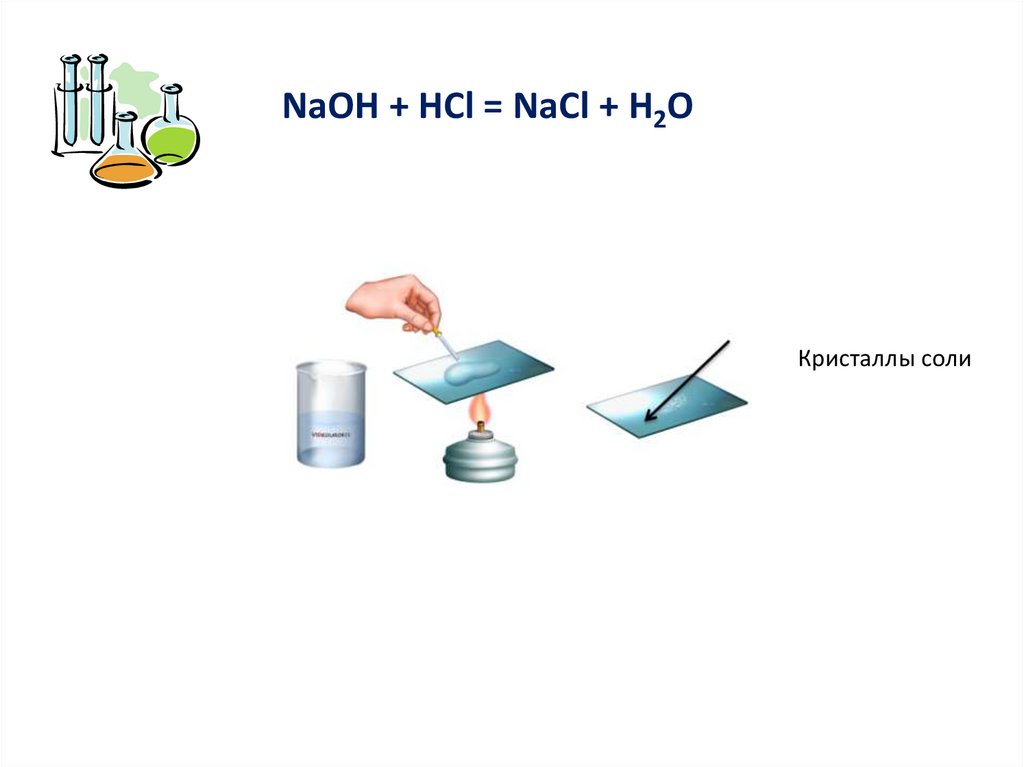
2. Реакция с основаниями5.
NaOH + HCl = NaCl + H2OКристаллы соли
6.
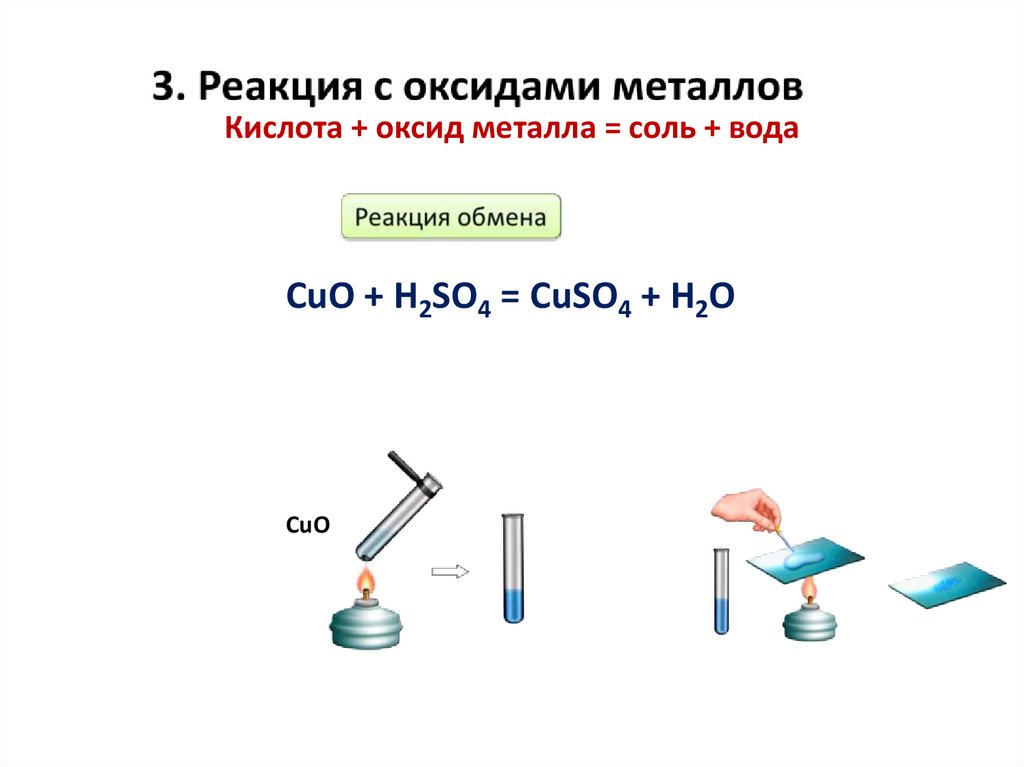
Кислота + оксид металла = соль + водаCuO + H2SO4 = CuSO4 + H2O
CuO
7.
4. Реакции с металламиКислота + металл = соль + водород
Реакции
замещения
8.
Для этих реакций необходимы условия:9.
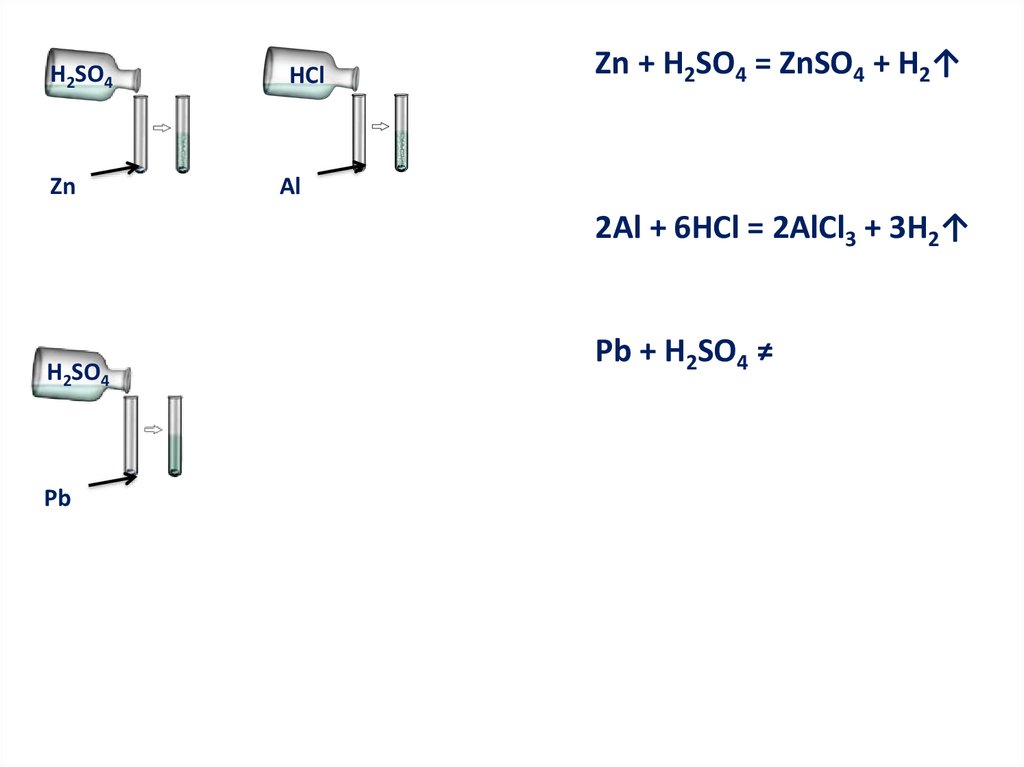
H2SO4Zn
HCl
Zn + H2SO4 = ZnSO4 + H2↑
Al
2Al + 6HCl = 2AlCl3 + 3H2↑
H2SO4
Pb
Pb + H2SO4 ≠
10.
Для этих реакций необходимы условия:Металл должен находиться в ряду напряжений до водорода;
Должна получиться растворимая соль;
Нерастворимые кислоты не вступают в реакцию с металлами;
11.
5. Реакция с солямиКислота + соль = новая кислота + новая соль
Реакция обмена
12.
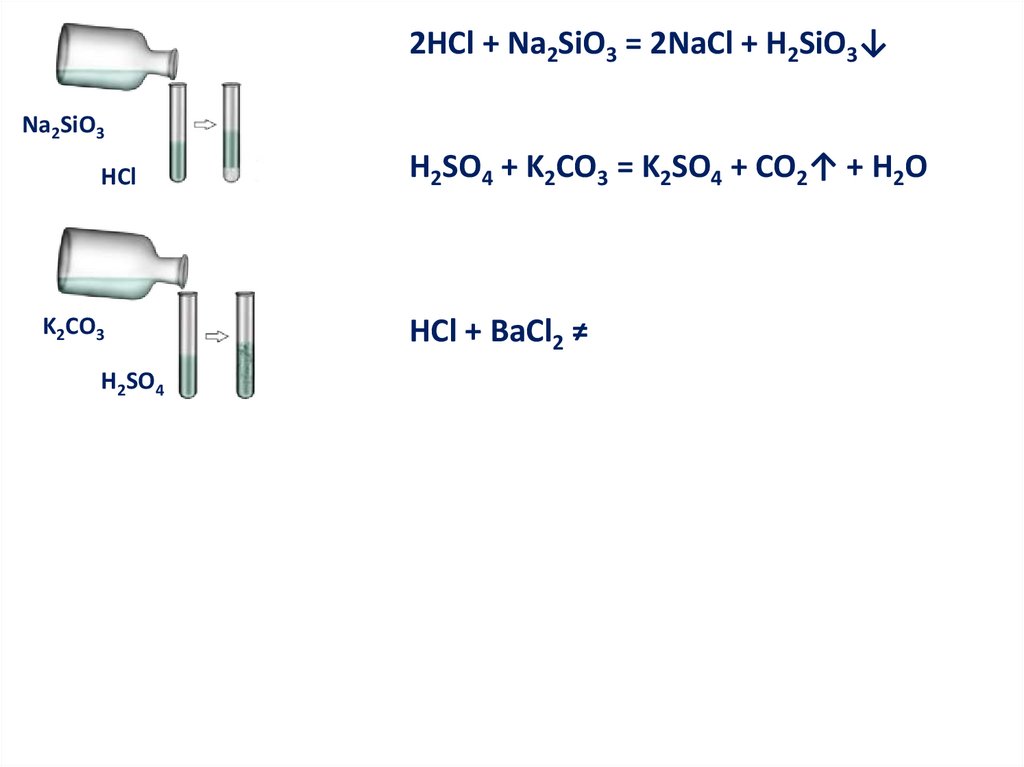
2HCl + Na2SiO3 = 2NaCl + H2SiO3↓Na2SiO3
HCl
K2CO3
H2SO4
H2SO4 + K2CO3 = K2SO4 + CO2↑ + H2O
HCl + BaCl2 ≠
13.
Запомните:Кислоты изменяют окраску индикаторов;
Кислоты реагируют с основаниями;
Кислоты реагируют с оксидами металлов;
Кислоты при определённых условиях реагируют с металлами
и солями.







 Химия
Химия








