Похожие презентации:
Химическая связь (11 класс)
1.
Химическая связь2.
Химическая связь – этовзаимодействие атомов, результатом
которого явлется образование молекулы
или кристалла
Кто участвует в образовании ХС? За счёт
чего?
Какие виды ХС существуют?
3.
Ковалентная связь – связь междудвумя атомами неметаллов,
возникающая за счёт образования
общих электронных пар
КХС может образовываться разными
способами (по разным механизмам)
1. Обменный
2. Донорно-акцепторный
4.
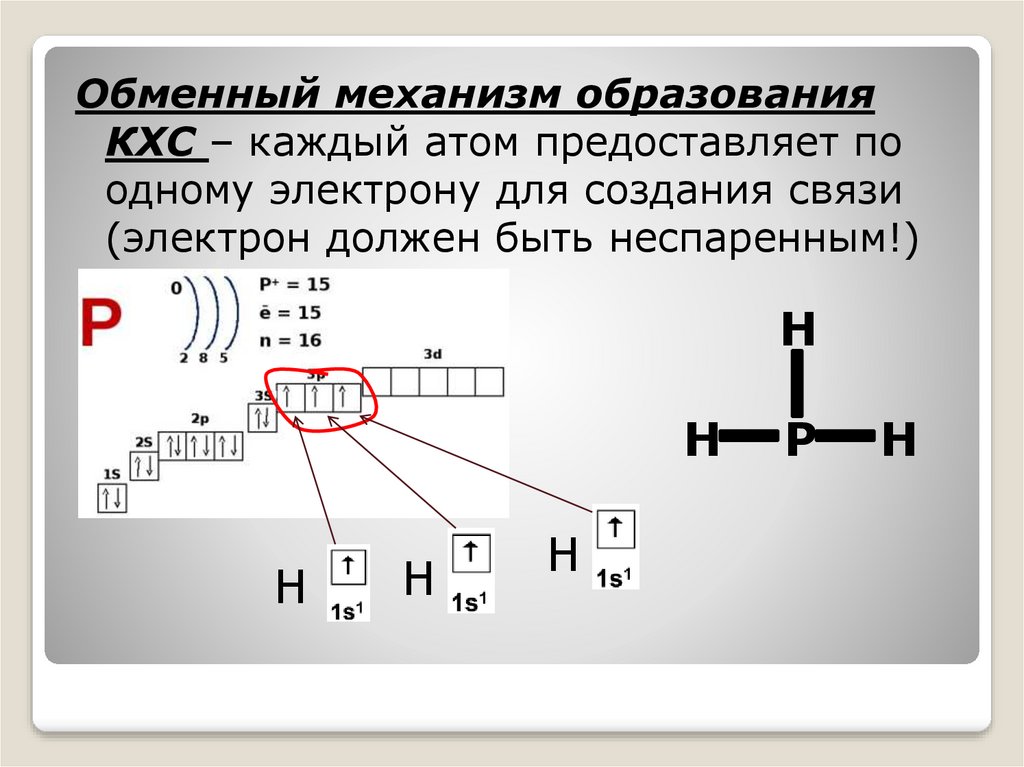
Обменный механизм образованияКХС – каждый атом предоставляет по
одному электрону для создания связи
(электрон должен быть неспаренным!)
Н
Н
Н
Н
Н
Р
Н
5.
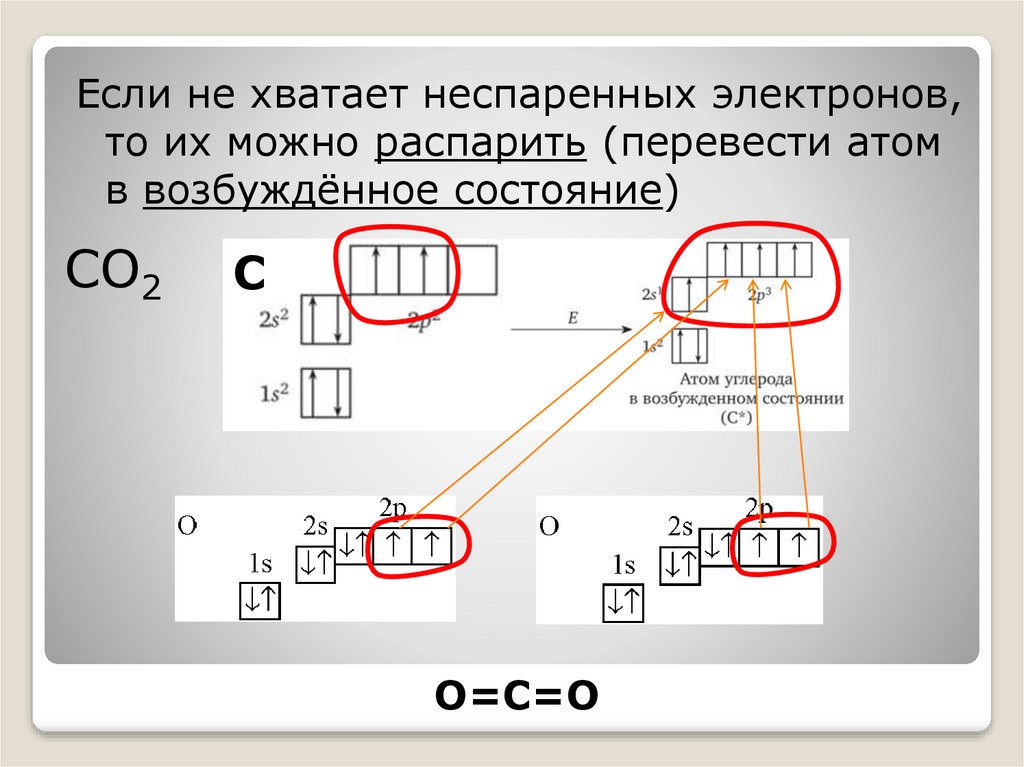
Если не хватает неспаренных электронов,то их можно распарить (перевести атом
в возбуждённое состояние)
СО2
С
О=С=О
6.
Донорно-акцепторный механизм –один атом (донор) предоставляет свою
электронную пару, а другой (акцептор)
– пустую орбиталь
H
H
Н
Н
Н
N
H
Н+
NH4+ - катион аммония
7.
Виды ковалентной связи1. Неполярная (Cl2, N2, H2, O2)
2. Полярная
Если атомы, образующие связь, разные,
то вследствие разной
электроотрицательности (?) один из
атомов будет оттягивать к себе общую
электронную пару. Образуется два
полюса – частично отрицательный и
частично положительный
8.
9.
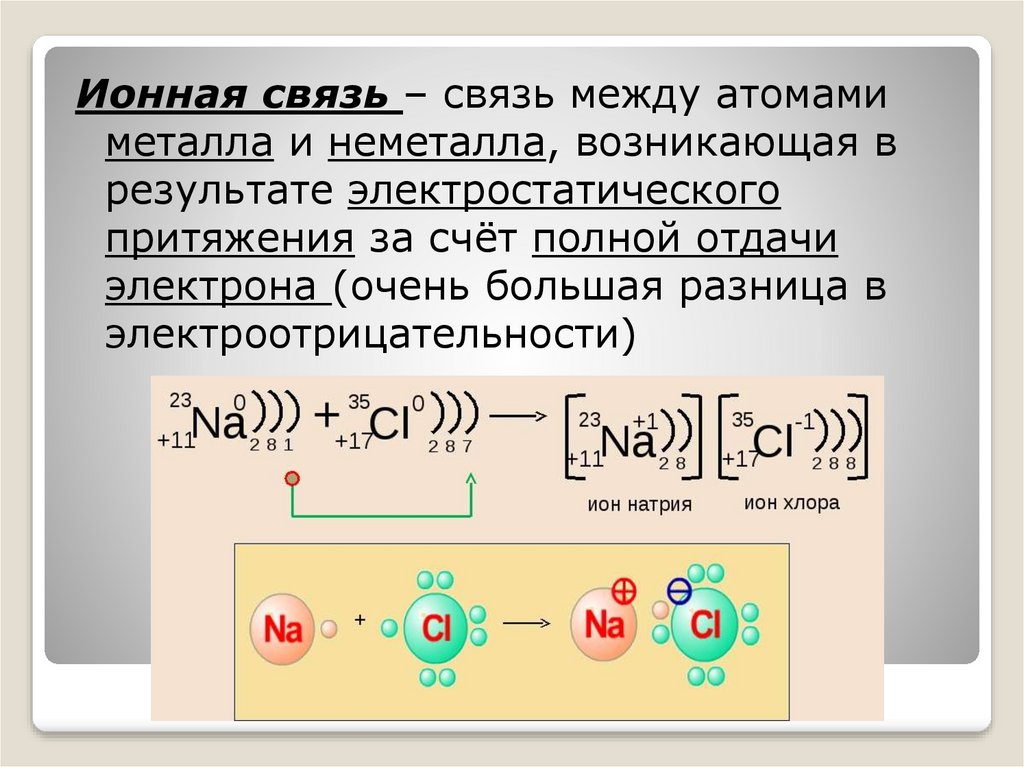
Ионная связь – связь между атомамиметалла и неметалла, возникающая в
результате электростатического
притяжения за счёт полной отдачи
электрона (очень большая разница в
электроотрицательности)
10.
Металлическая связь – связь междуположительными ионами в кристаллах
металлов за счёт притяжения
относительно свободных электронов
11.
В связи с этим и свойства металлов:1. Ковкость
2. Пластичность
3. Металлический блеск
4. Теплопроводность
5. Электропроводность
12.
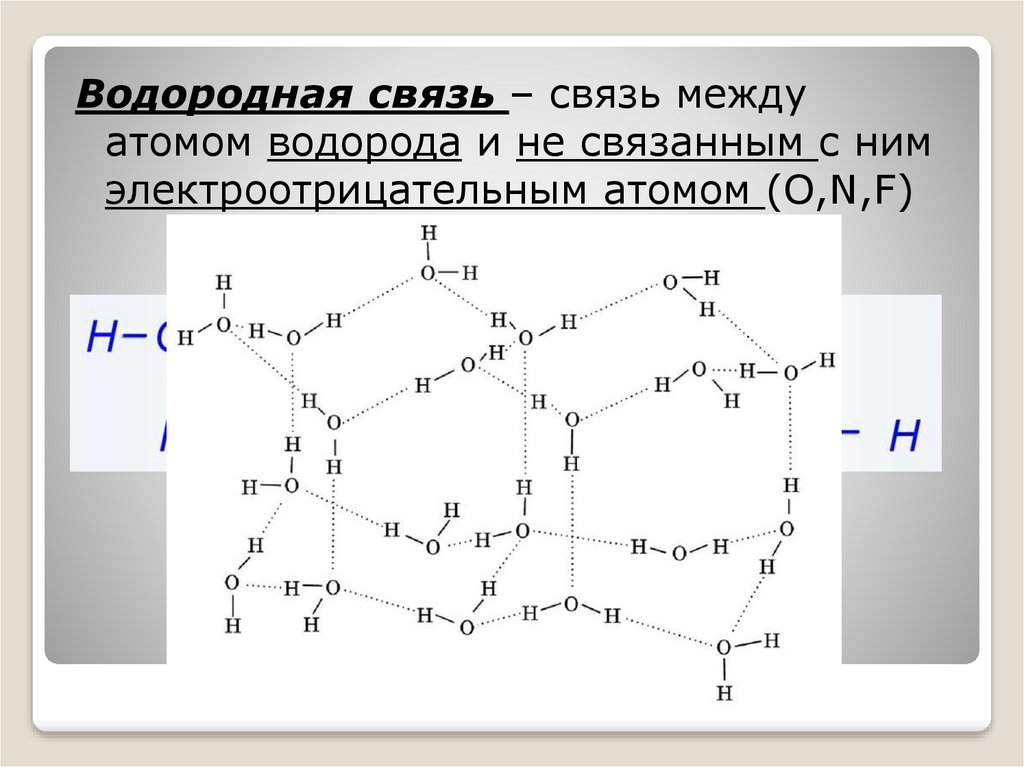
Водородная связь – связь междуатомом водорода и не связанным с ним
электроотрицательным атомом (O,N,F)
13.
Сравните:Ткип (H2S)= -60оС
Ткип (H2Se)= -41оС
Ткип (H2Te)= -2оС
Какая, судя по этому ряду, должна быть
температура кипения у воды?
Почему вода – универсальный растворитель?
14.
Кристаллические решёткиМногие твёрдые тела имеют
кристаллическое строение. Такое
строение называется кристаллической
решёткой.
В узлах кристаллической решётки могут
находиться разные частицы
15.
У ионных веществ – ионная КР(в узлах ионы)
У атомных - …..
У молекулярных - ….
У металлических - ….
16.
17.
Свойства веществ:1. Твёрдые, растворимы
в воде, тугоплавкие,
не проводят эл. ток
2. Твёрдые, прочные,
высокие Тпл,
нерастворимы
3. Легко плавятся,
не проводят эл. ток,
непрочные
4. Разные Тпл, ковкие,
пластичные, проводят
эл. ток, тепло, блестят
Вещества:
А. NaCl, K2S
Б. Ca, Mg, Fe
B. I2, H2O, S8
Г. C(алмаз),Si,B
18.
Домашнее задание:Параграфы 7-10
Задания 3-4 стр. 43
Определить вид ХС в веществах:
K2O, N2, OF2, O3, NaI, Ga, C2H6, Au, C,
MgS
Предположить вид кристаллической
решётки для твёрдых состояний данных
веществ














 Химия
Химия








