Похожие презентации:
Альдегиды. Карбоновые кислоты и их производные
1.
12.
Цели:1.
2.
Познакомиться с классом альдегидов, его
свойствами. Выяснить области применения
альдегидов.
Познакомиться с карбоновыми кислотами и
их производными. Узнать свойства
карбоновых кислот и их производных,
определить области применения.
2
3.
34.
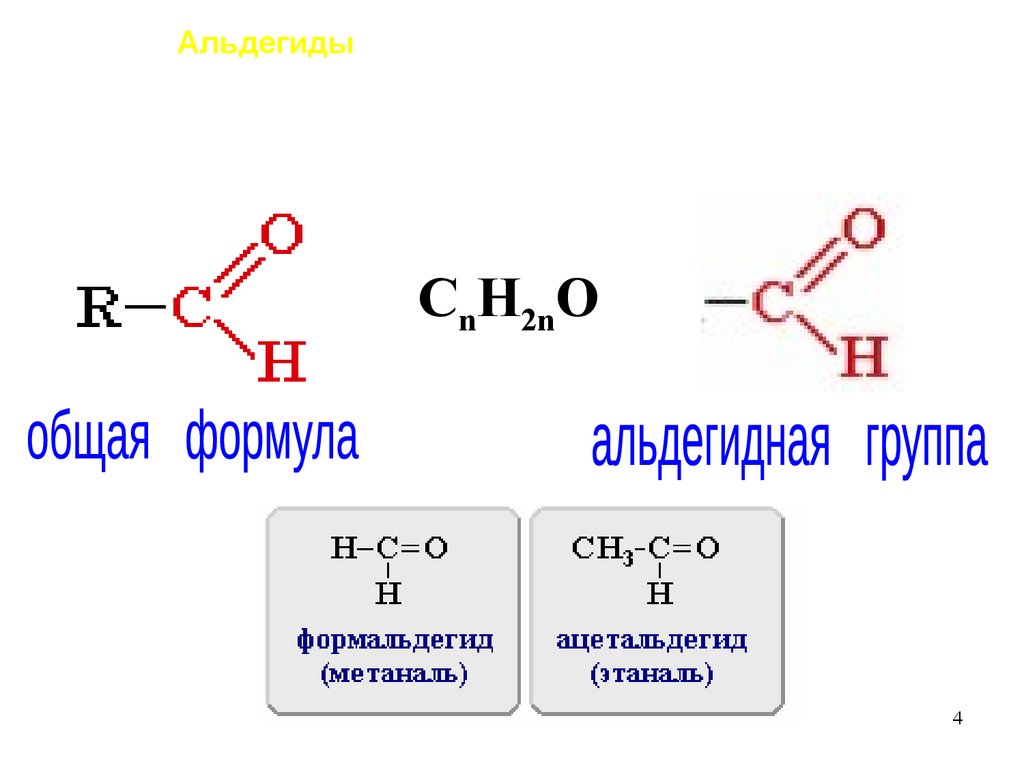
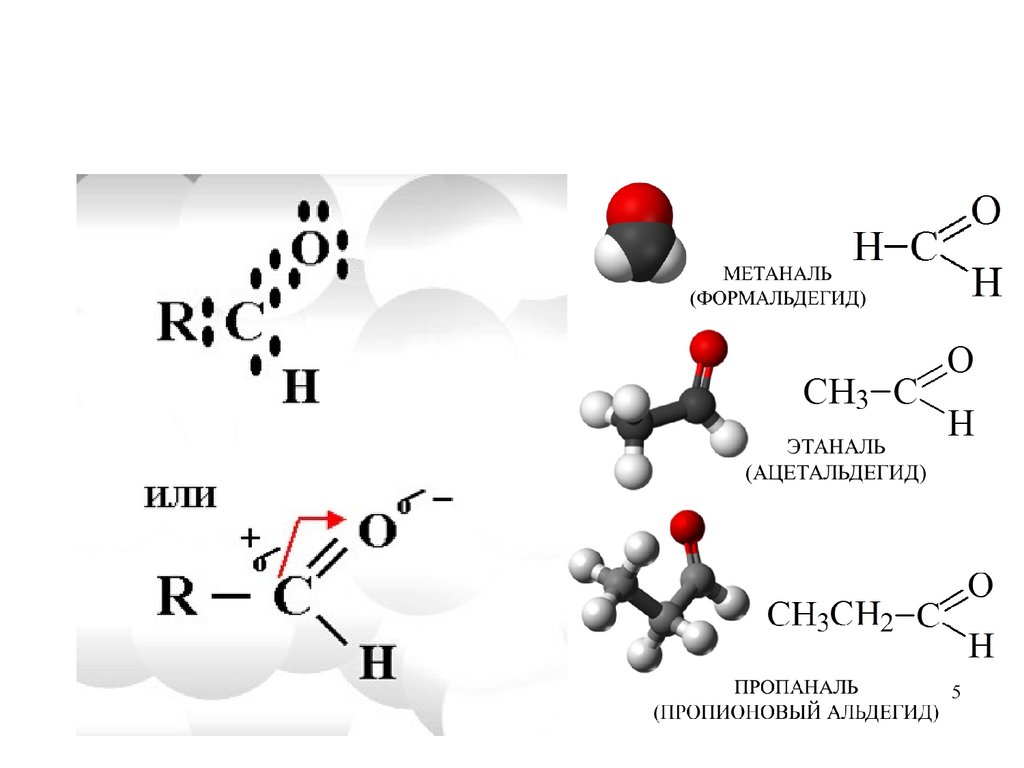
Альдегиды – это органические вещества, молекулы,которых содержат карбонильную группу,
соединенную с углеводородным радикалом и атомом
водорода
CnH2nO
4
5.
56.
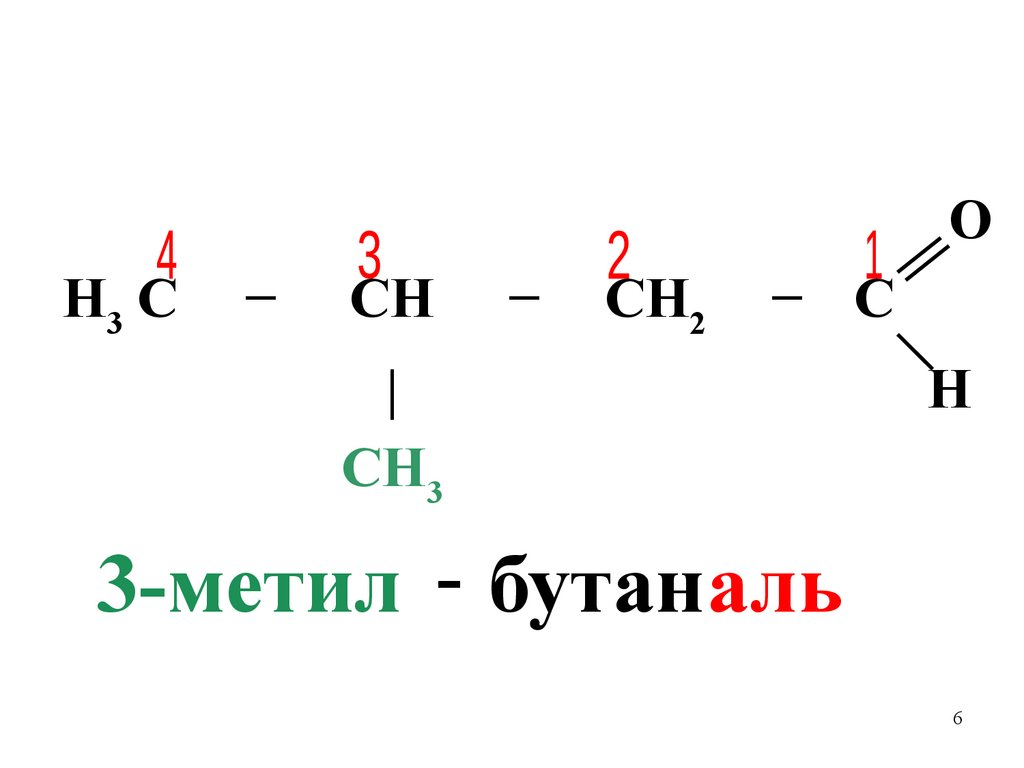
Номенклатура альдегидов(международная)
O
H3 C
−
CH
−
CH2
− C
|
CH3
H
3-метил - бутаналь
6
7.
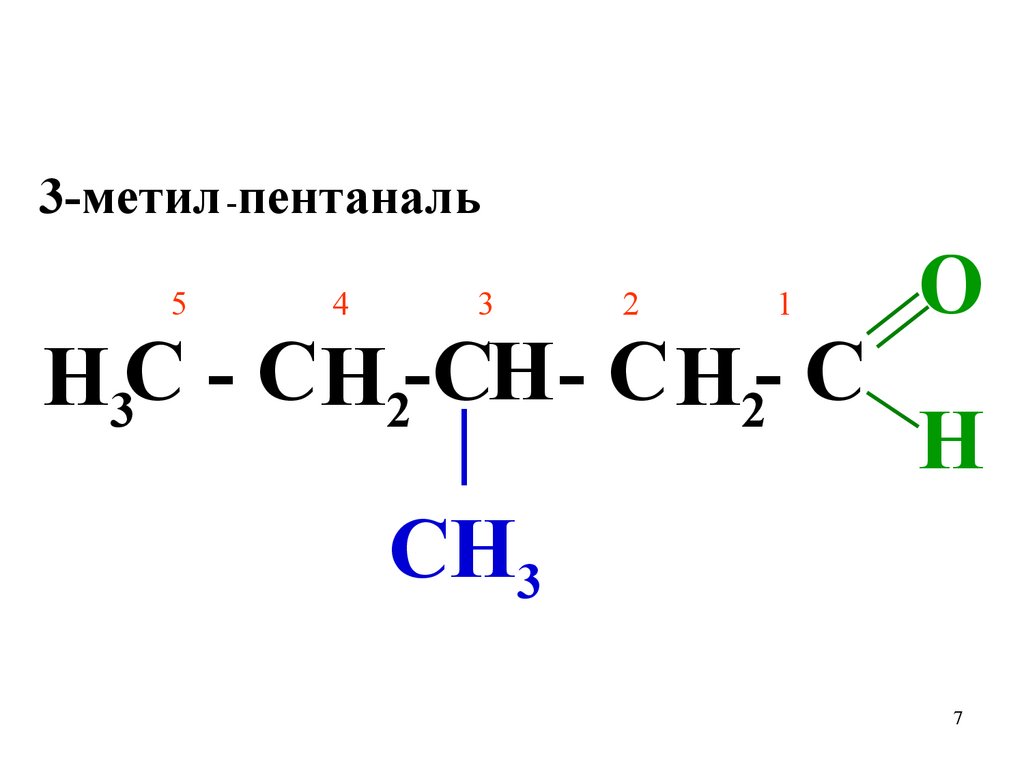
Как составить формулуальдегида по названию?
3-метил -пентаналь
5
4
3
2
1
O
H3С - СH2-СH - С H2- С
|
H
CH3
7
8.
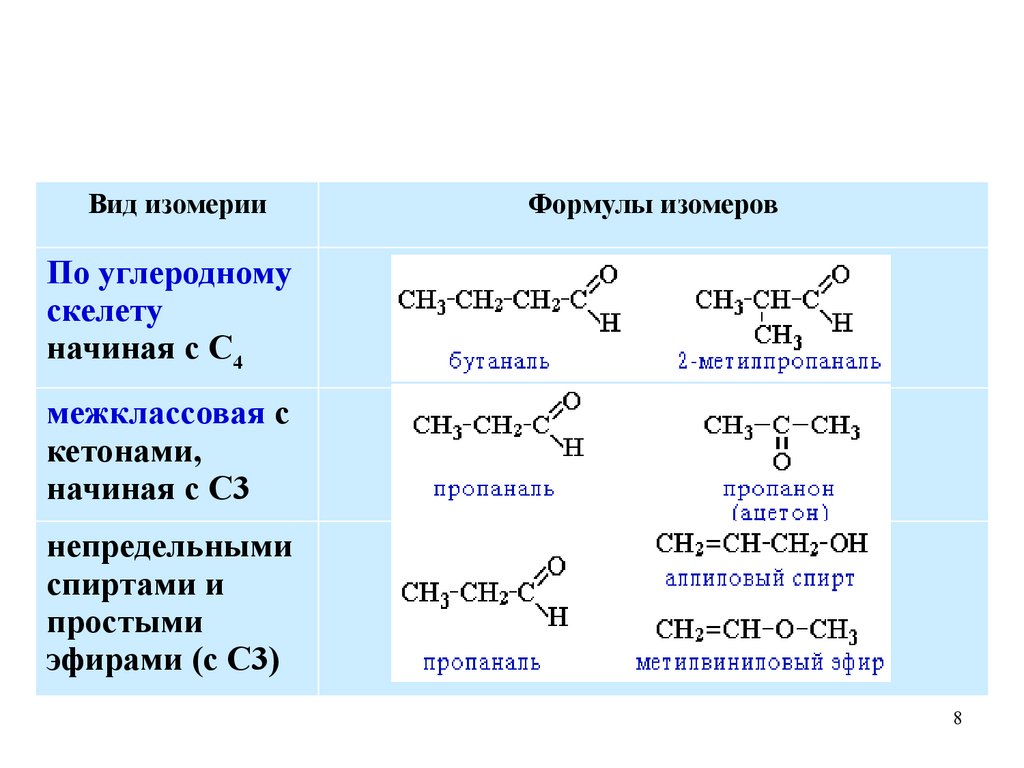
ИзомерияВид изомерии
Формулы изомеров
По углеродному
скелету
начиная с С4
межклассовая с
кетонами,
начиная с С3
непредельными
спиртами и
простыми
эфирами (с С3)
8
9.
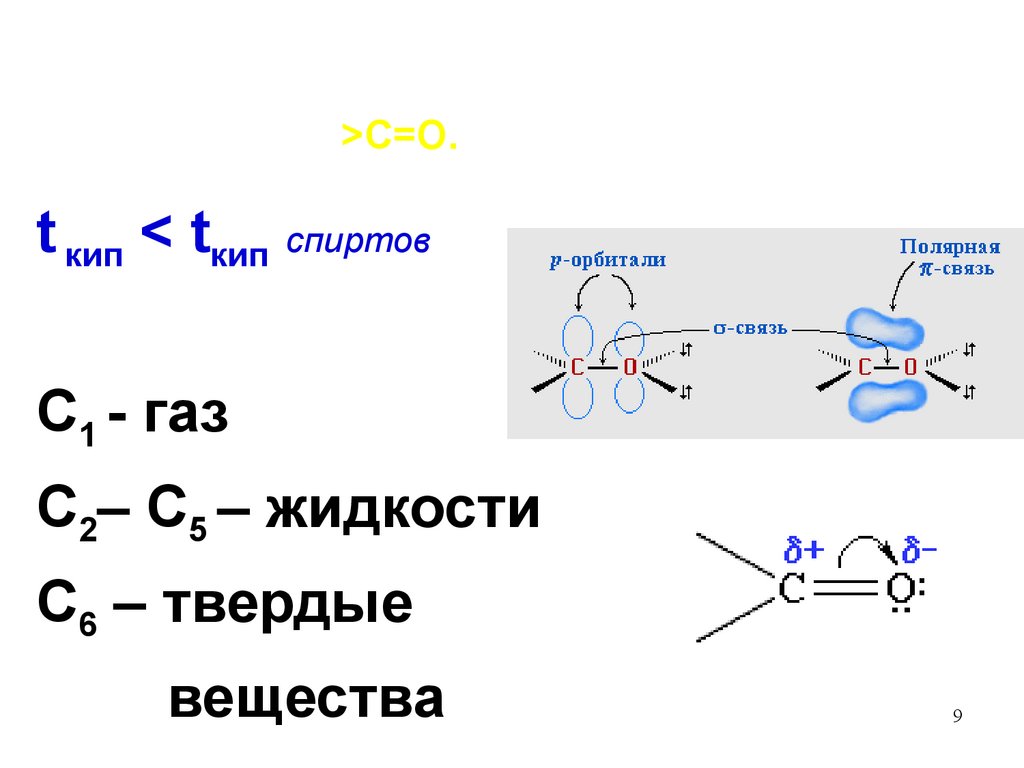
Физические свойства альдегидовопределяются строением карбонильной
группы >C=O.
t кип < tкип спиртов
С1 - газ
С2– С5 – жидкости
С6 – твердые
вещества
9
10.
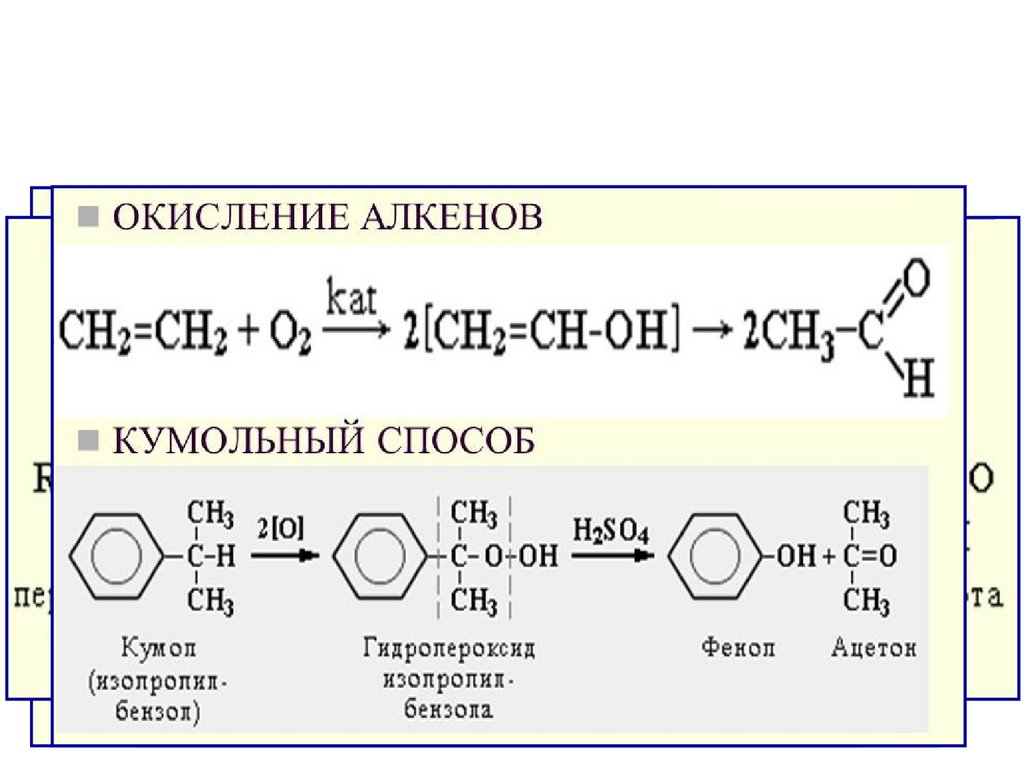
Получение10
11.
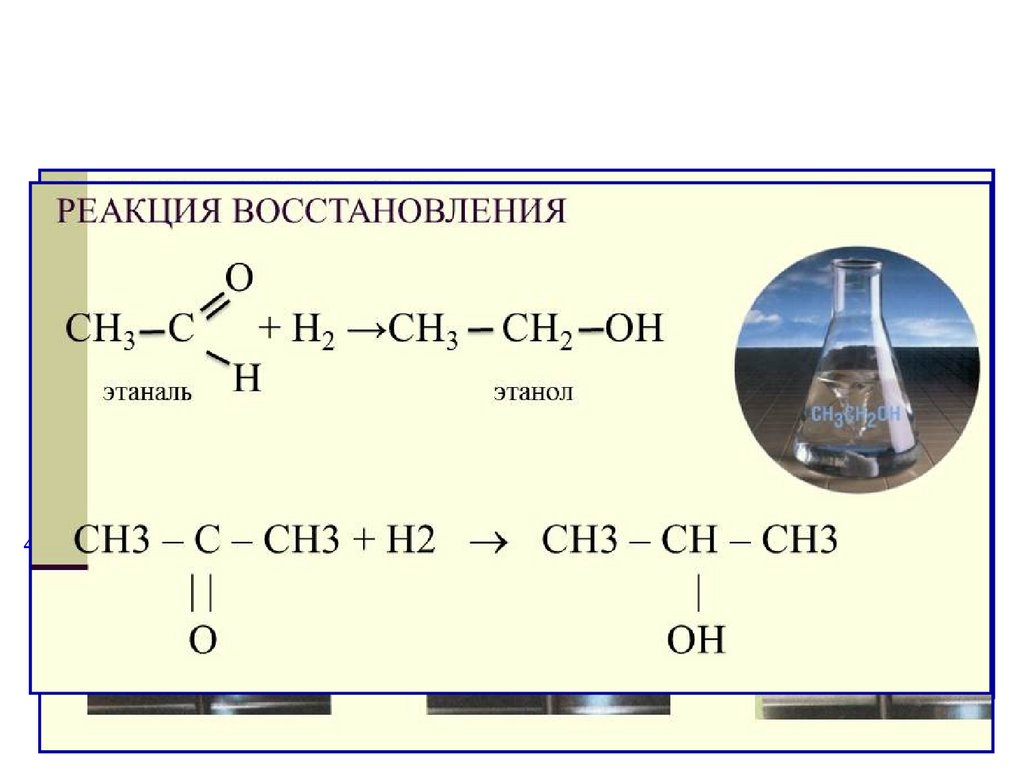
Химические реакциивосстановления
полимеризации
присоединения
окисления
11
12.
Основные химическиесвойства
4.
СH2O
+
реакция полимеризации
СH2
+ H2O
12
13.
Применение альдегидов14.
Применение альдегидов14
15.
Применение альдегидов15
16.
1617.
Карл Вильгельм Шееле17
18.
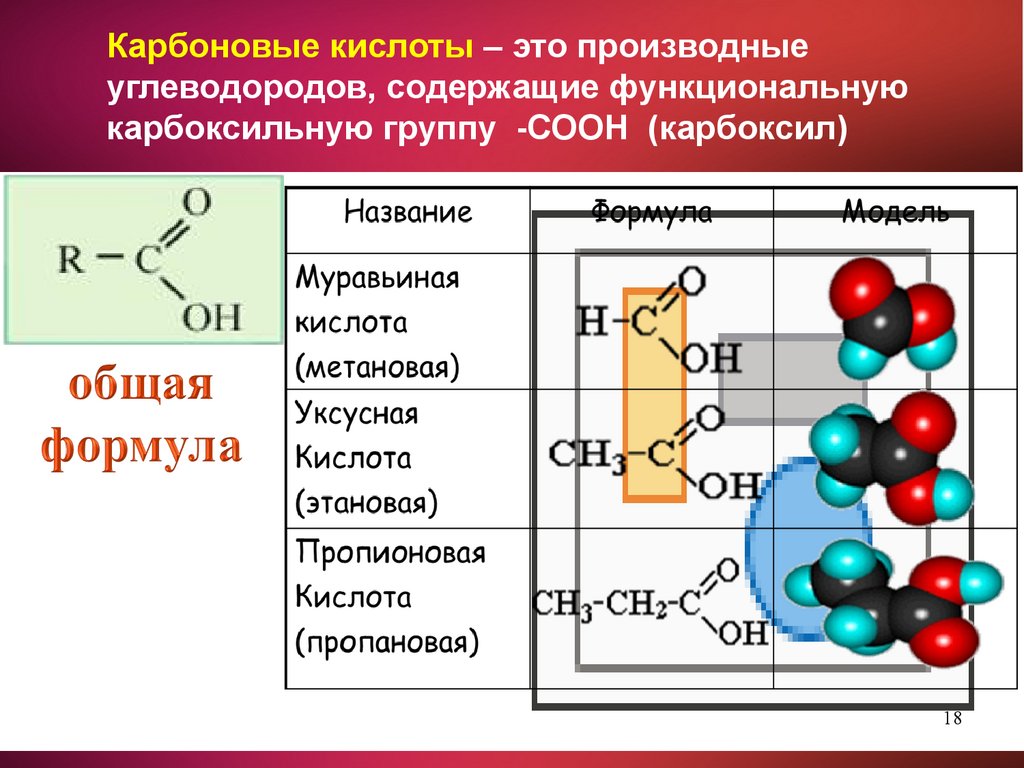
Карбоновые кислоты – это производныеуглеводородов, содержащие функциональную
карбоксильную группу -СООН (карбоксил)
18
19.
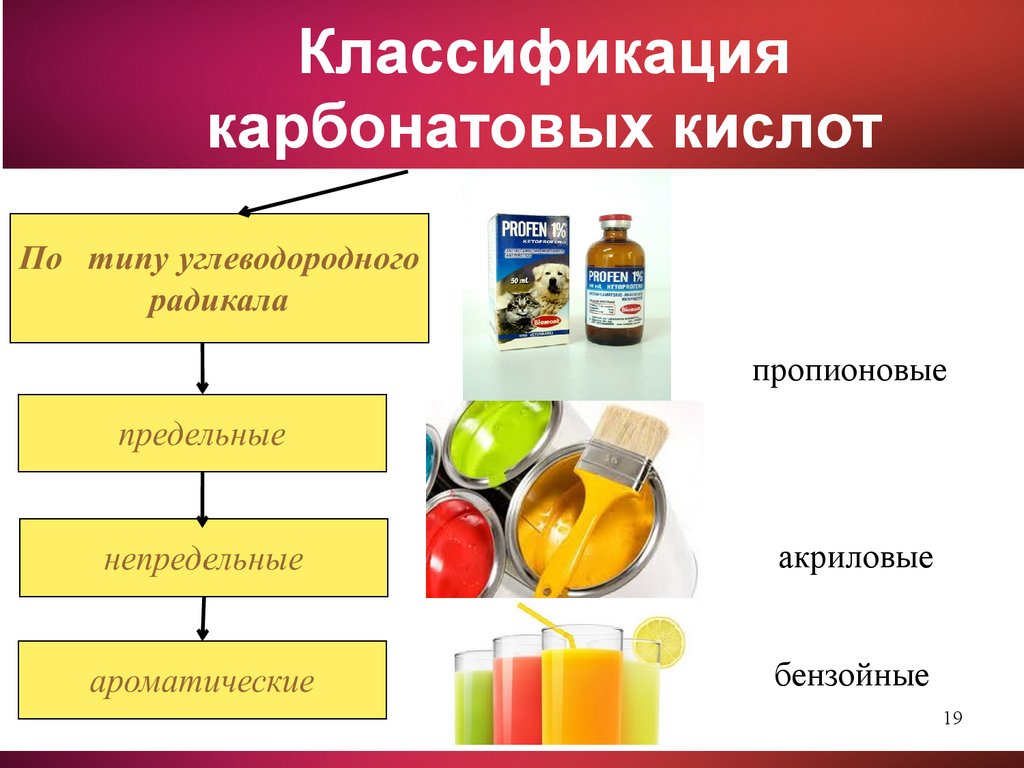
Классификациякарбонатовых кислот
пропионовые
акриловые
бензойные
19
20.
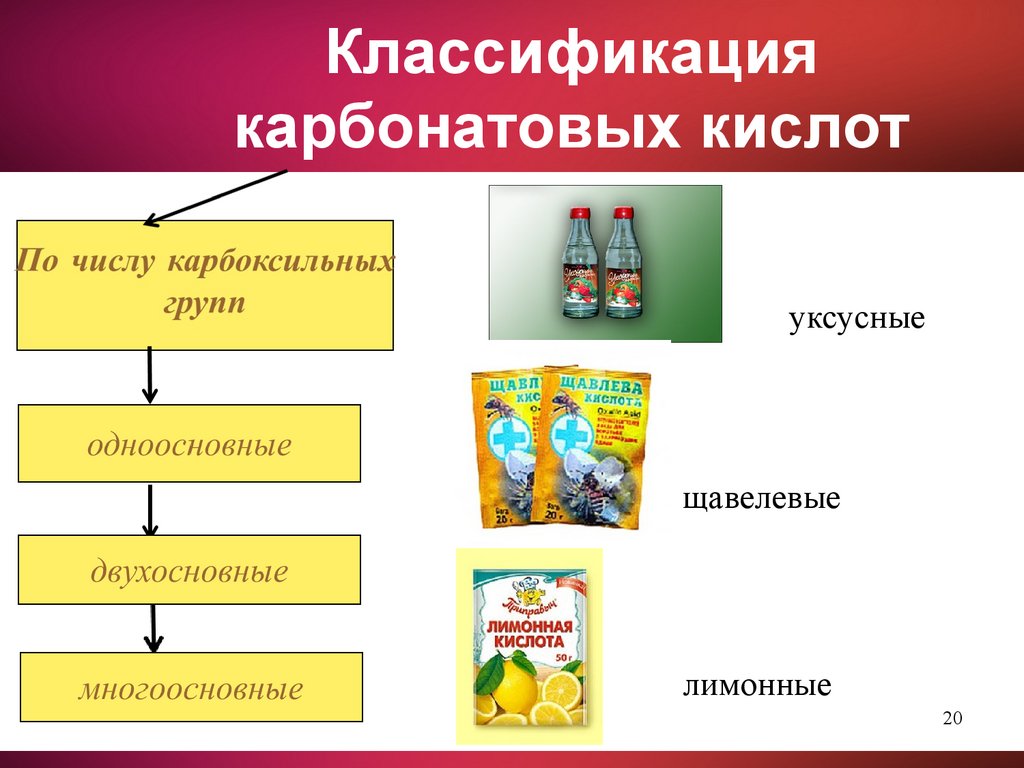
Классификациякарбонатовых кислот
уксусные
щавелевые
лимонные
20
21.
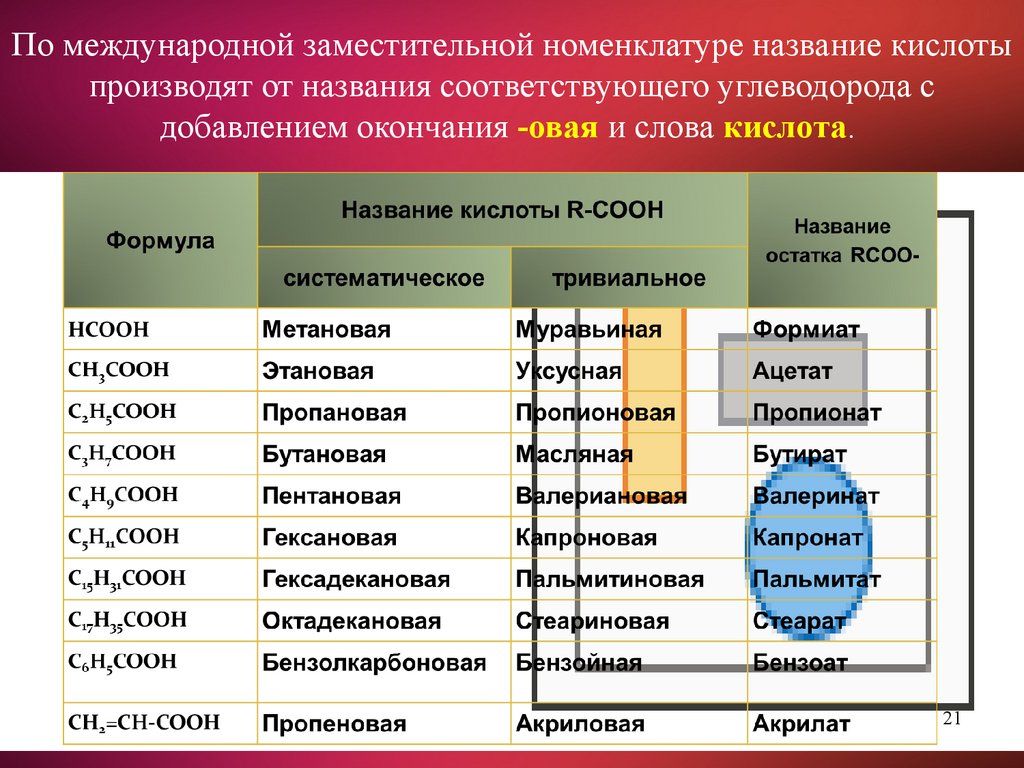
По международной заместительной номенклатуре название кислотыпроизводят от названия соответствующего углеводорода с
добавлением окончания -овая и слова кислота.
21
22.
Номенклатура и изомерияНумерацию цепи
всегда начинают с
атома углерода
карбоксильной
группы, поэтому в
названиях
положение группы СООН не указывают.
Например:
5
4
3
2
О
СН3-СН2-СН-СН2-С
СН3
1
Внутри класса
возможна только
изомерия
углеродной цепи.
Первые три
члена
гомологического
ряда изомеров не
имеют.
22
23.
Физические свойства23
24.
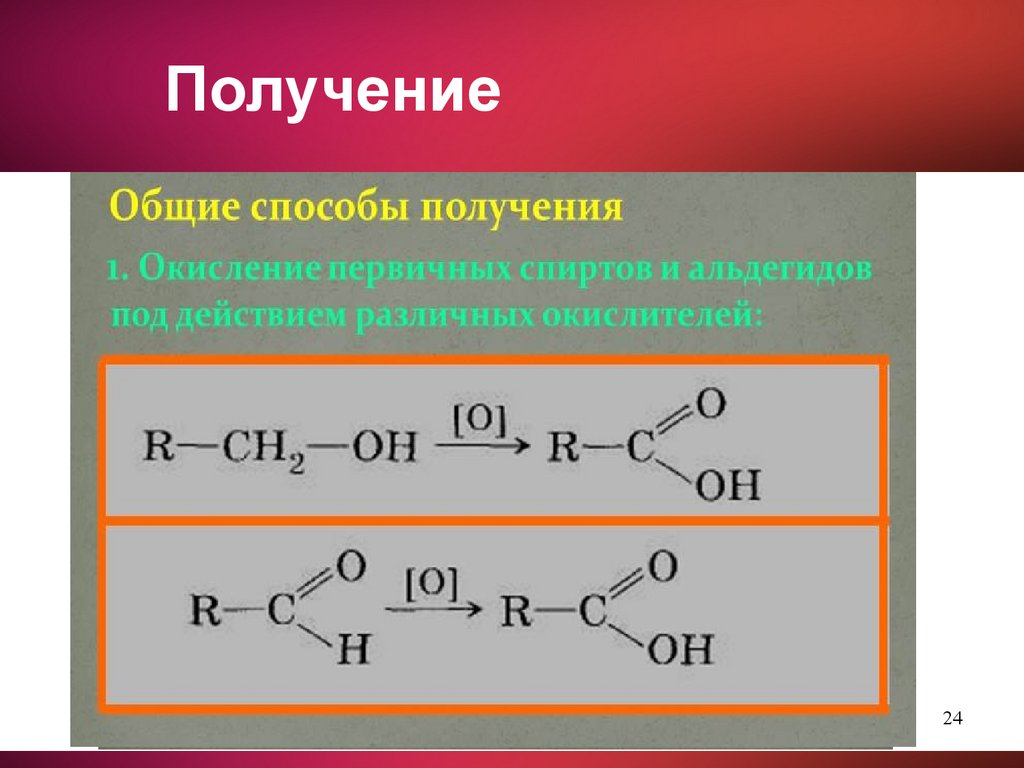
Получение24
25.
Химические свойства25
26.
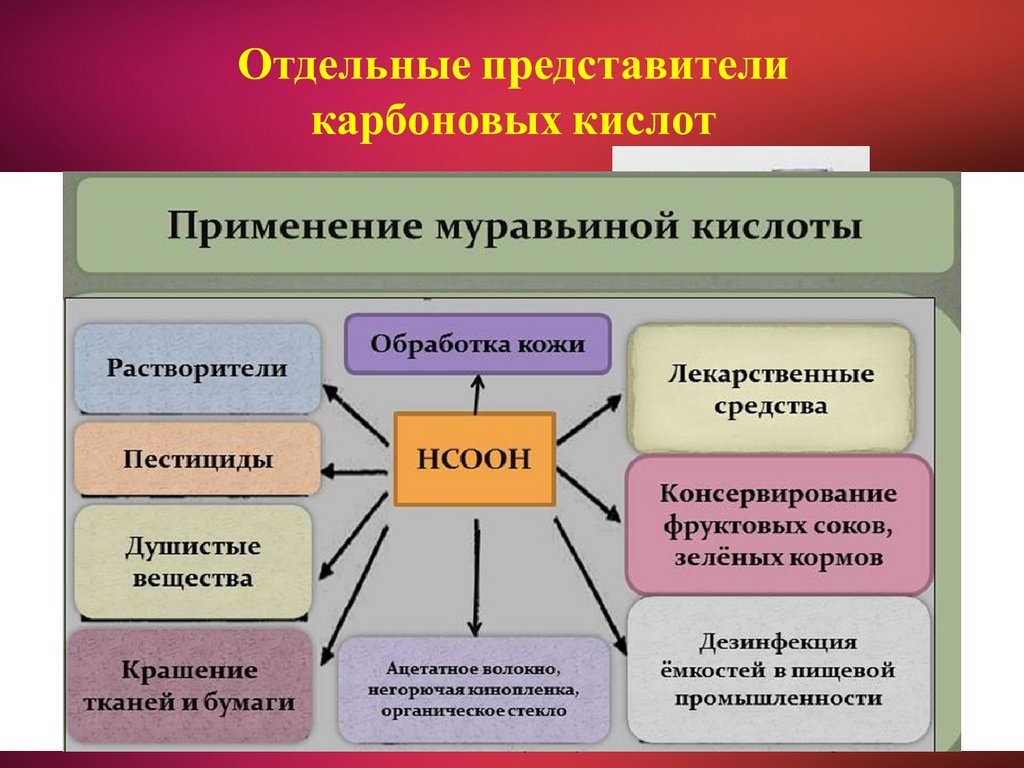
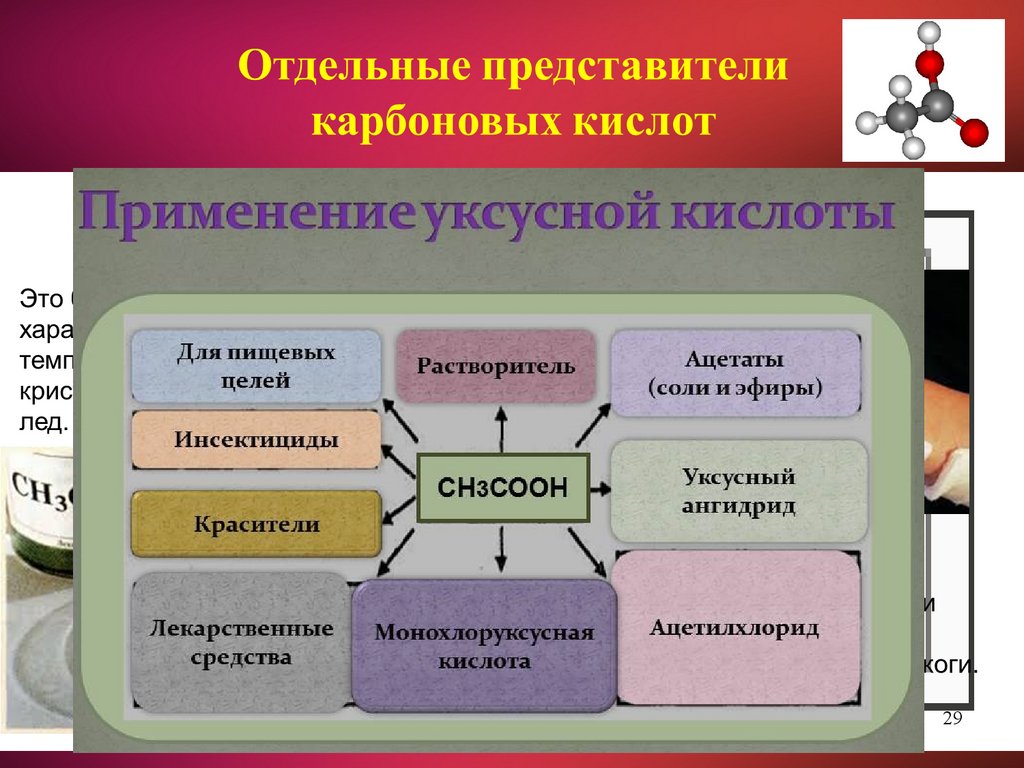
Применениекарбоновых кислот
Искусственные
волокна
26
27.
Карбоновые кислоты широкораспространены в природе
!
27
28.
2829.
2930.
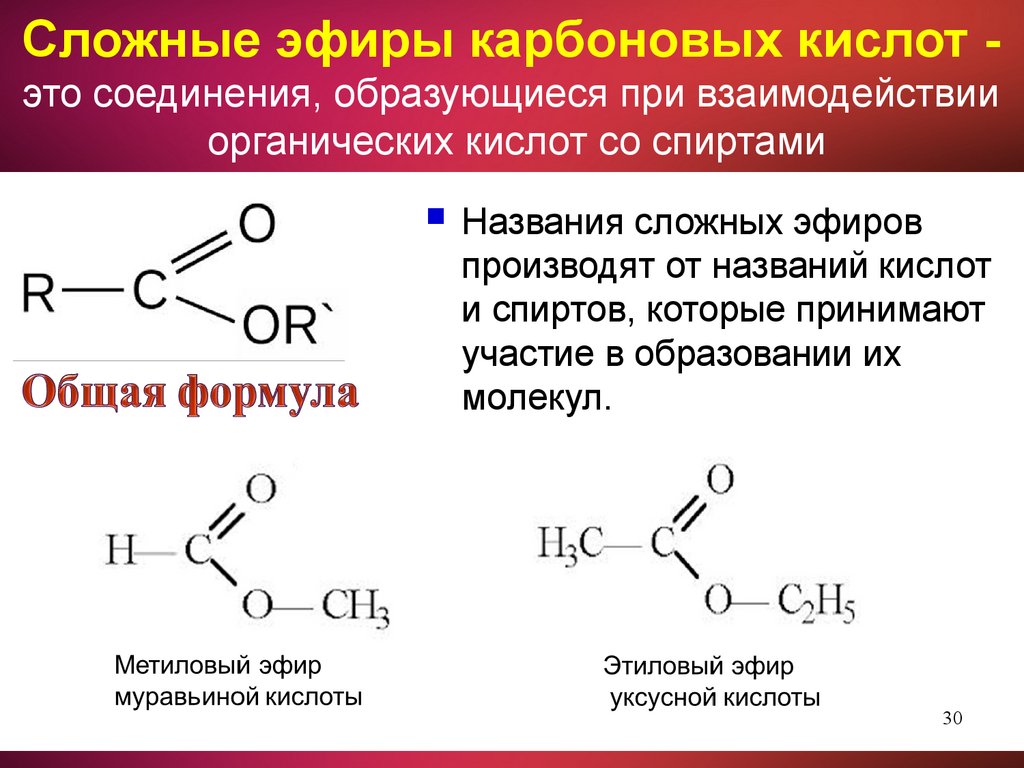
Сложные эфиры карбоновых кислот это соединения, образующиеся при взаимодействииорганических кислот со спиртами
Названия сложных эфиров
производят от названий кислот
и спиртов, которые принимают
участие в образовании их
молекул.
30
31.
Физические и химическисвойства
31
32.
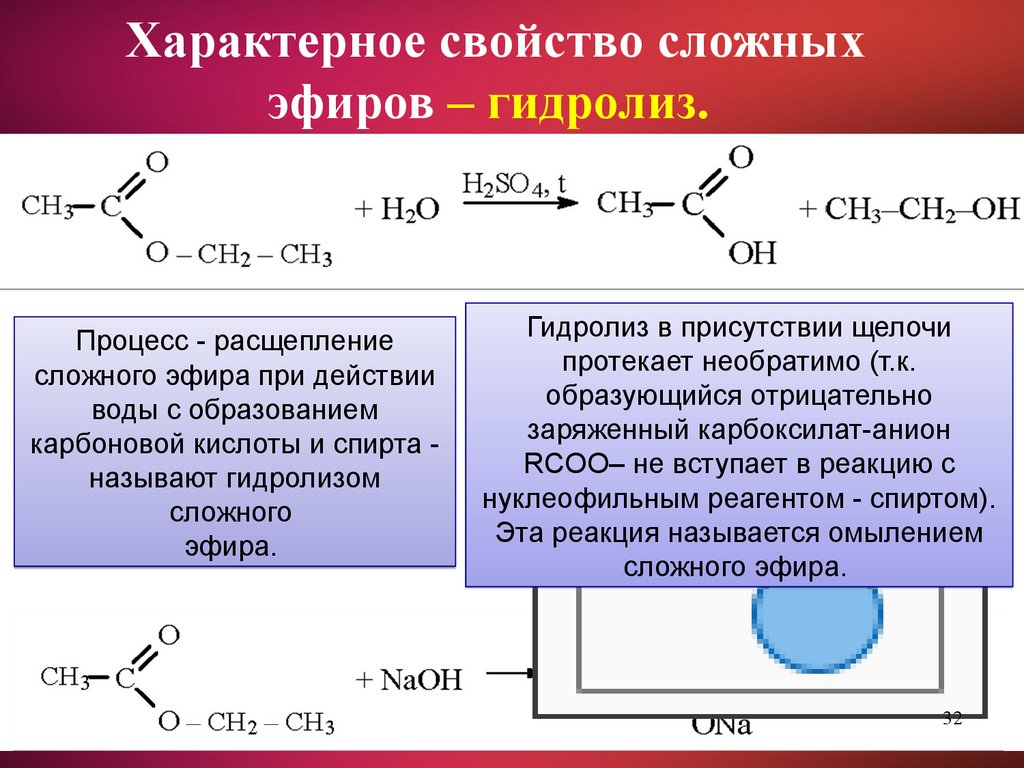
Характерное свойство сложныхэфиров – гидролиз.
Процесс - расщепление
сложного эфира при действии
воды с образованием
карбоновой кислоты и спирта называют гидролизом
сложного
эфира.
Гидролиз в присутствии щелочи
протекает необратимо (т.к.
образующийся отрицательно
заряженный карбоксилат-анион
RCOO– не вступает в реакцию с
нуклеофильным реагентом - спиртом).
Эта реакция называется омылением
сложного эфира.
32
33.
Нахождение в природе33
34.
Применение34
35.
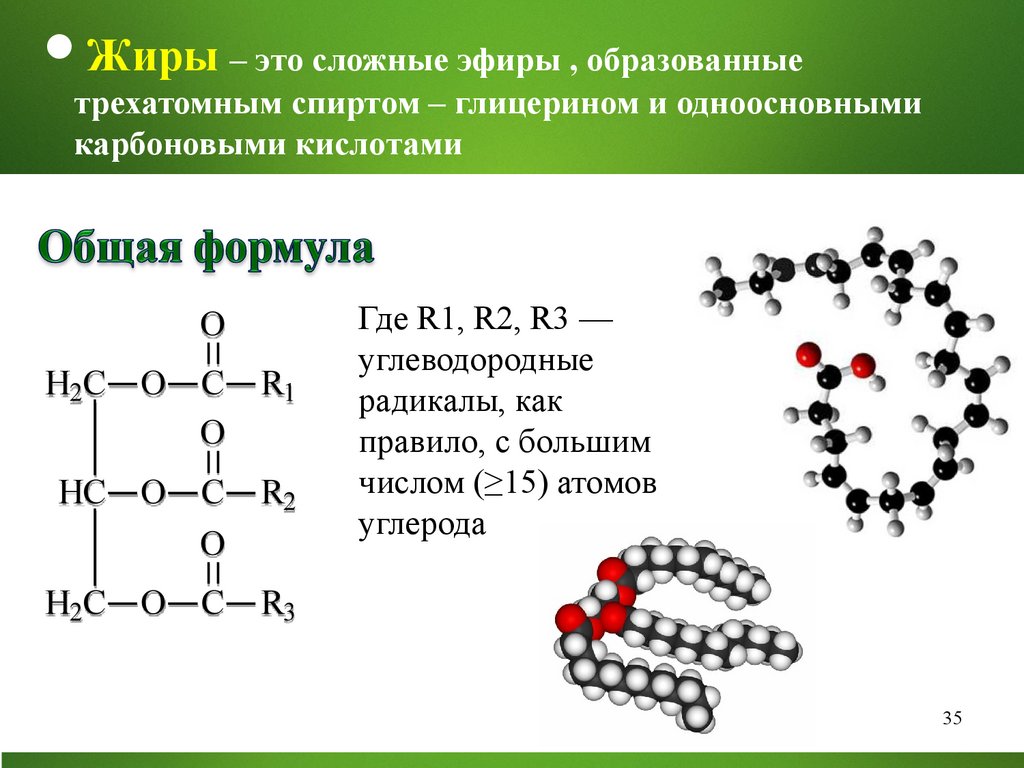
Жиры – это сложные эфиры , образованныетрехатомным спиртом – глицерином и одноосновными
карбоновыми кислотами
Где R1, R2, R3 —
углеводородные
радикалы, как
правило, с большим
числом (≥15) атомов
углерода
35
36.
История изучения жировК.Шееле в 1779 г. установил что в состав жиров входит глицерин.
М.Шеврель в 1823 году установил, что, жиры разлагаются на
глицерин и карбоновые кислоты
М.Бертло в 1854 году осуществил синтез жира как сложного эфира.
36
37.
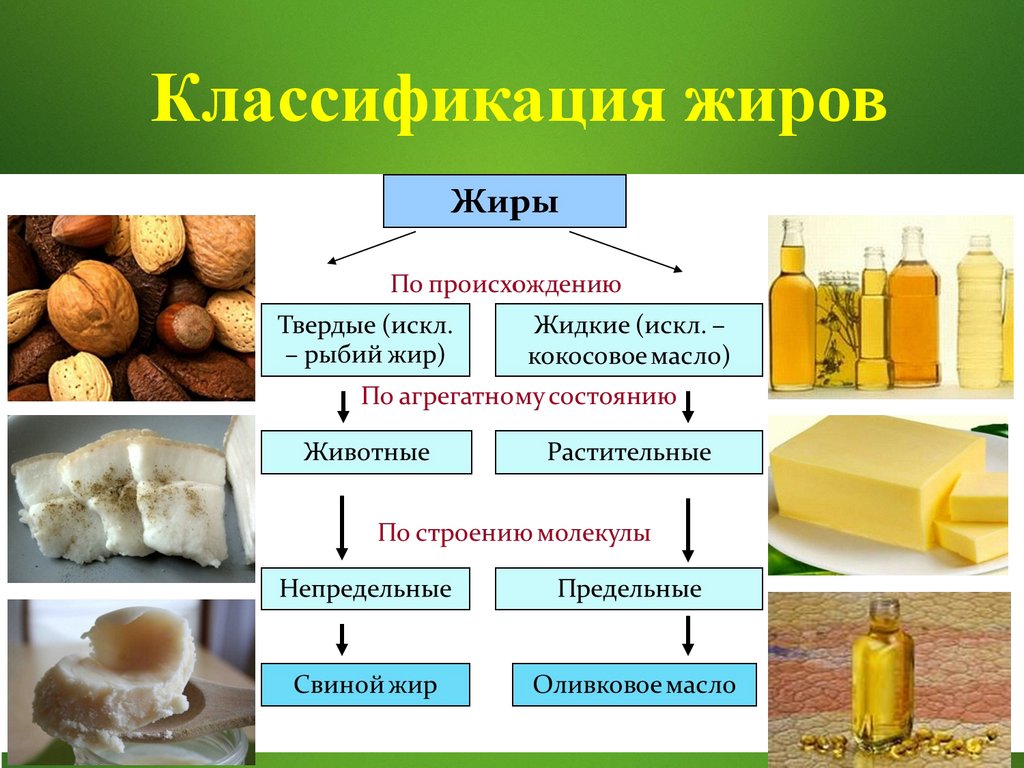
Классификация жиров37
38.
Физические свойства1.
2.
3.
1. Жиры не растворимы в воде
2. Жиры не растворимы в спирте
3. Жиры растворимы в бензине
4. Плотность их меньше плотности воды
5. Если при комнатной температуре они имеют
твердое агрегатное состояние, то их называют
жирами, а если жидкое, то – маслами.
6. У жиров низкие температуры кипения и
плавления
7. Высокая вязкость
8. Слабо проводят тепло и электричество
38
39.
Химические свойстваЭтот процесс используют в технике для получения глицерина, карбоновых
кислот и мыла. Для получения глицерина и карбоновых кислот жир нагревают
с водой (при 170˚С и при повышенном давлении) в автоклавах:
При длительном хранении в обычных условиях жиры, например, сливочное
масло, подвергаются частичному гидролизу. Образовавшаяся масляная
кислота придает сливочному маслу неприятный вкус и
запах. Этот процесс называют прогорканием.
39
40.
Щелочной гидролиз (омыление)При проведении гидролиза в щелочной среде (в растворе щелочи или
карбоната натрия) выделяются натриевые соли карбоновых кислот, которые
являются мылами. Поэтому щелочной гидролиз жиров называют омылением:
40
41.
4142.
Применение жиров42
43.
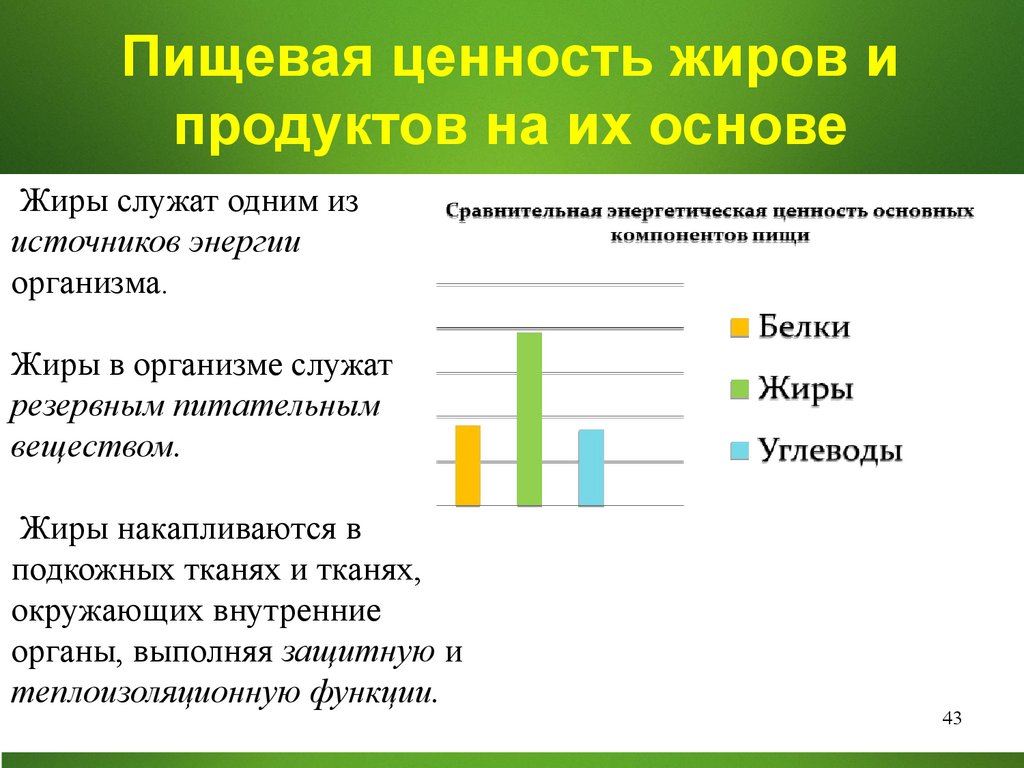
Пищевая ценность жиров ипродуктов на их основе
Жиры служат одним из
источников энергии
организма.
Жиры в организме служат
резервным питательным
веществом.
Жиры накапливаются в
подкожных тканях и тканях,
окружающих внутренние
органы, выполняя защитную и
теплоизоляционную функции.
43
44.
Маргарин – этотонкодисперсная
эмульсия, в состав
которой входят твердый
жир, растительное
масло, молоко,
ароматизаторы,
витамины, сахар, соль,
пищевые красители. Его
используют в
хлебопекарной,
кондитерской
промышленности, в сети
общественного питания.
Майонез – это также
тонкодисперсная
эмульсия растительного
масла с водой, яичным
порошком, сухим
молоком, сахаром,
уксусом и специями. Его
применяют в качестве
приправы к
разнообразным
кулинарным блюдам для
повышения их
питательности и
44
облагораживания вкуса.
45.
Мыла и синтетическиемоющие средства
Мыла – это натриевые или калиевые соли
высших предельных одноосновных
карбоновых кислот
Калиевые соли – это жидкие мыла,
натриевые соли – твердые мыла.
Калиевые мыла лучше растворимы в воде,
содержатся в шампунях и кремах для бритья.
Натриевые мыла ограниченно растворимы,
Используются для получения хозяйственного
и туалетного мыла.
При получении туалетного мыла добавляют
душистые и красящие вещества –
антисептики.
45
46.
Получение мылаВ настоящее время мыло получают
нейтрализацией синтетических кислот:
⃗ 15 H 31 COOK + H 2 O
С15 H 31 COOH+KOH ❑C
пальмитат калия
(жидкое мыло)
⃗ C H COONa + H O
С15 H 31 COOH+NaOH ❑
15
31
2
пальмитат натрия
(твердое мыло)
Кислоты, необходимые для
производства мыла, преимущественно
получают каталитическим окислением
парафинов нефти:
2С32 H 66 +5 O2⃗
кат . ,t 4 C15 H 31 COOH+2 H 2 O
пальмитиновая кислота
46
47.
Недостатки мыла47
48.
Синтетические моющиесредства
Одну из групп синтетических
моющих средств составляют соли
сложных эфиров высших спиртов и
серной кислоты. В отличие от
обычного мыла СМС не подвергаются
гидролизу, поэтому их растворы
нейтральны. Они сохраняют моющее
действие в жесткой и даже морской
воде, так как образующиеся при этом
кальциевые и магниевые соли
растворимы. СМС входят в состав
разнообразных стиральных порошков.
48
49.
Контрольные вопросы_________________
_____________
49
50.
Домашнее заданиеСоставьте структурные
Выучить
формулы следующих
тривиальные
карбоновых кислот:
названия низших
1. 3-этилоктановая кислота
карбоновых кислот.
2. метилпропановая кислота Напишите
уравнения реакций
3. 3,5,5 – триметилгесановая
следующих
кислота
превращений:
4. 2-метил-3-этилгептановая
Этан – хлорэтан –
кислота
5. 2,4-диметилпентановая
- этанол – этаналь –
кислота
-уксусная кислота50
51.
Источники► Учебник по химиии 11 класс Новошинский,
Новошинская.
► http://chemistry-chemists.com/N6_2011/U1/
ChemistryAndChemists_6_2011-U1-6.html
► http://ppt4web.ru/khimija/karbonovye-kisloty2.html
► http://www.chemistry.ssu.samara.ru/vrml/link19.htm
http://mscience.ru/edu_articles/ochemistry_articles/
171-klassifikaciya-i-nomenklatura-karbonovyhkislot.html(таблицы)
► www.alhimic.ucoz.ru/load/26-1-0-39
► www.alleng.ru/edu/chem1.htm
► www.uchportal.ru/load/60-1-0-9056
51
52.
Проект по химиипо разделу:
«Функциональные
производные
Подготовили ученики
углеводородов» на тему:
11 «А» кл. МБОУ СОШ№65:
«Альдегиды. Карбоновые
кислоты и их производные» Сенная Наталья
Альшанова Кристина
Ермакова Анна
Витязева Елизавета
52
Скибин Максим






























 Химия
Химия








