Похожие презентации:
Наркотические анальгетики. Ненаркотические анальгетики. Лечение мигрени. Лекция №11
1.
Лекция №11.Тема:
Наркотические анальгетики.
Ненаркотические анальгетики.
Лечение мигрени.
Ст. преп. каф. фундаментальной
медицины БФУ им. И.Канта, к.м.н.
Пятых Е.А.
2.
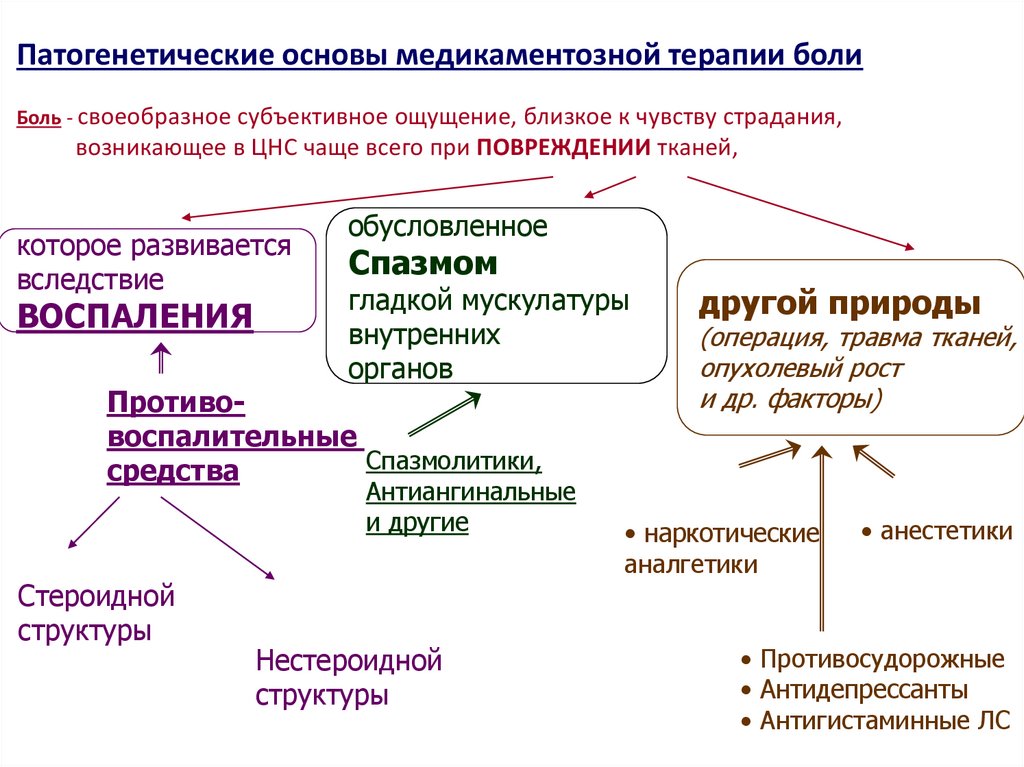
Патогенетические основы медикаментозной терапии болиБоль - своеобразное субъективное ощущение, близкое к чувству страдания,
возникающее в ЦНС чаще всего при ПОВРЕЖДЕНИИ тканей,
которое развивается
вследствие
ВОСПАЛЕНИЯ
обусловленное
Спазмом
гладкой мускулатуры
внутренних
органов
Противовоспалительные
Спазмолитики,
средства
Антиангинальные
и другие
Стероидной
структуры
Нестероидной
структуры
другой природы
(операция, травма тканей,
опухолевый рост
и др. факторы)
• наркотические
аналгетики
• анестетики
• Противосудорожные
• Антидепрессанты
• Антигистаминные ЛС
3.
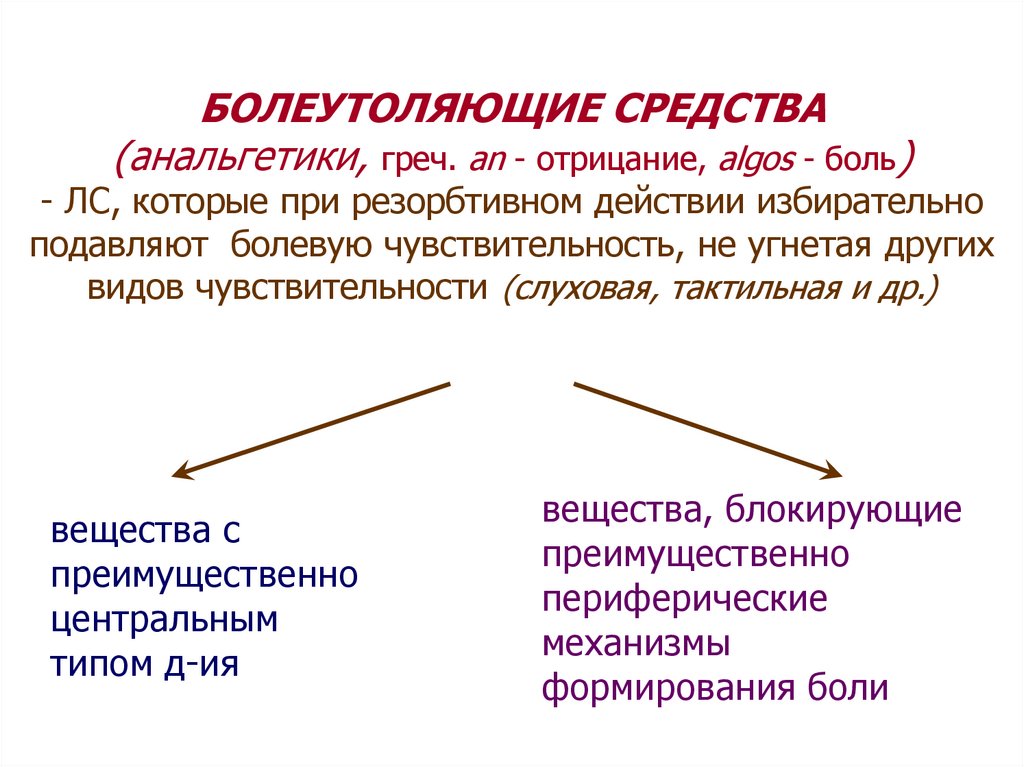
БОЛЕУТОЛЯЮЩИЕ СРЕДСТВА(анальгетики, греч. аn - отрицание, algos - боль)
- ЛС, которые при резорбтивном действии избирательно
подавляют болевую чувствительность, не угнетая других
видов чувствительности (слуховая, тактильная и др.)
вещества с
преимущественно
центральным
типом д-ия
вещества, блокирующие
преимущественно
периферические
механизмы
формирования боли
4.
Аспирин был создан в лабораториях немецкой компании Bayer, ранее производившей лишь
анилиновые красители. Новая лаборатория состояла из двух отделов – фармацевтического, где
шла разработка лекарств, и фармакологического, где их испытывали на животных.
Фармацевтический отдел возглавил Артур Эйхенгрюн, а фармакологический – профессор Генрих
Дрезер. По распоряжению Эйхенгрюна Феликс Хоффман 10 августа 1897 г. получил образцы
ацетилсалициловой кислоты в форме, возможной для медицинского применения (запись в
лабор. журнале: длительное нагревание смеси, состоящей из двух частей салициловой к-ты и
трех частей уксусного ангидрида, дает возможность получить очень чистую ацетилсалициловую
к-ту). Bayer зарегистрировала новое ЛС под торговой маркой «Аспирин» (патент США от 6 марта
1899 г.).
В этом же году Хоффман проводит эксперименты по ацетилированию
морфина, получая лекарственный героин.
«А» – ацетилирование
«спир» - от Shiraea (лат) – название Таволги,
растения из которого впервые была
выделена салициловая кислота
5.
Наркотические анальгетики растительного исинтетического происхождения избирательно
подавляют восприятие боли и повышают ее
переносимость, уменьшают эмоциональную
окраску и вегетативное сопровождение боли,
вызывают лекарственную зависимость.
Слово «анальгезия» — утрата болевой
чувствительности — происходит от греческих
слов an — отрицание и algos — боль.
6.
ХАРАКТЕРНЫЕ ЧЕРТЫ НАРКОТИЧЕСКИХАНАЛЬГЕТИКОВ
1. Сильная
анальгетическая
активность,
позволяющая купировать практически любую боль.
2. Особое влияние на ЦНС:
- наркотические анальгетики способны вызывать
эйфорию, при повторных применениях привыкание
и зависимость (как психическую, так и физическую).
Зависимость формируется очень быстро, особенно к
алкалоидам опия (наиболее быстро у женщин и у
детей – 3-4 раза)
6
7.
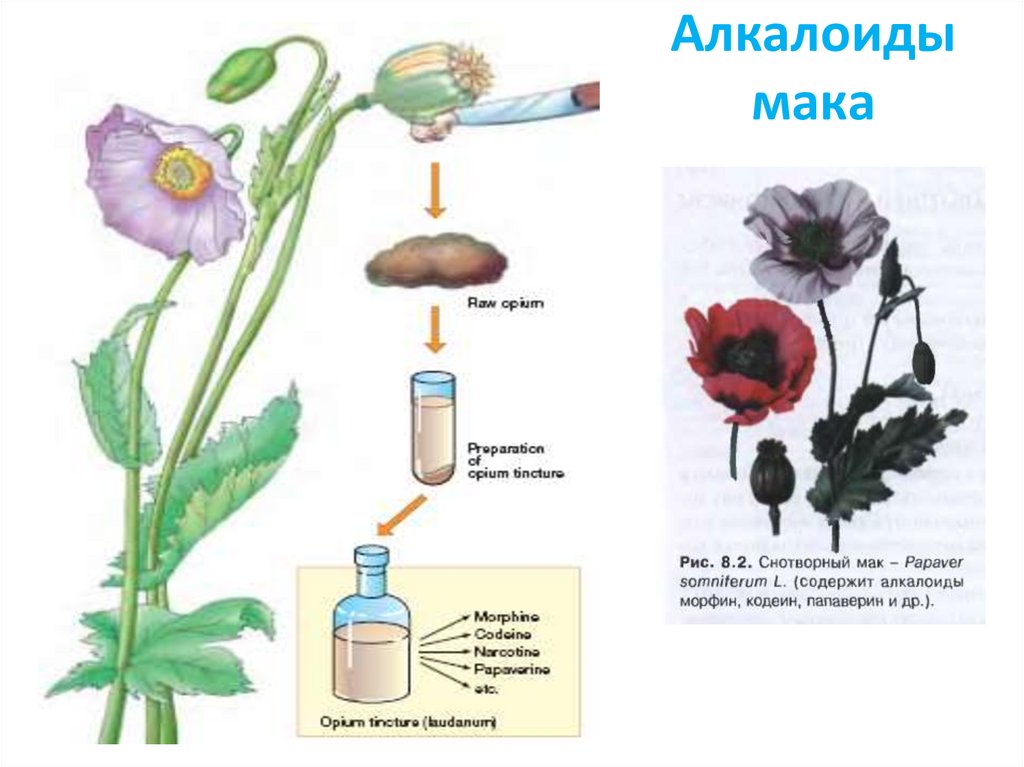
• Природным источником наркотическиханальгетиков является опий (греч. opos — сок) —
высохший млечный сок снотворного мака (Papaver
somniferum). Родина этого растения — Малая
Азия. Впервые опий упоминается в клинописных
табличках Шумера (IV тысячелетие до н. э.).
• Действие опия на человека описал греческий врач
Теофраст (372 — 287 до н.э.). В Средние века
популярность опия как обезболивающего средства
возродили Парацельс (1493 — 1541) и Томас
Сиденхем (1624 — 1689).
8.
Алкалоиды опия представляют собойпроизводные фенантрена и изохинолина.
- Структуру фенантрена имеют морфин (10%),
кодеин (0,5 %) и тебаин (0,2 %). Из них
анальгетиками являются морфин и кодеин
(греч. kodeia — маковая головка).
- Производные изохинолина папаперин (1
%), носкапин (6 %), лауданозин проявляют
свойства миотропных спазмолитиков.
9.
Морфин был выделен из опия ганноверскимфармацевтом Вильгельмом Сертюрнером в 1806 г.
Название алкалоида дано по имени Морфея —
древнегреческого крылатого бога сна, сына
Гипноса (греч. morphe — форма, так как бог
являлся в сновидениях в образах
людей, животных и
природных стихий).
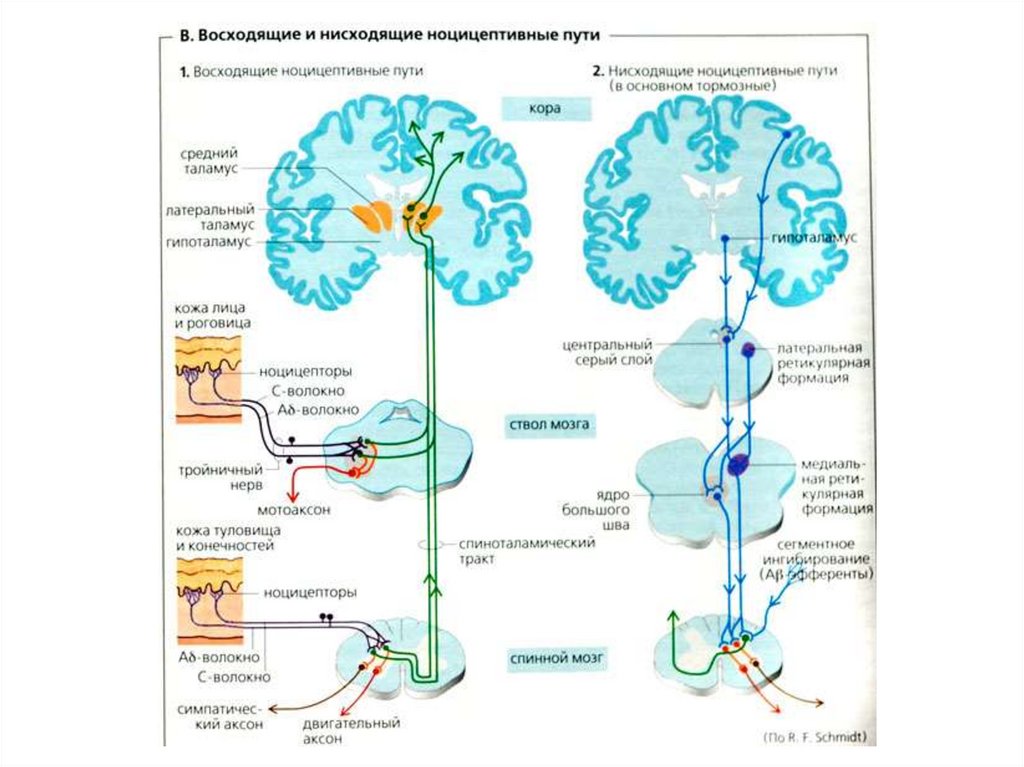
10.
Ноцицептивная система (греч. посео — повреждаю)воспринимает, проводит болевые импульсы и
формирует реакции на боль.
В восприятии повреждающих (ноцицептивных)
стимулов участвуют свободные
неинкапсулированные н. окончания — ноцицепторы.
Механо- и терморецепторы возбуждаются при
сильных механических и термических раздражениях.
Активацию хеморецепторов вызывают повторное
тепловое воздействие, электрический ток, химические
вещества — алгогены (брадикинин, гистамин,
серотонин, ацетилхолин, аденозин, простагландины
группы Е, лейкотриены, цитокины, ионы К + и Н + ).
11.
Механо- и терморецепторы передают болевыесигналы по миелинизированным волокнам А δ,
полимодальные хеморецепторы — по
немиелинизированным волокнам С.
С активацией миелинизированных афферентов
связывают ощущение дискриминационной боли.
Возбуждение немиелинизированных волокон
сопровождается плохо локализованным, неприятным
диффузным жгучим ощущением.
12.
Специфический (неоспиноталамическии) путь высокопороговые специфические ноцицепторы(преимущ. механо- и терморецепторы),
быстропроводящие афферентные волокна А δ ,
специфические ноцицептивные нейроны (задние рога
СМ, вентробазальные ядра таламуса, соматосенсорная
кора).
Путь является малонейронным, быстрым, проводит
пороговую эпикритическую боль.
13.
Неспецифический (палеоспиноталамический) путь —низкопороговые полимодальные ноцицепторы
(преимущ. хеморецепторы), медленнопроводящие
немиелинизированные С-афференты, неспецифические
ноцицептивные нейроны (задние рога СМ,
интраламинарные ядра таламуса, кора лобной доли).
Этот путь образует многочисленные коллатерали к
ретикулярной формации продолговатого и среднего
мозга, лимбич. системе, гипоталамусу. Проводит
протопатическую боль. Пространственная и временная
суммация слабых раздражений происходит в ядрах
таламуса.
14.
15.
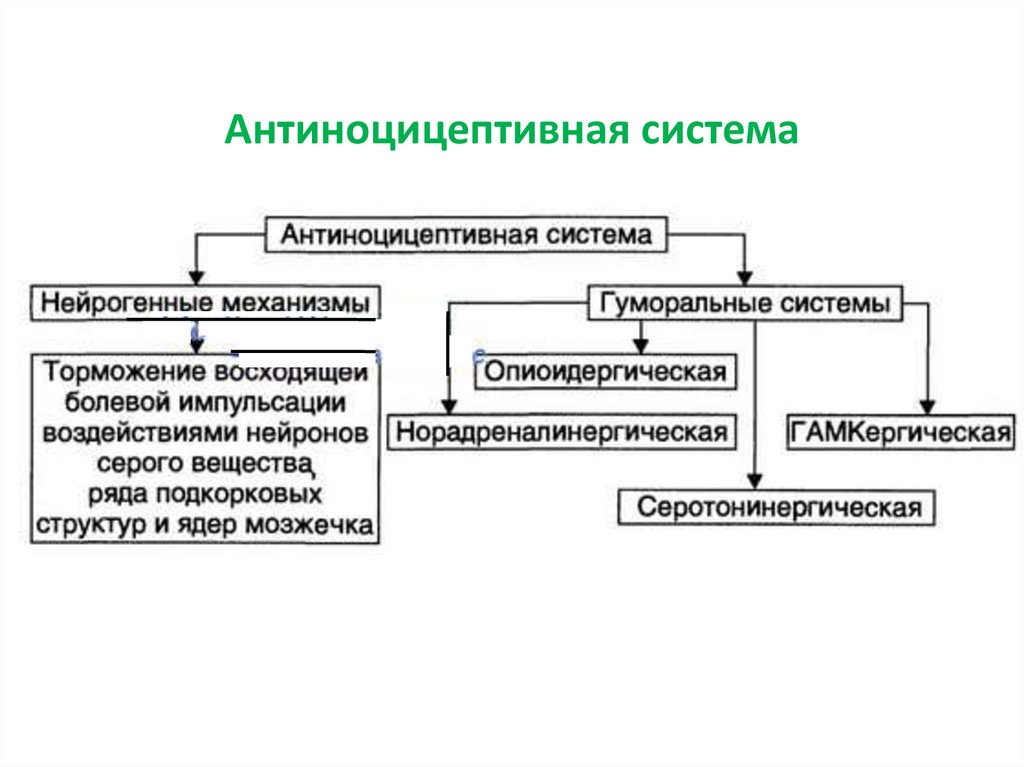
Антиноцицептивная система (АЦС) нарушаетвосприятие боли, проведение болевых импульсов
и формирование реакций на боль. Болевые
импульсы возбуждают нейроны АЦС, что ведет по
принципу отрицательной обратной связи к
угнетению передачи болевых сигналов.
Ноцицептивная и АЦС регулируют болевую
чувствительность в процессе постоянного
взаимодействия. Выделение нейромедиаторов
боли тормозят рецепторы опиоидов,
каннабиоидов, глицина, ГАМК (А и В типов).
16.
Опиоидная АЦС представлена нейронами центральногосерого вещества ГМ. Аксоны этих нейронов образуют пути к
коре больших полушарий, лимбической системе, полосатому
телу, таламусу, гипоталамусу, ретикулярной формации,
продолговатому и СМ.
Медиаторами опиоидной АЦС являются пептиды:
· лей-энкефалин (тирозин-глицин-глицин-фенилаланин-лейцин);
· мет-энкефалин (тирозин-глицин-глицин-фенилаланин-метионин);
· динорфин А (17 аминокислот, включая пентапептид лей-энкефалина);
· динорфин В (13 аминокислот, включая пентапептид лей-энкефалина);
· β-эндорфин (31 аминокислота, включая пентапептид мет-энкефалина).
17.
Антиноцицептивная система18.
Опиоидные пептиды и наркотические анальгетикивзаимодействуют с метаботропными опиоидными рецепторами
трех типов — µ, κ и δ:
· µ-опиоидные рецепторы вызывают супраспинальную (µ 1 ) и
спинальную (µ 2 ) анальгезию, седативный эффект, эйфорию,
лекарственную зависимость, гипотермию, регулируют процессы
обучения и памяти, аппетит, суживают зрачки, угнетают ДЦ (µ 2 ),
увеличивают тонус гл. м. (µ 2 );
· к-опиоидные рецепторы вызывают супраспинальную (к 3 ) и
спинальную (к 1 ) анальгезию, седативный, психотомиметический
эффекты, спазм гл. м., регулируют питьевую и пищевую мотивации,
угнетают дыхание, повышают диурез (к,);
· δ-опиоидные рецепторы вызывают супраспинальную (δ 1 , δ 2 ) и
спинальную (δ 2 ) анальгезию, гипотермию, регулируют
познавательную деятельность, настроение, двигательную
активность, обоняние, моторику ЖКТ, функции ССС, угнетают
дыхание, оказывают центральное гипотензивное действие.
19.
Опиоидные рецепторы имеют 65 % одинаковыхаминокислот. Они посредством G-белков ингибируют
аденилатциклазу и тормозят синтез цАМФ, а также вызывают
гиперполяризацию мембран, открывая калиевые каналы (µ,
δ) и блокируя кальциевые каналы (к).
В синапсах, передающих болевые импульсы, опиоидные R
локализованы на пре- и постсинаптической мембранах.
Воздействие на опиоидные R пресинаптической мембраны
С-волокон уменьшает выделение медиаторов
ноцицептивных сигналов.
Постсинаптические R, вызывая гиперполяризацию нейронов,
блокируют проведение импульсов в ноцицептивной системе.
20.
КЛАССИФИКАЦИЯ НАРКОТИЧЕСКИХ АНАЛЬГЕТИКОВI. Агонисты опиатных рецепторов:
А. Препараты, получаемые из опия: морфина г/х, омнопон, кодеин.
В. Синтетические средства:
а) производные пиперидина: промедол, фентанил, пиритрамид;
б) производные фенантрена: трамадола гидрохлорид
II. Агонисты-антагонисты и частичные агонисты
опиатных рецепторов:
пентазоцин (фортрал), буторфанол (морадол), бупренорфин (бупренекс), налбуфин (нубаи
III Антагонисты опиатных рецепторов:
налоксон (наркан), налтрексон.
21.
КЛАССИФИКАЦИЯ ПО ХИМИЧЕСКОМУ СТРОЕНИЮПРЕПАРАТЫ АЛКАЛОИДОВ ОПИЯ ФЕНАНТРЕНОВОГО РЯДА
• Морфин Кодеин
Омнопон Морфилонг
ПОЛУСИНТЕТИЧЕСКИЕ ПРЕПАРАТЫ
• Этилморфин Бупренорфин
Налбуфин
СИНТЕТИЧЕСКИЕ НАРКОТИЧЕСКИЕ АНАЛЬГЕТИКИ
• Производные фенилпиперидина.
Промедол Фентанил Суфентанил
Алфентанил
Производные морфинана
• Буторфанол
• Производные бензморфана
• Пентазоцин
Производные разных химических групп
• Тилидин Трамал Просидол
22.
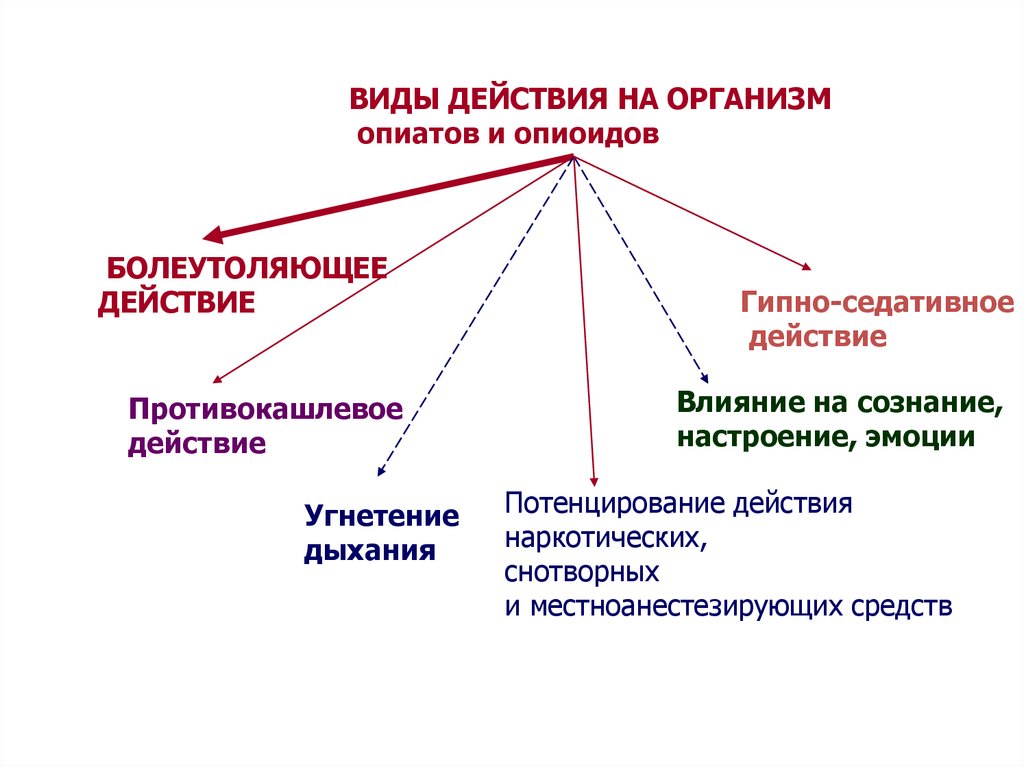
ВИДЫ ДЕЙСТВИЯ НА ОРГАНИЗМопиатов и опиоидов
БОЛЕУТОЛЯЮЩЕЕ
ДЕЙСТВИЕ
Противокашлевое
действие
Угнетение
дыхания
Гипно-седативное
действие
Влияние на сознание,
настроение, эмоции
Потенцирование действия
наркотических,
снотворных
и местноанестезирующих средств
23.
МЕХАНИЗМ ДЕЙСТВИЯАНАЛЬГЕТИЧЕСКОЕ ДЕЙСТВИЕ
Клеточный уровень: ↑поляризация мембраны восприн-й клетки за счёт активации
К+каналов и ↑выхода калия, ↓поступления Са+2 в клетку и↓ аденилатциклазы.
Взаимодействие опиоидных анальгетиков (и эндогенных опиоидных пептидов) с
пресинаптическими опиатными R→ к торможению высвобождения «болевых»
медиаторов из пресинаптических окончаний (>значение имеет вещество Р).
Активация постсинаптических опиатных R→ к ↓возбудимости нервных клеток,
восприн-х болевые импульсы. Феномен «растормаживания» подкорковых
противоболевых систем и ↑ нисходящих тормозных влияний к нейронам СМ
(участвующим в передаче боли).
На системном уровне малое ↑болевого порога и <эффективность препаратов при
надпороговых раздражениях, (при разрезе кожи) - требуются большие дозы. Глубокое
угнетение процесса суммации подпороговых болевых раздражений на всех уровнях
проведения боли, физиологическая основа опиоидной аналгезии.
Преимущественная эфф-ть при хр. Болях из внутренних органов с относительно
редкими болевыми интероR, где процесс Σ раздражений особенно важен для их
проведения. Наличие противотревожного и эйфоризирующего д-я, которое
подавляет ожидание боли, сглаживает восприятие и оценку болевых ощущений.
24.
ПО ХАРАКТЕРУ ДЕЙСТВИЯ НА ОПИАТНЫЕ РЕЦЕПТОРЫАГОНИСТЫ опиатных R (полные)
•Активируют все типы R (на мю1- , дельта- и каппа- R (производные
фенантрена, изохинолина-папаверин)
Морфин, кодеин, Омнопон, Синтетические: Дигидрокодеин, Фентанил,
Алфентанил, Ремифентанил, Cуфентанил, Тримеперидин (промедол)
Пиритрамид
ЧАСТИЧНЫЕ АГОНИСТЫ
•Активируют преимущ. мю-R (мю-1 >, чем мю-2).
•Бупренорфин (бупренекс)
АГОНИСТЫ-АНТАГОНИСТЫ
•Активируют каппа- и сигма- R и блокирующие мю- и дельта-R.
Пентозацин (фортрал), буторфанол (морадол,стадол), Нальбуфин налорфин
(преимущ-но антагонист мю-R, не используется в качестве анальгетика).
АНТАГОНИСТЫ опиатных R (конкурентные) вытесняют из связи с R
наркотические анальгетики. Блокируют все типы опиатных R. Налоксон,
налтрексон. Не используют в качестве анальгетиков, применяют в качестве
антагонистов при остром отравлении наркотическими анальгетиками
25.
ВЛИЯНИЕ НА ЦНСКора больших полушарий
• Морфин как агонист µ-опиоидных рецепторов
вызывает эйфорию и седативный эффект,
переходящий в чуткий, поверхностный, богатый
сновидениями сон.
• Агонисты к-опиоидных R (пентазоцин, налорфин),
подавляя освобождение дофамина,
вызывают дисфорию в виде беспокойства,
депрессии, неприятных, странных мыслей,
дезориентации, ночных кошмаров, галлюцинаций.
Буторфанол и налбуфин вызывают дисфорию реже
и в мягкой форме.
26.
Гипоталамус и железы внутренней секреции• Морфин уменьшает освобождение в гипоталамусе
рилизинг-гормонов для гонадотропинов и АКТГ,
поэтому вторично подавляет секрецию
фолликулостимулирующего, лютеинизирующего
гормонов, АКТГ, глюкокортикоидов и тестостерона.
Повышает выделение пролактина, гормона роста и
вазопрессина. В больших дозах, активируя центр
теплоотдачи, вызывает гипотермию.
Средний мозг
• Морфин, активируя µ- и к-опиоидные R в ядрах
глазодвигательного нерва, вызывает миоз и легкий
спазм аккомодации.
27.
Продолговатый мозг. Дыхательный центр• Морфин ослабляет реакцию ДЦ на возбуждающие стимулы со
стороны ретикулярной формации, снижает его чувствительность к
углекислому газу и ацидозу, при этом сохраняется активирующее
влияние каротидных клубочков.
• Фентанил угнетает ДЦ и вызывает ригидность дыхат. мускулатуры —
синдром «деревянной грудной клетки».
• Трамадол и анальгетики с комбинированным действием нарушают
дыхание слабее морфина.
• Бупренорфин уменьшает вызываемое фентанилом угнетение ДЦ без
ослабления анальгетического эффекта.
• Морфин тормозит функцию экспираторных нейронов, участвующих в
кашлевом рефлексе.
Центр блуждающего нерва
• Морфин, возбуждая дорзальное ядро блуждающего нерва, вызывает
брадикардию и бронхоспазм (также освобождает гистамин из тучных
клеток).
28.
Рвотный центр
Морфин вызывает тошноту у 40 % людей и рвоту у 15 % как
стимулятор хеморецепторов триггерной зоны рвотного центра.
Другие наркотические анальгетики обладают слабым рвотным
эффектом.
Сосудодвигательный центр
Морфин в терапевтических дозах не изменяет функцию
сосудодвигательного центра, при отравлении вызывает его угнетение.
Спинной мозг
Морфин усиливает спинальные сухожильные рефлексы, но подавляет
супраспинальные рефлексы.
29.
ВЛИЯНИЕ НА СЕРДЕЧНО-СОСУДИСТУЮ СИСТЕМУ• Морфин вызывает ортостатическую гипотензию
вследствие брадикардии и расширения сосудов.
• Промедол при введении в вену вызывает тахикардию.
• Трамадол, пентазоцин и буторфанол, освобождая
норадреналин из периферических симпатических нервов,
повышают ЧСС и АД.
У больных стенокардией пентазоцин и буторфанол
увеличивают давление крови в аорте и легочной артерии,
конечно-диастолическое давление, работу сердца.
30.
ВЛИЯНИЕ НА ОРГАНЫ С ГЛАДКОЙ МУСКУЛАТУРОЙ• Морфин вызывает бронхоспазм, спазм сфинктеров желудка, к-ка, ЖВ
и МВ путей, тормозит перистальтику к-ка.
• Нарушение перистальтики в сочетании с повышением вязкости
содержимого к-ка сопровождается обстипацией.
• Спазмогенное действие других анальгетиков выражено слабее.
• Морфин увеличивает давление в желчном пузыре в 10 раз; подавляет
рефлексы на мочеиспускание и дефекацию; удлиняет роды, нарушает
дыхание плода.
• Промедол повышает сократительную деятельность матки, не
препятствуя открытию ее шейки; меньше морфина вызывает
дыхательные расстройства у плода.
• Пентазоцин плохо проникает через плацентарный барьер и слабо
влияет на дыхание плода.
31.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ:перед операцией и в послеоперационном периоде;
тяжелые травмы;
неоперабельные злокачественные
новообразования (для облегчения душевных и
физических страданий);
при болях ишемического (инфаркт миокарда,
стенокардия, эндартериит) или спастического
(почечная, печеночная колика) генеза;
острый отек легких;
кашель;
диарея;
премедикация.
32.
Алкалоидымака
33.
Морфина гидрохлоридПоказания: отек легких, острые и хр. боли у онколог-х
б-х, травмы, шок, ОИМ, боли после операции.
Действие ч/з 10-15 мин п/к введения и ч/з 20-30 мин
внутрь.
Длит-ть анальгетического д-ия 4-6 ч.
↓tтела,
↓диурез
(↑АДГ),
миоз,
↓
ДЦ,
противокашлевая акт-ть, ↓ рвотный центр, но ↑R
пусковой зоны IV желудочка, ↓ЧСС (↑блужд.н.),
↓АД, ↑тонус гл.м., ↓ перистальтики к-ка,
↑сфинктеров ЖКТ, ↓секреции поджел.железы и
выделения желчи, ↑всасывания воды из к-ка и
запоры, ↑тонус сфинктера Одди и желчных протоков,
↑ тонус и сократимость мочеточников, ↑ сфинктер
мочевого пузыря и затруднение мочеотделения,
↑тонус бр. м.
34.
• Метаболизизует в печени, при этом часть морфинаметаболизируется до морфин-6-глукуронида,
который является фармакологически активным и по
анальгетической активности несколько превосходит
морфин.
• Основной путь элиминации морфина – выделение
с желчью.
• Морфин подвергается энтеро-гепатической
циркуляции: после поступления с током крови в
печень, часть морфина выделяется с желчью в 12перстную кишку, где она вновь всасывается и с
током крови вновь поступает в печень, после чего
процесс повторяется.
35.
ОСТРОЕ ОТРАВЛЕНИЕ МОРФИНОМ• При в/в введ. средняя терапевтическая доза морфина
составляет 10 мг, средняя токсическая — 30 мг, средняя
летальная — 120 мг.
• Симптомы отравления морфином: эйфория, утрата
болевых реакций, гипотермия, рост ВЧД, отек мозга,
клонико-тонические судороги, ступор, переходящий в
кому.
• Спинальные сухожильные рефлексы сохраняются.
Аритмия, арт. гипотензия, отек легких, миоз (при
сильной гипоксии - мидриаз), рвота, задержка
мочеиспускания и дефекации, гипогликемия,
потливость. Дыхание поверхностное, редкое (2 — 4 в
мин). Бронхоспазм. Смерть от паралича ДЦ.
• Для постановки диагноза - три симптома: кома, сужение
зрачков и угнетение дыхания.
36.
• Неотложные меры помощи при отравлениинаправлены на ликвидацию дыхательных
расстройств.
• Проводят ИВЛ под положительным
давлением, отсасывают бронхиальное
отделяемое. Используют конкурентные
антагонисты — налоксон или налтрексон. Они
эффективны при интоксикации любыми
наркотическими анальгетиками (при
отравлении средствами с комбинированным
действием необходимы большие дозы). При
использовании налоксона дыхание становится
более частым, чем до отравления.
37.
• В дозах 12 — 24 мг налоксон не влияет на функции ЦНС ивнутренних органов. В больших дозах – вызывает сонливость,
ухудшает память, повышает систолическое АД, стимулирует
секрецию рилизинг-гормонов для гонадотропинов и АКТГ, а
также увеличивает выделение пролактина, глюкокортикоидов
и катехоламинов.
• Налтрексон в больших дозах обладает гепатотоксичностью,
вызывает тошноту, рвоту, головную боль, тревогу, дисфорию,
кожную сыпь.
• После восстановления нормального дыхания удаляют
невсосавшийся яд из ЖКТ.
• Активированный уголь или калия перманганат в 0,05 % р-ре.
Оба антидота применяют повторно и независимо от пути
введения морфина. Промывание требует особой
осторожности (опасность судорог, разрыва пищевода,
аспирации угля при рвоте).
38.
ХРОНИЧЕСКОЕ ОТРАВЛЕНИЕ НАРКОТИЧЕСКИМИАНАЛЬГЕТИКАМИ
• Наиболее опасны героин и синтетическое средство aметилфентанил (его наркогенный потенциал в 600 раз
выше, чем у морфина).
• Героин - диацетилморфин. Подвергается
деацетилированию в двух последовательных
реакциях. В крови образуется 6-моноацетилморфин
при участии псевдохолинэстеразы плазмы и
ацетилхолинэстеразы эритроцитов. Вторую реакцию
деацетилирования, в которой образуется морфин,
катализирует только ацетилхолинэстераза эритроцитов.
Период полуэлиминации героина в крови составляет 3
мин.
Наркомания характеризуется психической, физической
зависимостью и привыканием!
39.
Ранние признаки абстинентного синдрома(появляются через 5 — 7 дней после отмены):
страстное желание принимать наркотическое средство;
усталость, раздражительность, бессонница, тревога, дисфория;
спонтанная боль, атаксия, частое дыхание, гипертермия;
зевота, тошнота, рвота, диарея;
расширение зрачков;
потливость, пилоэрекция («гусиная кожа»);
артериальная гипертензия.
Спустя 6 мес. после прекращения приема наркотических
анальгетиков сохраняются тревога, бессонница, дыхательные
расстройства.
• Привыкание позволяет переносить 0,25 — 0,5 г морфина без
симптомов острого отравления.
40.
Омнопон (пантопон)- смесь алкалоидов опия фенантренового и
изохинолинового ряда. Кол-во алкалоидов в
омнопоне в 3—5 раз > чем в опии.
Быстро всасывается, дей-е проявляется
быстро. В отличие от морфина <↓дыхание, <
повышает тонус гл.м.
41.
Промедол• По обезболивающей акт-ти меньше
морфина в 2 раза. Д-ет 3-4 ч.
• Меньше тошнота, рвота, угнетение ДЦ.
↑сократимость миометрия и расслабляет
зев.
• Снижает тонус мочеточников, бронхов.
• Спазмогенный эффект меньше, чем у
морфина.
42.
Кодеин- алкалоид из опия, полусинтетический.
Обладает слабым наркот-м эффектом,
↓кашлевой центр. Входит в состав
п/кашлевых ЛС.
Слабее морфина, меньше тормозит деят-ть
ЖКТ, бывают запоры.
Таб. «Кодтерпин», «Пенталгин плюс»,
«Седальгин-Нео»,
«Нурофен
плюс»,
«Терпинкод Н», «Солпадеин».
Может
вызывать
зависимость
при
повторных приемах.
43.
ПОЛУСИНТЕТИЧЕСКИЕ ПРЕПАРАТЫБупренорфин
Частичный агонист μ-R.
Анальгетическое д-ие выше, чем у морфина в 2060 раз. Меньше д-ет на ЖКТ. 96% св.с б.кр.
Основная часть неизмененного в-ва
выделяется к-ком, метаболиты – почками.
Налбуфин
Агонист κ-R, антагонист μ-R.
Акт-ть как у морфина. Лекарственная
зависимость развивается редко.
44.
СИНТЕТИЧЕСКИЕ НАРКОТИЧЕСКИЕАНАЛЬГЕТИКИ
Фентанил
• часто комбинируют для получения др. видов
обезболивания.
Нейролептанальгезия – вид обезболивания,
кот-й достигается совместным введением
нейролептиков короткого д-я (Дроперидол) +
наркот-й анальгетик короткого д-я (Фентанил).
Позволяет
проводить
кратковрем-е
оперативные вмешательства, перевязки.
45.
Фентанил• Анальгетическая акт-ть больше, чем у морфина в
100-400 раз.
• действует кратковременно (препарат «скорой
помощи») при ОИМ, коликах, ИБС
• выражено ↓ ДЦ
• Повышает тонус скел. м., вызывает спастическое
сокращение межреберных мышц
• ↓ЧСС (вводить атропин)
• Макс эффект при в/в - через 1-3 мин. Длит-ть - 2030 мин.
• Перераспределяется в органах (ниже конц. в ЦНС,
выше- в периф. тк.).
46.
Пентазоцин (фортрал, лексир)• Агонист-антагонист
• Агонист δ- и κ-R, антагонист μ-R.
• Меньше анальгетическое д-ие и длит-ть дия. Нет эйфории. Меньше угнетает ДЦ,
реже вызывает запор.
• Повышает давление в легочной артерии.
Повышает центральное венозное давление
→ ↑преднагрузку на с. → ↑работу с.
Противопоказан при ИМ!
47.
Буторфанол (стадол, морадол)• Агонист κ-R, антагонист μ-R.
• Активнее морфина в 3-5 раз.
• Дыхание угнетает меньше, чем морфин.
Лекарственная зависимость реже.
• Повышает давление в легочной
артерии→↑работу с. Противопоказан при
ИМ!
48.
Анальгетики со смешанным типом д-я:опиоидный+неопиоидный
Трамадол (трамал)
Взаимод-ет с опиоидными R и д-ет на
моноаминергическую
систему.
Уменьшает
нейрональный захват серотонина и НА. Трамадол в
5-10 раз < активен, чем морфин. Мало влияет на
дыхание и ЖКТ. Биодоступность 68%, в/в – ч/з 5-10
мин анальгезия, внутрь - 30-40 мин, длит-ть - 3-5 ч.
Метаболизируется в печени. Есть активные
метаболиты.
Показания: средние и сильные хр. и острые боли.
Побочные эф.: головная боль, головокружение,
потливость, ↓АД,↑ЧСС, сухость во рту, запор, боли в
животе, высыпания, судороги при больших дозах.
49.
НЕОПИОИДНЫЕ ЛС ЦЕНТРАЛЬНОГО Д-Я САНАЛЬГЕТ-Й АКТИВ-Ю
АДРЕНЕРГИЧЕСКИЕ
• Клофелин (α2-АМ)
ТРИЦИКЛИЧЕСКИЕ АНТИДЕПРЕССАНТЫ (при хр.болях)
• Амитриптилин Имизин (↓нейрональный захват серотона, НА)
ОБЩИЕ АНЕСТЕТИКИ
• Закись азота
Трилен
Фторотан
Кетамин (диссоц-я анастезия неконкурентный антогонист NMDA рецепторов)
АГОНИСТЫ ГАМК-РЕЦЕПТОРОВ
ТНIР
ГАМК-А рецепторы
• Баклофен ГАМК-Б рецепторы
ПРОТИВОЭПИЛЕПТИЧЕСКИЕ ПРЕПАРАТЫ (при хр.болях)
•Производные дибензазепина
Карбамазепин
•Производные бензодиазепина
Клоназепам
ПРОТИВОГИСТАМИННЫЕ ПРЕПАРАТЫ
Димедрол
50.
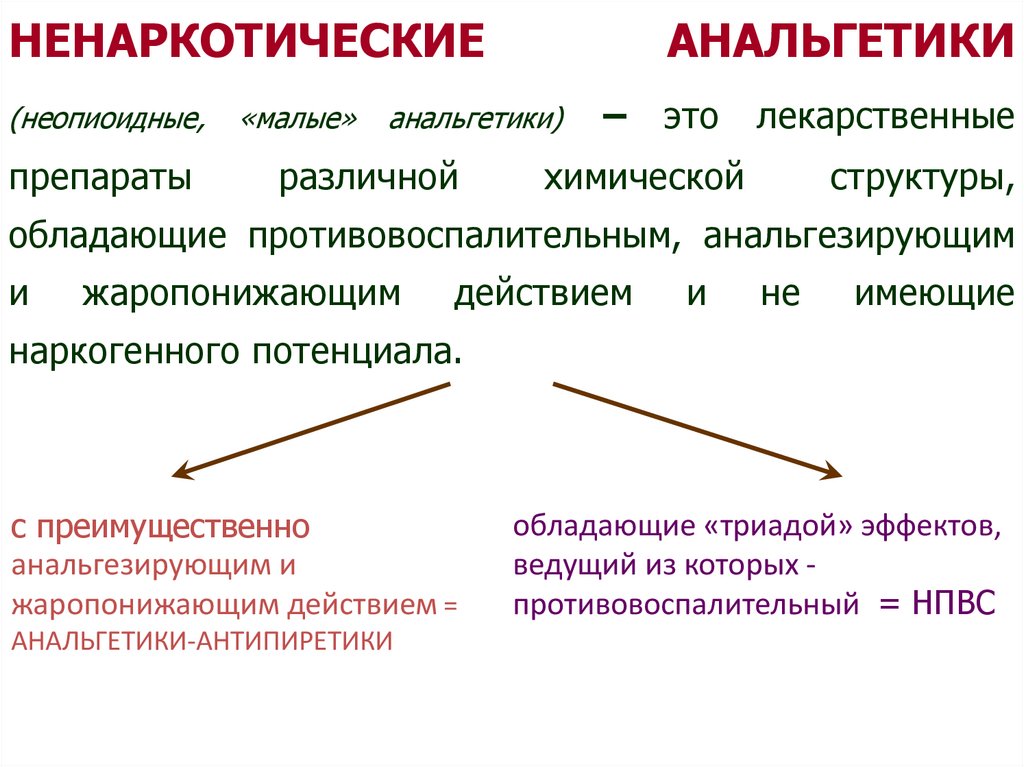
НЕНАРКОТИЧЕСКИЕ(неопиоидные,
препараты
«малые»
АНАЛЬГЕТИКИ
это
лекарственные
химической
структуры,
анальгетики)
различной
–
обладающие противовоспалительным, анальгезирующим
и
жаропонижающим
действием
и
не
имеющие
наркогенного потенциала.
с преимущественно
анальгезирующим и
жаропонижающим действием =
АНАЛЬГЕТИКИ-АНТИПИРЕТИКИ
обладающие «триадой» эффектов,
ведущий из которых противовоспалительный = НПВС
51.
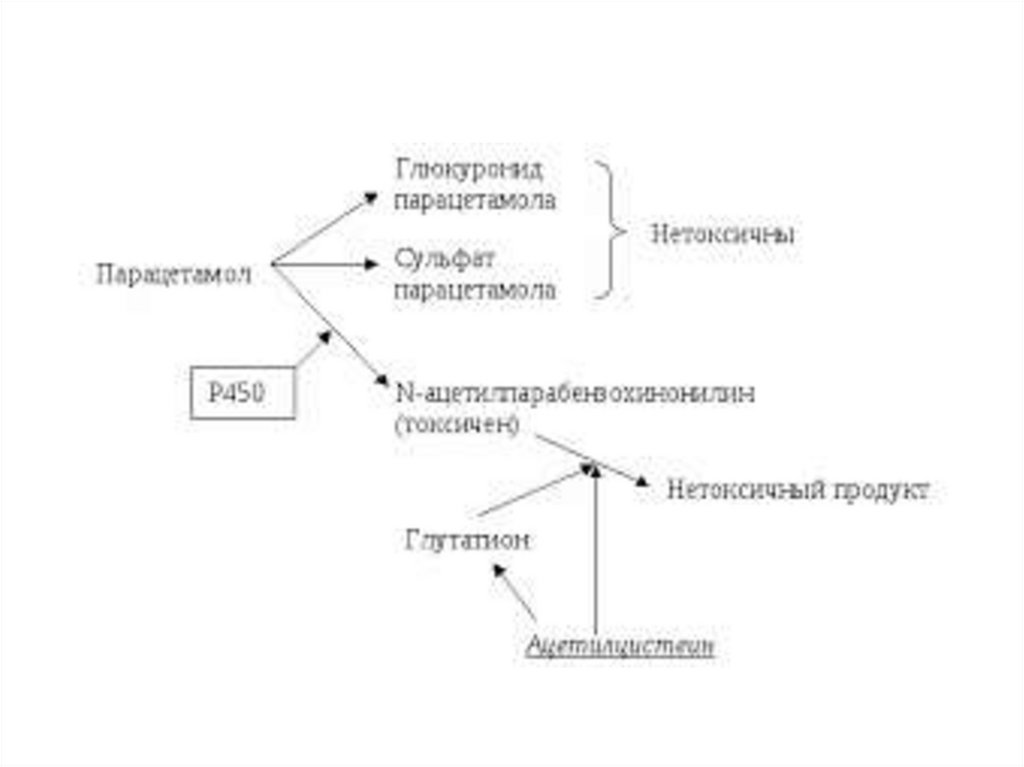
Парацетамол (ацетаминофен,панадол, эффералган)
- Активный метаболит фенацетина.
Ингибирует ЦОГ-3 → ↓синтеза ПГ в ЦНС
С мах - 30-60 мин. Т1/2 – 1-3ч.
Плохо св. с б. крови.
Небольшая терапевтическая широта!
Вызывает поражение печени и почек из-за
накопления токсичного метаболита Nацетил-n-бензохинонимина.
52.
53.
Парацетамол• У детей до 12 лет недостаточность
цитохрома Р-450 и → преобладает
сульфатный путь биотрансформации →
токсичные продукты не образуются.
54.
Отравление парацетамолом• Клиническая картина: поражение печени
(желтуха, печеночная недостаточность, кома) и
почек (почечная недостаточность).
Лечение: промывание желудка, ацетилцистеин
(антидот парацетамола).
Ацетилцистеин (повышает образование глютатиона
в печени) и метионин (стимулирует конъюгацию)
эффективны в первые 12 ч. после отравления,
пока не наступили необратимые изменения
клеток.
14
55.
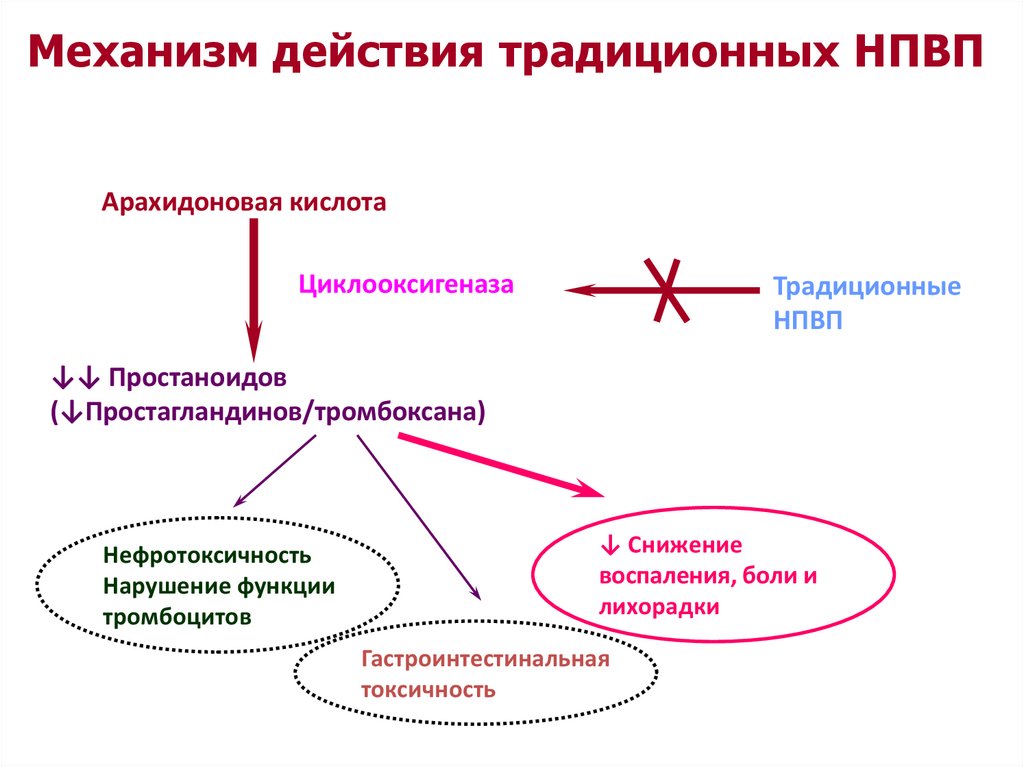
Механизм действия традиционных НПВПАрахидоновая кислота
Циклооксигеназа
Традиционные
НПВП
↓↓ Простаноидов
(↓Простагландинов/тромбоксана)
Нефротоксичность
Нарушение функции
тромбоцитов
↓ Снижение
воспаления, боли и
лихорадки
Гастроинтестинальная
токсичность
56.
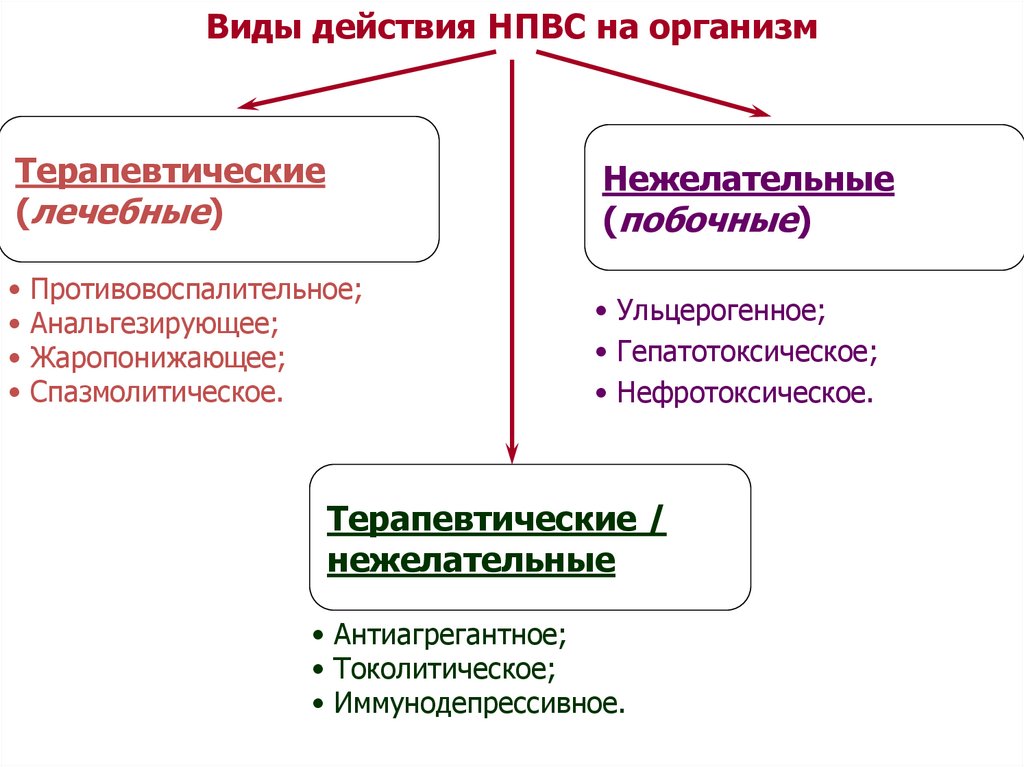
Виды действия НПВС на организмТерапевтические
(лечебные)
Нежелательные
(побочные)
• Противовоспалительное;
• Анальгезирующее;
• Жаропонижающее;
• Спазмолитическое.
• Ульцерогенное;
• Гепатотоксическое;
• Нефротоксическое.
Терапевтические /
нежелательные
• Антиагрегантное;
• Токолитическое;
• Иммунодепрессивное.
57.
МЕХАНИЗМ ПРОТИВОВОСПАЛИТЕЛЬНОГОДЕЙСТВИЯ
Препараты в большей степени ограничивают развитие
экссудативной и пролиферативной фаз воспаления
Противовоспалительный эффект связан с тем, что эти препараты:
– угнетают образование из арахидоновой кислоты медиаторов боли,
воспаления и лихорадки – простагландинов, в следствие снижения
активности фермента циклооксигеназы 2-го типа (в здоровых тканях
практически отсутствует и экспрессируется только при воспалении);
– угнетают синтез и высвобождение медиаторов воспаления (серотонина,
гистамина) из тучных клеток;
– угнетают активность гиалуронидазы – фермента, расщепляющего
гиалуроновую кислоту, являющуюся основным веществом
соединительной ткани, тем самым ограничивают процесс экссудации;
– ингибируют синтез коллагена фибробластами грануляционной ткани,
подавляют пролиферативную фазу воспаления.
58.
МЕХАНИЗМ АНАЛЬГЕТИЧЕСКОГО ДЕЙСТВИЯАнальгетический эффект НПВС возникает через 0,5 – 2 часа
и
является,
в
основном,
следствием
ведущего
противовоспалительного действия.
Кроме периферического компонента болеутоляющего
действия, у ННА имеется и центральный механизм, который
связан с их влиянием на таламичекие центры, торможение
которых приводит к ослаблению проведения импульсов к коре
головного
мозга,
а
также
препятствуют
повышению
концентрации простагландинов в спинномозговой жидкости, что
тормозит развитие вторичной гиперальгезии.
При этом они не влияют на опиатную систему мозга, не
вызывают психическую и физическую зависимость.
59.
МЕХАНИЗМ ЖАРОПОНИЖАЮЩЕГО ДЕЙСТВИЯСнижают температуру тела (через 0,5 - 2 часа), только
если она повышена, т.е. при лихорадке, что связано с
ингибированием
синтеза
простагландинов
в
центре
терморегуляции в гипоталамусе.
Препараты
вследствие
значительно
расширения
усиливают
сосудов
теплоотдачу
кожи,
оболочек, повышения функции потовых желез.
слизистых
60.
Побочные эффекты НПВС(и частота их встречаемости)
Желудочно-кишечные (1-4%)
Диспепсия,
Эрозии и язвы (чаще в желудке) ,
Поражение кишечника (возможная причина анемии),
Поражение печени (обычно умер. повышение печен. ф-тов)
Поражение пищевода
Почечные (наиболее часто их вызывает индометацин)
Нарушение клубочковой фильтрации
Повышение АД
Сосочковый некроз
Интерстициальный нефрит
61.
Побочные эффекты НПВС(и частота их встречаемости)
Неврологические
Головные боли (наиболее часто их вызывает индометацин )
Асептический менингит (ибупрофен, кетопрофен, флурбипрофен,
напроксен)
Кожные
Зуд, кожная сыпь
Гематологические (наиболее часто их вызывает фенилбутазол, очень
редко – индометацин)
Включая агранулоцитоз
Гиперчувствительность (наиболее частая причина – ацетилсалициловая
кислота) БА, крапивница, пневмония
Другие
Ототоксичность (наиболее частая причина – ацетилсалициловая кислота)
Бесплодие у женщин
Стоматит, сиаладенит, кардит, васкулит, панкреатит (наиболее часто –
фенилбутазон)
Сульфонамидная аллергия (целекоксиб, назначение противопоказано)
Бронхоспазм (ЦОГ-2 ингибиторы вызывают реже, чем «стандартные»
НПВП)
62.
Отравление салицилатами• Клиника отравления: головная боль, звон в ушах,
нарушение зрения и психики, тошнота, рвота,
диарея, боли в эпинастрии, респираторный
алкалоз, гипокалиемия, гипертермия.
• Лечение: промывание желудка, активированный
уголь, солевые слабительные, форсированный
диурез, гемодиализ, перитонеальный диализ,
переливание крови, наружное охлаждение тела.
13
63.
Мигрень - одно из наиболее древних ираспространенных заболеваний , более 5000 лет.
Мигренью страдали –
Юлий Цезарь
Исаак Ньютон
Карл Маркс
Чарльз Дарвин
Фредерик Шопен
Зигмунд Фрейд
Чехов А.П.
Чайковский П.И. и др.
64.
МигреньТриптаны - агонисты серотониновых
рецепторов 5HT 1B и 5HT 1D типа
• Суматриптан – «золотой стандарт»,
• Золмитриптан ,
• Элетриптан
65.
• Оказывая непосредственное действие на постсинаптическиесеротониновые R сосудистой стенки, триптаны вызывают
сужение избыточно расширенных церебральных сосудов. Это
снижает стимуляцию болевых R сосудистой стенки и
способствует ум. боли.
• Триптаны обладают высокой селективностью в отношении
кровеносных сосудов твердой мозговой оболочки и
незначительной в отношении коронарных и периферических
сосудов.
• Триптаны ингибируют выделение алгогенных и вазоактивных
белков (субстация Р, пептид, связанный с геном кальцитонина)
из периваскулярных волокон тройничного нерва и ум.
нейрогенное воспаление. Блокируют проведение боли на
уровне спинномозгового ядра тройничного нерва.
• Предполагается, что центральный механизм д-ия
обусловливает продолжительность д-ия 5НТ 1 агонистов,
способствует ум. рецидивов головной боли и обеспечивает
эффективность препаратов в отношении сопутствующих
тошноты, рвоты, светобоязни и звукобоязни.
66.
Триптаны• Противопоказания: ИБС, нарушение
кровоснабжения мозга, аритмии, БА, тяжелая
АГ, тяжелые нарушения ф-ции печени и почек,
аллергия или непереносимость компонентов
препарата.
• Побочные эффекты: тошнота, диарея,
тахикардия, стенокардия, частое
мочеиспускание с увеличением объема мочи,
снижение тонуса мышц, слабость, мышечная
боль, ощущение слабости, головокружения,
снижение осязательных функций, сонливость,
аллергические реакции.
























































 Медицина
Медицина