Похожие презентации:
Альдегиды и кетоны
1.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ«КРАСНОЯРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ ПРОФЕССОРА В.Ф. ВОЙНО-ЯСЕНЕЦКОГО»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ
Преподаватель химии: Агафонова Н.В.
1
2.
План лекции:1.Состав альдегидов и кетонов.
2.Номенклатура и типы изомерии.
3.Физические свойства.
4.Химические свойства.
5.Получение альдегидов и кетонов.
6.Сравнительные свойства кетонов.
7.Применение.
2
3.
34.
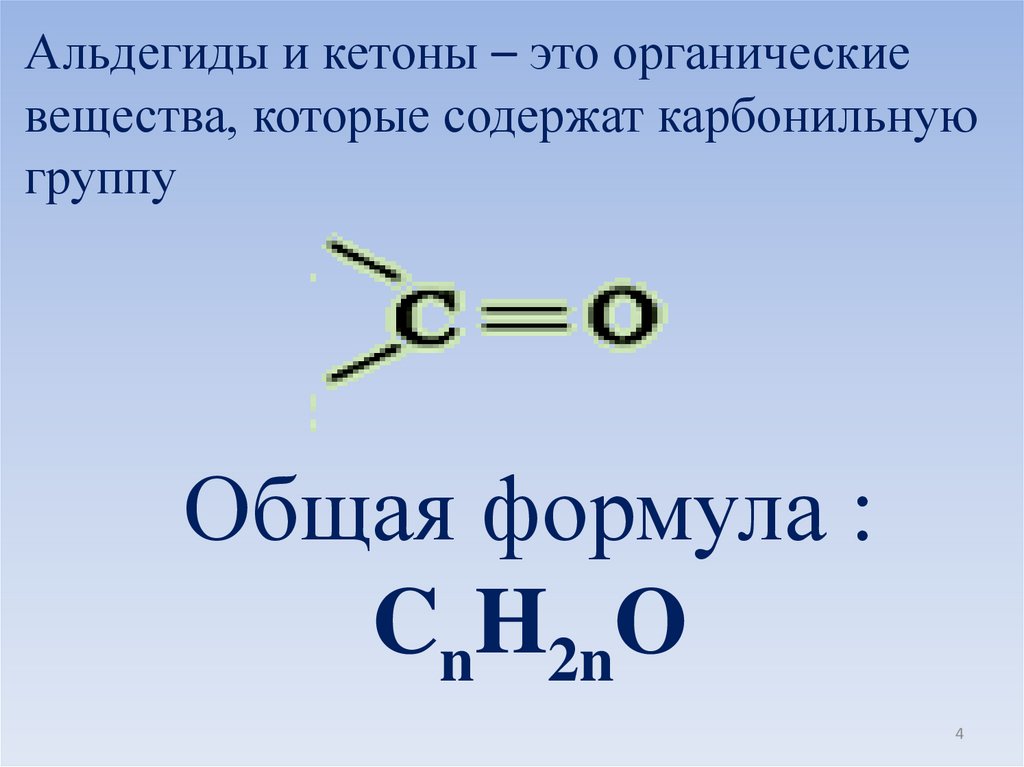
Альдегиды и кетоны – это органическиевещества, которые содержат карбонильную
группу
Общая формула :
CnH2nO
4
5.
Если карбонильная группа связанас одним углеводородным
радикалом и водородом, то такие
карбонильные соединения
называются альдегидами
Если карбонильная связанна с
двумя одинаковыми или разными
радикалами – кетонами
5
6.
67.
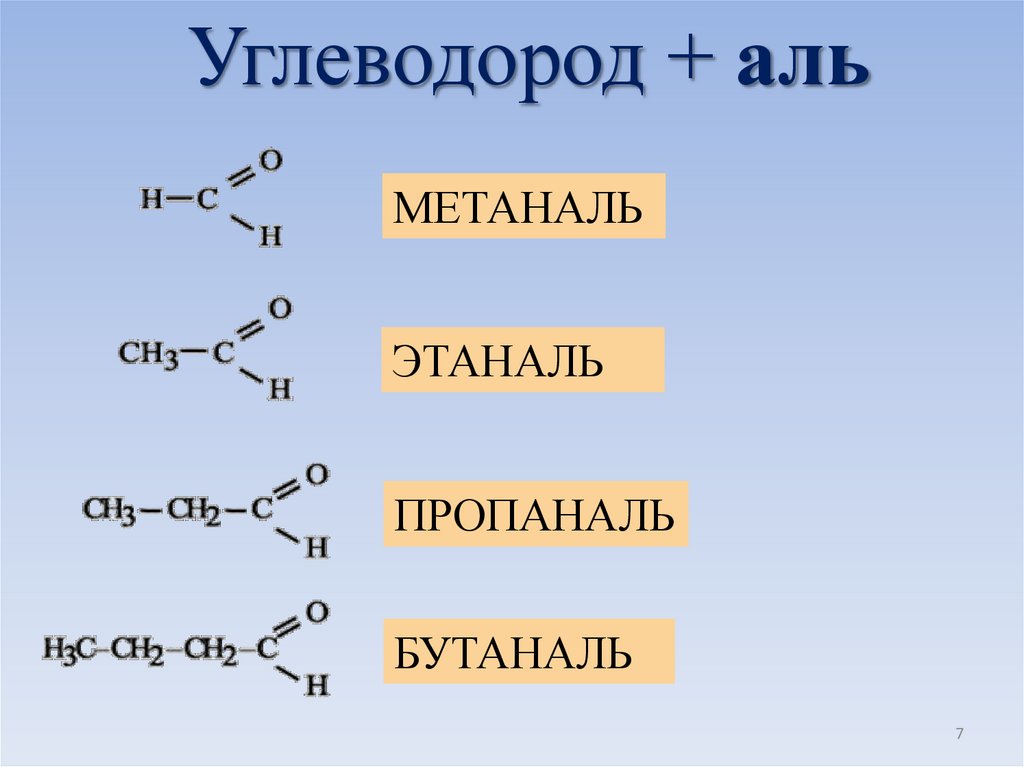
Углеводород + альМЕТАНАЛЬ
ЭТАНАЛЬ
ПРОПАНАЛЬ
БУТАНАЛЬ
7
8.
Тривиальные названия – производные отназваний соответствующих кислот
8
9.
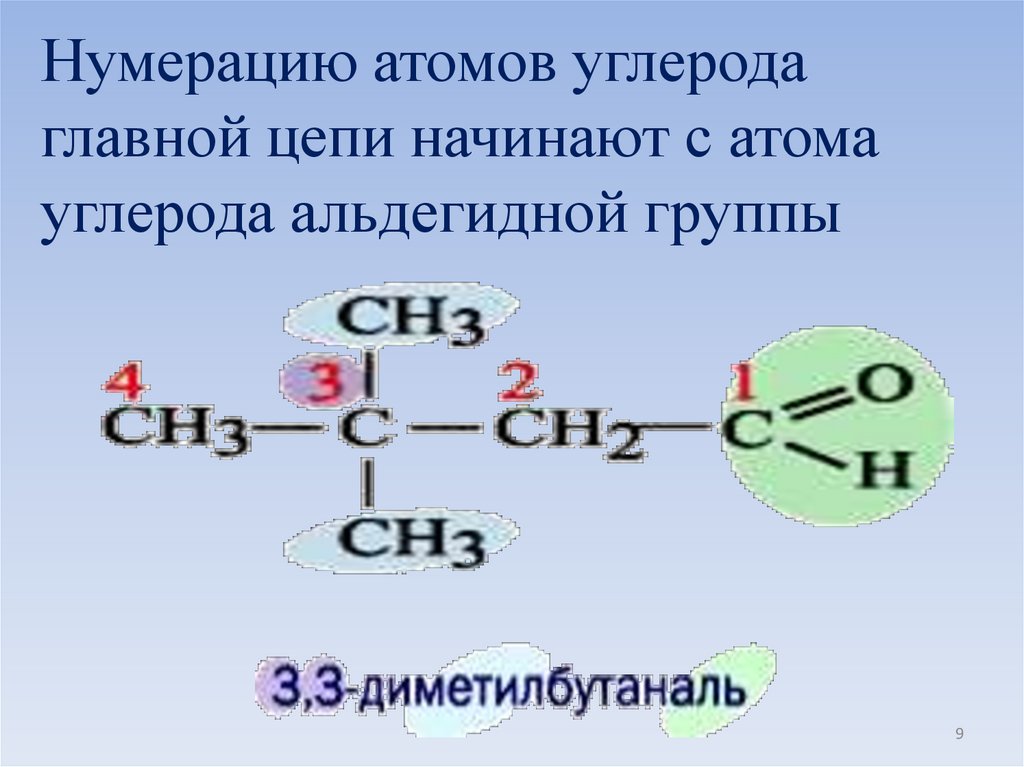
Нумерацию атомов углеродаглавной цепи начинают с атома
углерода альдегидной группы
9
10.
В названии кетонов кетогруппу обозначаютсуффиксом –он и цифрой, которая указывает
номер атома углерода карбонильной группы
O
CH3 C
CH3
пропанон,
диметилкетон
(ацетон)
O
CH3CH2 C
CH3
бутанон
метилэтилкетон
10
11.
альдегидыИзомерия положения
карбонильной группы
Межклассовая
изомерия
Изомерия
углеродного
скелета
ИЗОМЕРИЯ
кетоны
11
12.
Межклассовая изомерияCH3CH2 C
пропаналь
(пропионовый
альдегид)
O
H
O
CH3 C
CH3
пропанон,
диметилкетон
(ацетон)
12
13.
3. Физические свойствабензальдегид
формальдегид
уксусный
альдегид
13
14.
1415.
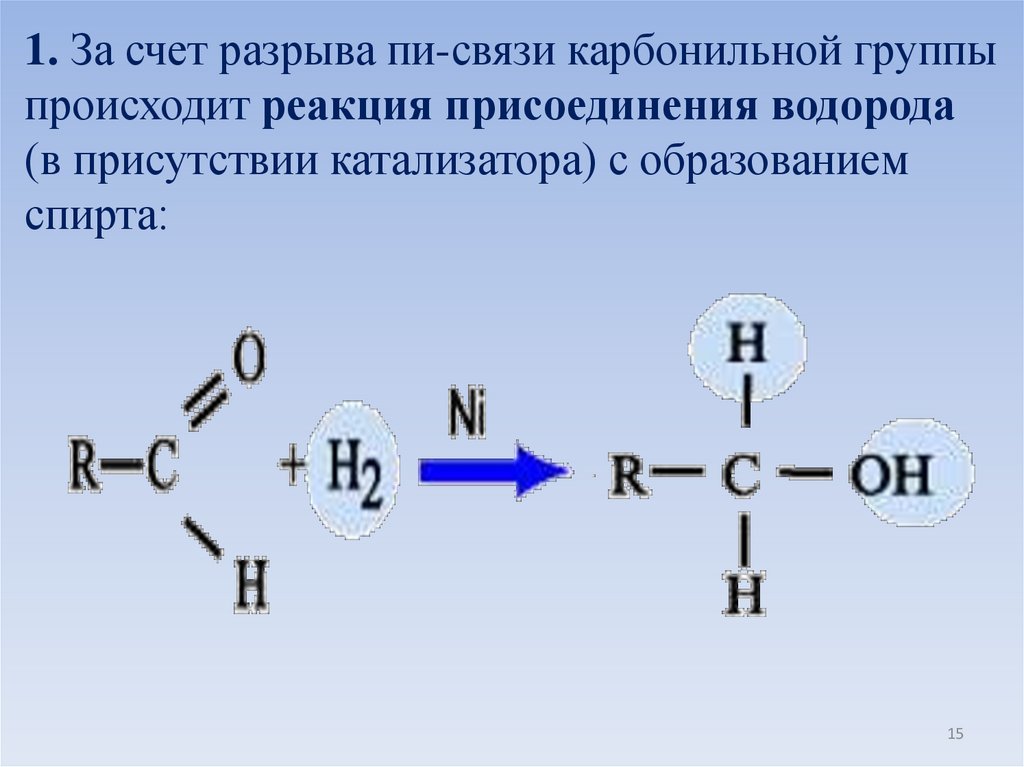
1. За счет разрыва пи-связи карбонильной группыпроисходит реакция присоединения водорода
(в присутствии катализатора) с образованием
спирта:
15
16.
2. Реакция окисленияОбщая схема:
16
17.
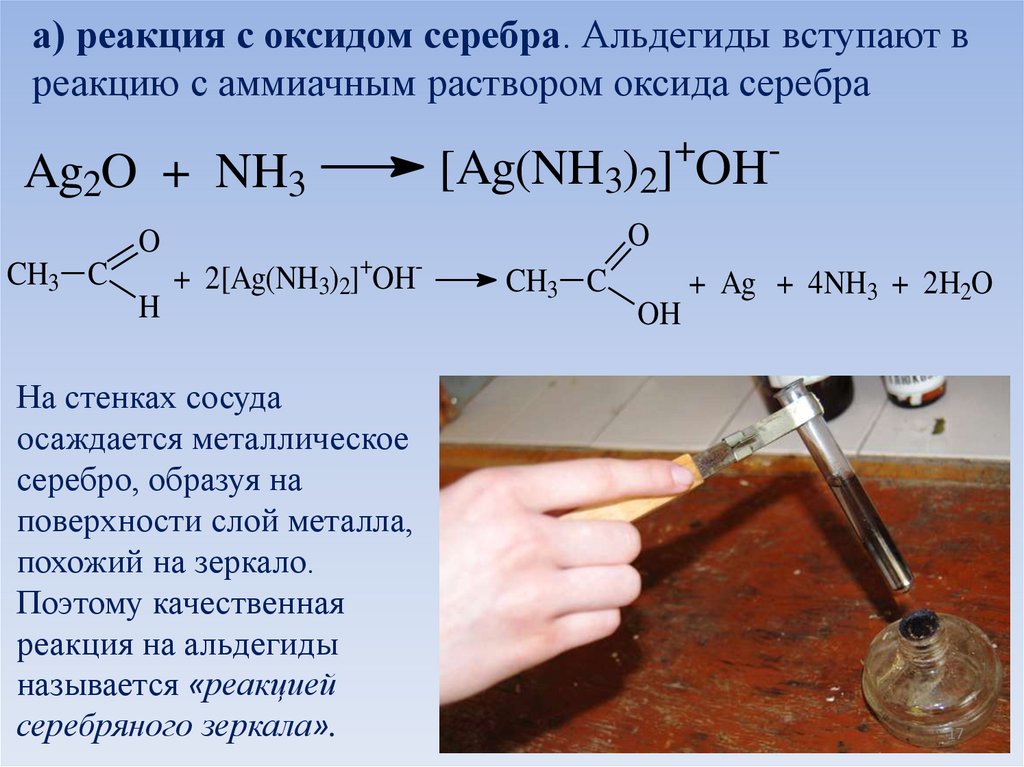
а) реакция с оксидом серебра. Альдегиды вступают вреакцию с аммиачным раствором оксида серебра
Ag2O + NH3
O
CH3 C
H
+
-
[Ag(NH3)2] OH
O
+ 2[Ag(NH3)2]+OH-
На стенках сосуда
осаждается металлическое
серебро, образуя на
поверхности слой металла,
похожий на зеркало.
Поэтому качественная
реакция на альдегиды
называется «реакцией
серебряного зеркала».
CH3 C
OH
+ Ag + 4NH3 + 2H2O
17
18.
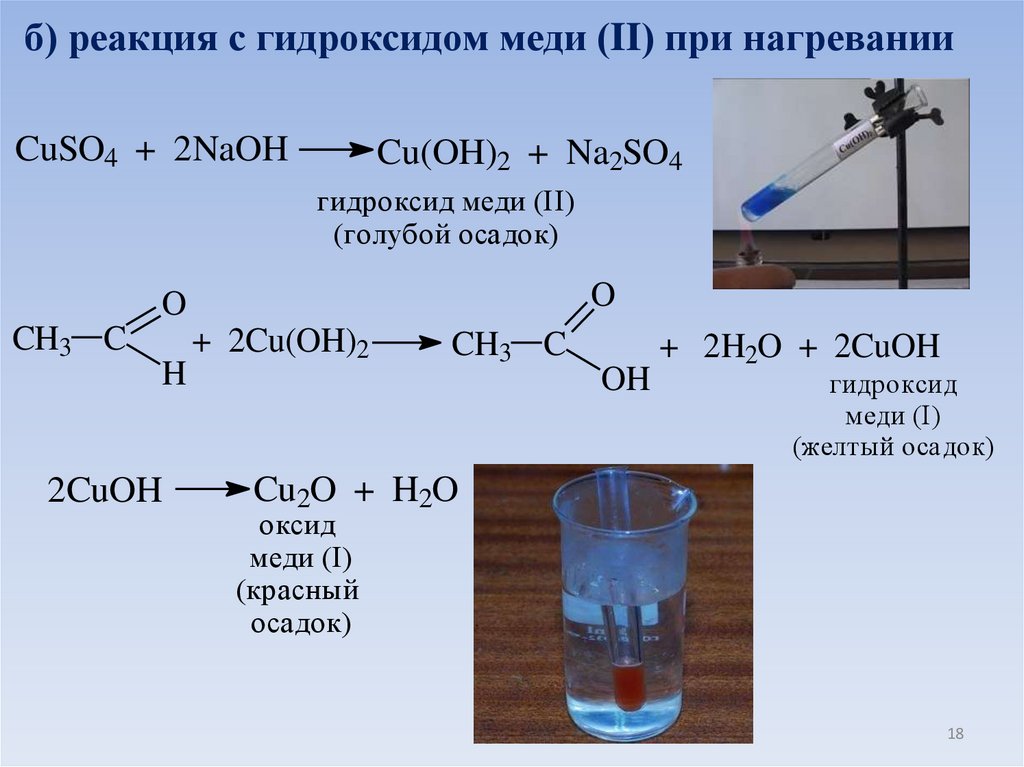
б) реакция с гидроксидом меди (II) при нагреванииCuSO4 + 2NaOH
Cu(OH)2 + Na2SO4
гидроксид меди (II)
(голубой осадок)
O
O
CH3 C
H
2CuOH
+ 2Cu(OH)2
CH3 C
OH
+ 2H2O + 2CuOH
гидроксид
меди (I)
(желтый осадок)
Cu2O + H2O
оксид
меди (I)
(красный
осадок)
18
19.
3. Реакция замещения19
20.
4. Полимеризация20
21.
2122.
1. Окислением спиртовCH3CH2OH
[O]
этанол
CH3CHCH3
O
CH3 C
H
этаналь
[O]
[O]
O
CH3 C
OH
этановая кислота
уксусная кислота
CH3CCH3
OH
O
пропанол-2
пропанон
ацетон
22
23.
2. Дегидрирование спиртовПрисоединение воды к ацетилену в присутствии солей
ртути (II) приводит к образованию ацетальдегида:
Кетоны получают при гидратации других гомологов
ряда алкинов:
23
24.
2425.
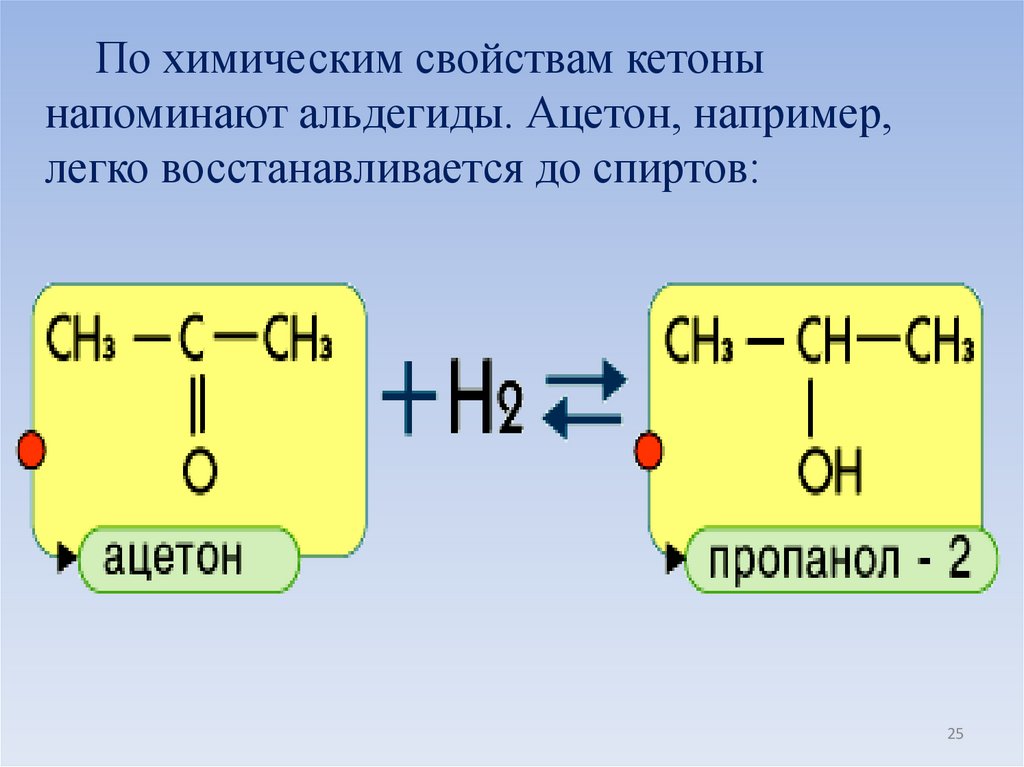
По химическим свойствам кетонынапоминают альдегиды. Ацетон, например,
легко восстанавливается до спиртов:
25
26.
2627.
Формальдегид27
28.
40% водный раствор формальдегида –формалин
28
29.
Уротропин (CH2)6N429
30.
Ванилин С8Н8О330
31.
Цитраль3,7-диметил-2,6-октадиеналь(запах лимона)
31
32.
n-Гидроксифенилбутанон-2С10Н20О2
32
33.
Феромоны33
34.
Контрольные вопросы1. Что объединяет альдегиды и кетоны? Какие вещества
называются альдегидами, а какие кетонами?
2. Приведите общую формулу гомологического ряда альдегидов.
3. Какова номенклатура альдегидов и кетонов?
4. Какие типы изомерии характерны карбонильным соединениям?
5. Какие химические свойства могут проявлять альдегиды?
6. Какими способами можно получить альдегиды и кетоны?
7. Приведите примеры природных источников нахождения
альдегидов и кетонов.
8. Какова сфера применения карбонильных соединений?
34
35.
Спасибо за внимание35




























 Химия
Химия








