Похожие презентации:
Альдегиды и кетоны
1. АЛЬДЕГИДЫ И КЕТОНЫ
2. ОПРЕДЕЛЕНИЕ
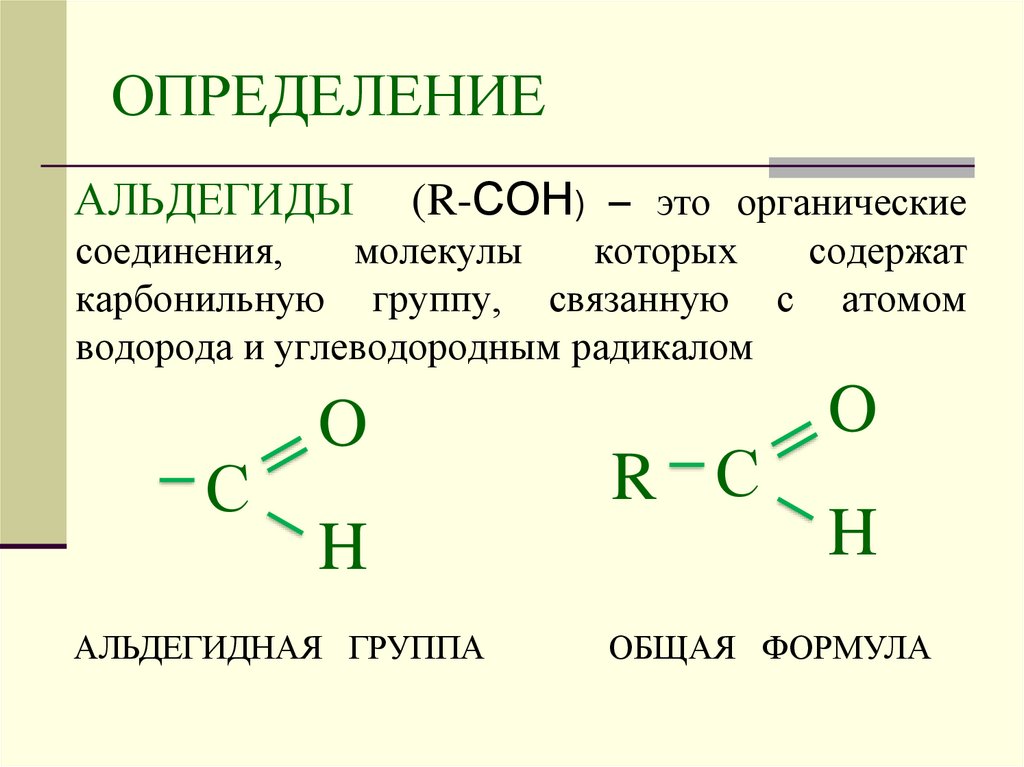
АЛЬДЕГИДЫ(R-СOН) – это органические
соединения,
молекулы
которых
содержат
карбонильную группу, связанную с атомом
водорода и углеводородным радикалом
С
O
H
АЛЬДЕГИДНАЯ ГРУППА
R С
O
H
ОБЩАЯ ФОРМУЛА
3. КЕТОНЫ
КЕТОНЫ– органические вещества, в
молекулах которых карбонильная группа
связана
с
двумя
углеводородными
радикалами
R1 – C – R2
||
O
Общая формула
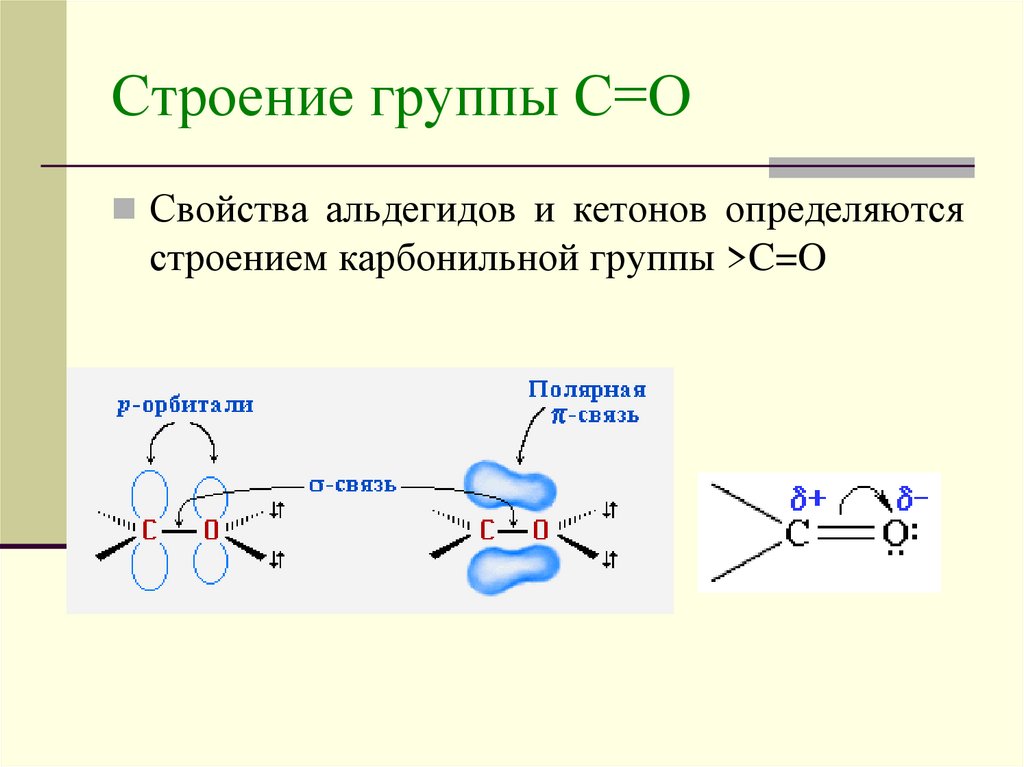
4. Строение группы С=О
Свойства альдегидов и кетонов определяютсястроением карбонильной группы >C=O
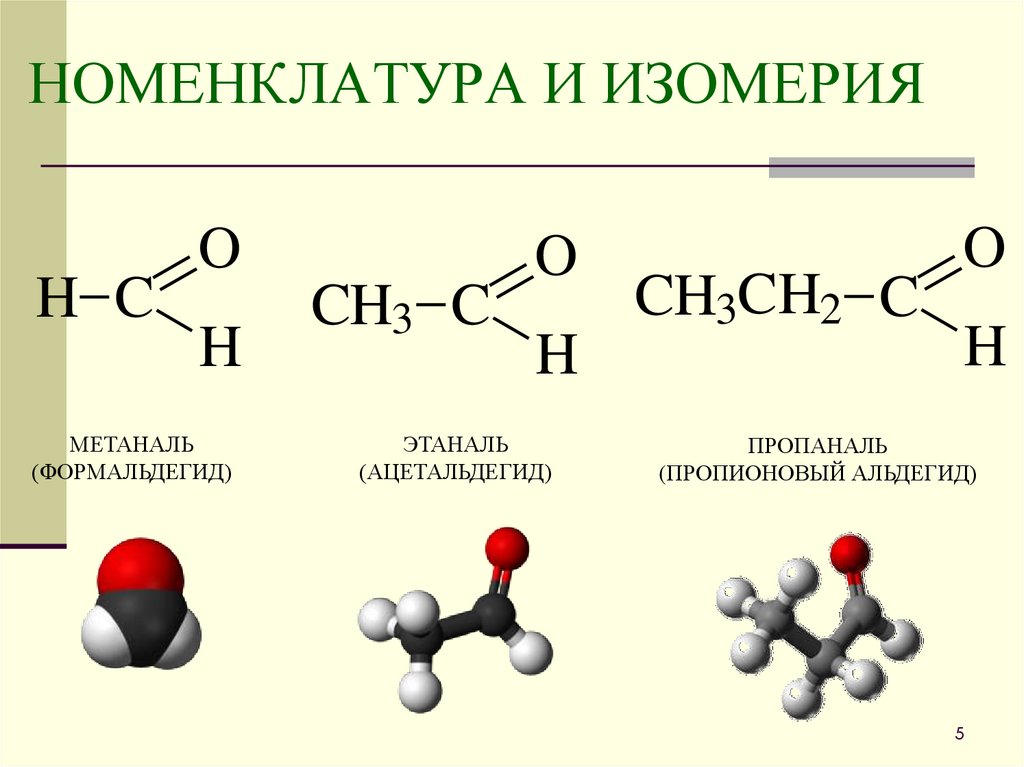
5. НОМЕНКЛАТУРА И ИЗОМЕРИЯ
H CO
H
МЕТАНАЛЬ
(ФОРМАЛЬДЕГИД)
CH3 C
O
H
ЭТАНАЛЬ
(АЦЕТАЛЬДЕГИД)
CH3CH2 C
O
H
ПРОПАНАЛЬ
(ПРОПИОНОВЫЙ АЛЬДЕГИД)
5
6. ИЗОМЕРИЯ
Изомерияуглеродного скелета
Межклассовая
изомерия
(с кетонами)
Межклассовая
изомерия
(с непредельными
спиртами и простыми
эфирами)
7. НОМЕНКЛАТУРА КЕТОНОВ
Пентанон-23-Метилбутанон-2
Пентанон-3
Ацетон или пропанон-2
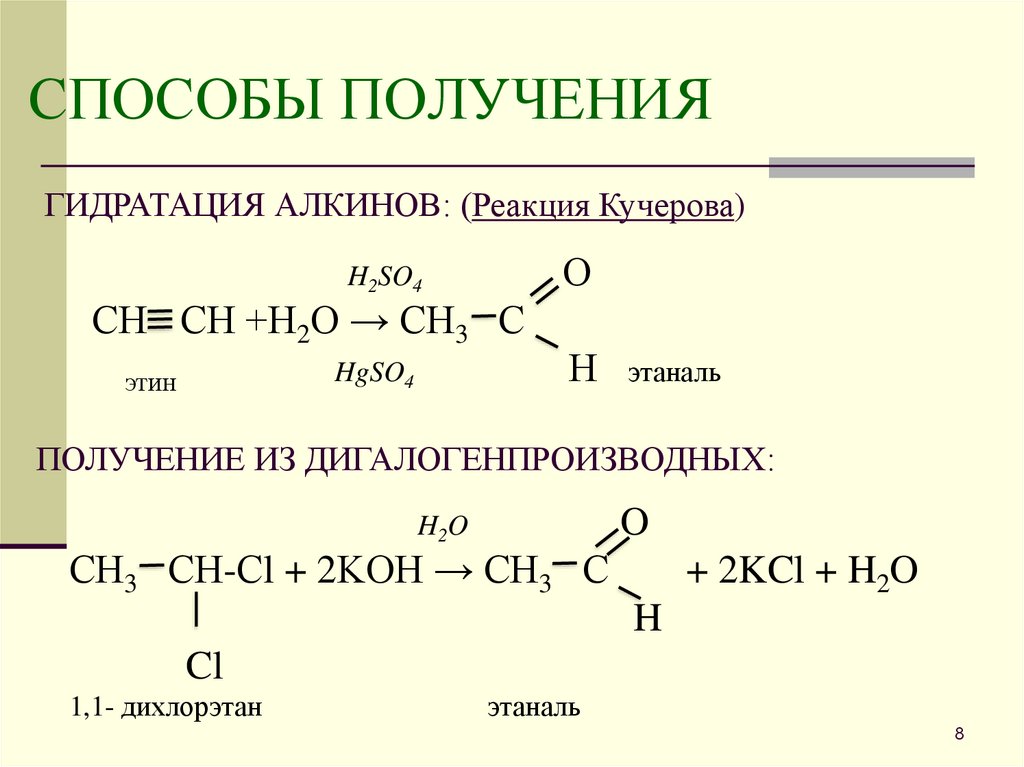
8. СПОСОБЫ ПОЛУЧЕНИЯ
ГИДРАТАЦИЯ АЛКИНОВ: (Реакция Кучерова)О
H2SO4
СН СН +Н2О → СН3 С
HgSO4
этин
Н
этаналь
ПОЛУЧЕНИЕ ИЗ ДИГАЛОГЕНПРОИЗВОДНЫХ:
O
H2O
СН3 СН-Сl + 2KOH → СН3 С
+ 2KCl + H2O
H
Cl
1,1- дихлорэтан
этаналь
8
9. СПОСОБЫ ПОЛУЧЕНИЯ
ДЕГИДРИРОВАНИЕ СПИРТОВO
//
Cu,t°
CH3 – CH2 – CH2 – OH СH3 – CH2 – C
+ H2
пропанол-1
\
пропаналь H
Cu,t°
СH3 – CH – CH3 CH3 – C – CH3 + H2
|
||
OH
O
пропанол-2
пропанон - 2 (ацетон)
9
10. СПОСОБЫ ПОЛУЧЕНИЯ
ОКИСЛЕНИЕ АЛКЕНОВ11. ХИМИЧЕСКИЕ СВОЙСТВА
РЕАКЦИИ ОКИСЛЕНИЯРеакция серебряного зеркала (качественная реакция!):
О
СН3 С
аммиачный раствор
+ 2Ag2О → СН3 С
Н
t°
О
+ Ag↓
OН
11
12. ХИМИЧЕСКИЕ СВОЙСТВА
РЕАКЦИИ ОКИСЛЕНИЯРеакция с гидроксидом меди –качественная реакция! Она используется в
медицинских биохимических лабораториях для обнаружения альдегидов
при анализах на сахар в крови и моче
О
СН3 С
этаналь
t°
О
+ 2Cu(OH)2↓→ СН3 С
+ 2H2O + Cu2O↓
Н
голубой
осадок
этановая кислота
OН
гидроксид
меди (I)
(кирпично-красный)
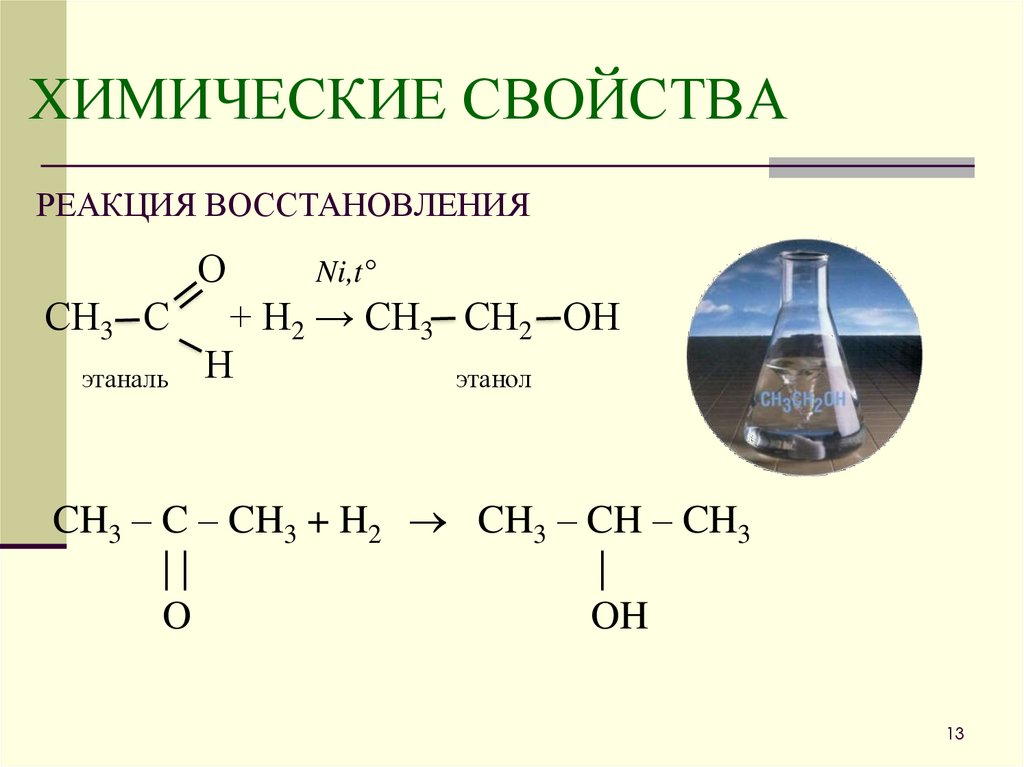
13. ХИМИЧЕСКИЕ СВОЙСТВА
РЕАКЦИЯ ВОССТАНОВЛЕНИЯО
СН3 С
этаналь
Ni,t°
+ Н2 → СН3 СН2 ОН
Н
этанол
CH3 – C – CH3 + H2 CH3 – CH – CH3
||
|
O
OH
13
14. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
ПАРФЮМЕРИЯ• Альдегид анисовый, обепин
– жидкость с приятным
запахом мимозы
• Альдегид дециловый,
деканаль – при разбавлении
появляются нотки запаха
апельсиновой корки
15. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
ПОЛИМЕРНЫЕ МАТЕРИАЛЫФенолформальдегидные смолы
16. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
ПРОИЗВОДСТВО ВЕЩЕСТВУксусная кислота
Этилацетат
Формалин











 Химия
Химия








