Похожие презентации:
Альдегиды и кетоны
1. АЛЬДЕГИДЫ И КЕТОНЫ
*АЛЬДЕГИДЫ ИКЕТОНЫ
2. ОПРЕДЕЛЕНИЕ
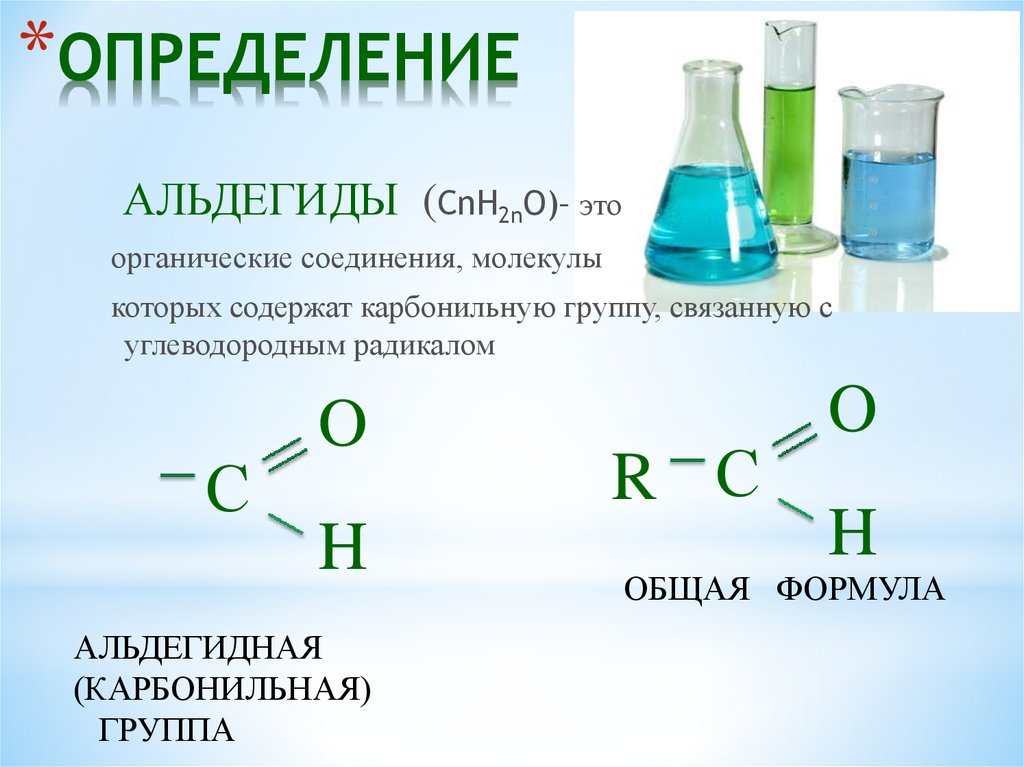
*ОПРЕДЕЛЕНИЕАЛЬДЕГИДЫ (СnH2nO)– это
органические соединения, молекулы
которых содержат карбонильную группу, связанную с
углеводородным радикалом
С
O
H
АЛЬДЕГИДНАЯ
(КАРБОНИЛЬНАЯ)
ГРУППА
R С
O
H
ОБЩАЯ ФОРМУЛА
3. КЕТОНЫ
*КЕТОНЫ – органические вещества, вмолекулах которых карбонильная
группа связана с двумя
углеводородными радикалами
R1 – C – R2
||
O
Общая формула
*КЕТОНЫ
4.
*Свойства альдегидов икетонов определяются
строением карбонильной
группы >C=O
5.
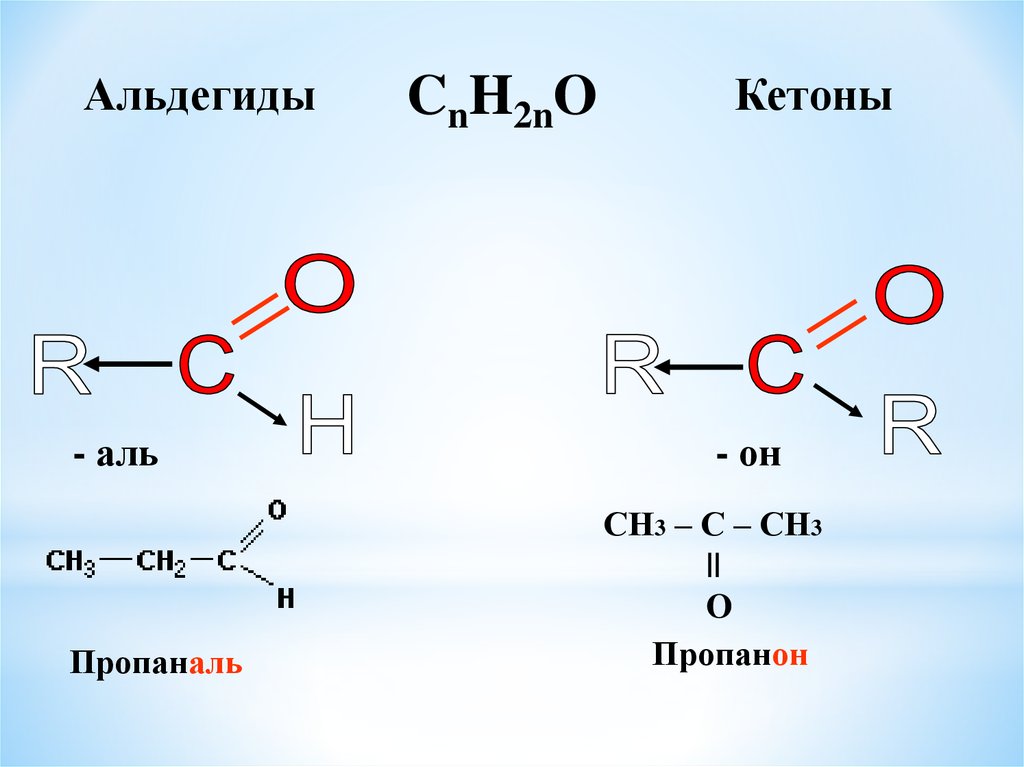
Альдегиды- аль
Пропаналь
CnH2nO
Кетоны
- он
СН3 – С – СН3
||
O
Пропанон
6. НОМЕНКЛАТУРА И ИЗОМЕРИЯ
*НОМЕНКЛАТУРА И ИЗОМЕРИЯH C
O
H
O
CH3 C
CH3CH2 C
H
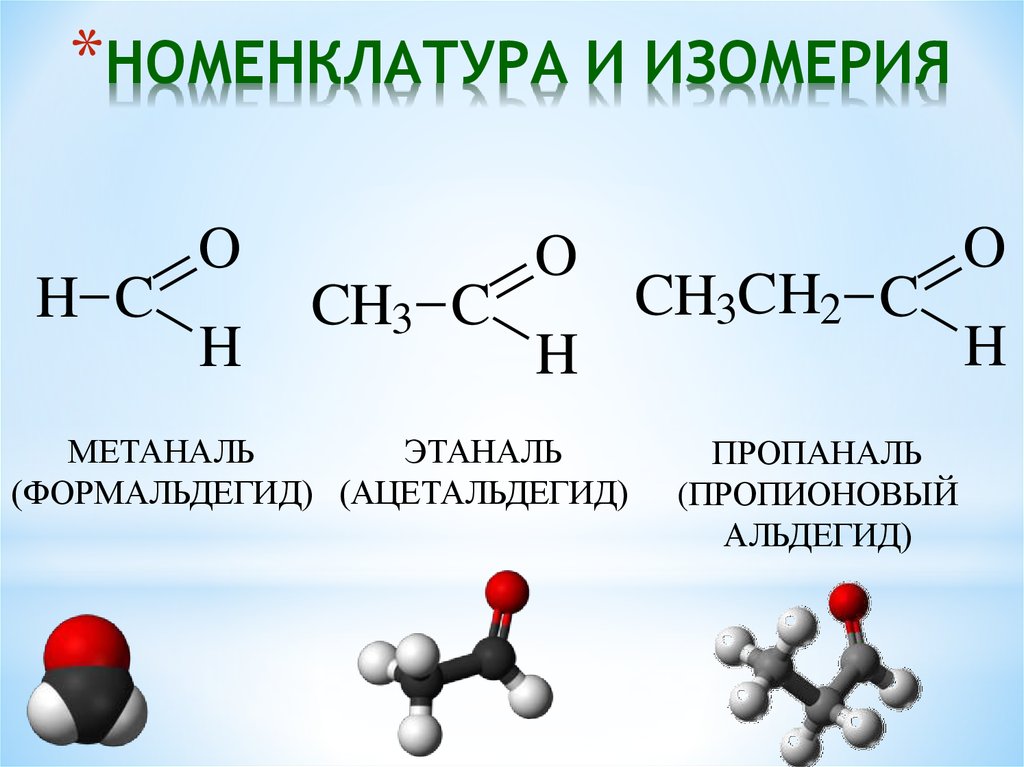
МЕТАНАЛЬ
ЭТАНАЛЬ
(ФОРМАЛЬДЕГИД) (АЦЕТАЛЬДЕГИД)
6
ПРОПАНАЛЬ
(ПРОПИОНОВЫЙ
АЛЬДЕГИД)
O
H
7. ИЗОМЕРИЯ
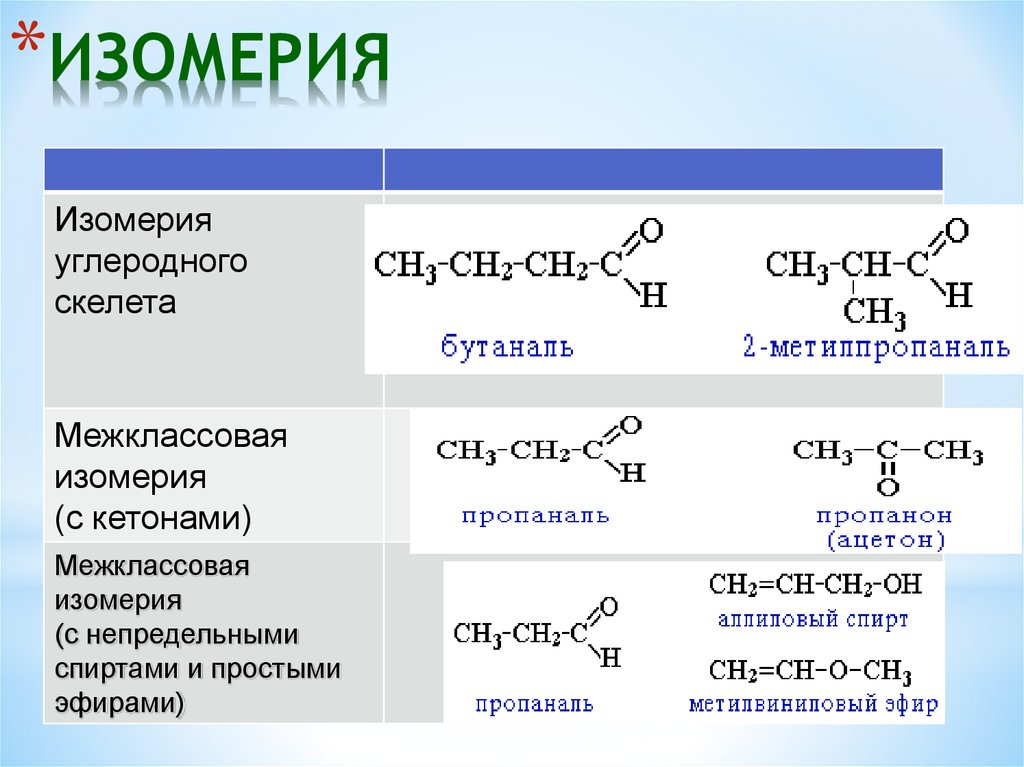
*ИЗОМЕРИЯИзомерия
углеродного
скелета
Межклассовая
изомерия
(с кетонами)
Межклассовая
изомерия
(с непредельными
спиртами и простыми
эфирами)
8. СПОСОБЫ ПОЛУЧЕНИЯ
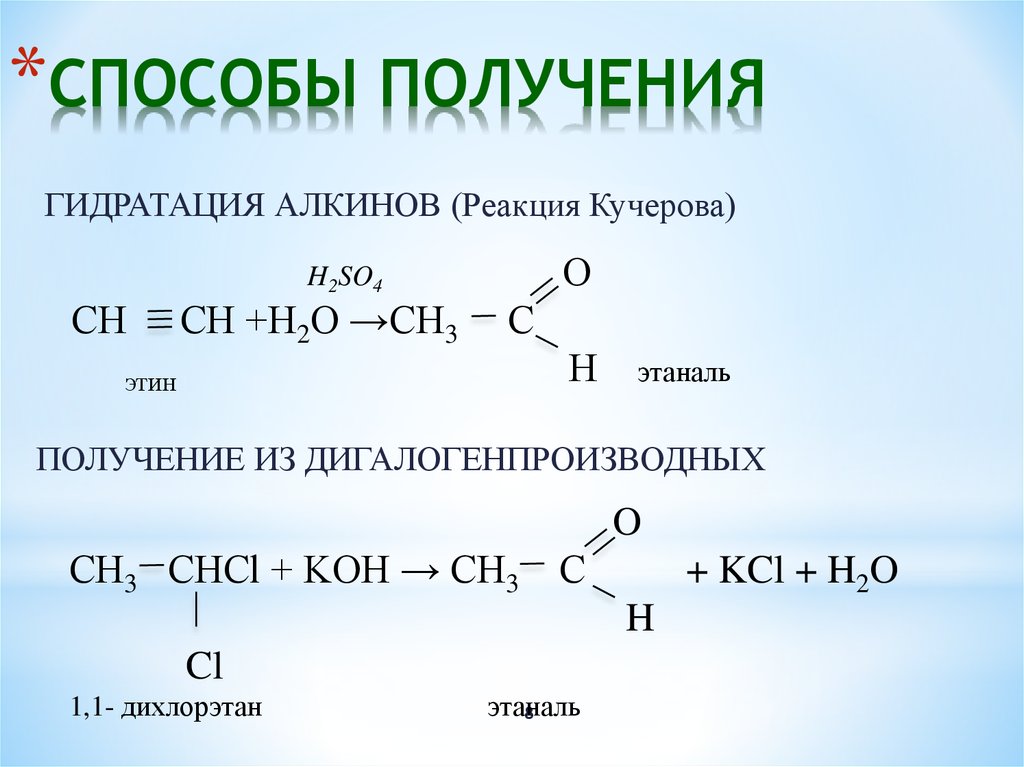
*СПОСОБЫ ПОЛУЧЕНИЯГИДРАТАЦИЯ АЛКИНОВ (Реакция Кучерова)
О
H2SO4
СН
СН +Н2О →СН3
С
Н
этин
этаналь
ПОЛУЧЕНИЕ ИЗ ДИГАЛОГЕНПРОИЗВОДНЫХ
O
СН3 СНСl + KOH → СН3
С
+ KCl + H2O
H
Cl
1,1- дихлорэтан
этаналь
8
9. СПОСОБЫ ПОЛУЧЕНИЯ
*СПОСОБЫ ПОЛУЧЕНИЯОкисление
спиртов
O
CuО,t
//
CH3 – CH2 – CH2 – OH CH3 – CH2 –– C + H2О + Cu
\
H
Cu,t
СH3 – CH – CH3 CH3 – C – CH3 + H2О + Cu
|
||
OH
O
пропанон - 2 (ацетон)
9
10. СПОСОБЫ ПОЛУЧЕНИЯ
*СПОСОБЫПОЛУЧЕНИЯ
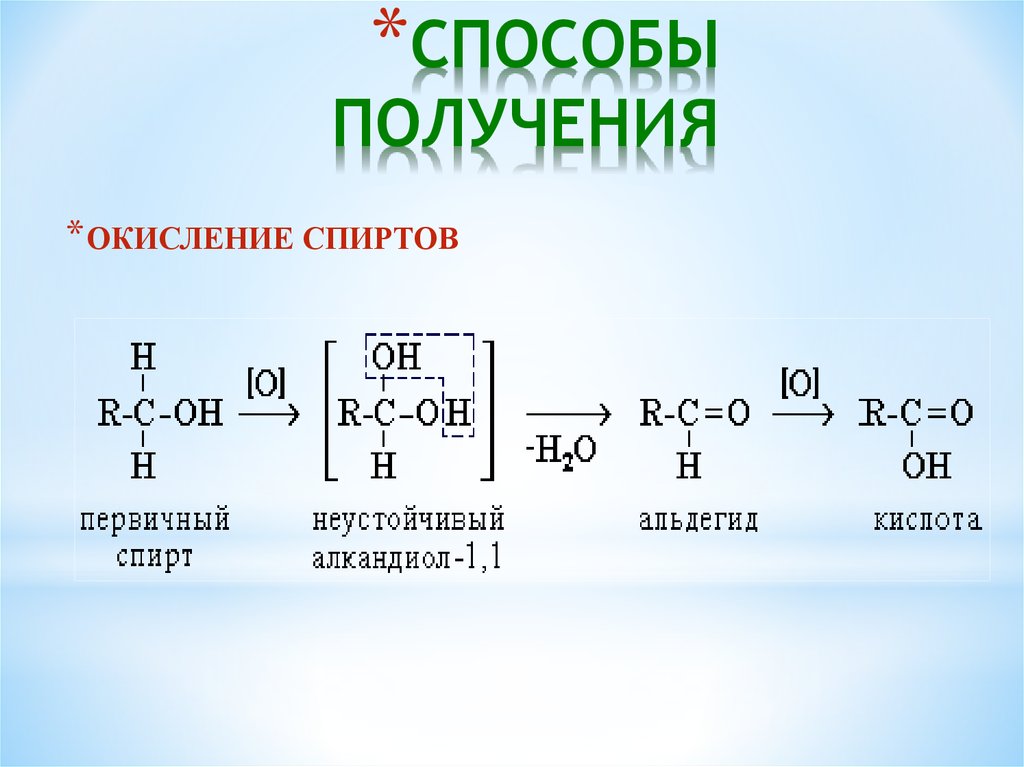
* ОКИСЛЕНИЕ СПИРТОВ
11. СПОСОБЫ ПОЛУЧЕНИЯ
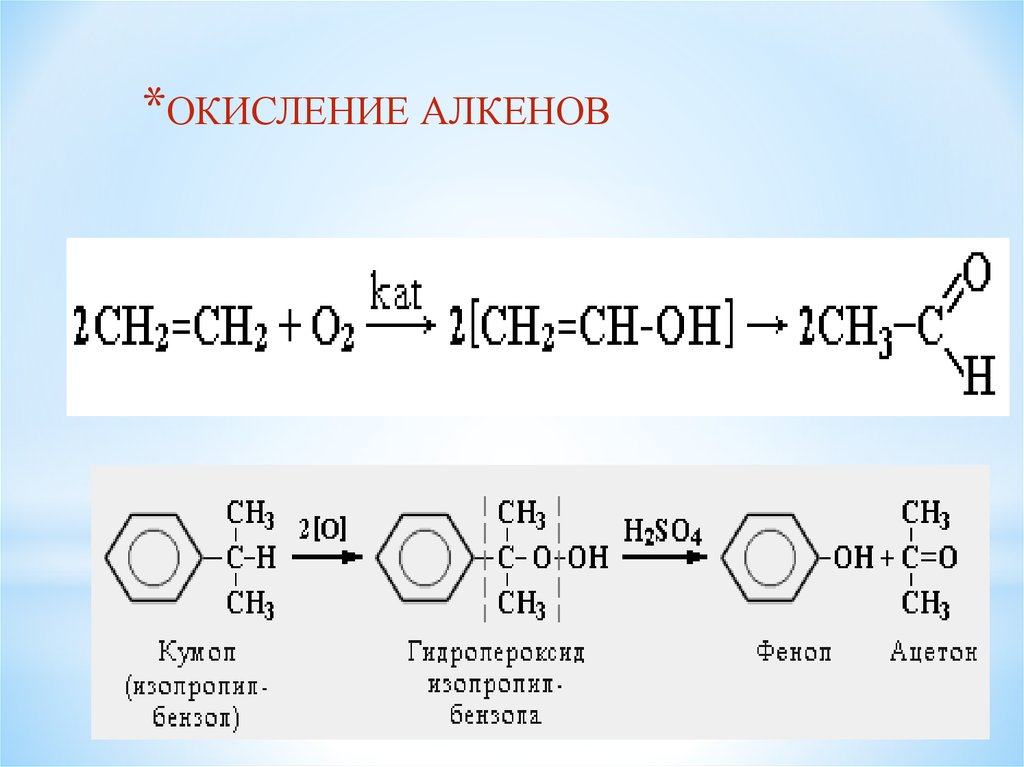
*ОКИСЛЕНИЕ АЛКЕНОВ* КУМОЛЬНЫЙ СПОСОБ
*СПОСОБЫ
ПОЛУЧЕНИЯ
12. ХИМИЧЕСКИЕ СВОЙСТВА
*ХИМИЧЕСКИЕ СВОЙСТВАРЕАКЦИИ ОКИСЛЕНИЯ
Реакция серебряного зеркала
О
СН3 С
+ 2[Ag(NH3)2]OH → СН3
Н
12
О
С + Ag + 4NH3 + 2H2O
OН
13. ХИМИЧЕСКИЕ СВОЙСТВА
*ХИМИЧЕСКИЕ СВОЙСТВАРЕАКЦИИ ОКИСЛЕНИЯ
Реакция с гидроксидом меди
СН3 С
этаналь
О
О
+ 2Cu(OH)2 → СН3 С
+ 2H2O + Cu2O
OН
гидроксид
Н
этановая кислота
меди (I)
(кирпично-красный)
14. ХИМИЧЕСКИЕ СВОЙСТВА
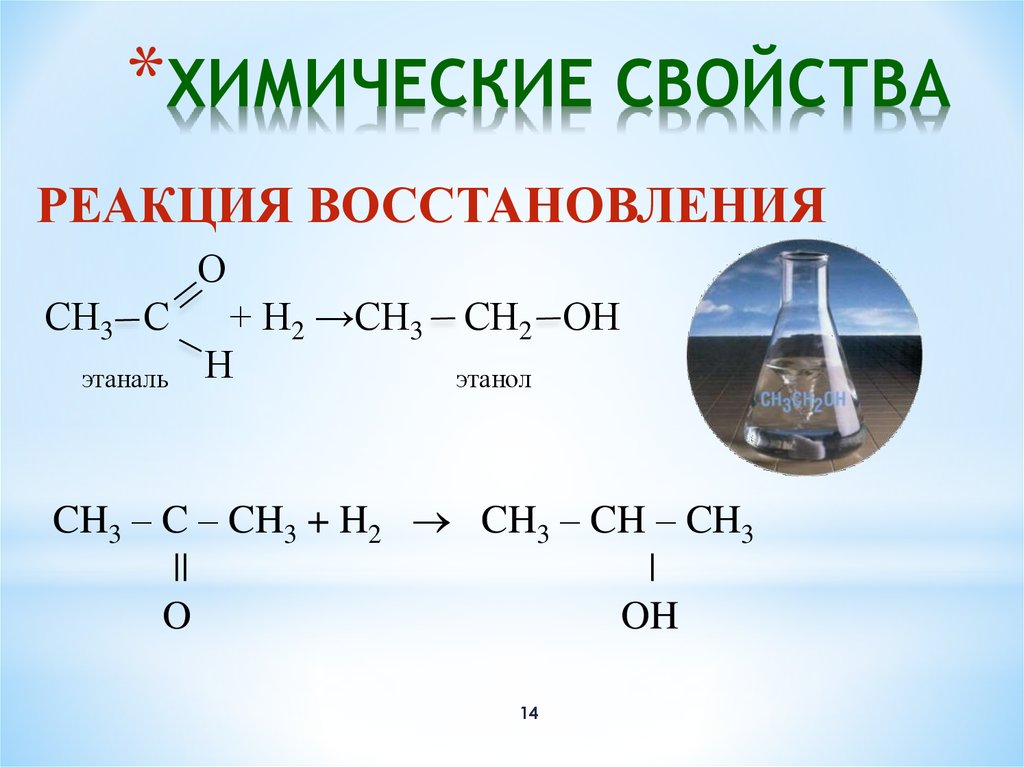
*ХИМИЧЕСКИЕ СВОЙСТВАРЕАКЦИЯ ВОССТАНОВЛЕНИЯ
О
СН3 С
этаналь
+ Н2 →СН3
Н
СН2 ОН
этанол
CH3 – C – CH3 + H2 CH3 – CH – CH3
||
|
O
OH
14
15. ХИМИЧЕСКИЕ СВОЙСТВА
*ХИМИЧЕСКИЕСВОЙСТВА
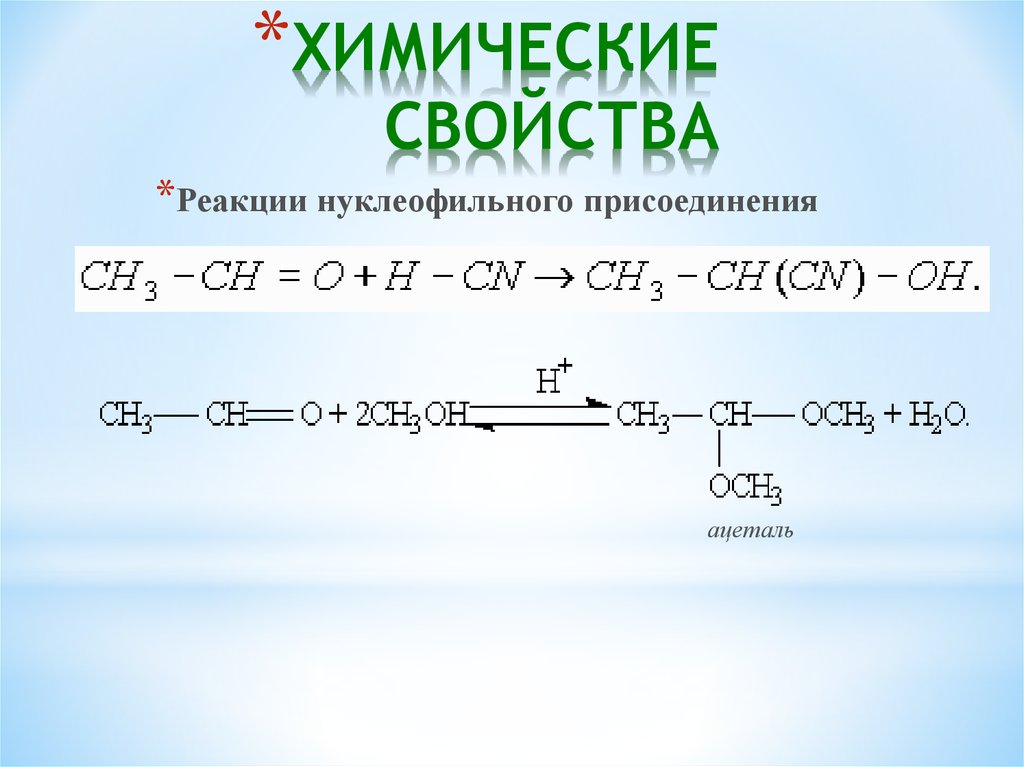
*Реакции нуклеофильного присоединения
синильная к-та
гидроксинитрил
ацеталь
16. ХИМИЧЕСКИЕ СВОЙСТВА
*ХИМИЧЕСКИЕСВОЙСТВА
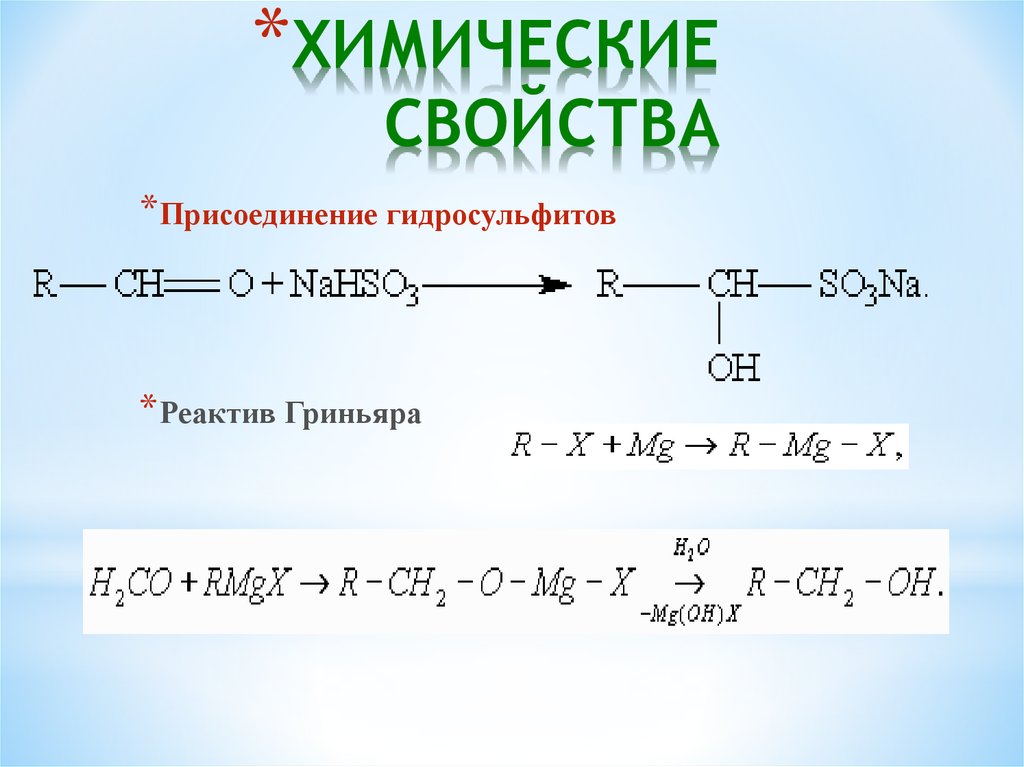
* Присоединение гидросульфитов
* Реактив Гриньяра
17.
18. ХИМИЧЕСКИЕ СВОЙСТВА
*ХИМИЧЕСКИЕСВОЙСТВА
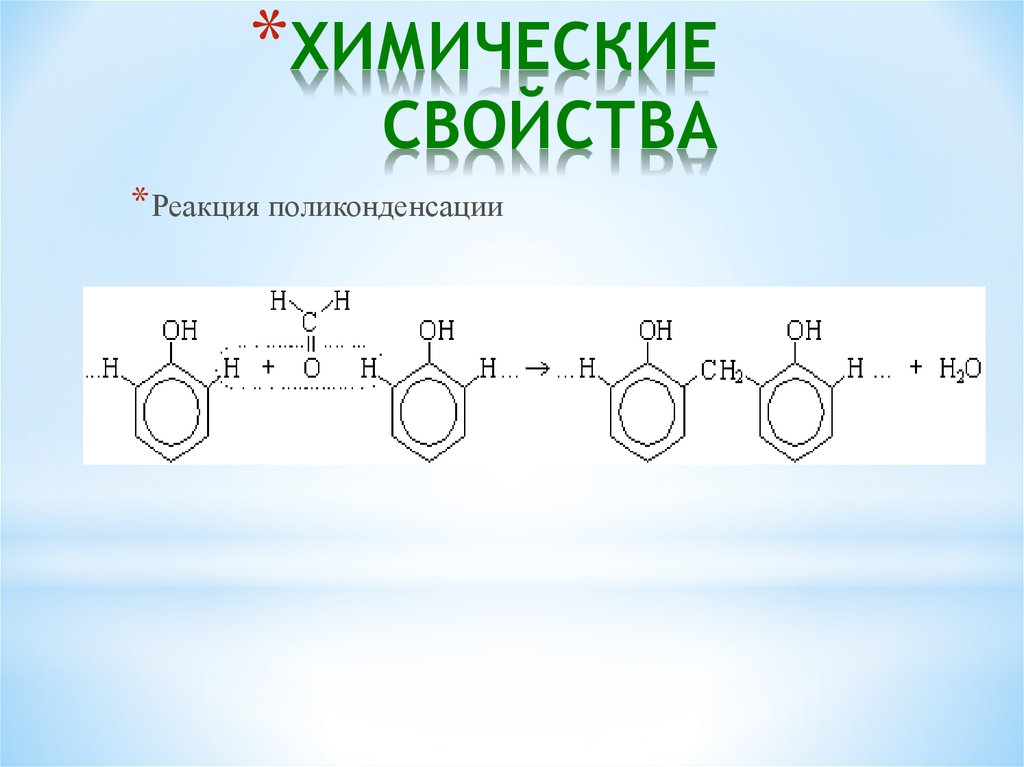
* Реакция поликонденсации
19. Кето-енольная таутомерия
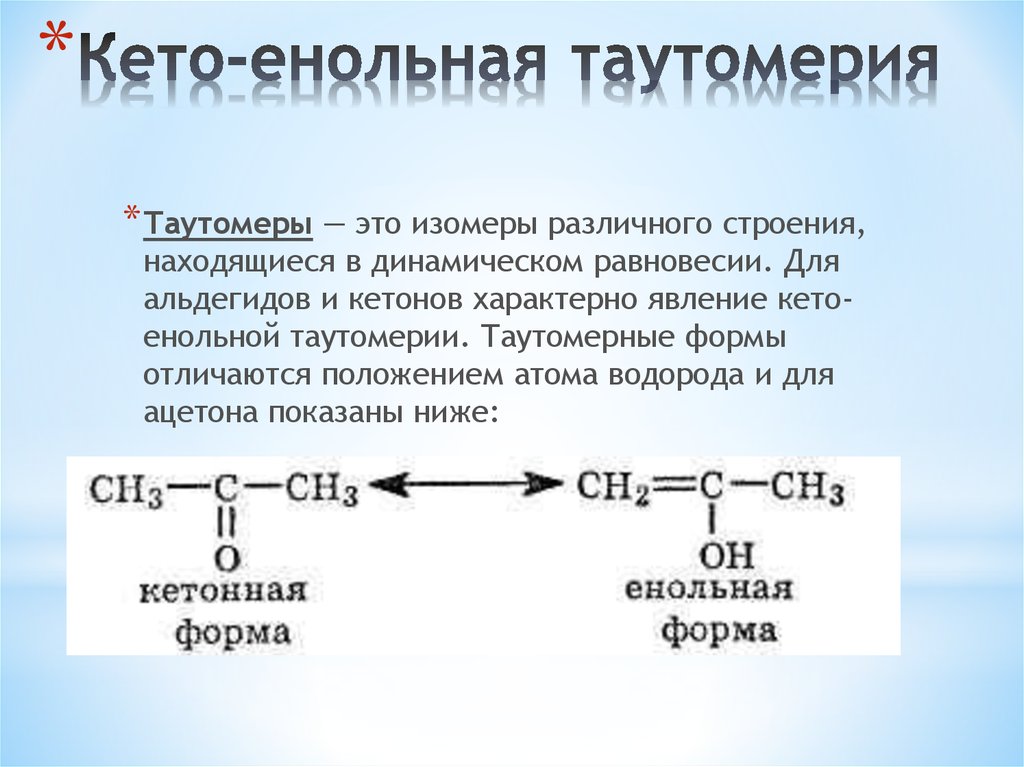
** Таутомеры — это изомеры различного строения,
находящиеся в динамическом равновесии. Для
альдегидов и кетонов характерно явление кетоенольной таутомерии. Таутомерные формы
отличаются положением атома водорода и для
ацетона показаны ниже:
20. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
*ПРИМЕНЕНИЕ АЛЬДЕГИДОВПАРФЮМЕРИЯ
• Альдегид анисовый, обепин
– жидкость с приятным
запахом мимозы
• Альдегид дециловый,
деканаль – при разбавлении
появляются нотки запаха
апельсиновой корки
21.
ЦитральЗапах
цитрусовых
обусловлен
данным
диеновым
альдегидом. Его применяют в качестве отдушки средств
бытовой химии, косметических и парфюмерных веществ.
22.
Альдегиды в природеКоричный альдегид
Коричный альдегид содержится в масле корицы, его
получают перегонкой коры дерева корицы .
Применяется в кулинарии в виде палочек или порошка.
23.
Альдегиды в природеБензальдегид
Бензальдегид – жидкость с запахом горького
миндаля.
Встречается в косточках и семечках,
особенно в абрикосах и персиках.
24.
Кетоны в природеГептанон-2
Это соединение представляет собой жидкость
гвоздичным запахом.
Гептаноном-2 обусловлен запах многих плодов
молочных продуктов, например, сыра «Рокфор»
с
и
25.
n-Гидроксифенилбутанон-2Этот кетон обуславливает в основном запах
спелых ягод малины.
Его включают в состав синтетических
душистых композиций
26. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
* ПРИМЕНЕНИЕ АЛЬДЕГИДОВПОЛИМЕРНЫЕ МАТЕРИАЛЫ
Фенолформальдегидные смолы
27. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
* ПРИМЕНЕНИЕ АЛЬДЕГИДОВПРОИЗВОДСТВО ВЕЩЕСТВ
Уксусная кислота
Этилацетат
Формалин















 Химия
Химия








