Похожие презентации:
Функциональные производные одноосновных карбоновых кислот. Лекция
1.
Лекция 12.10.2024Функциональные производные
одноосновных карбоновых
кислот
Лектор Ибрагимов Ш.Н.
2.
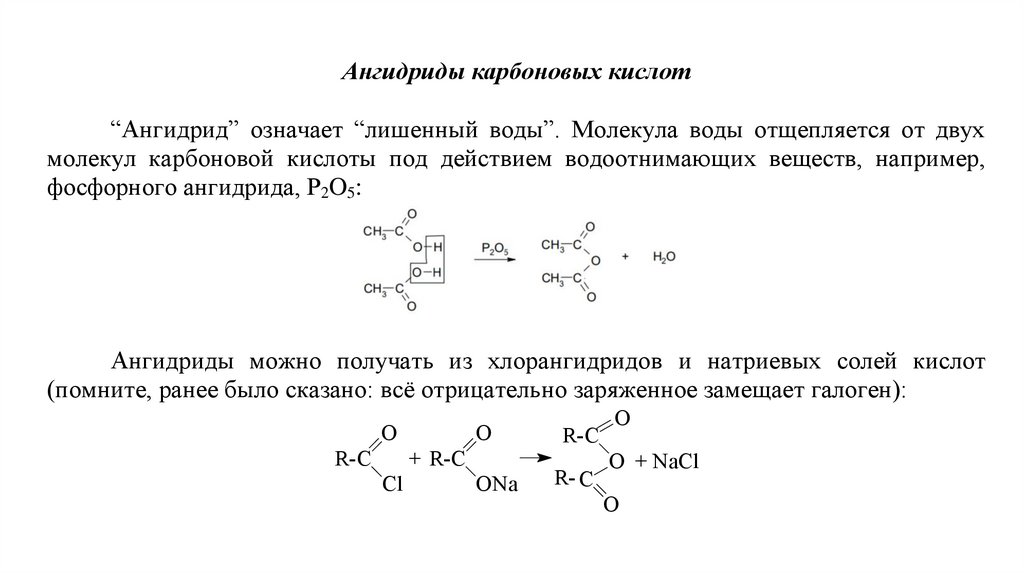
Ангидриды карбоновых кислот“Ангидрид” означает “лишенный воды”. Молекула воды отщепляется от двух
молекул карбоновой кислоты под действием водоотнимающих веществ, например,
фосфорного ангидрида, P2O5:
Ангидриды можно получать из хлорангидридов и натриевых солей кислот
(помните, ранее было сказано: всё отрицательно заряженное замещает галоген):
O
R-C
O
+ R-C
Cl
ONa
R-C
R- C
O
O + NaCl
O
3.
Галогенангидриды (ацилгалогениды) карбоновых кислотАнгидриды минеральных кислот пятихлористый или треххлористый фосфор
(PCl5, PCl3); хлористый тионил (SOCl2); хлористый сульфурил (SO2Cl2) замещают
любые гидроксильные группы в любом соединении (органическом или
неорганическом). В случае карбоновых кислот образуются хлорангидриды карбоновых
кислот:
CH3COOH + PCl5
CH3C(O)Cl + POCl3 + HCl
4.
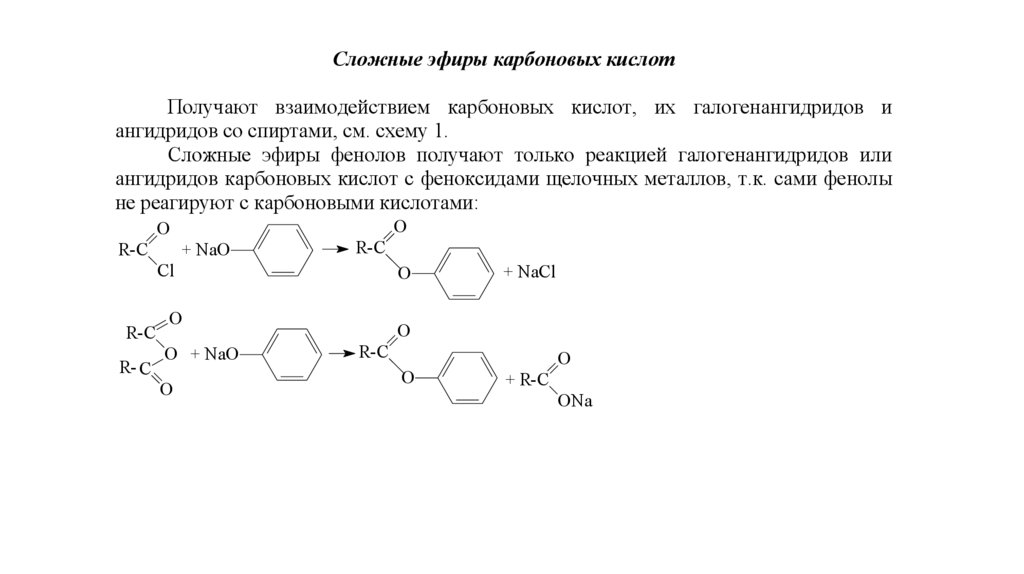
Сложные эфиры карбоновых кислотПолучают взаимодействием карбоновых кислот, их галогенангидридов и
ангидридов со спиртами, см. схему 1.
Сложные эфиры фенолов получают только реакцией галогенангидридов или
ангидридов карбоновых кислот с феноксидами щелочных металлов, т.к. сами фенолы
не реагируют с карбоновыми кислотами:
O
O
R-C
+ NaO
R-C
Cl
R-C
R- C
O
O
O + NaO
O
+ NaCl
O
R-C
O
O
+ R-C
ONa
5.
Амиды карбоновых кислотПолучают реакцией ангидридов или галогенангидридов карбоновых кислот с
аммиаком или аминами, см. схему 1.
Реакция карбоновых кислот с аммиаком протекает иначе. Она начинается с
образования аммонийных солей, которые при нагревании теряют воду и превращаются
в амиды:
Амиды можно получать гидролизом нитрилов. Реакция протекает по схеме
присоединения по π-связи нитрильной группы с изомеризацией продукта
присоединения:
CH3
C N + H2O
CH3
C
N
OH H
аналог енола
изомеризация
O
R-C
NH2
Аммиак и амины реагируют со сложными эфирами. Продукты реакции – амиды,
см. схему 1.
6.
Нитрилы карбоновых кислотПолучают дегидратацией амидов, а также реакцией замещения галогенов на
цианогруппу:
O
ToC
R-C
NH2 - H2O
CH3CH2Cl + KCN
R
C N
CH3CH2CN + KCl
Соли карбоновых кислот
Реакция была рассмотрена на предыдущей лекции.
7.
Химические свойства карбоновых кислот и их производныхЕще раз обращаю Ваше внимание на материал предыдущей лекции: все
реакции карбоновых кислот и их производных протекают по схеме
замещения остатка в ацильной группе на остаток молекулы второго
участника реакции. Это положение подтверждается уравнениями
реакций, приведенными в схеме 1.
8.
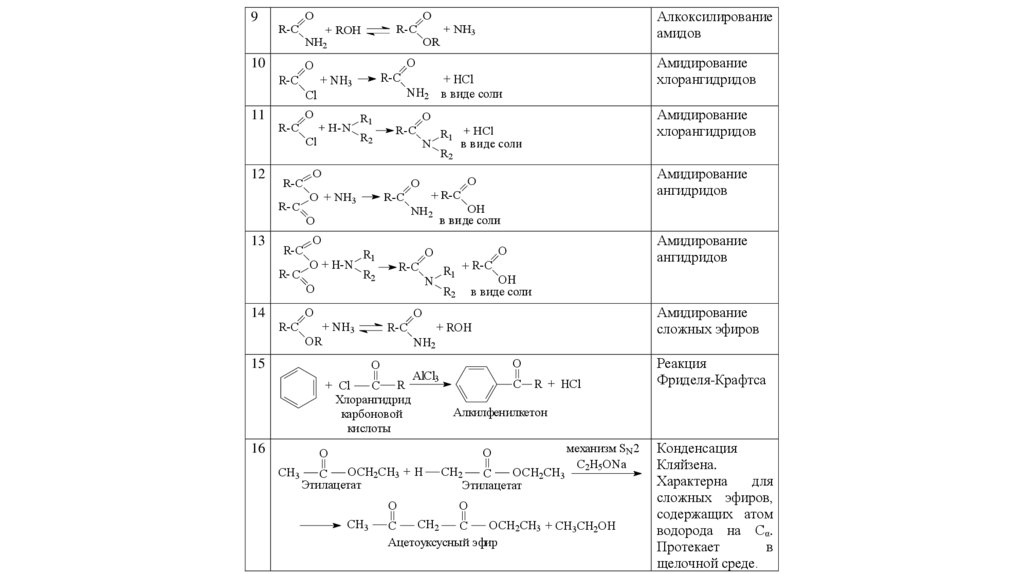
Схема 1.Реакции карбоновых кислот и их производных
(Взаимные превращения карбоновых кислот и их производных).
Общий вид реакции
1
O
R-C
Cl
2
R-C
R- C
O
+ H2O
2R-C
OH
O
R-C
O
+ H2O
R-C
+ ROH
OH
O
R-C
Гидролиз
ангидридов
O
O + H2O
OR
4
+ HCl
OH
O
O
3
R-C
O
+ H2O
NH2
Тип реакции
Гидролиз
хлорангидридов
R-C
+ NH3
OH
в виде соли
Гидролиз
сложных
эфиров
Гидролиз
амидов
9.
O5
O
R-C
+ ROH
R-C
OH
6
O
R-C
R-C
R- C
+ ROH
+ HCl
R-C
OR
O
O + ROH
O
R-C
+ R1OH
OR
+ R-C
R-C
+ ROH
OR1
Этерификация
ангидридов
OH
O
O
R-C
O
OR
O
8
Этерификация
хлорангидридов
O
Cl
7
OR
+ H2O
Этерификация
кислот
Переэтерификация
сложных эфиров
10.
9O
R-C
+ ROH
NH2
10
Cl
11
+ H-N
R-C
R-C
+ NH3
O
R-C
R1
R2
R-C
R- C
O
R-C
O
14
+ R-C
O
O
N
OH
в виде соли
R2
Амидирование
сложных эфиров
O
OR
+ NH3
R-C
+ ROH
NH2
15
O
+ Cl
C R
Хлорангидрид
карбоновой
кислоты
O
AlCl3
C
R + HCl
O
OCH2CH3 + H
C
Этилацетат
O
CH3
Реакция
Фриделя-Крафтса
Алкилфенилкетон
O
CH3
Амидирование
ангидридов
R1 + R-C
R-C
R2
Амидирование
ангидридов
O
OH
в виде соли
O
R-C
16
R2
NH2
O
R1
+ HCl
в виде соли
R1
N
O
O + H-N
Амидирование
хлорангидридов
O
R-C
O
13
Амидирование
хлорангидридов
+ HCl
в виде соли
NH2
O + NH3
R- C
+ NH3
O
Cl
12
OR
O
R-C
Алкоксилирование
амидов
O
R-C
CH2
OCH2CH3
C
Этилацетат
механизм SN2
C2H5ONa
O
CH2
OCH2CH3 + CH3CH2OH
C
C
Ацетоуксусный эфир
Конденсация
Кляйзена.
Характерна
для
сложных эфиров,
содержащих атом
водорода на Сα.
Протекает
в
щелочной среде.







 Химия
Химия








