Похожие презентации:
Свойства оснований
1.
Ильина И.В., руководитель ЦДОШ, учитель химии МБОУ «Средняяобщеобразовательная школа №27 имени А.А. Дейнеки» г. Курска
E-mail мой: ilina.irina71@mail.ru
2.
Свойства оснований3.
Основание – сложные вещества, которые состоятиз металла и одной или несколько гидроксогрупп
Общая формула Ме(ОН)n
Окрашивают лакмус в синий цвет
Окрашивают метиловый оранжевый
в жёлтый цвет
Окрашивают фенолфталеин в
малиновый цвет
4.
Щёлочи –растворимые в воде
основания
Вступают в реакцию
нейтрализации с
кислотами
5.
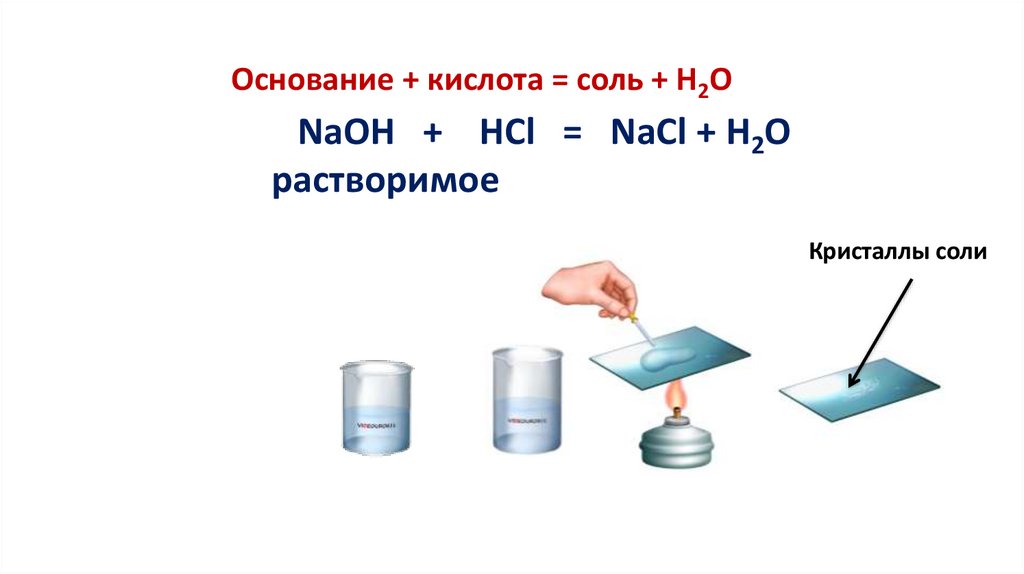
Основание + кислота = соль + Н2ОNaOH + HCl = NaCl + H2O
растворимое
Кристаллы соли
6.
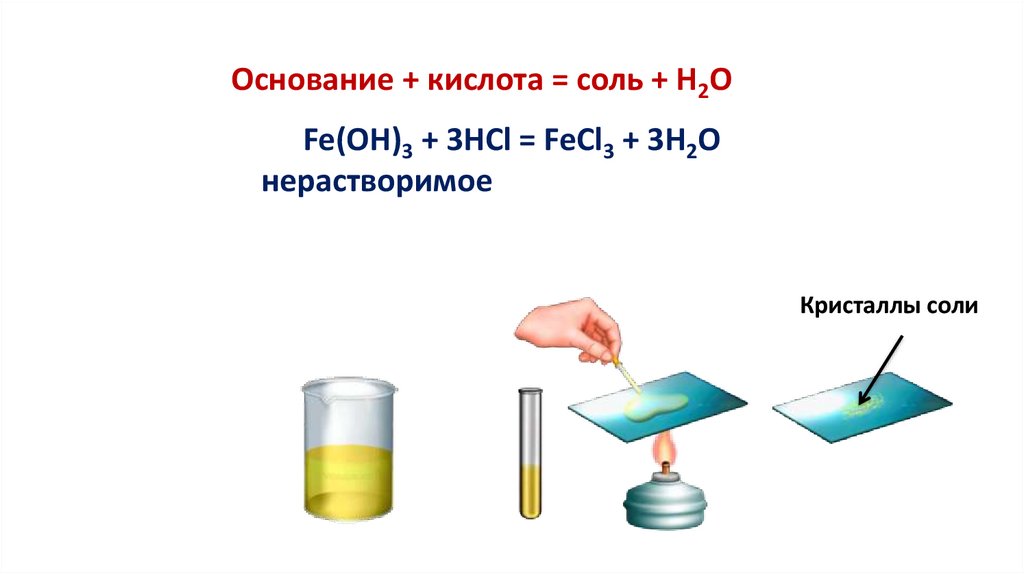
Основание + кислота = соль + Н2ОFe(OH)3 + 3HCl = FeCl3 + 3H2O
нерастворимое
Кристаллы соли
7.
Нерастворимые основанияпри нагревании разлагаются
Щёлочи при нагревании
не разлагаются
8.
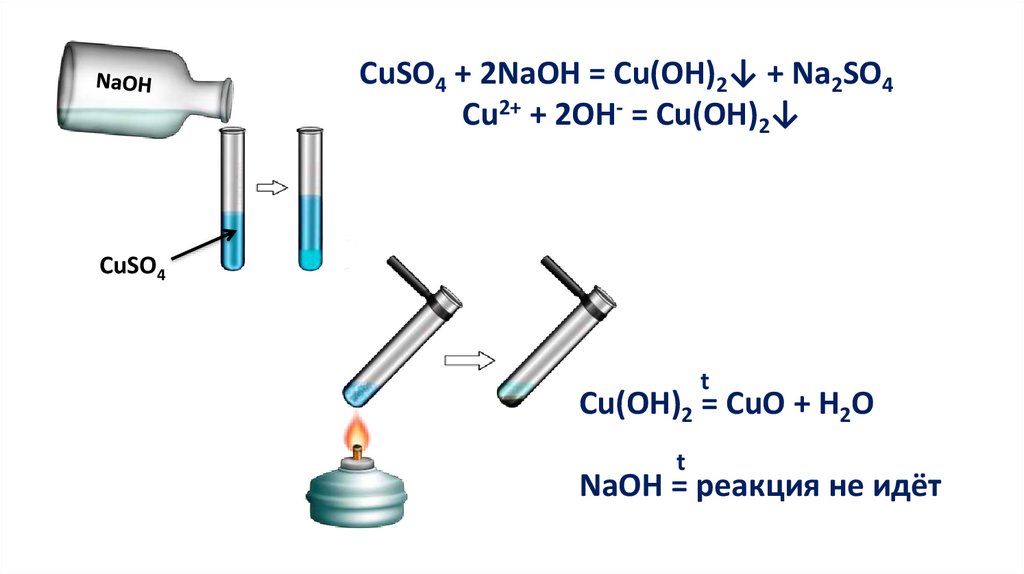
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4Cu2+ + 2OH- = Cu(OH)2↓
CuSO4
t
Cu(OH)2 = CuO + H2O
t
NaOH = реакция не идёт
9.
Щёлочи вступают вреакцию обмена с
растворимыми солями
Образуется новая соль и
новое основание
Должен образоваться
осадок (нерастворимое
основание) или газ
10.
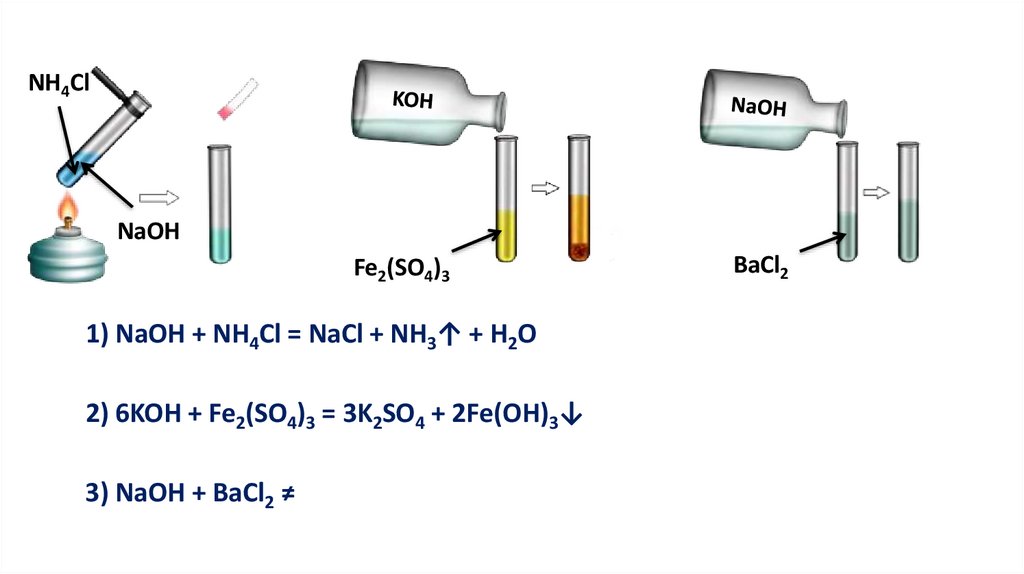
NH4ClNaOH
Fe2(SO4)3
1) NaOH + NH4Cl = NaCl + NH3↑ + H2O
2) 6KOH + Fe2(SO4)3 = 3K2SO4 + 2Fe(OH)3↓
3) NaOH + BaCl2 ≠
BaCl2
11.
Щёлочи реагируют скислотными и
амфотерными оксидами
12.
Реакции с амфотерными основаниямиZn(OH)2 + 2NaOH = Na2[Zn(OH)4]
тетрагидроксоцинкат
натрия
t
Zn(OH)2 + 2NaOH = Na2ZnO2 + 2H2O
цинкат натрия
13.
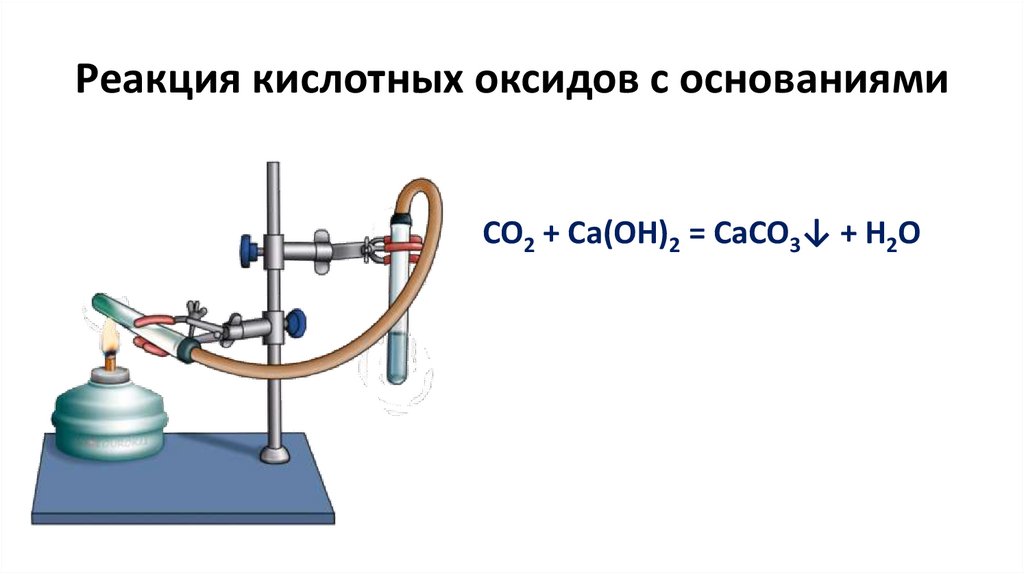
Реакция кислотных оксидов с основаниямиCO2 + Ca(OH)2 = CaCO3↓ + H2O
14.
Мы – жители непростые,Нас очень много на Земле!
Особым даром обладая,
Мы растворяемся в воде.
А как на кожу попадём,
Мы тут же сильно обожжем.
Окрасим лакмус в синий цвет,
Без нас нейтрализации нет.
Без нас не обойдётесь тут!
Скажите, как же нас зовут?
Щёлочи
15.
Домашнее задание1. Параграф 24
2. Упражнения №1, №3 и №4 (после параграфа)
Пишите в электронный журнал или на мою почту.
E-mail мой: ilina.irina71@mail.ru










 Химия
Химия








