Похожие презентации:
Спирты, фенолы, простые эфиры и их тиоаналоги. (Лекция 9)
1. Спирты, фенолы, простые эфиры и их тиоаналоги
2.
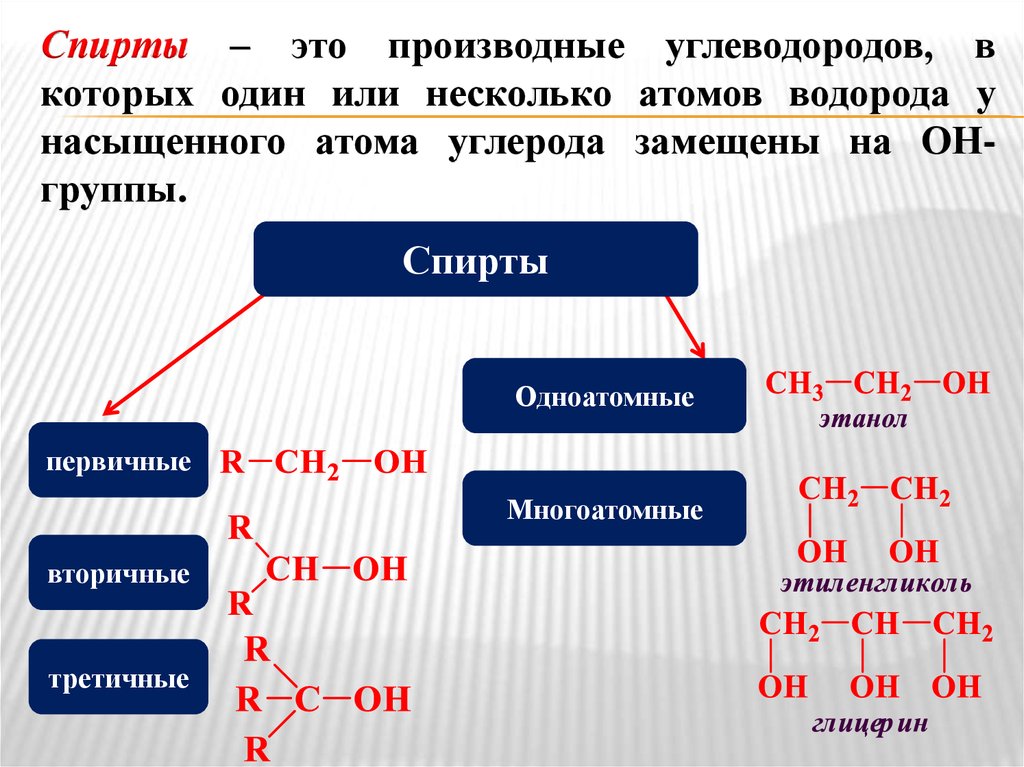
Спирты – это производные углеводородов, вкоторых один или несколько атомов водорода у
насыщенного атома углерода замещены на ОНгруппы.
Спирты
Одноатомные
первичные
Многоатомные
вторичные
третичные
3. Способы получения одноатомных спиртов
Гидратация алкеновЩелочной гидролиз галогенпроизводных
Восстановление карбонильных соединений
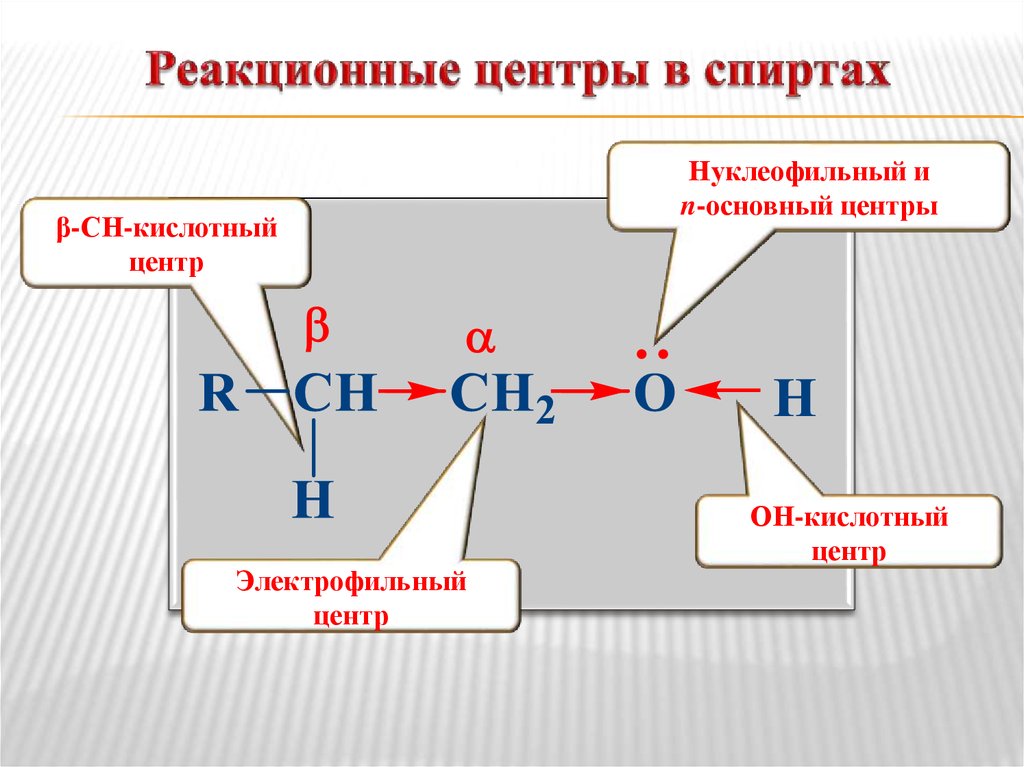
4. Реакционные центры в спиртах
β-СН-кислотныйцентр
Электрофильный
центр
Нуклеофильный и
n-основный центры
ОН-кислотный
центр
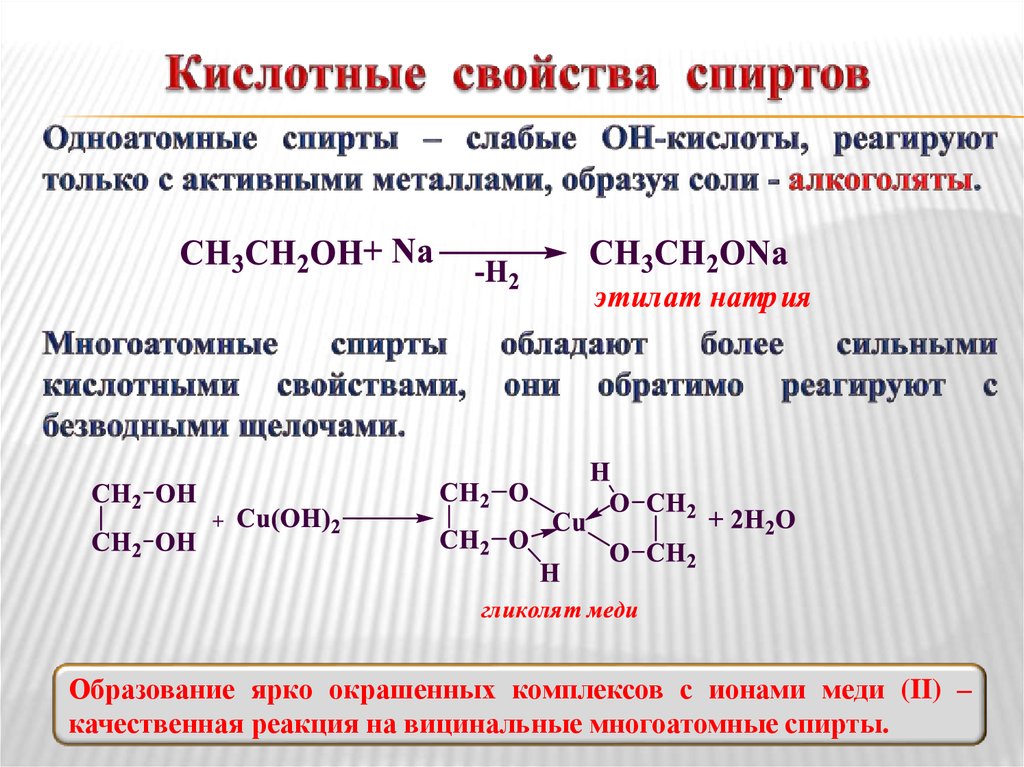
5. Кислотные свойства спиртов
Образование ярко окрашенных комплексов с ионами меди (II) –качественная реакция на вицинальные многоатомные спирты.
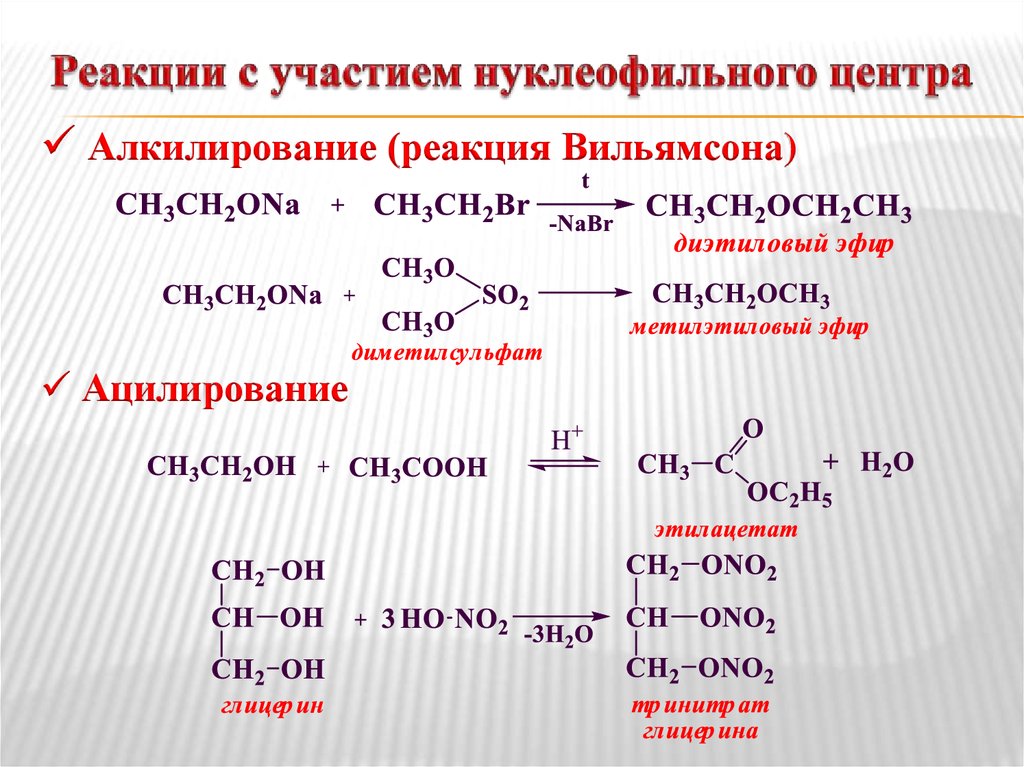
6. Реакции с участием нуклеофильного центра
Алкилирование (реакция Вильямсона)Ацилирование
7. Реакции с участием электрофильного центра
ОН-группа является плохо уходящей группой, поэтому , чтобы еезаместить, необходимо превратить ее в хорошо уходящую группу (Н2О) .
Проба Лукаса
Третичные спирты - быстрое расслоение смеси на 2 фазы;
Вторичные спирты – медленное помутнение с постепенным
расслоением на 2 фазы;
Первичные спирты – прозрачные, изменений нет.
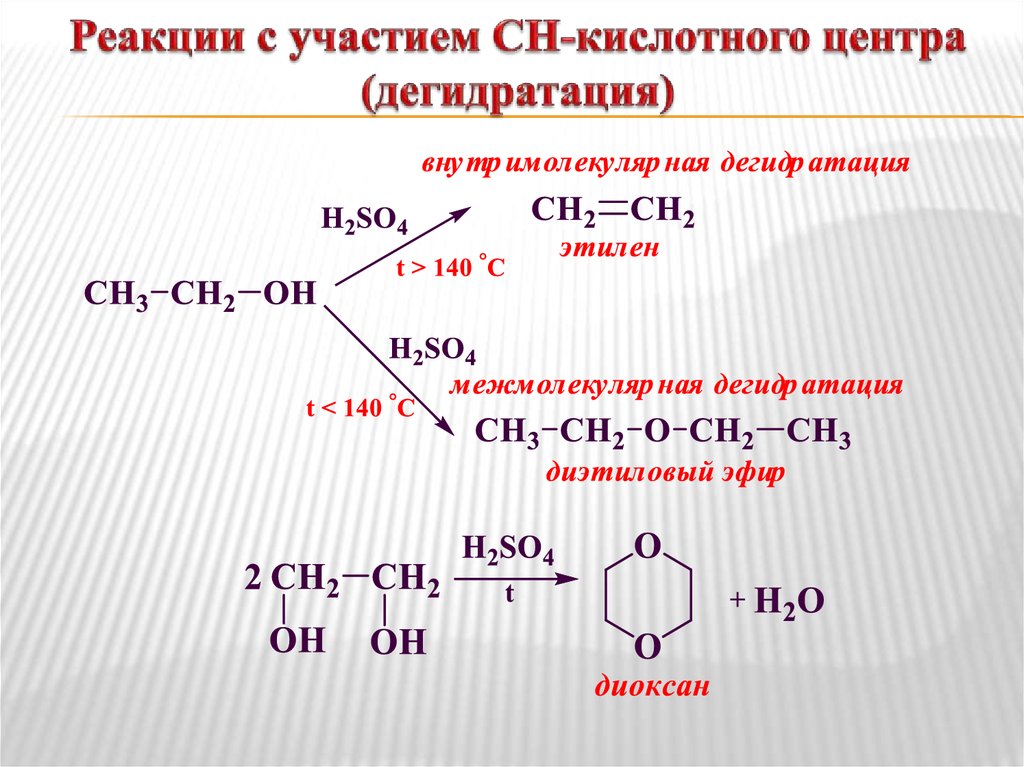
8. Реакции с участием СН-кислотного центра (дегидратация)
9. Окисление спиртов
Первичные спирты окисляются до альдегидов, а затем – докарбоновых кислот
Вторичные спирты окисляются легче первичных до
кетонов
Гликольное расщепление вицинальных диолов
10.
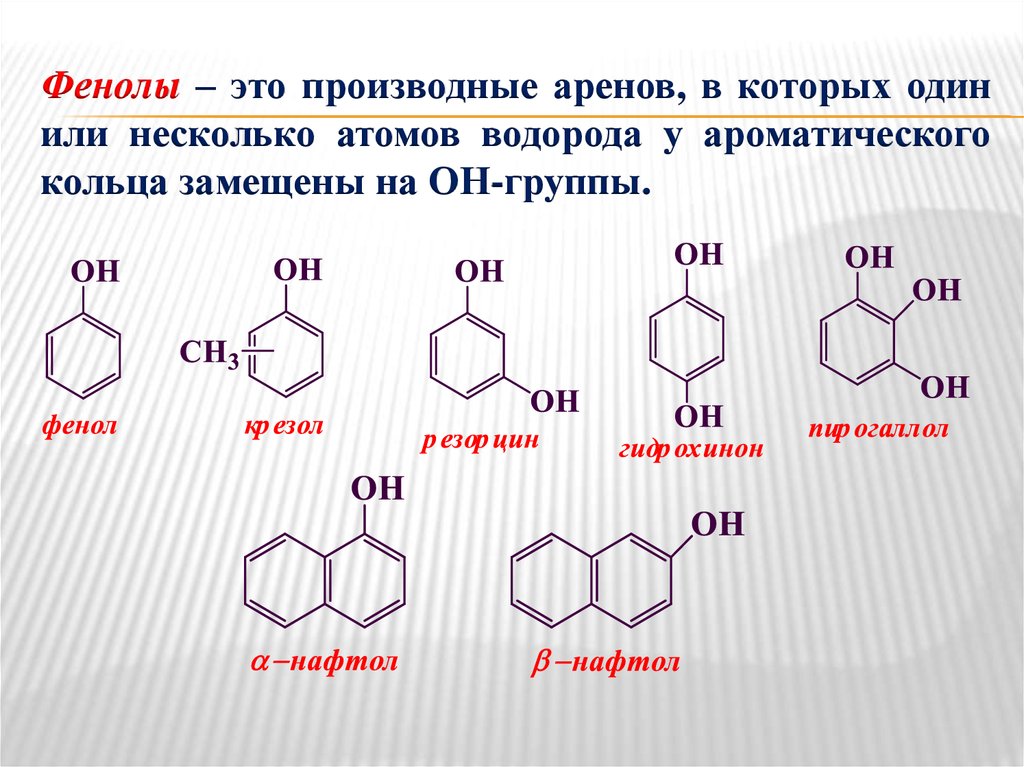
Фенолы – это производные аренов, в которых одинили несколько атомов водорода у ароматического
кольца замещены на ОН-группы.
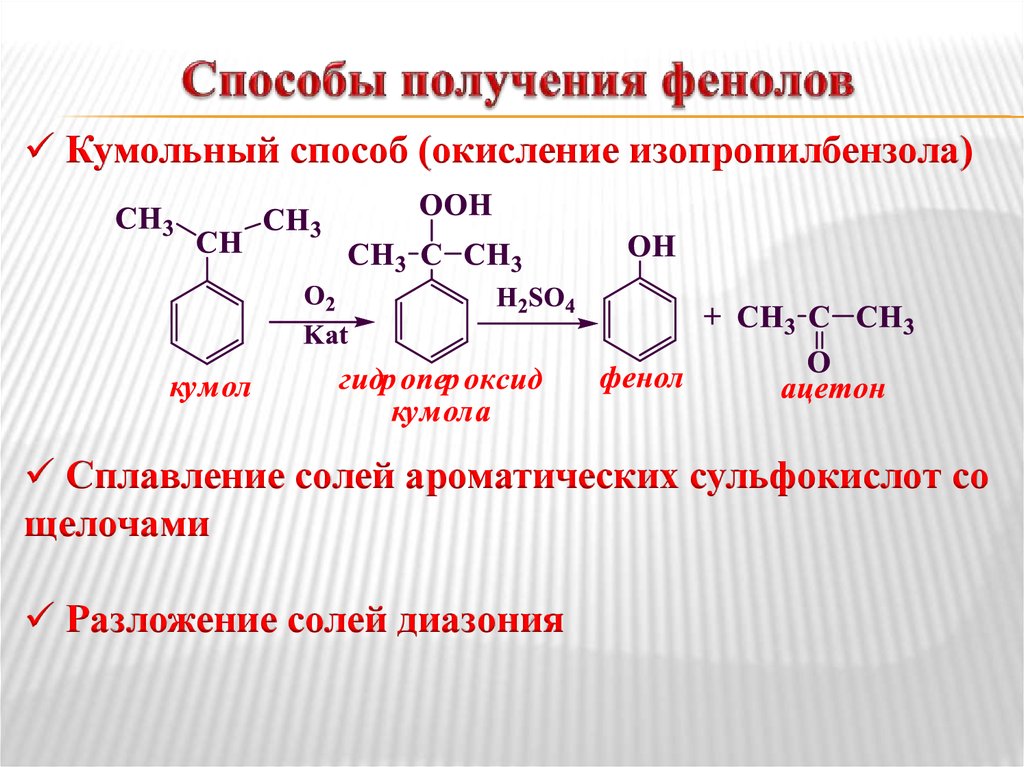
11. Способы получения фенолов
Кумольный способ (окисление изопропилбензола)Сплавление солей ароматических сульфокислот со
щелочами
Разложение солей диазония
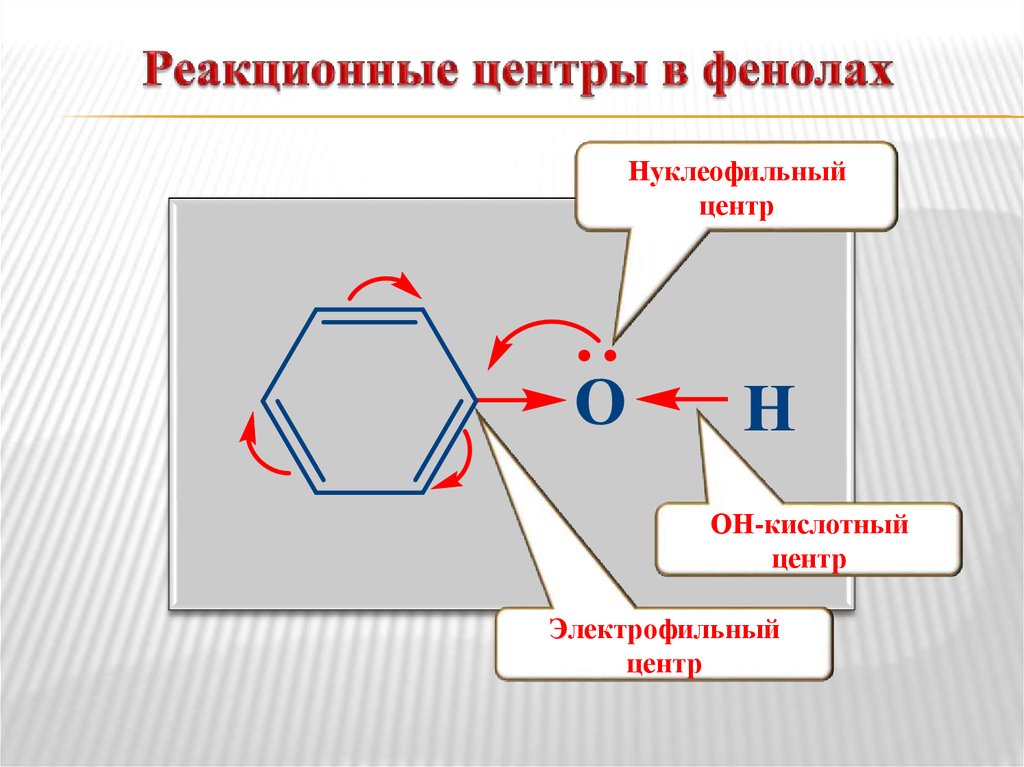
12. Реакционные центры в фенолах
Нуклеофильныйцентр
ОН-кислотный
центр
Электрофильный
центр
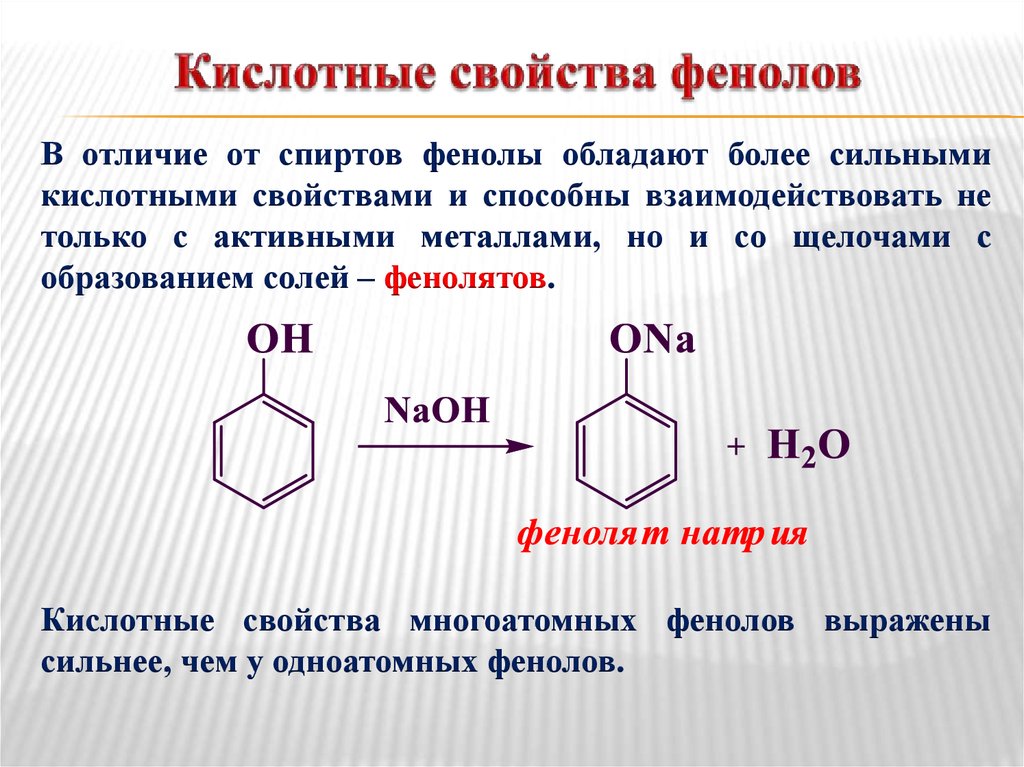
13. Кислотные свойства фенолов
В отличие от спиртов фенолы обладают более сильнымикислотными свойствами и способны взаимодействовать не
только с активными металлами, но и со щелочами с
образованием солей – фенолятов.
Кислотные свойства многоатомных фенолов выражены
сильнее, чем у одноатомных фенолов.
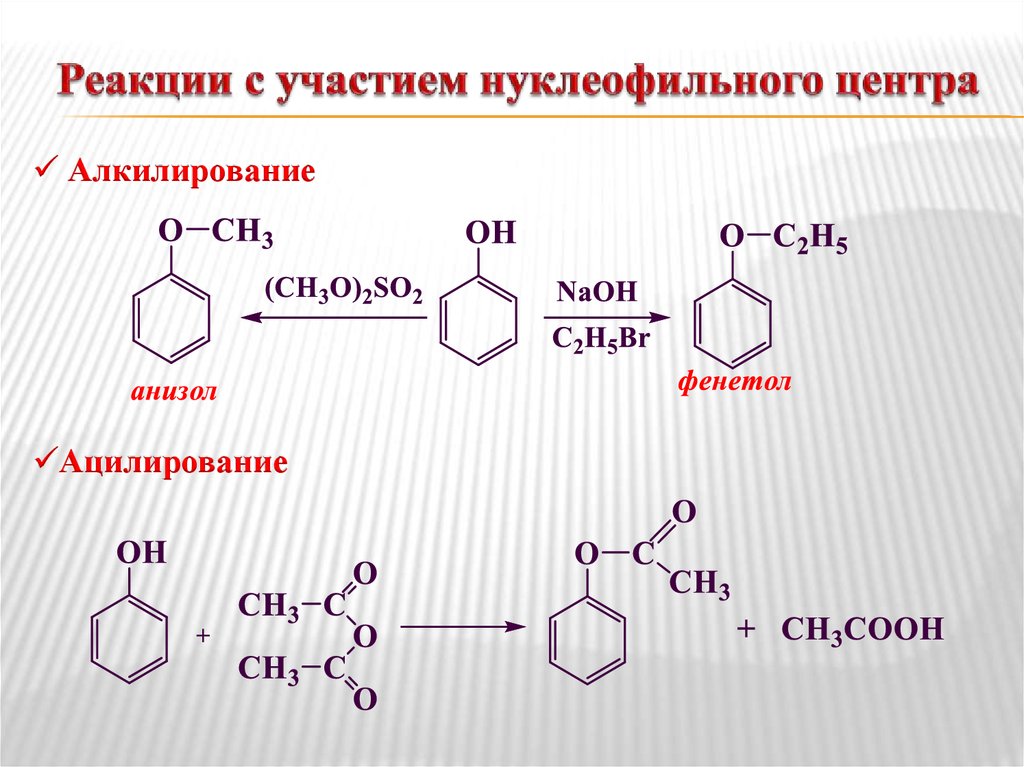
14. Реакции с участием нуклеофильного центра
АлкилированиеАцилирование
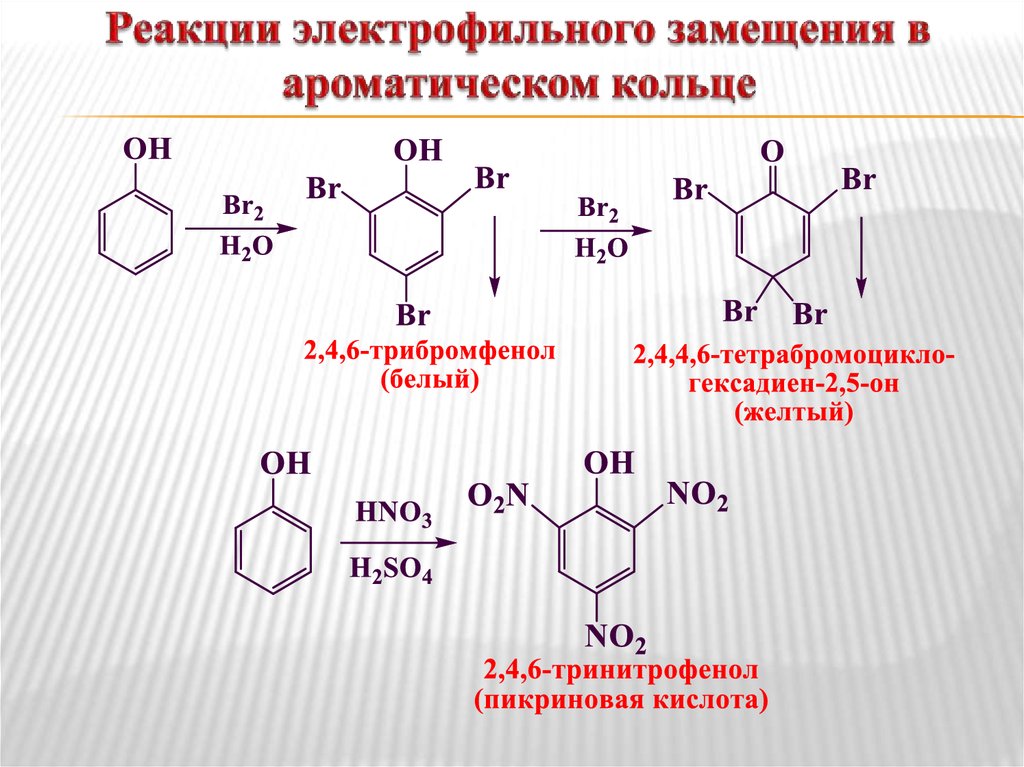
15. Реакции электрофильного замещения в ароматическом кольце
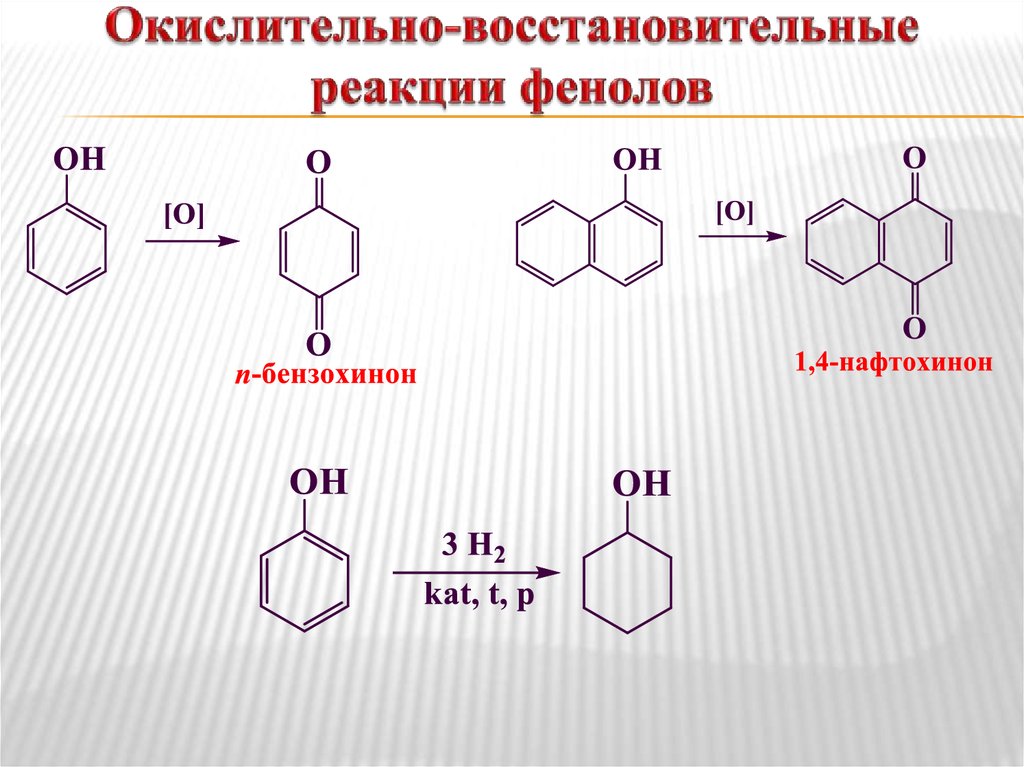
16. Окислительно-восстановительные реакции фенолов
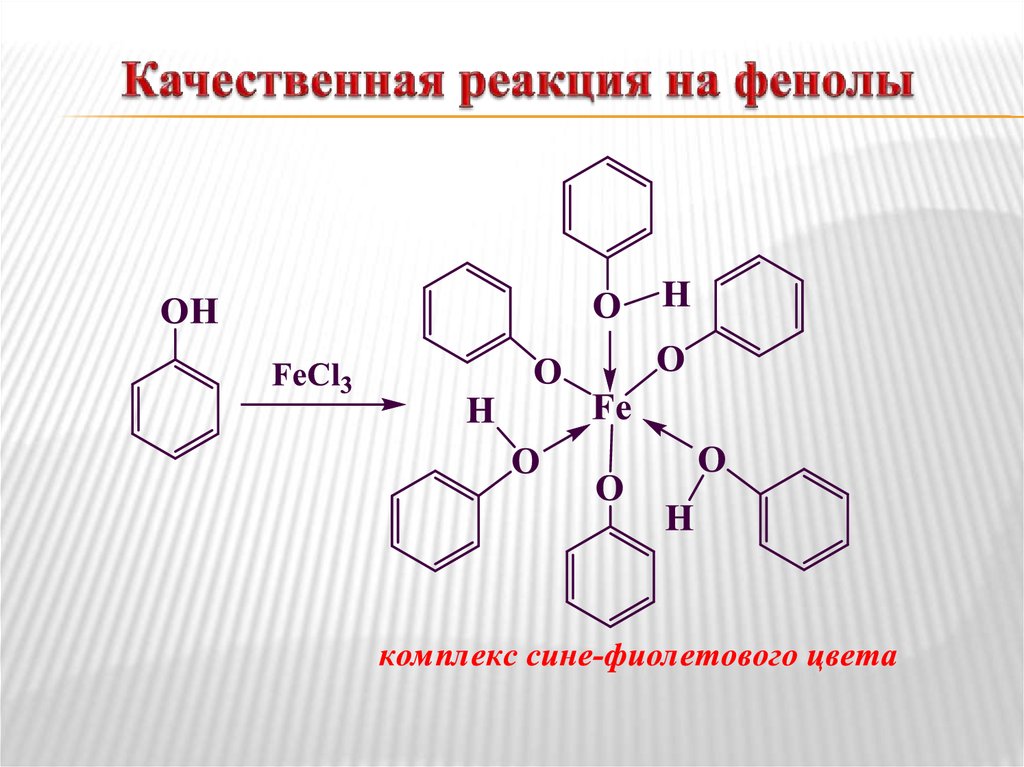
17. Качественная реакция на фенолы
18.
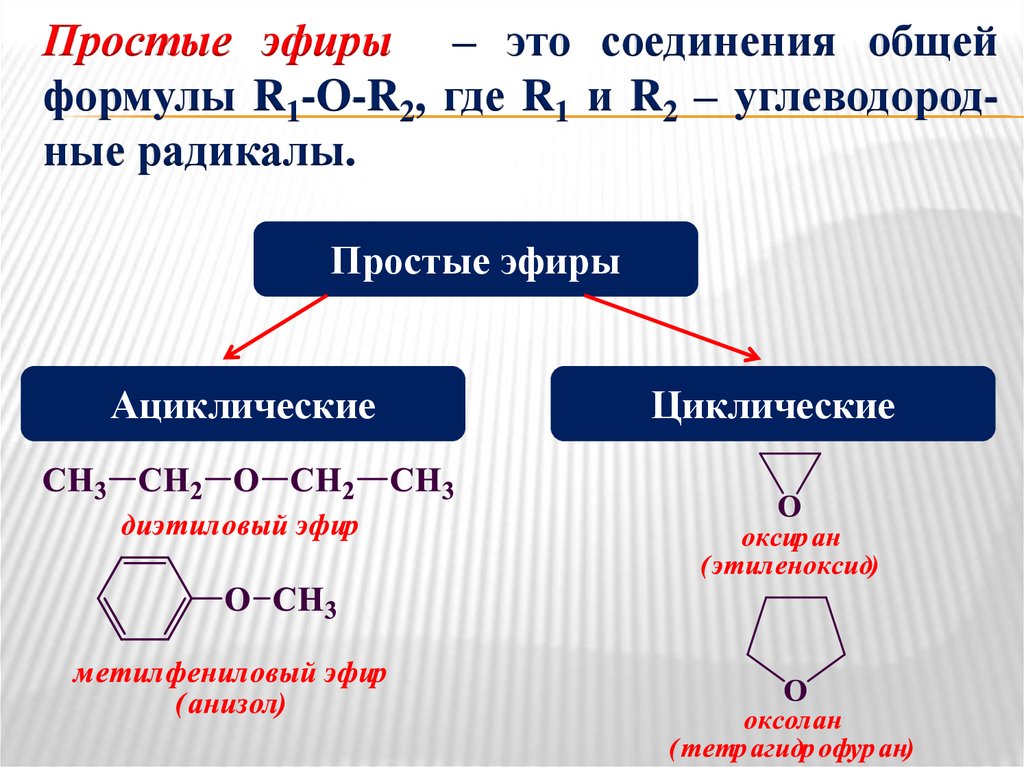
Простые эфиры – это соединения общейформулы R1-O-R2, где R1 и R2 – углеводородные радикалы.
Простые эфиры
Ациклические
Циклические
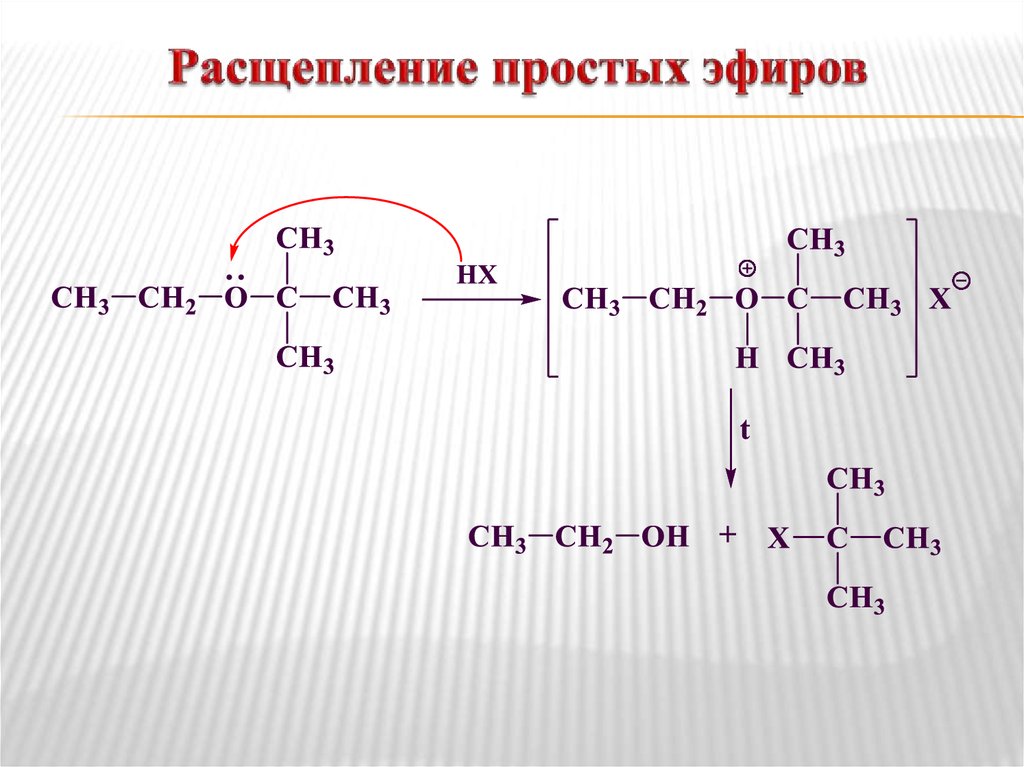
19. Расщепление простых эфиров
20.
Тиолы – это производные углеводородов, вкоторых
атом
водорода
замещен
на
меркаптогруппу SH.
Сульфиды – это серные аналоги простых
эфиров, имеющие общую формулу R1-S-R2.
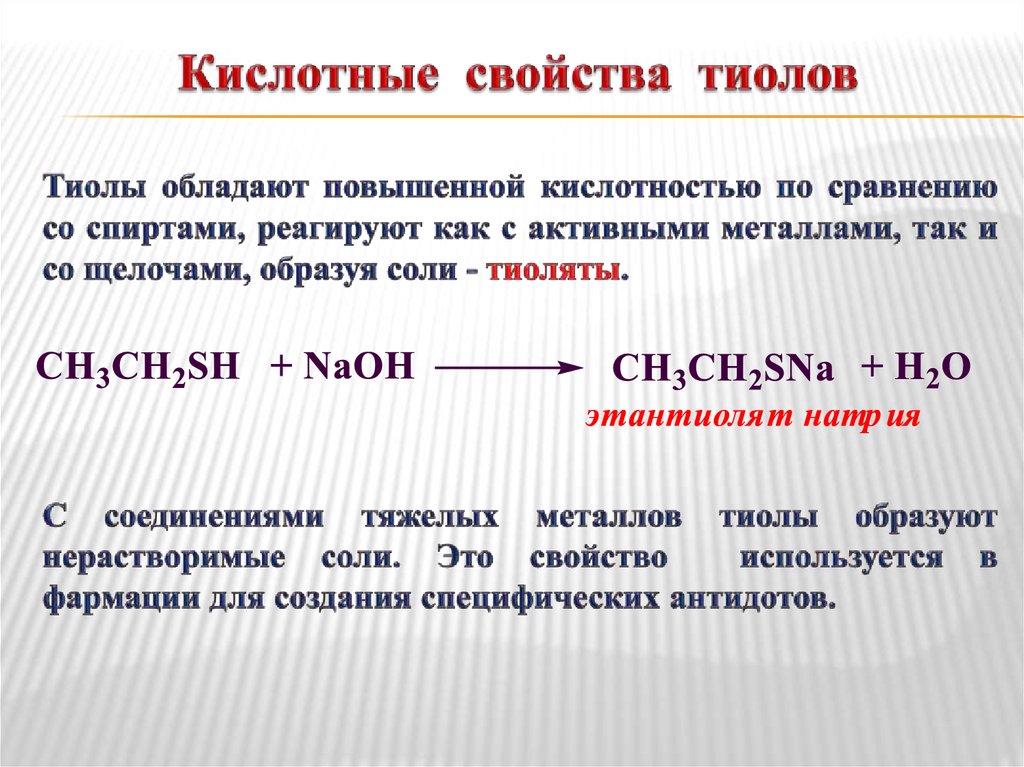
21. Кислотные свойства тиолов
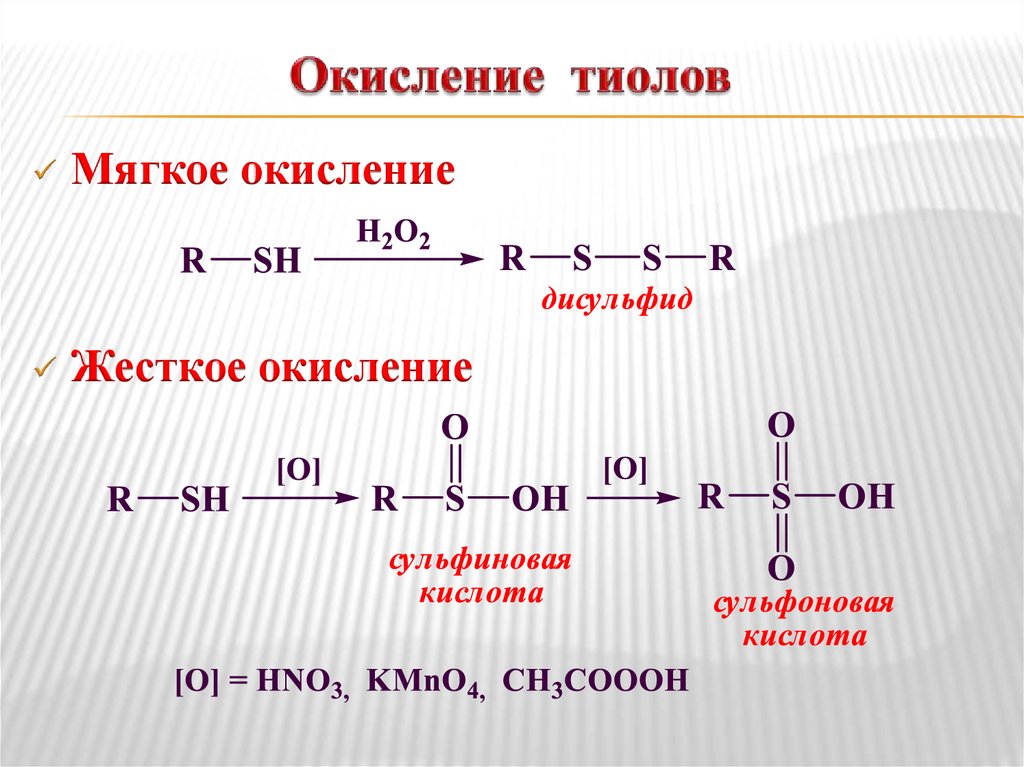
22. Окисление тиолов
Мягкое окислениеЖесткое окисление





 Химия
Химия








