Похожие презентации:
Ионная связь
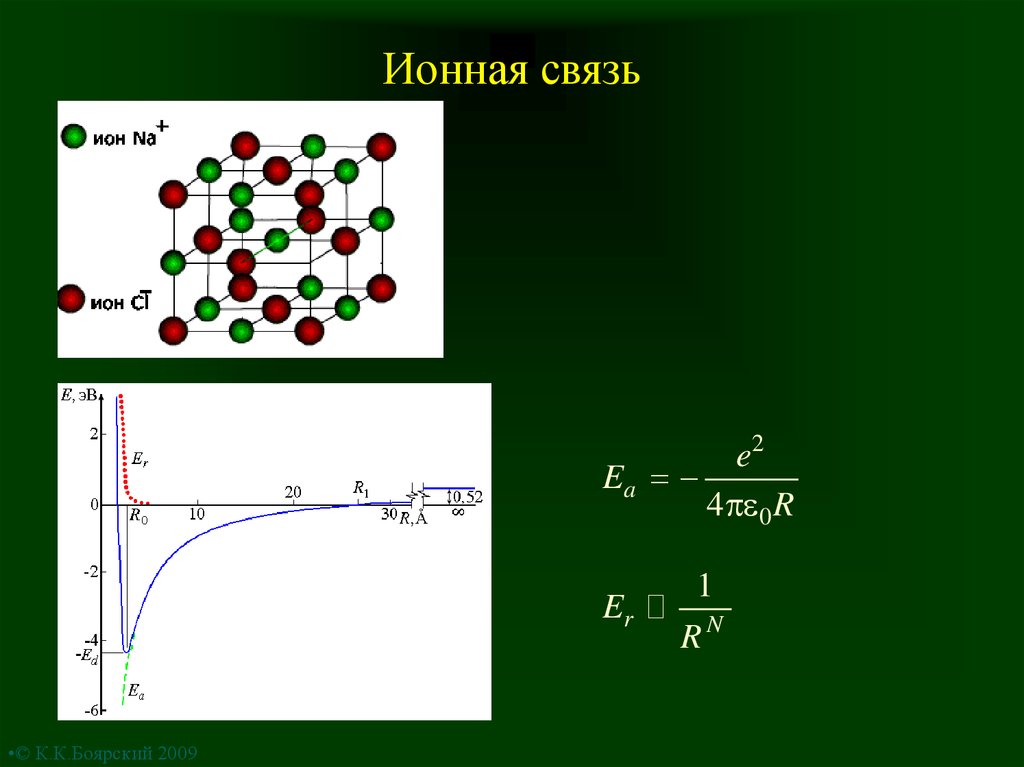
1. Ионная связь
e2Ea
4 0 R
Er
•© К.К.Боярский 2009
1
RN
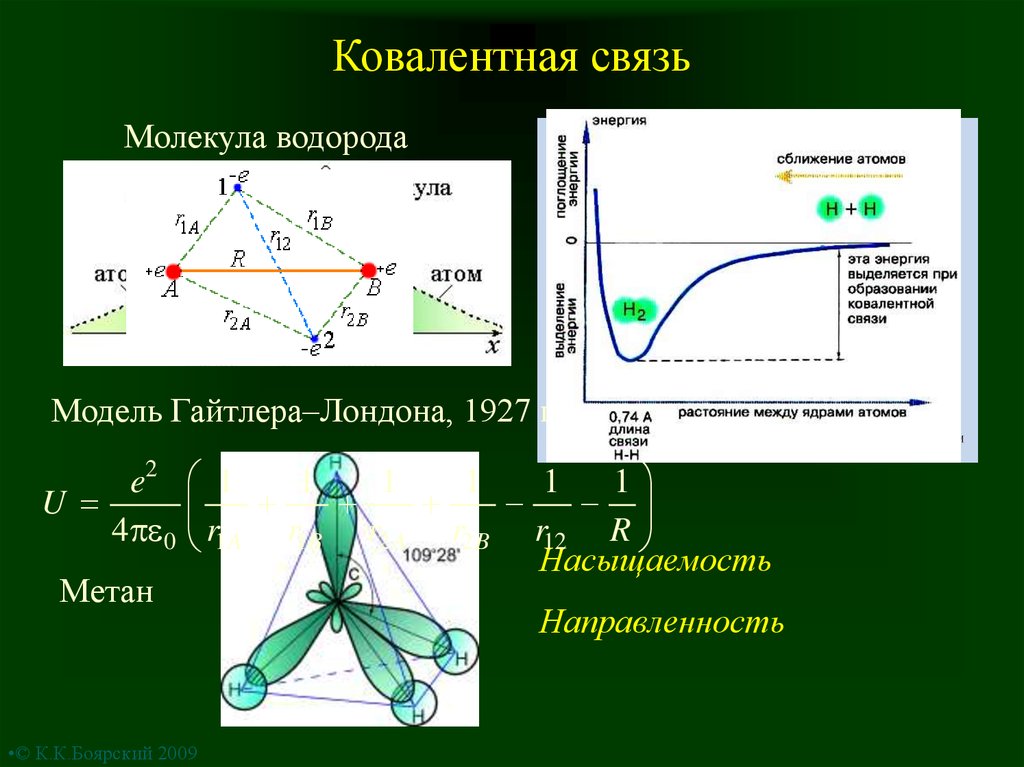
2. Ковалентная связь
Молекула водородаМодель Гайтлера–Лондона, 1927 г.
e2
U
4 0
Метан
1
1
1
1
1
1
r1 A r1B r2 A r2 B r12 R
Насыщаемость
•© К.К.Боярский 2009
Направленность
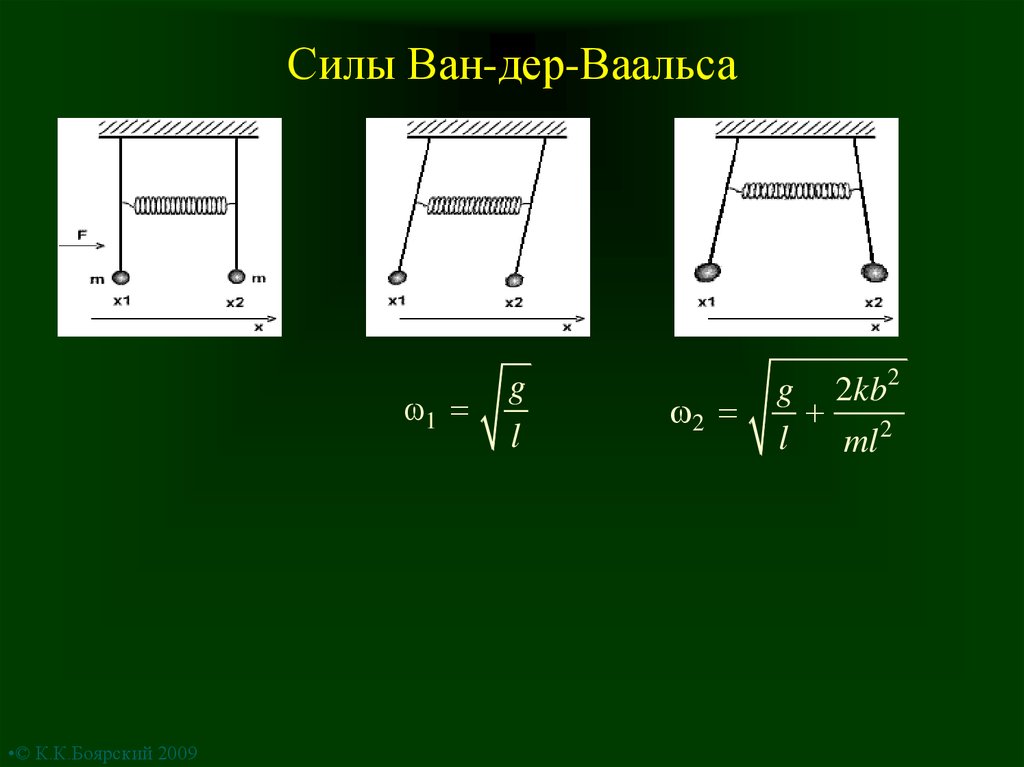
3. Силы Ван-дер-Ваальса
1•© К.К.Боярский 2009
g
l
2
g 2kb2
l
ml 2
4. Силы Ван-дер-Ваальса
U12p1 p2
e2 x 1 x 2
3
4 0 R
4 0 R 3
1
1
1
2
2
2
2 2
2 2
U
x
x
U
q1,2 mx
x
2
U
m
q
m
2
12
1 0 21
1 1
2 q2
2
2
2
2
1,2
1,2
2
e
02
4 0 mR 3
e2
e4
0 1
3 2
2 2
6 4
8 0 mR 0 32 0 mR 0
e4
E 0
32 2 02 mR 6 03
•© К.К.Боярский 2009
F
E
R
1
R7
5. Адиабатическое приближение
E Ee Ev ErКолебательная энергия
Ev
Ee
Ev v 1 2 v
me
M
Вращательная энергия
I 2r
L2
Er
2
2I
2
J J 1
2I
E Ee v 1 2 v
•© К.К.Боярский 2009
2
Er me
Ee M
BJ J 1
J J 1
2I
Er
Ev
Ee
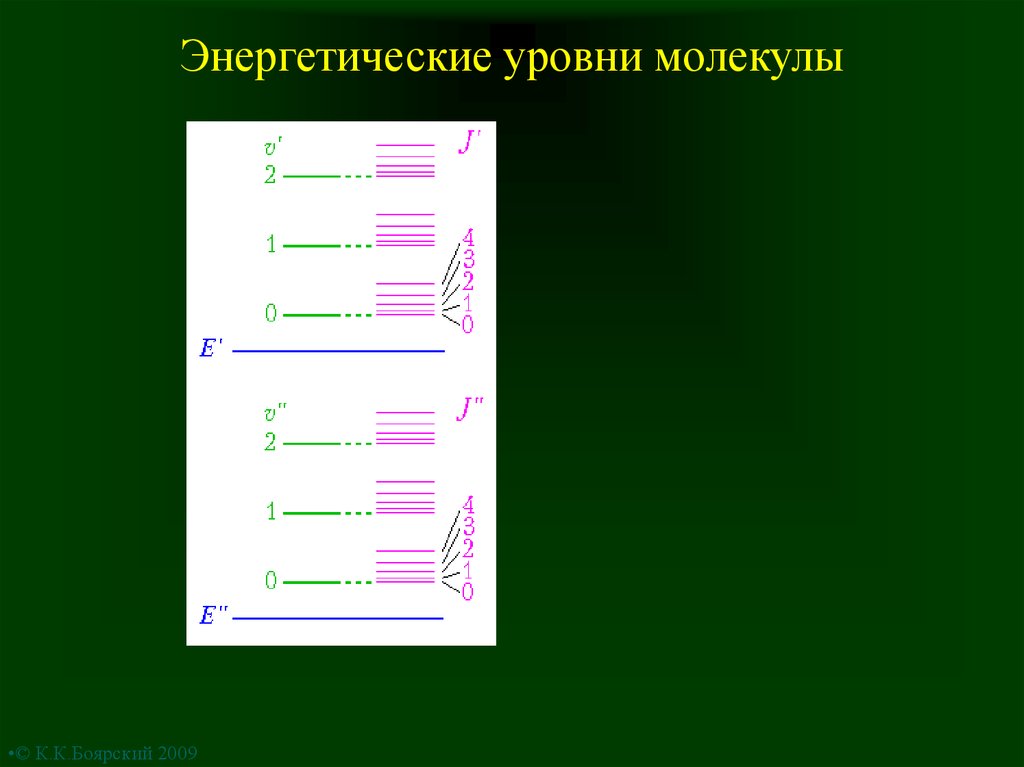
6. Энергетические уровни молекулы
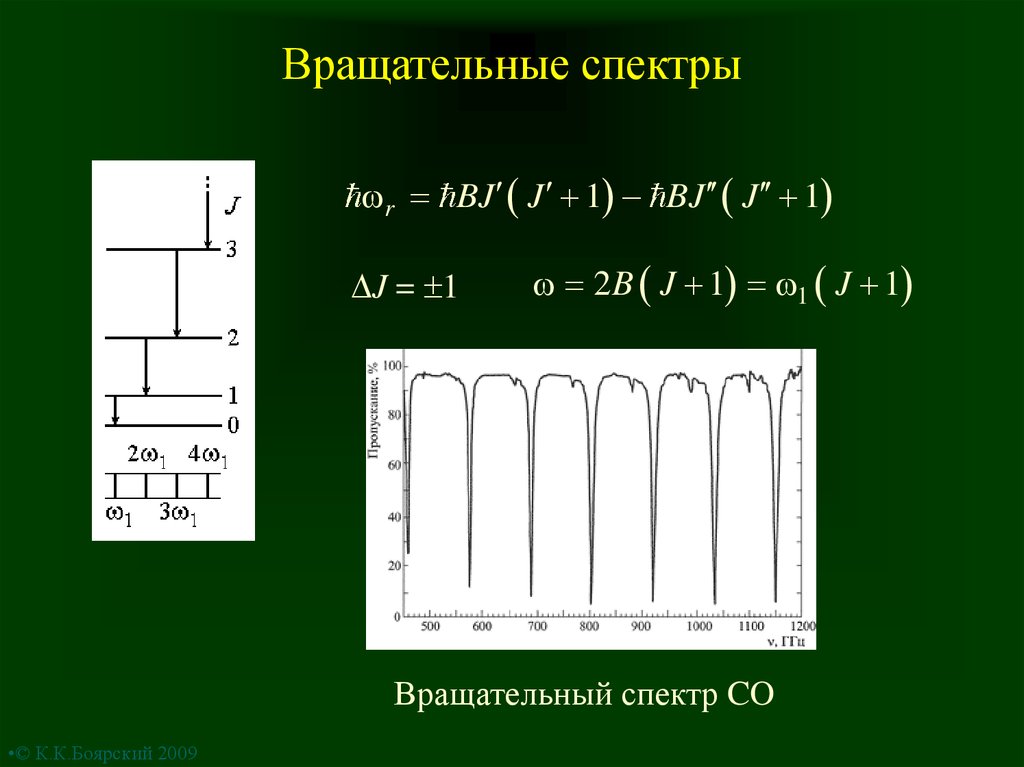
•© К.К.Боярский 20097. Вращательные спектры
r BJ J 1 BJ J 1J = 1
2B J 1 1 J 1
Вращательный спектр CO
•© К.К.Боярский 2009
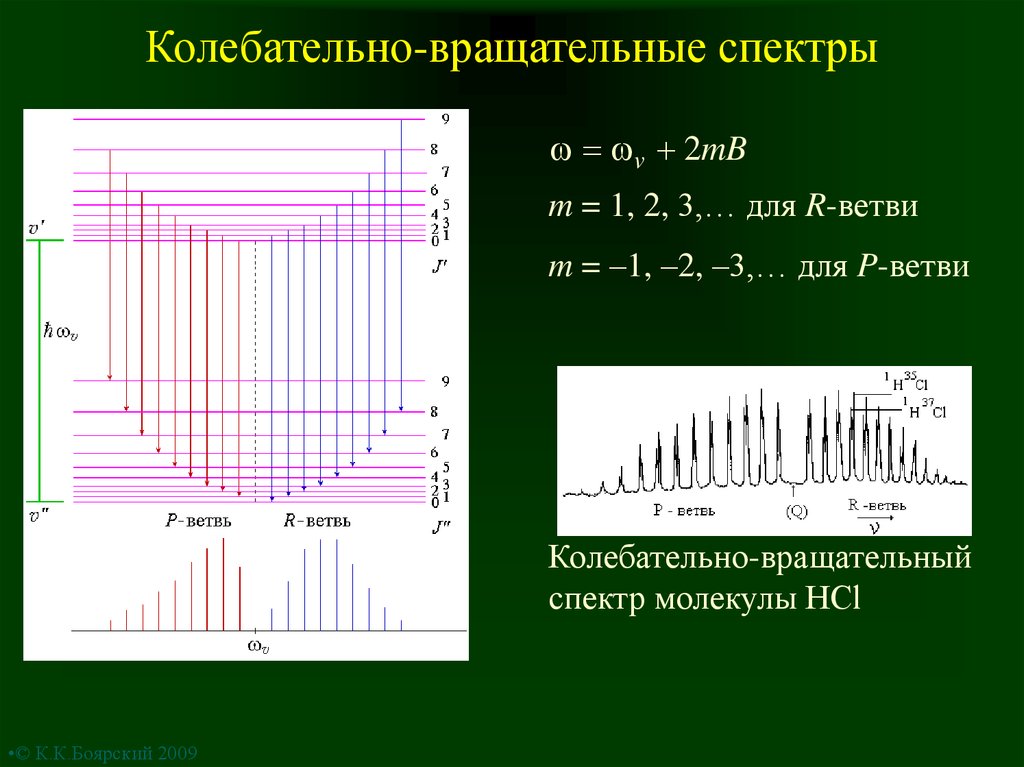
8. Колебательно-вращательные спектры
v 2mBm = 1, 2, 3,… для R-ветви
m = –1, –2, –3,… для P-ветви
Колебательно-вращательный
спектр молекулы HCl
•© К.К.Боярский 2009
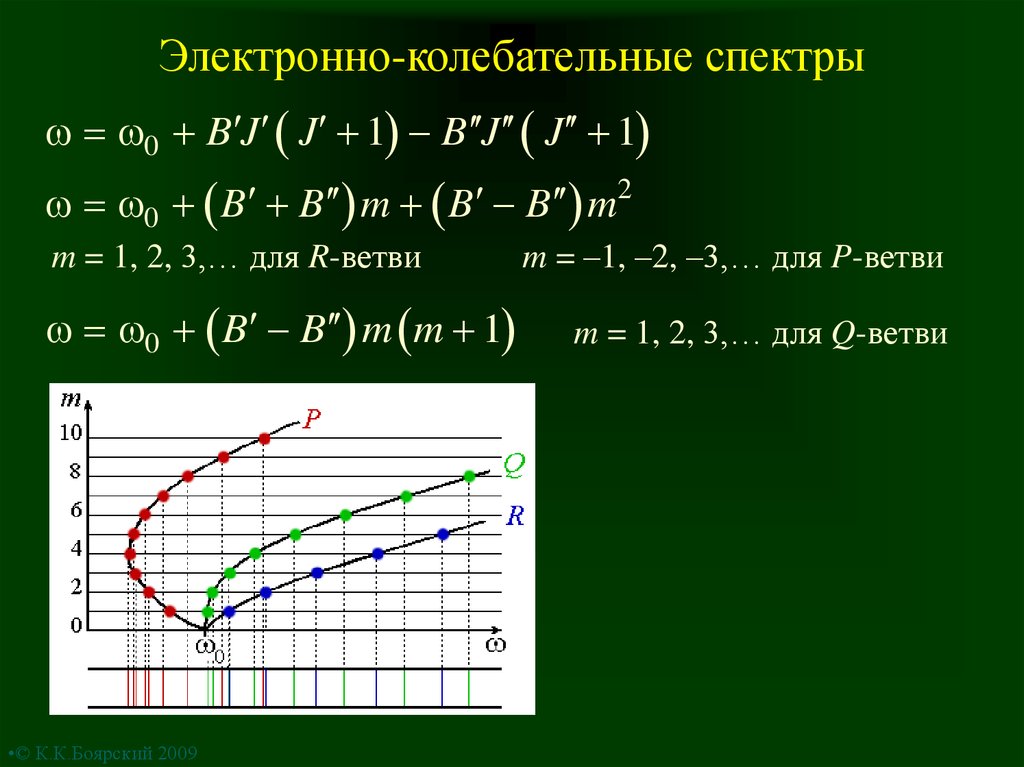
9. Электронно-колебательные спектры
0 B J J 1 B J J 10 B B m B B m2
m = 1, 2, 3,… для R-ветви
0 B B m m 1
•© К.К.Боярский 2009
m = –1, –2, –3,… для P-ветви
m = 1, 2, 3,… для Q-ветви
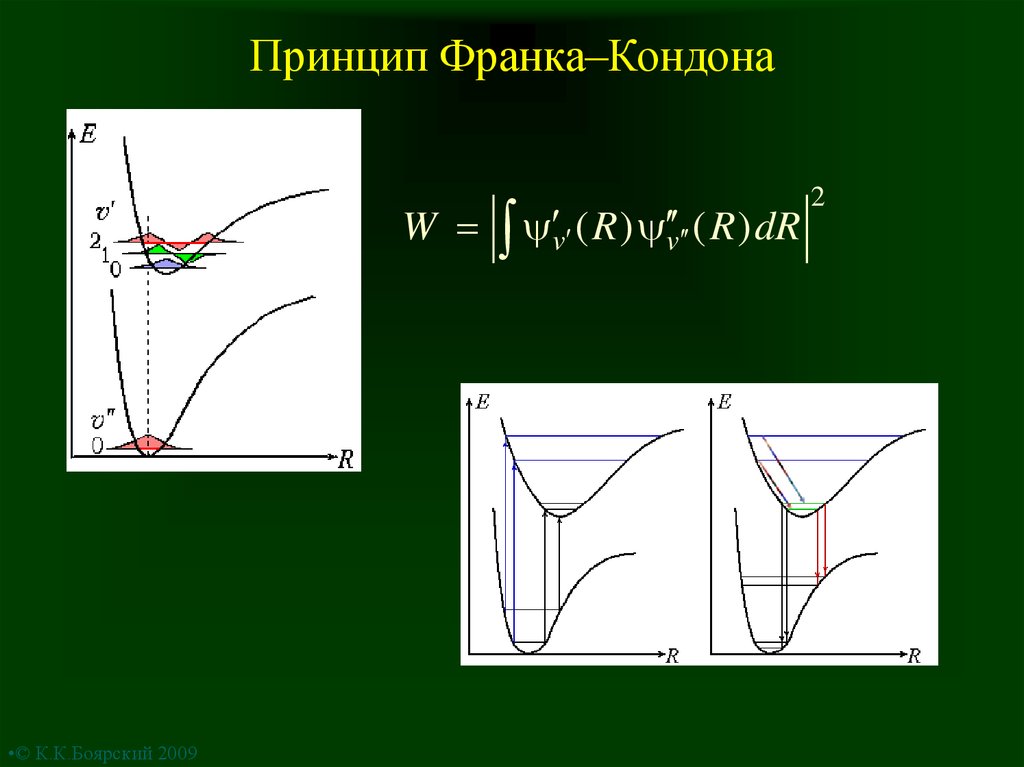
10. Принцип Франка–Кондона
W•© К.К.Боярский 2009
v ( R ) v ( R ) dR
2
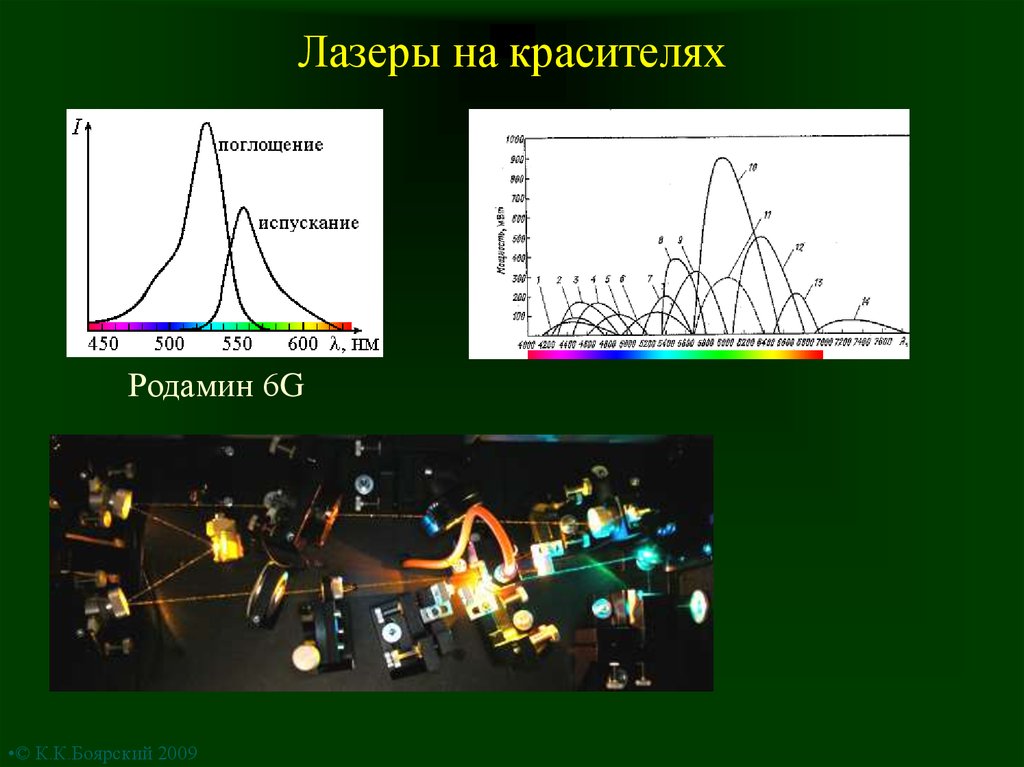
11. Лазеры на красителях
Родамин 6G•© К.К.Боярский 2009
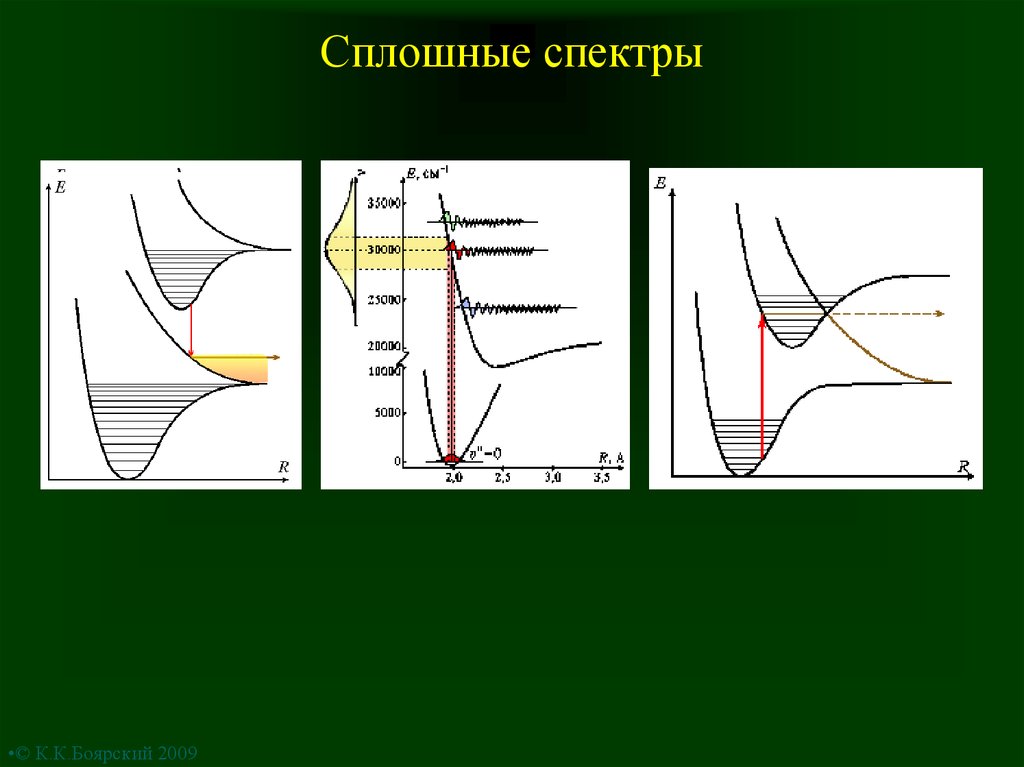
12. Сплошные спектры
•© К.К.Боярский 200913. Особенности молекулярных спектров
Спектры состоят из полос, каждая из которыхсодержит множество близких линий
Полосы имеют резкий кант с одной стороны
Полосы поглощения и испускания могут быть
смещены друг относительно друга
Наличие сплошных участков спектров поглощения и
испускания, не связанных с ионизацией
•© К.К.Боярский 2009



 Химия
Химия








