Похожие презентации:
Гетероциклические соединения
1. Гетероциклические соединения
2.
Гетероциклические соединения – это такиесоединения, молекулы которых содержат циклы
(кольца) состоящие не только из атомов углерода, но
и из атомов других элементов чаще всего атомов
азота,
серы,
кислорода,
которые
называются
гетероатомами (от греч. слова geterоs - разный).
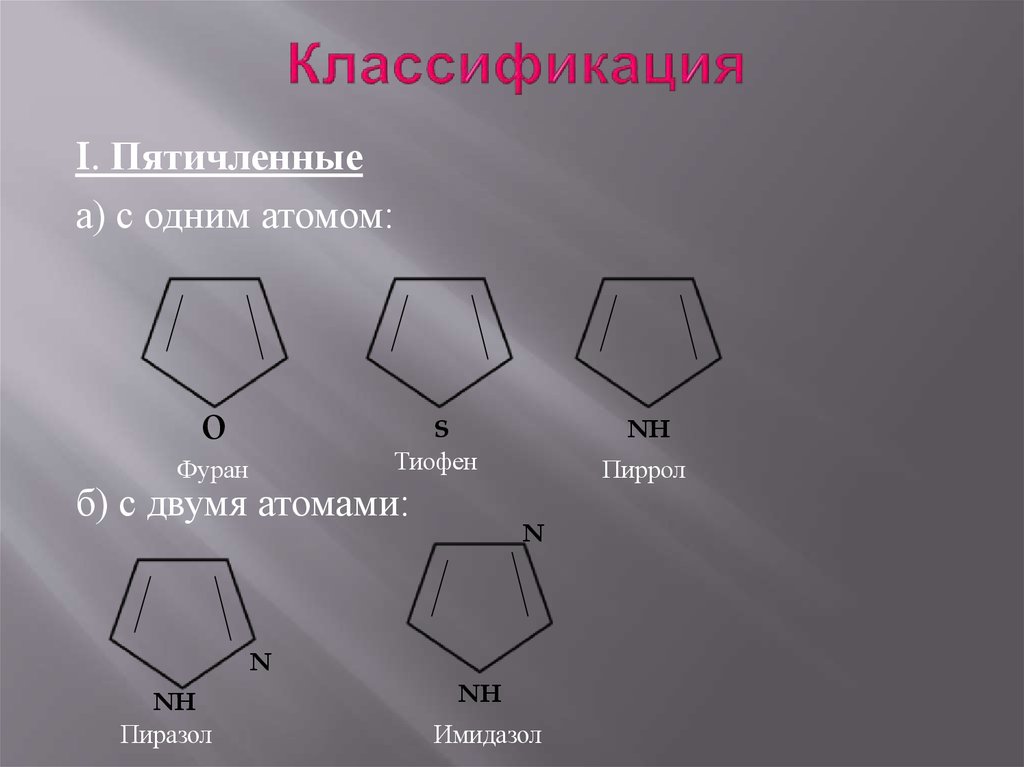
3. Классификация
I. Пятичленныеа) с одним атомом:
о
S
Тиофен
Фуран
б) с двумя атомами:
NH
Пиррол
N
N
NH
Пиразол
NH
Имидазол
4.
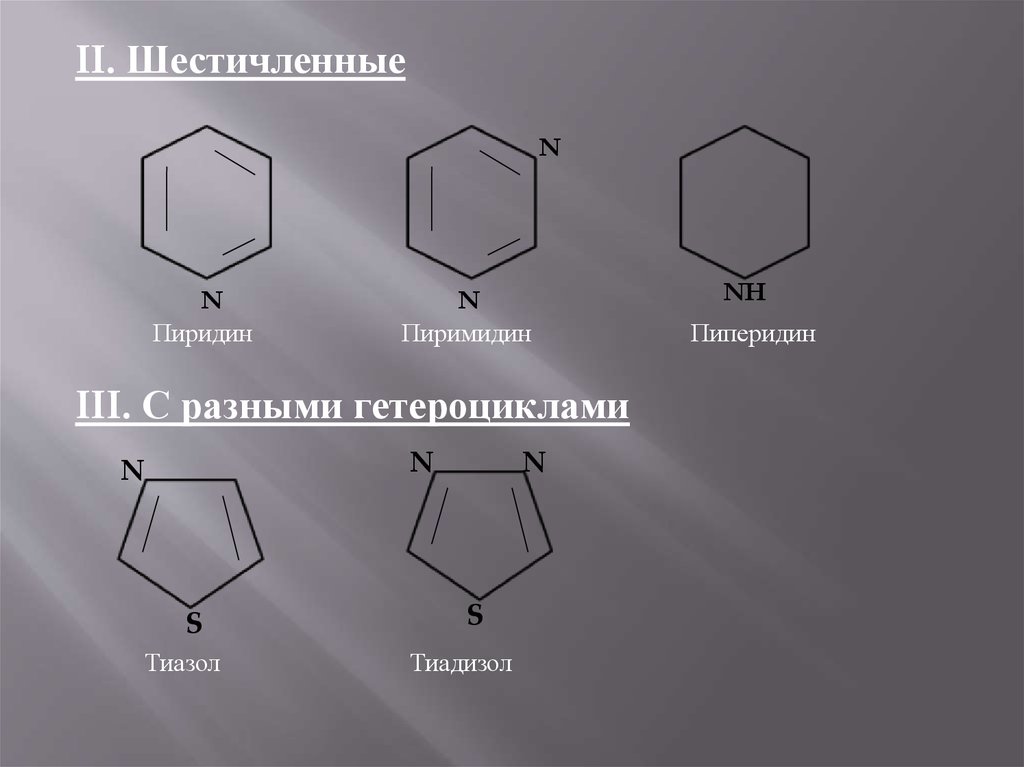
II. ШестичленныеN
N
Пиридин
N
Пиримидин
III. С разными гетероциклами
N
N
S
Тиазол
N
S
Тиадизол
NH
Пиперидин
5.
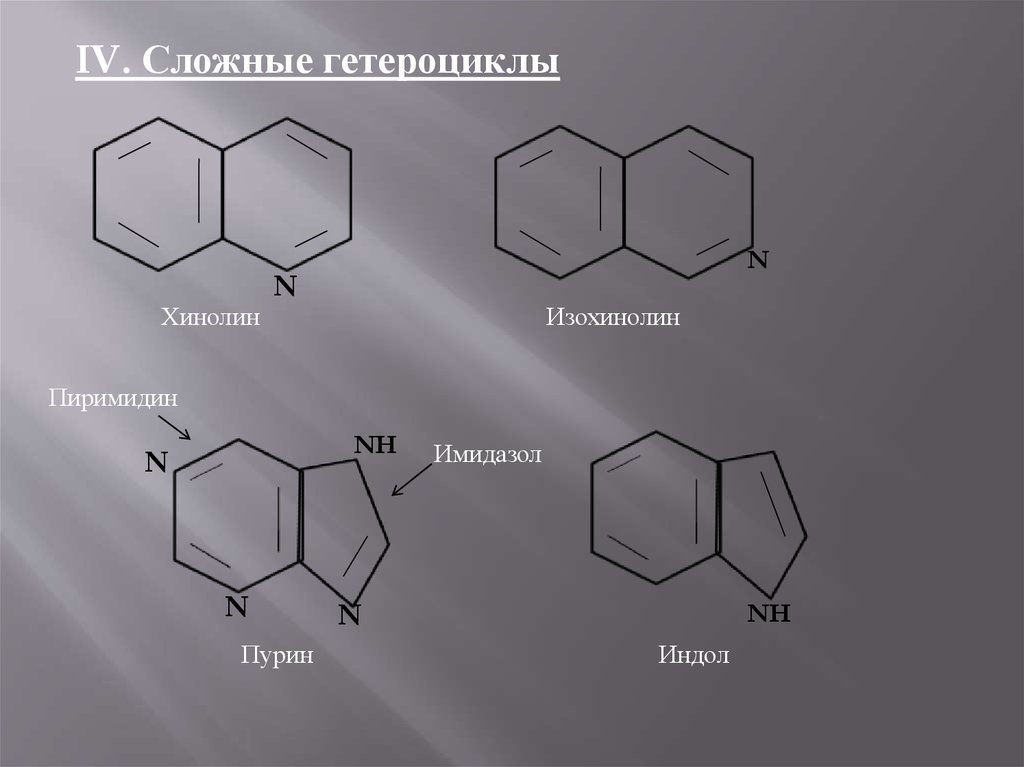
IV. Сложные гетероциклыХинолин
N
N
Изохинолин
Пиримидин
NH
N
N
Пурин
Имидазол
NH
N
Индол
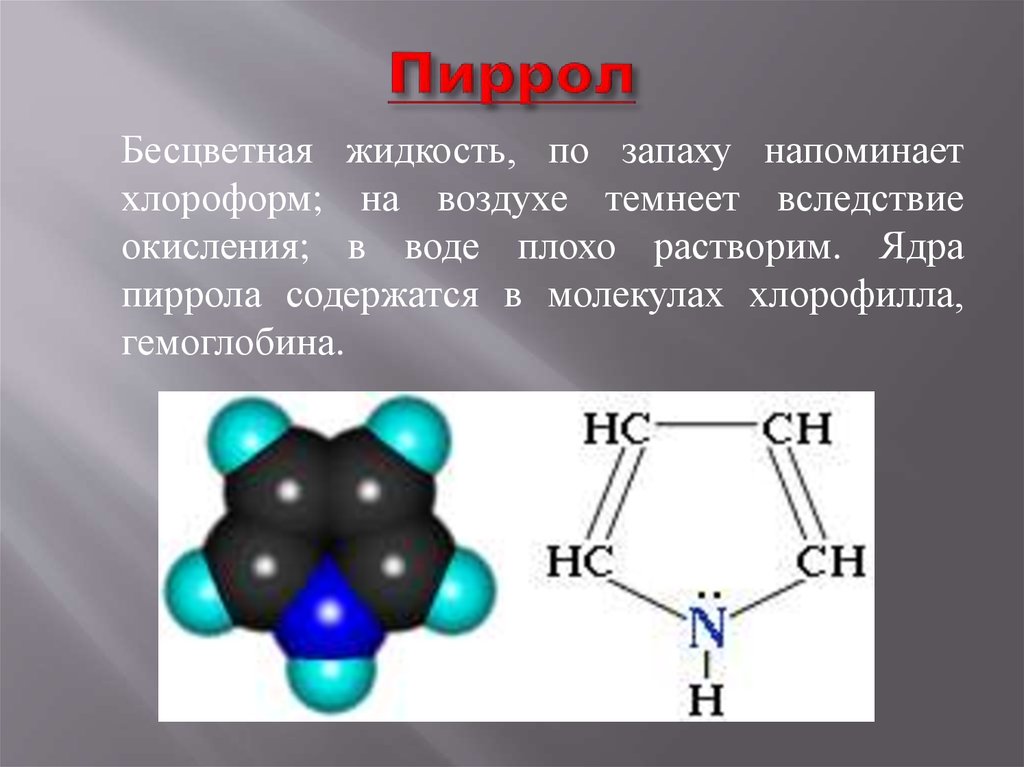
6. Пиррол
Бесцветная жидкость, по запаху напоминаетхлороформ; на воздухе темнеет вследствие
окисления; в воде плохо растворим. Ядра
пиррола содержатся в молекулах хлорофилла,
гемоглобина.
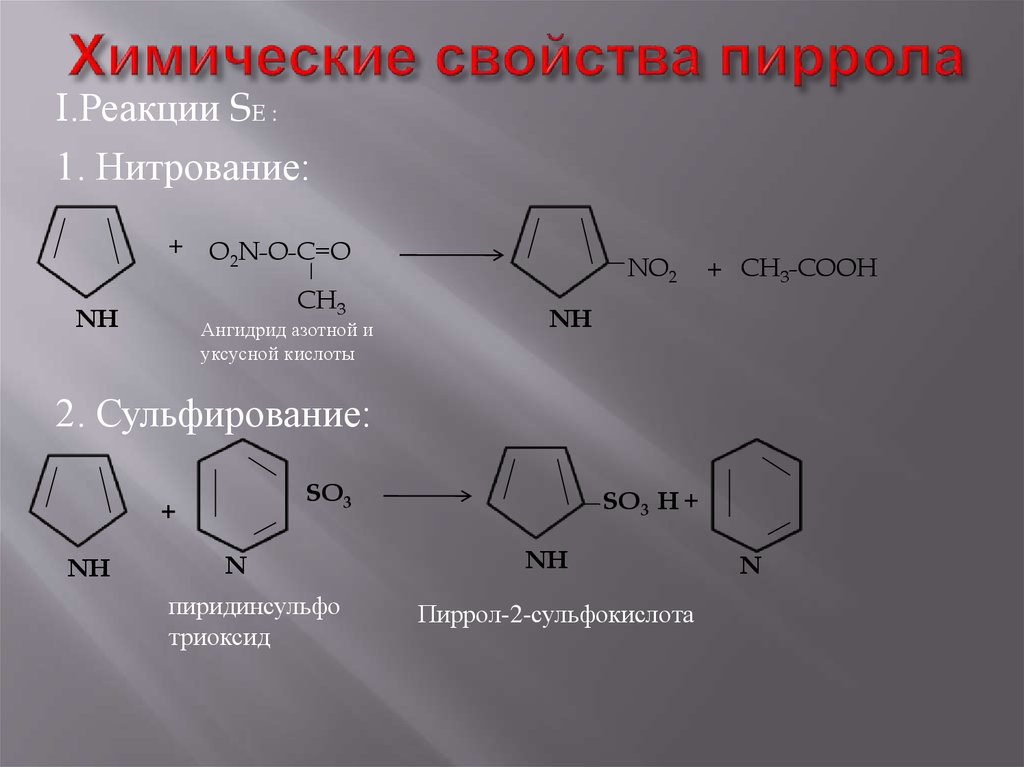
7. Химические свойства пиррола
I.Реакции SE :1. Нитрование:
+ O N-O-C=O
2
CH3
NH
Ангидрид азотной и
уксусной кислоты
NO2
+ CH3-COOH
NH
2. Сульфирование:
SO3
+
NH
N
пиридинсульфо
триоксид
SO3 H +
NH
Пиррол-2-сульфокислота
N
8.
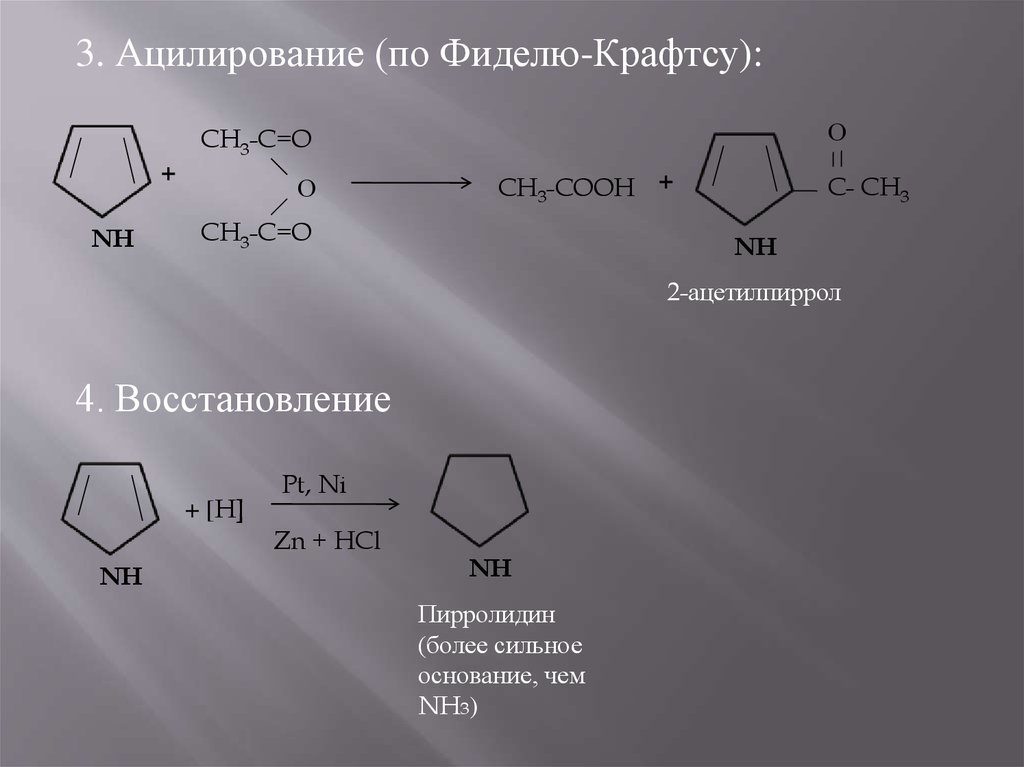
3. Ацилирование (по Фиделю-Крафтсу):О
CH3-C=O
+
NH
О
CH3-COOH +
CH3-C=O
C- CH3
NH
2-ацетилпиррол
4. Восстановление
+ [H]
Pt, Ni
Zn + HCl
NH
NH
Пирролидин
(более сильное
основание, чем
NH3)
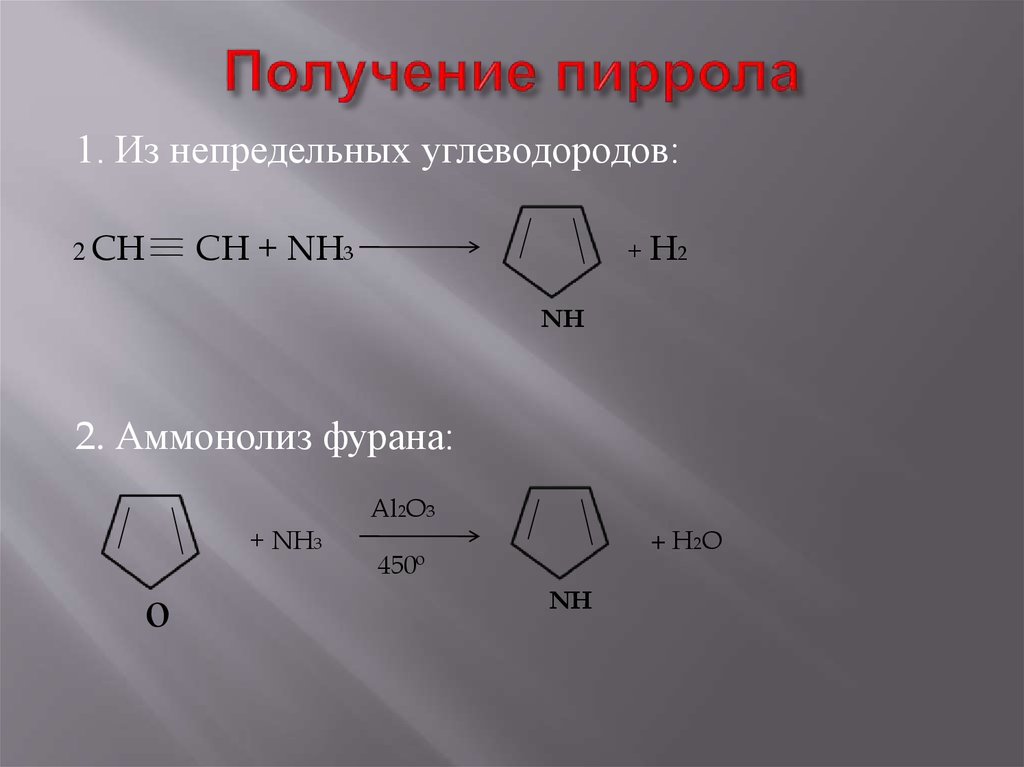
9. Получение пиррола
1. Из непредельных углеводородов:2 CH
CH + NH3
+ H2
NH
2. Аммонолиз фурана:
Al2O3
+ NH3
о
+ H2O
450º
NH
10. Фуран
Бесцветная легкокипящая жидкость. Похимическим свойствам напоминает пиррол; также
кислотоустойчив. Ароматичность выражена
слабее, чем у всех пятичленных гетероциклов.
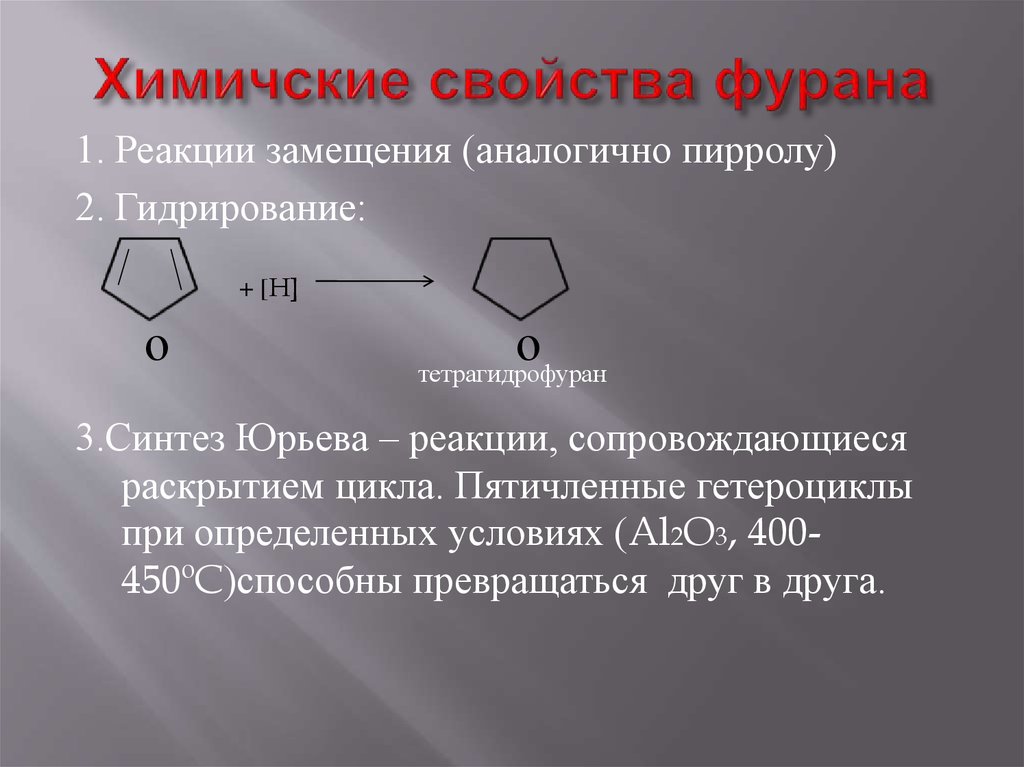
11. Химичские свойства фурана
1. Реакции замещения (аналогично пирролу)2. Гидрирование:
+ [H]
о
о
тетрагидрофуран
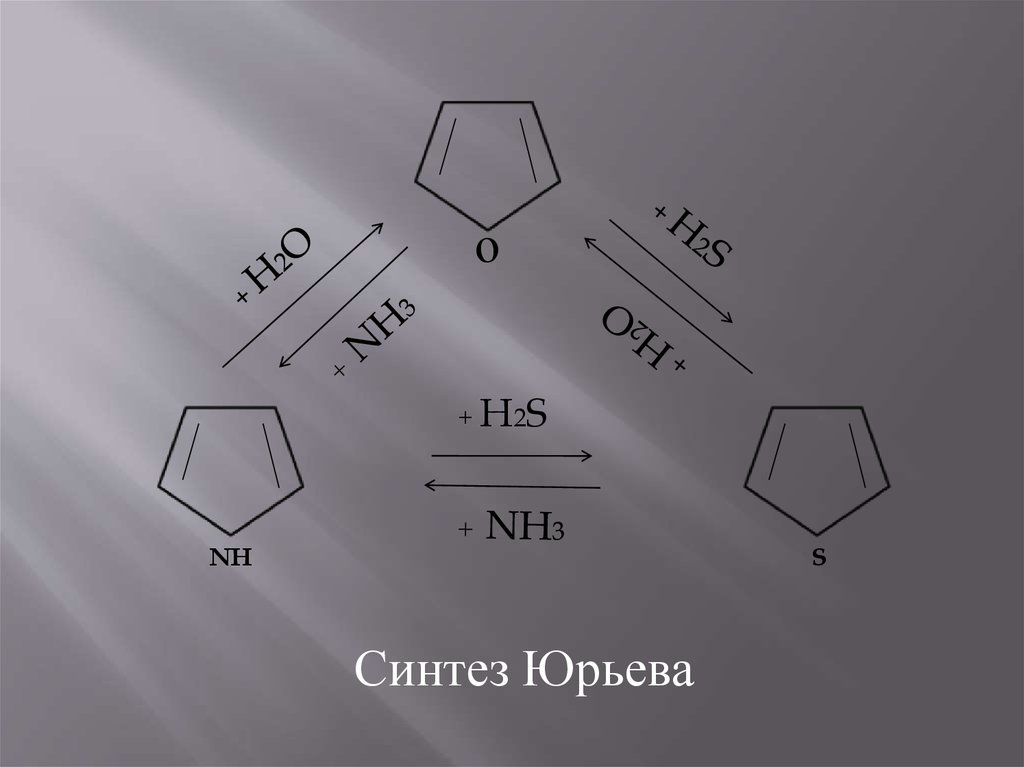
3.Синтез Юрьева – реакции, сопровождающиеся
раскрытием цикла. Пятичленные гетероциклы
при определенных условиях (Al2O3, 400450ºC)способны превращаться друг в друга.
12.
о+ H2S
NH
S
Синтез Юрьева
13. Фурфурол
Маслянистая жидкость с запахомC =O ржаного хлеба. Получают из
непищевых полисахаридов (отходы
о
древесины, салола и т.д.) По
H
химическим свойствам напоминает бензальдегид.
Производные фурфурола (гидрофурамид,
пирослизевая кислота и др.), предложено использовать
в сельском хозяйстве для протравливания семян, для
борьбы с сорняками гидрофурамид, феназон,
фурфурамид. Также применяется для получения
нитропроизводных фурана, которые обладают
антибактериальной активностью и применяются в
виде различных производных.
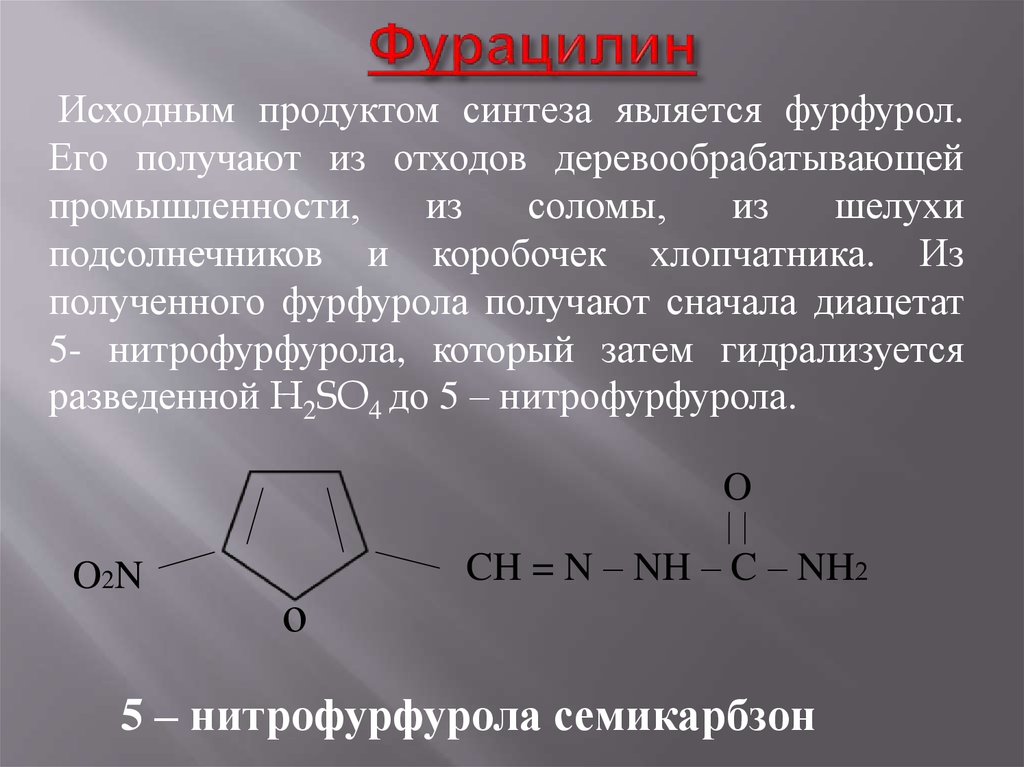
14. Фурацилин
Исходным продуктом синтеза является фурфурол.Его получают из отходов деревообрабатывающей
промышленности,
из
соломы,
из
шелухи
подсолнечников и коробочек хлопчатника. Из
полученного фурфурола получают сначала диацетат
5- нитрофурфурола, который затем гидрализуется
разведенной H2SO4 до 5 – нитрофурфурола.
O
O2N
о
CH = N – NH – C – NH2
5 – нитрофурфурола семикарбзон
15.
Свойства: Желтый или зеленовато-желтый мелкокристаллический порошок, горького вкуса, очень мало
растворим в воде, мало в спирте, не растворим в эфире,
растворим в щелочах.
Применение:
Антибактериальное средство, для
профилактики
и
лечения
гнойно-воспалительных
процессов. Применяется для полоскания горла, внутрь для
лечения бактериальной дизентерии. Назначают 0,02%
водные растворы. 0,066% спиртовые растворы.
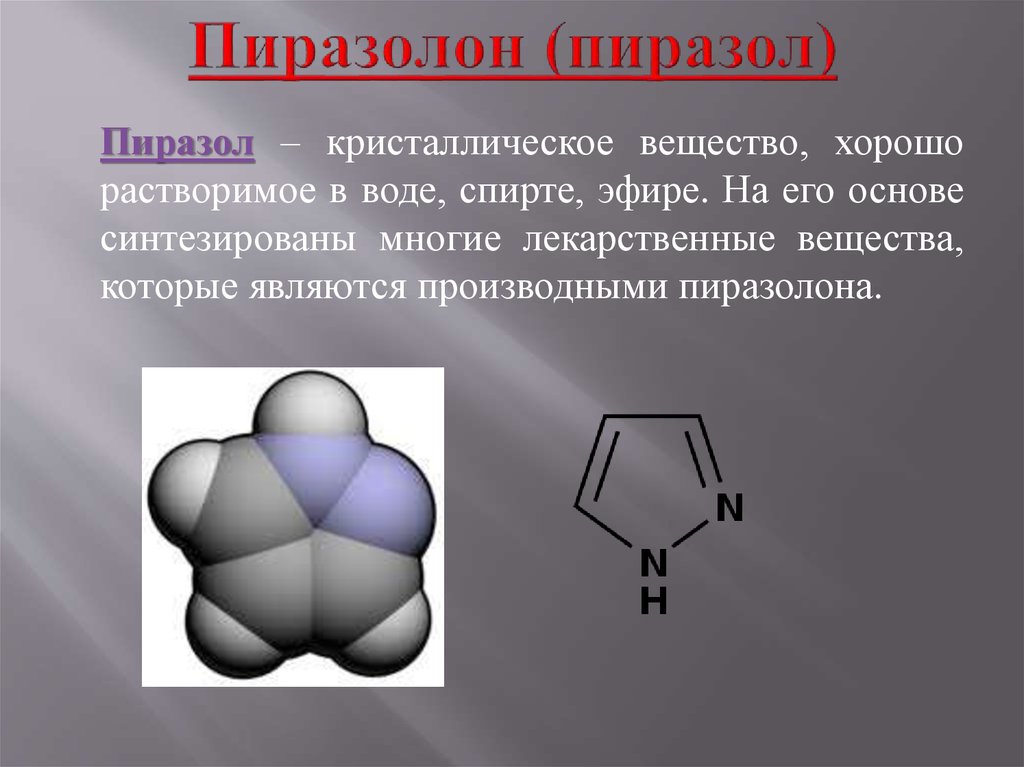
16. Пиразолон (пиразол)
Пиразол – кристаллическое вещество, хорошорастворимое в воде, спирте, эфире. На его основе
синтезированы многие лекарственные вещества,
которые являются производными пиразолона.
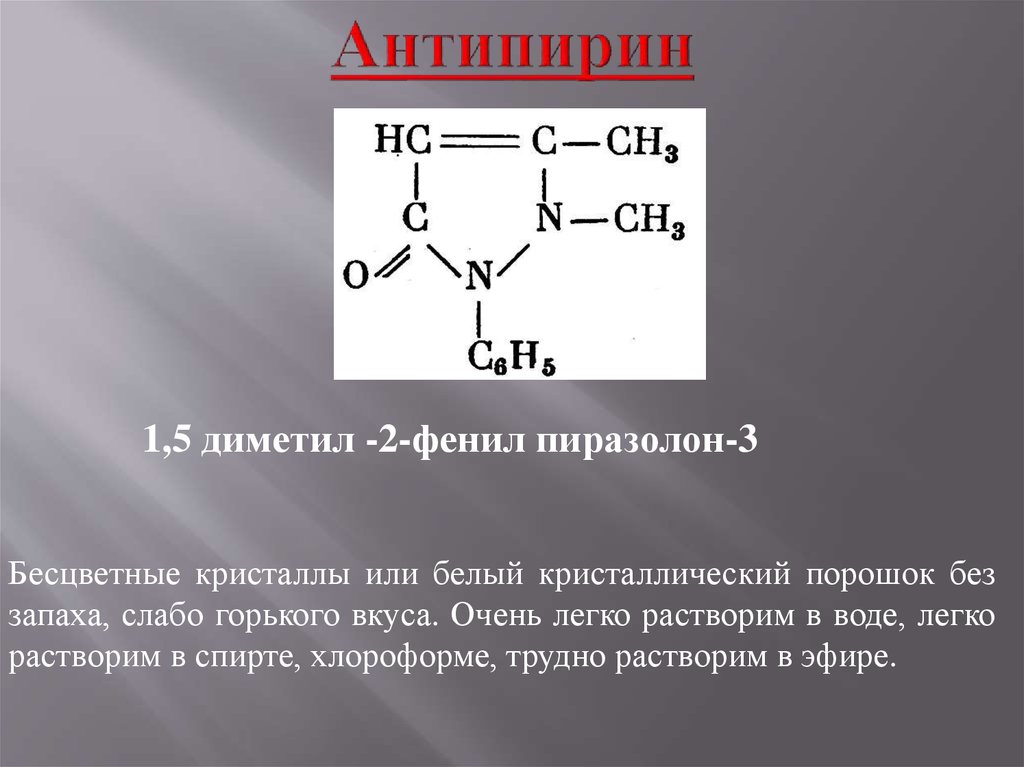
17. Антипирин
1,5 диметил -2-фенил пиразолон-3Бесцветные кристаллы или белый кристаллический порошок без
запаха, слабо горького вкуса. Очень легко растворим в воде, легко
растворим в спирте, хлороформе, трудно растворим в эфире.
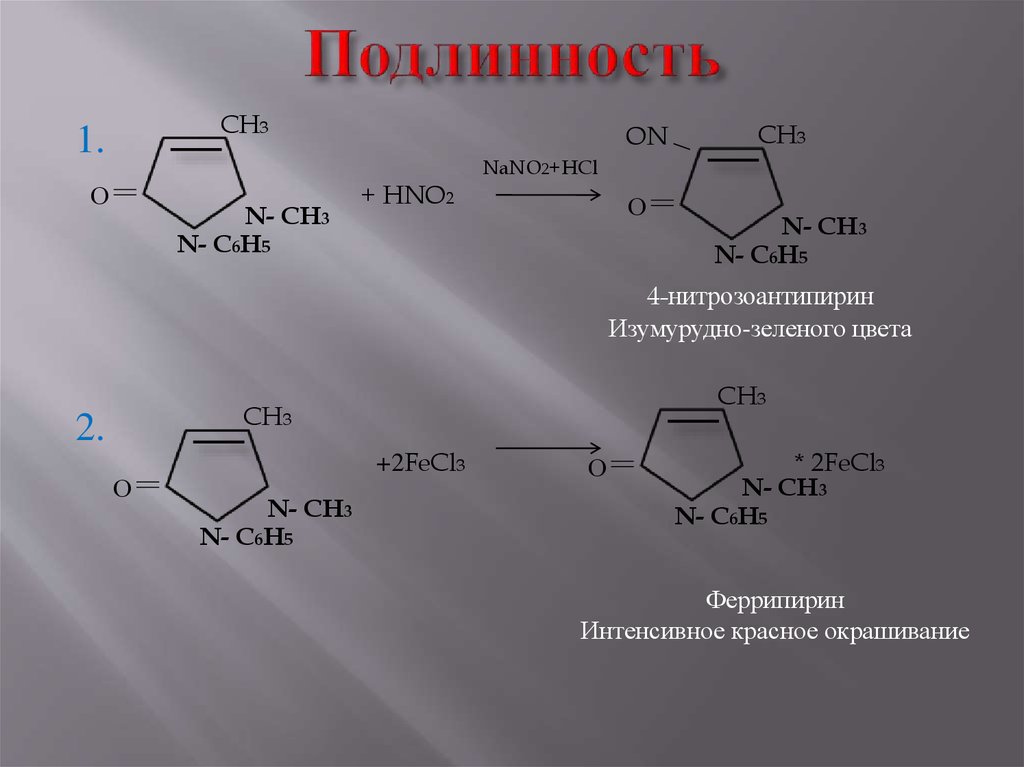
18. Подлинность
CH31.
О
N- CH3
N- C6H5
ON
+ HNO2
CH3
NaNO2+HCl
О
N- CH3
N- C6H5
4-нитрозоантипирин
Изумурудно-зеленого цвета
CH3
CH3
2.
О
+2FeCl3
N- CH3
N- C6H5
О
* 2FeCl3
N- CH3
N- C6H5
Феррипирин
Интенсивное красное окрашивание
19. Применение антипирина
Как болеутоляющее, жаропонижающее,противовоспалительное. Применяется при
головной боли, невралгии, ревматизме, при
простудных заболеваниях.
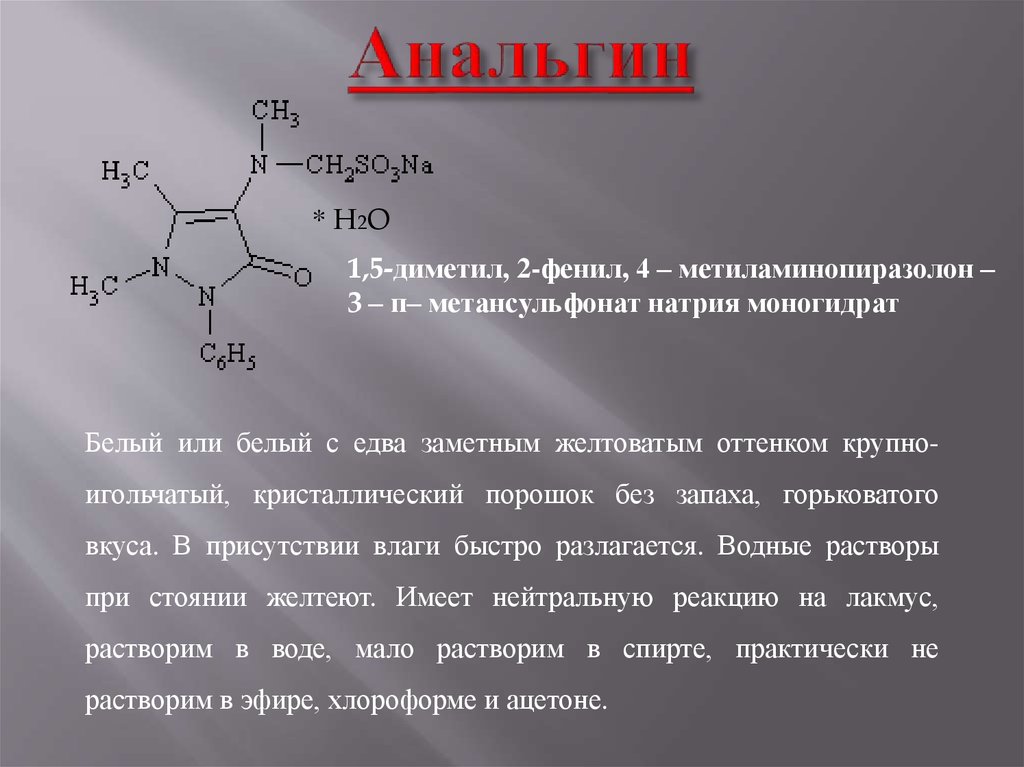
20. Анальгин
* H2 O1,5-диметил, 2-фенил, 4 – метиламинопиразолон –
3 – п– метансульфонат натрия моногидрат
Белый или белый с едва заметным желтоватым оттенком крупноигольчатый, кристаллический порошок без запаха, горьковатого
вкуса. В присутствии влаги быстро разлагается. Водные растворы
при стоянии желтеют. Имеет нейтральную реакцию на лакмус,
растворим в воде, мало растворим в спирте, практически не
растворим в эфире, хлороформе и ацетоне.
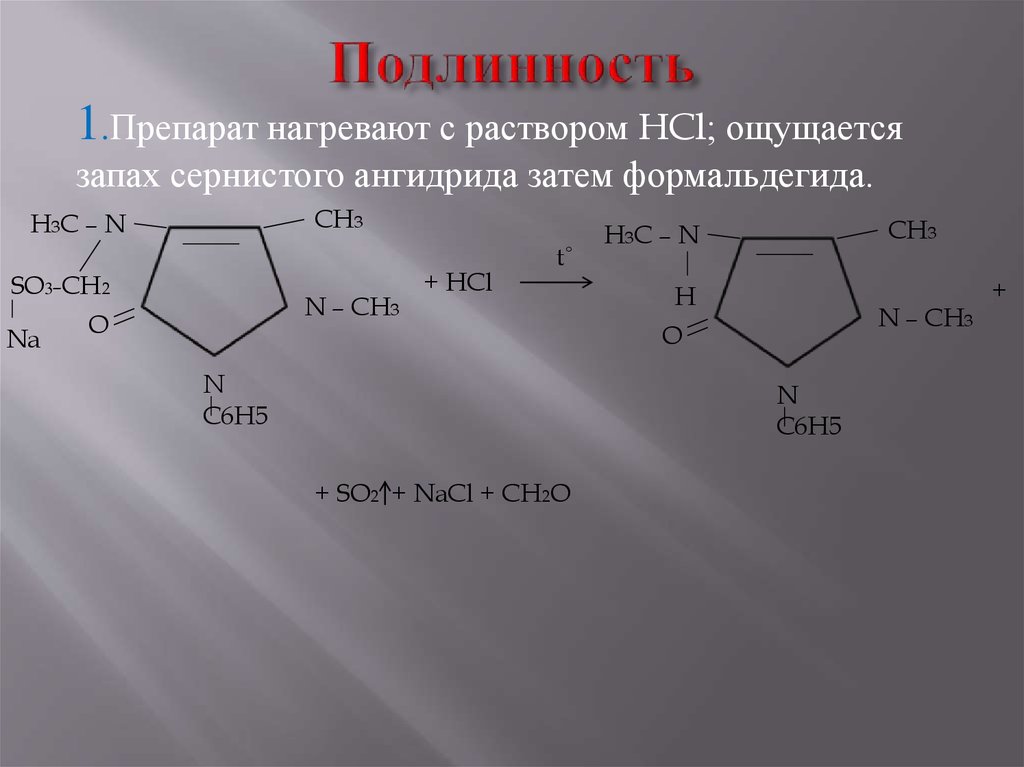
21. Подлинность
1.Препарат нагревают с раствором HCl; ощущаетсязапах сернистого ангидрида затем формальдегида.
CH3
H3C – N
SO3-CH2
Na
N – CH3
O
+ HCl
t˚
N
C6H5
CH3
H3C – N
H
N – CH3
O
N
C6H5
+ SO2 + NaCl + CH2O
+
22.
2. Реакция окисления анальгина KJO3 (c KJO3 реагируетобразующийся при гидролизе с соляной кислотой диоксид
серы):
( Анальгин +
H2O + спирт + HCl ) + KJO3
Раствор малинового цвета
При дальнейшем прибавлении реактива окраска усиливается и
выделяется бурый осадок выделевшегося йода:
5SO2 + 2 KJO3
4SO3 + K2SO4 + J2
3. C окислителем FeCl3 + HCl образуется синее, затем
фиолетовое окрашивание, затем темно-зеленое, затем желтое
и обесцвечивание нагревании.
23. Применение
Какболеутоляющее,
жаропонижающее,
противовоспалительное
средство.
Анальгин
является лучшим препаратом среди соединений
пиразолонового ряда по своей активности и
быстроте действия превосходит антипирин и
бутадион. Применяется при болях различного
происхождения
(головная
боль,
невралгия,
ревматизм, радикулит, грипп). ВД = 1,0 (3,0)






 Химия
Химия