Похожие презентации:
Гидрирование альдегидов и кетонов
1. Гидрирование альдегидов и кетонов
2.
OH3C
+ H2
C
R CH2 OH
H
R1 C R2+ H2
O
R1 HC R2
OH
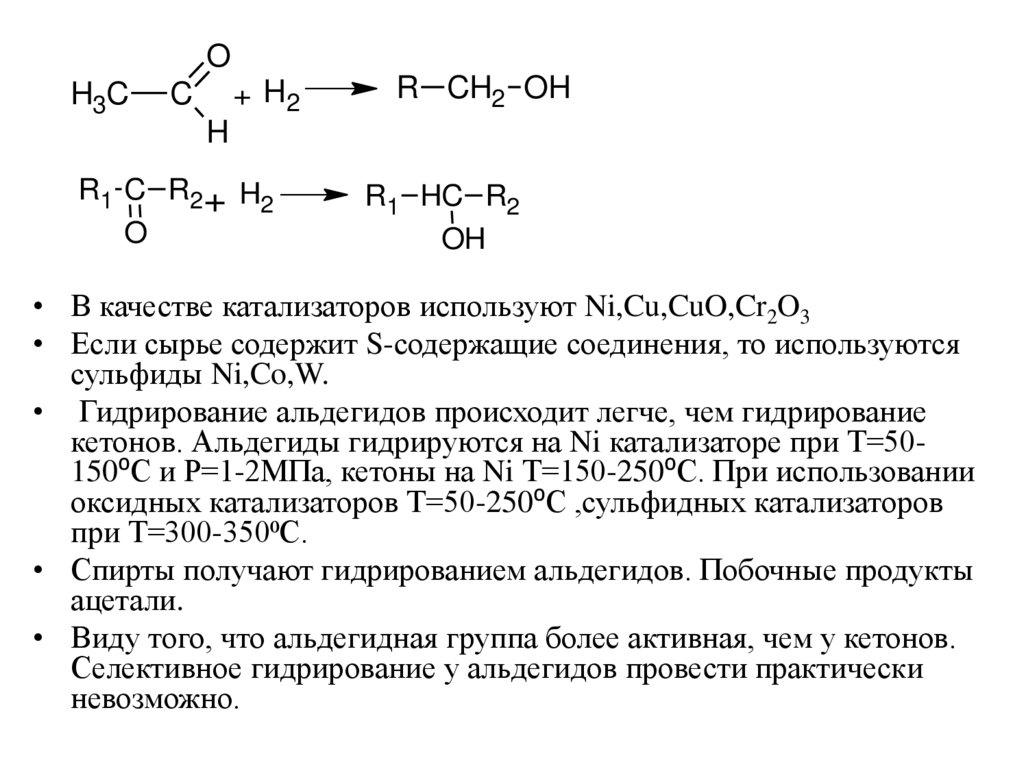
• В качестве катализаторов используют Ni,Cu,CuO,Cr2O3
• Если сырье содержит S-содержащие соединения, то используются
сульфиды Ni,Co,W.
• Гидрирование альдегидов происходит легче, чем гидрирование
кетонов. Альдегиды гидрируются на Ni катализаторе при Т=50150⁰С и Р=1-2МПа, кетоны на Ni Т=150-250⁰С. При использовании
оксидных катализаторов Т=50-250⁰С ,сульфидных катализаторов
при Т=300-350⁰С.
• Спирты получают гидрированием альдегидов. Побочные продукты
ацетали.
• Виду того, что альдегидная группа более активная, чем у кетонов.
Селективное гидрирование у альдегидов провести практически
невозможно.
3.
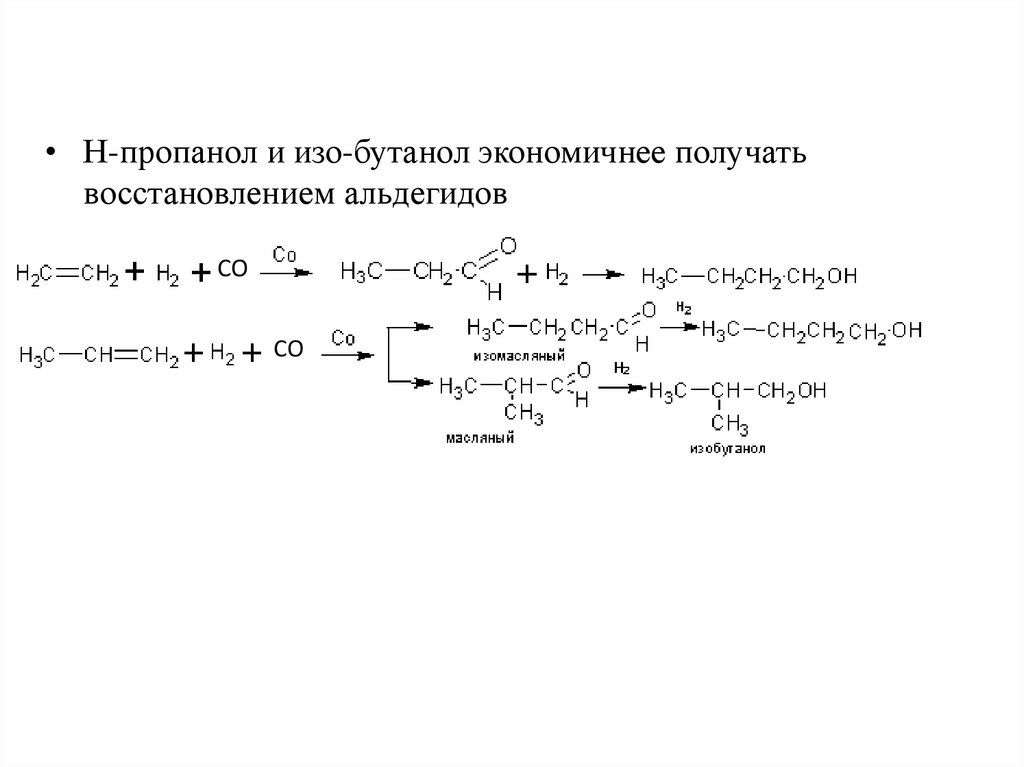
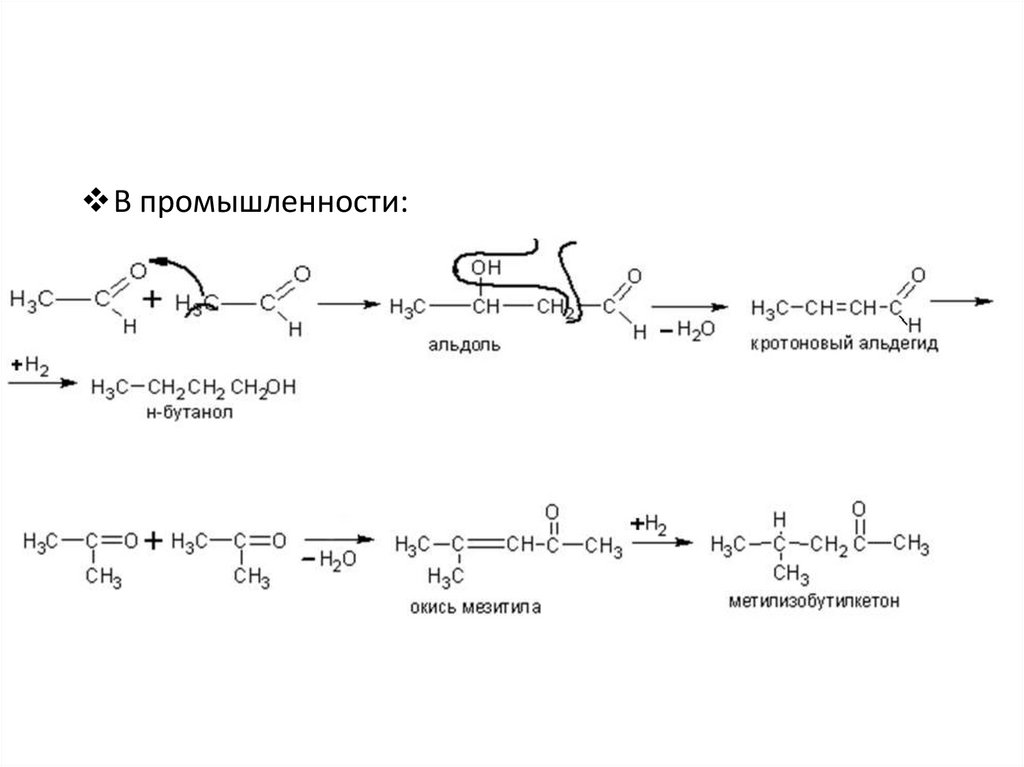
• Н-пропанол и изо-бутанол экономичнее получатьвосстановлением альдегидов
СО
СОСО
4.
RCHO +HO CH2 R
O
R HC
HO CH2 R
O
CH2 R
CH2 R
+ H2O
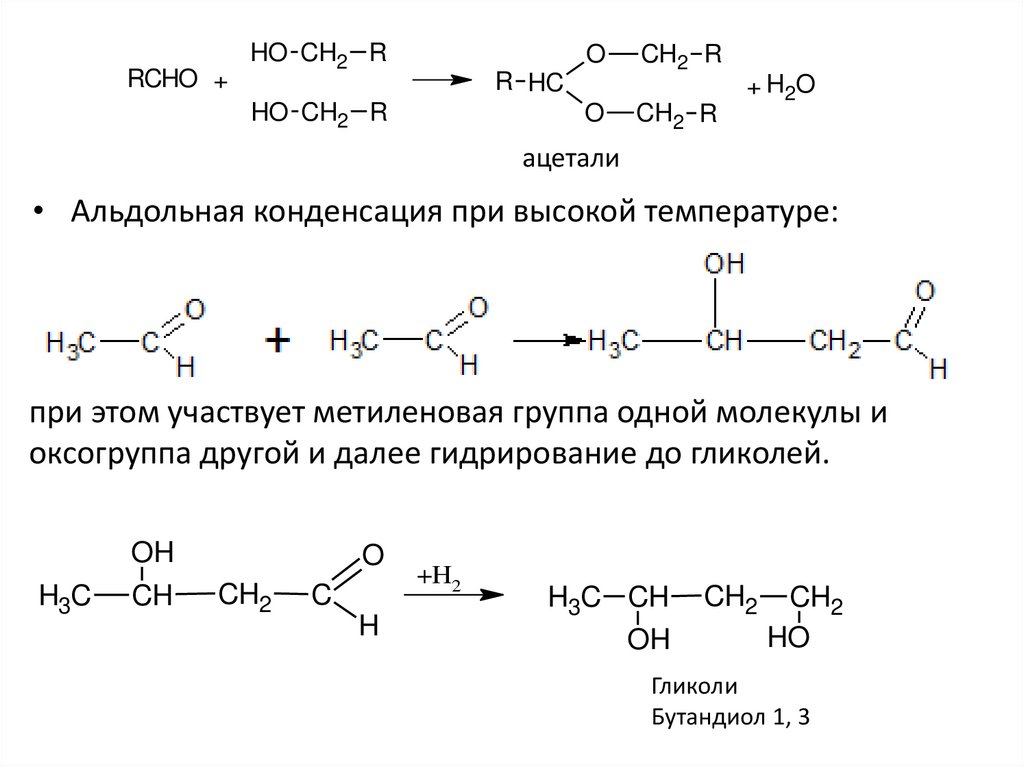
ацетали
• Альдольная конденсация при высокой температуре:
при этом участвует метиленовая группа одной молекулы и
оксогруппа другой и далее гидрирование до гликолей.
OH
H3C
CH
O
CH2
C
H
+H2
H3C CH
OH
CH2
CH2
HO
Гликоли
Бутандиол 1, 3
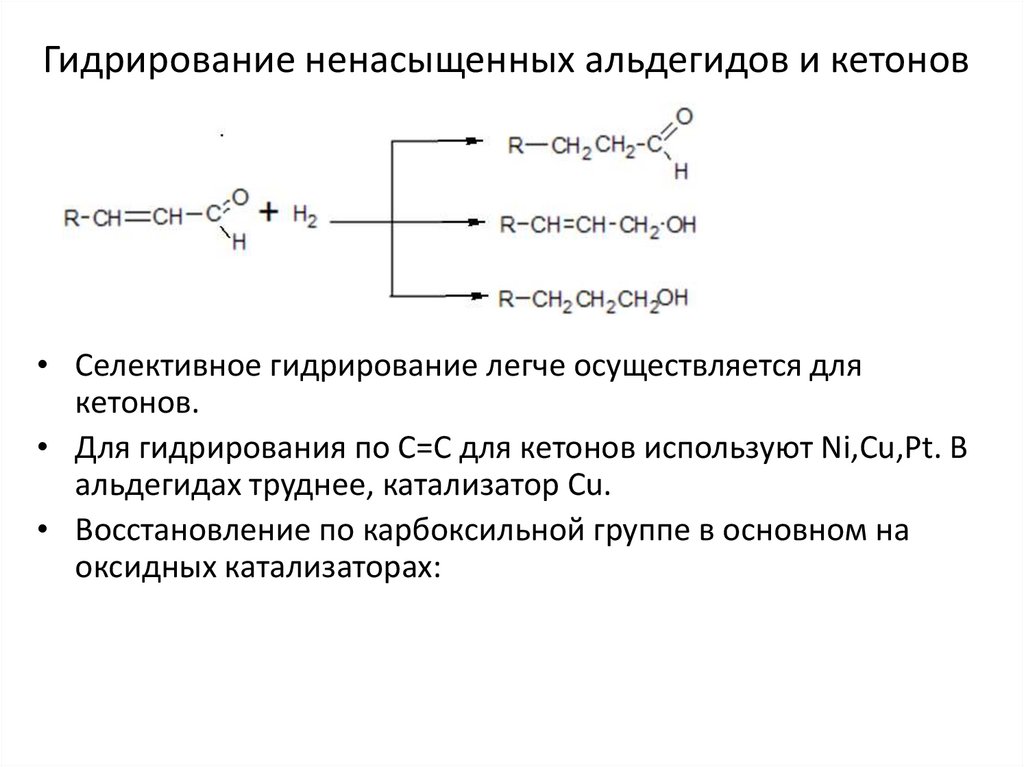
5. Гидрирование ненасыщенных альдегидов и кетонов
• Селективное гидрирование легче осуществляется длякетонов.
• Для гидрирования по С=С для кетонов используют Ni,Cu,Pt. В
альдегидах труднее, катализатор Cu.
• Восстановление по карбоксильной группе в основном на
оксидных катализаторах:
6.
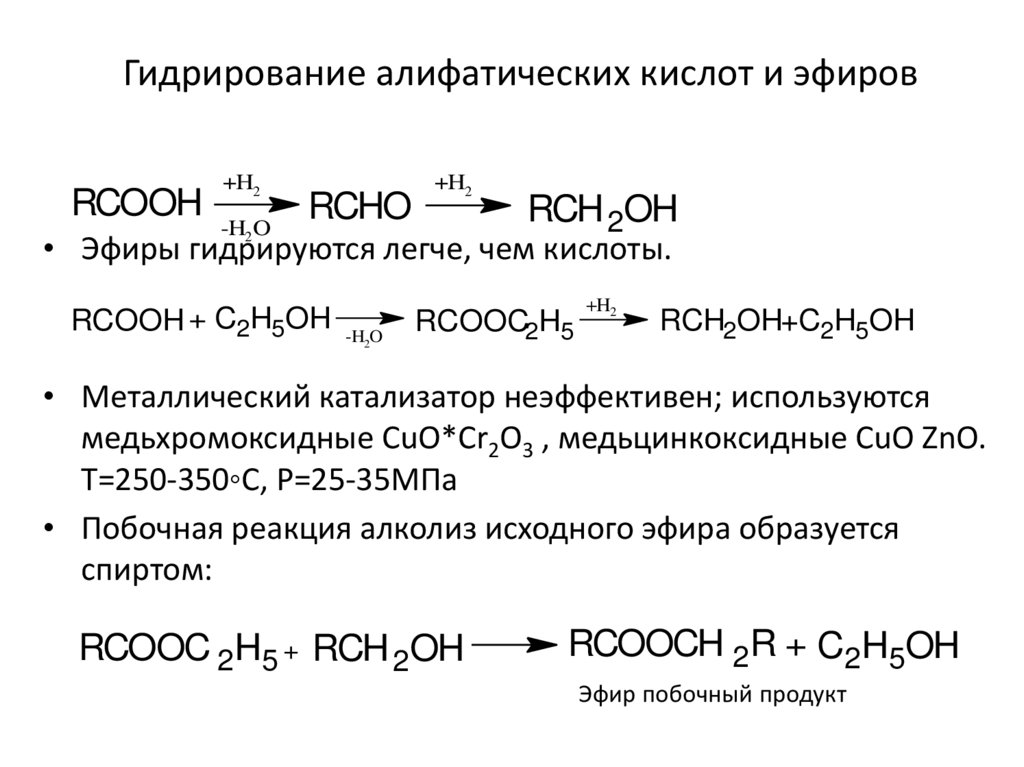
В промышленности:7. Гидрирование алифатических кислот и эфиров
RCOOH+H2
-H2 O
RCHO
+H2
RCH 2OH
• Эфиры гидрируются легче, чем кислоты.
RCOOH + C2H5OH
-H2O
RCOOC2H5
+H2
RCH2OH+C2H5OH
• Металлический катализатор неэффективен; используются
медьхромоксидные CuO*Cr2O3 , медьцинкоксидные CuO ZnO.
Т=250-350◦С, Р=25-35МПа
• Побочная реакция алколиз исходного эфира образуется
спиртом:
RCOOC 2H5 + RCH 2OH
RCOOCH 2R + C2H5OH
Эфир побочный продукт
8.
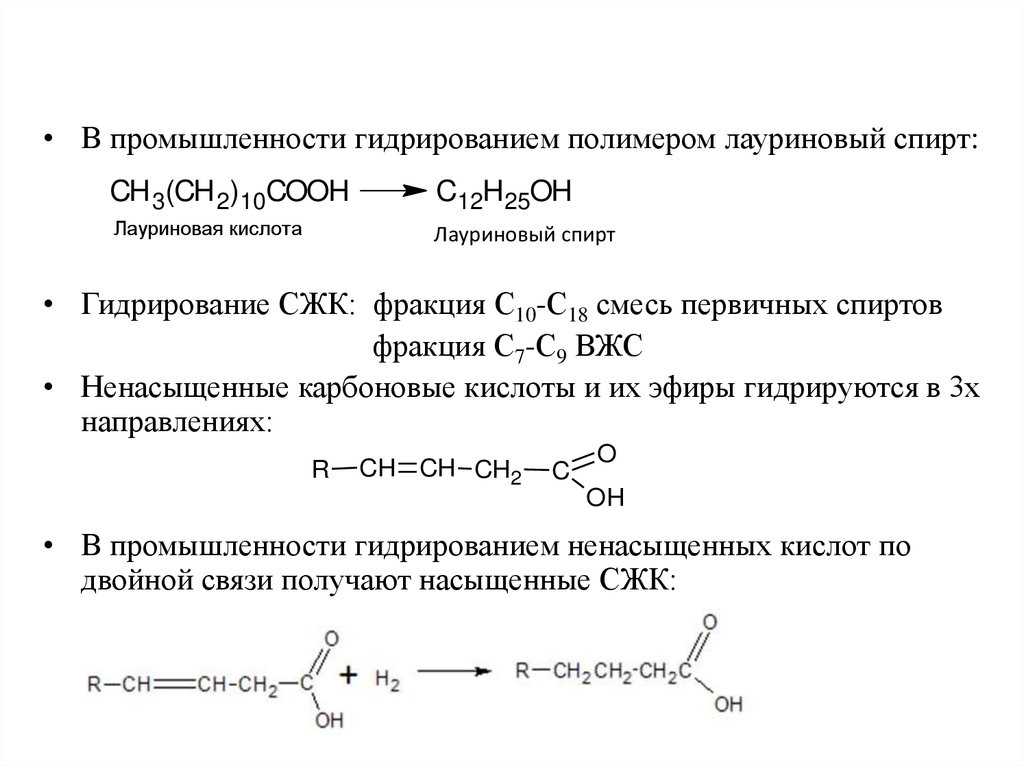
• В промышленности гидрированием полимером лауриновый спирт:CH 3(CH 2)10COOH
C12H25OH
Лауриновая кислота
Лауриновый спирт
• Гидрирование СЖК: фракция С10-С18 смесь первичных спиртов
фракция С7-С9 ВЖС
• Ненасыщенные карбоновые кислоты и их эфиры гидрируются в 3х
направлениях:
R
CH CH CH2
C
O
OH
• В промышленности гидрированием ненасыщенных кислот по
двойной связи получают насыщенные СЖК:
9.
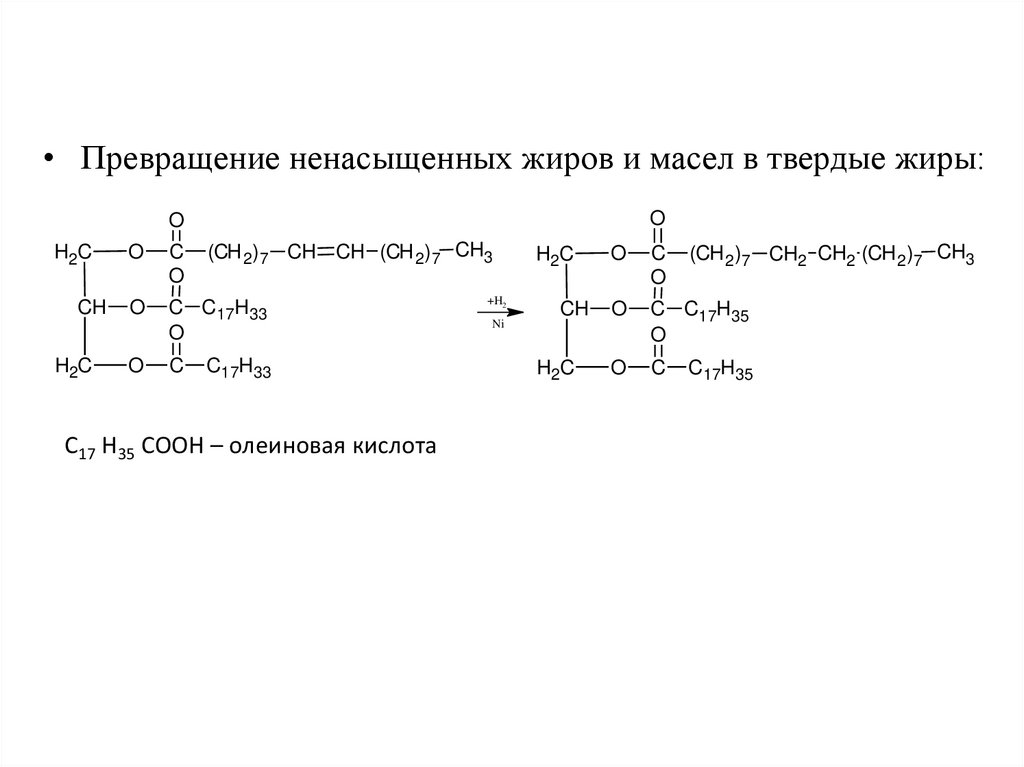
• Превращение ненасыщенных жиров и масел в твердые жиры:O
O
H2C
CH
H2C
(CH 2)7 CH CH (CH 2)7 CH3
O
C
O
O
C C17H33
O
O
C
C17H33
С17 H35 COOH – олеиновая кислота
+H2
Ni
H2C
CH
H2C
(CH 2)7 CH2 CH2 (CH 2)7 CH3
O
C
O
O
C C17H35
O
O
C
C17H35
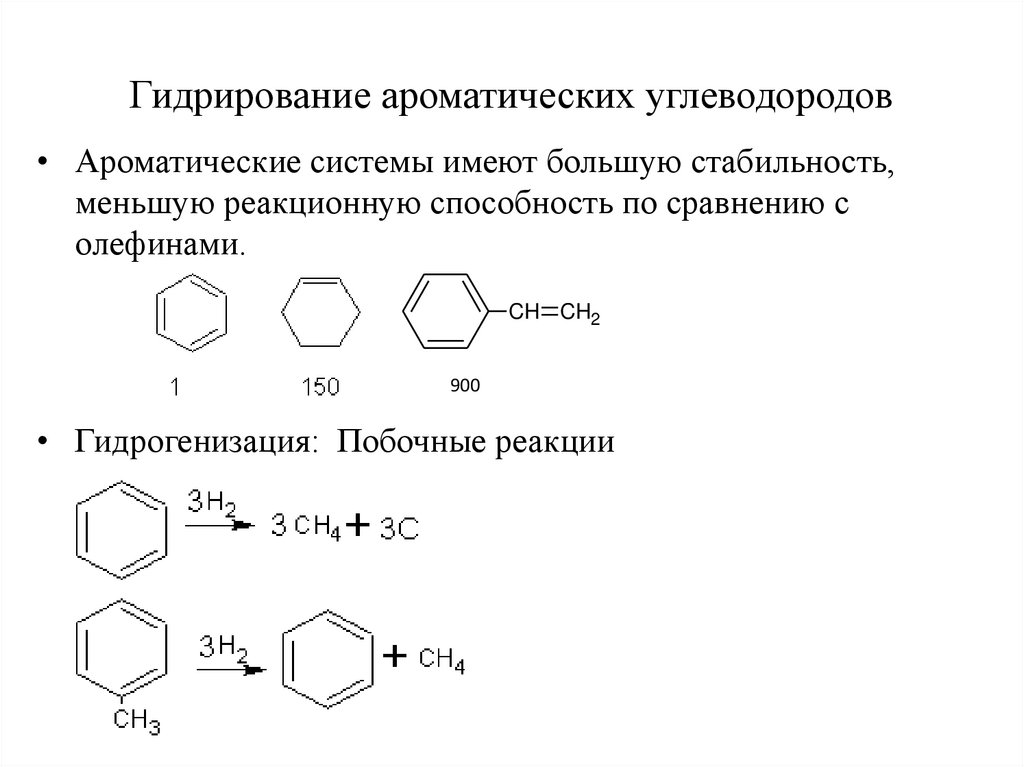
10. Гидрирование ароматических углеводородов
• Ароматические системы имеют большую стабильность,меньшую реакционную способность по сравнению с
олефинами.
CH CH2
900
• Гидрогенизация: Побочные реакции
11.
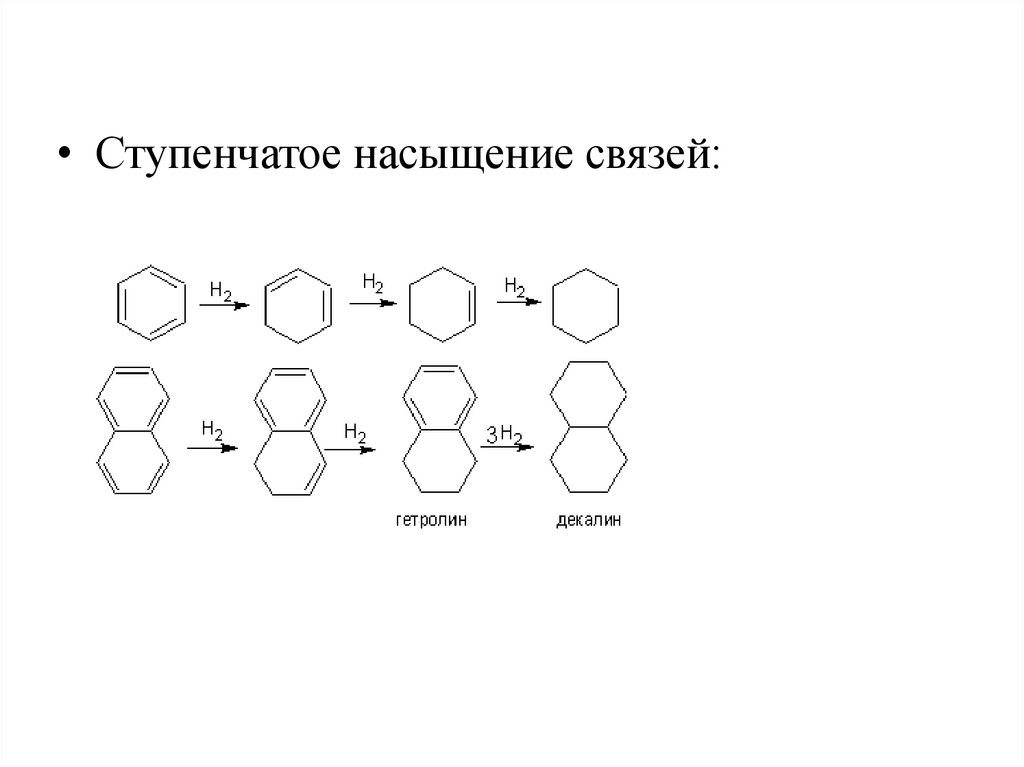
• Ступенчатое насыщение связей:12. Гидрирование ароматических кислородсодержащих соединений
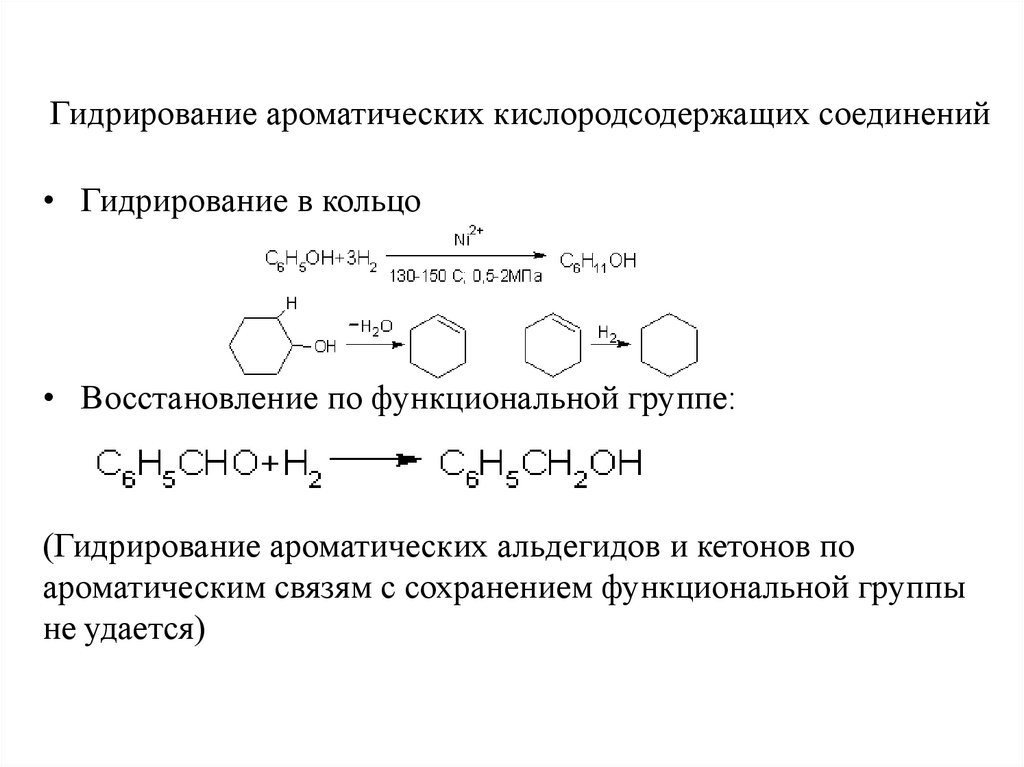
• Гидрирование в кольцо• Восстановление по функциональной группе:
(Гидрирование ароматических альдегидов и кетонов по
ароматическим связям с сохранением функциональной группы
не удается)
13.
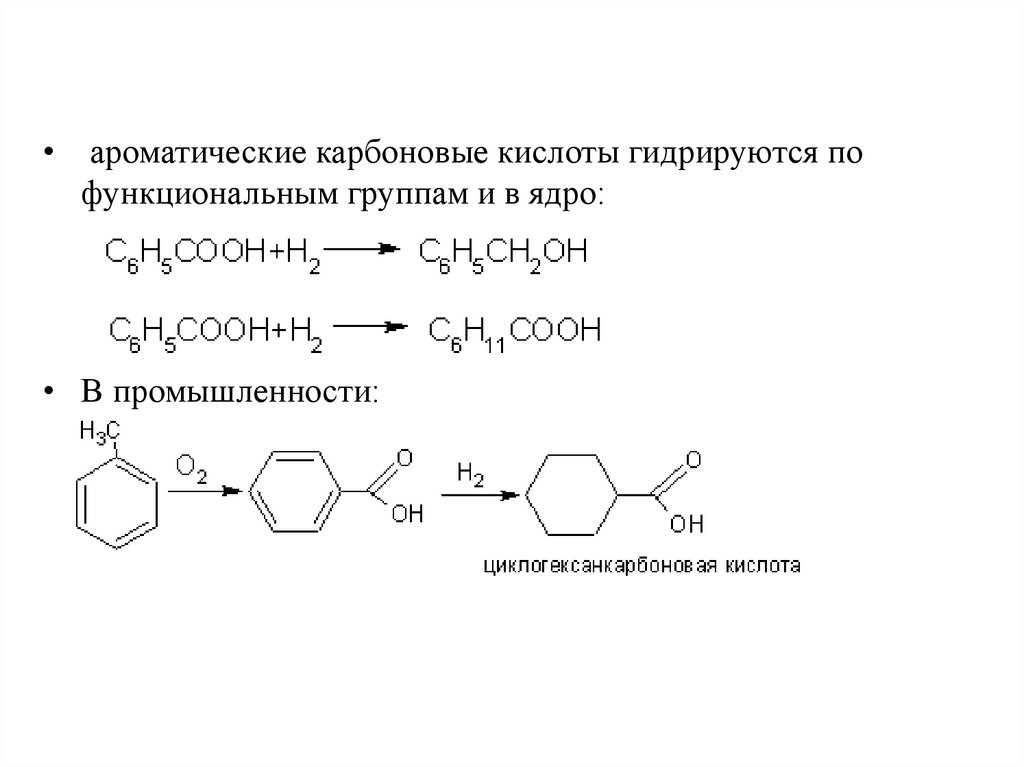
ароматические карбоновые кислоты гидрируются по
функциональным группам и в ядро:
• В промышленности:
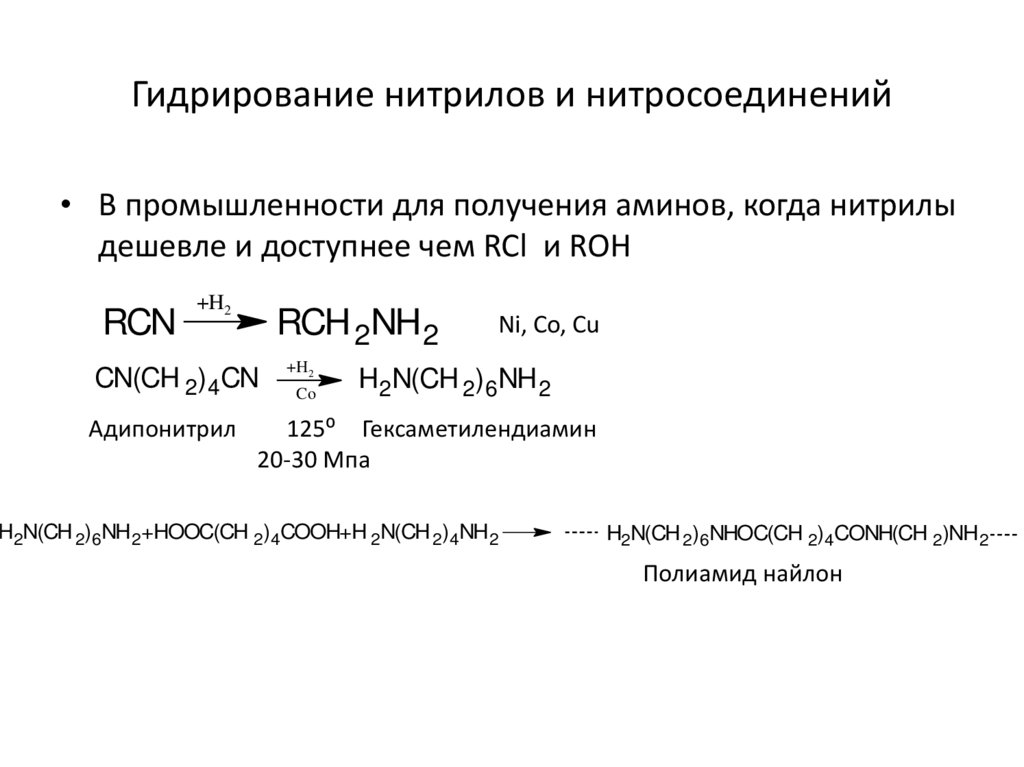
14. Гидрирование нитрилов и нитросоединений
• В промышленности для получения аминов, когда нитрилыдешевле и доступнее чем RCl и ROH
RCN
+H2
RCH 2NH 2
CN(CH 2)4CN
Адипонитрил
+H2
Co
Ni, Co, Cu
H2N(CH 2)6NH 2
125⁰ Гексаметилендиамин
20-30 Мпа
H2N(CH 2)6NH 2+HOOC(CH 2)4COOH+H 2N(CH 2)4NH 2
H2N(CH 2)6NHOC(CH 2)4CONH(CH 2)NH 2
Полиамид найлон
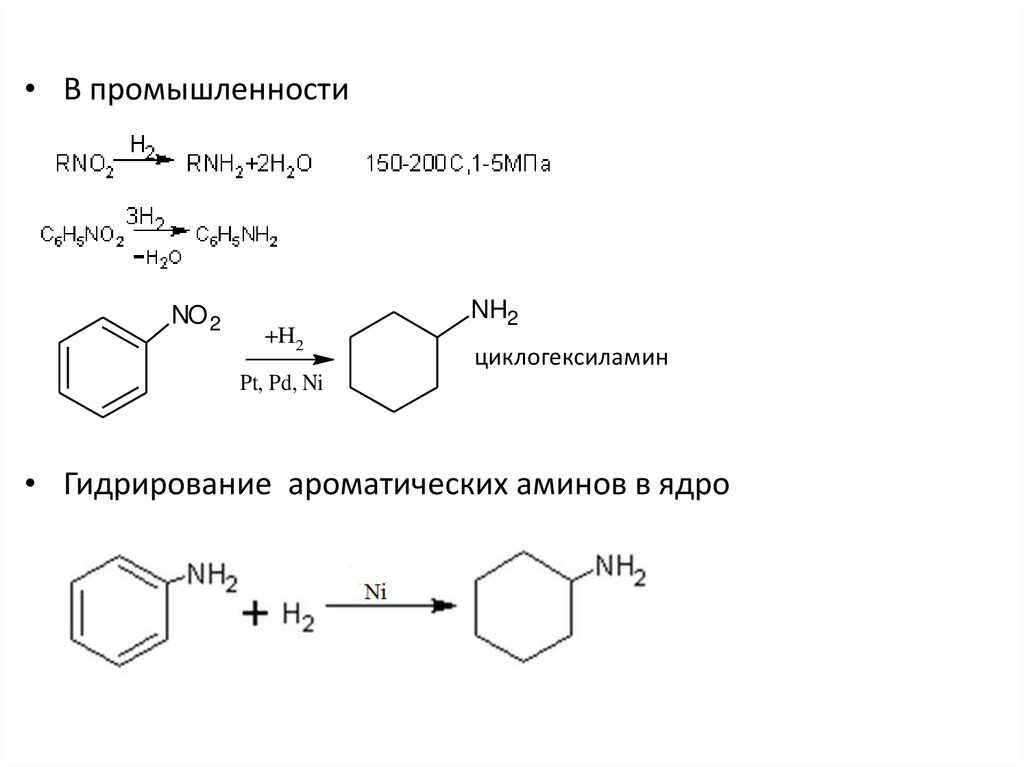
15.
• В промышленностиNO 2
+H2
NH2
циклогексиламин
Pt, Pd, Ni
• Гидрирование ароматических аминов в ядро

 Химия
Химия








