Похожие презентации:
Предельные одноатомные спирты
1.
«Предельные одноатомные спирты»2.
Понятие функциональнойгруппы
Функциональная группа -
совокупность атомов,
определяющая характерные
химические свойства данного
класса веществ.
- ОН гидроксильная группа
- СООН карбоксильная группа
- СОН альдегидная группа
3.
Напишите структурнуюформулу этана и один атом
водорода замените на ОН
группу:
СН3 – СН2 - ОН
4.
5.
Спиртами называются органическиевещества, молекулы которых
содержат одну или несколько
функциональных гидроксильных
групп, соединенных с
углеводородным радикалом.
6.
Из истории возникновенияалкоголя
Похититель рассудка — так именуют алкоголь с давних
времен. Чистый спирт начали получать в 5-7 веках
арабы и назвали « аль коголь», что означает «
одурманивающий». Об опьяняющих свойствах
спиртных напитков люди узнали не менее чем за 8000
лет до нашей эры – с появлением керамической
посуды, давшей возможность изготовления
алкогольных напитков из меда, плодовых соков и
дикорастущего винограда. Возможно, виноделие
возникло еще до начала культурного земледелия.
Так, известный путешественник Н.Н. Миклухо-Маклай
наблюдал папуасов Новой Гвинеи, не умевших еще
добывать огонь, но знавших уже приемы
приготовления хмельных напитков.
7.
8.
Спирты в РоссииВ дохристианскую эпоху на Руси
потребление алкоголя имело место главным
образом на языческих пиршествах (народный
и княжеский пиры, игрища, тризны).
Известно, что в Древней Руси пьянства не
было вовсе. Население Древней Руси
невыращивало виноград, и вино для
Причастного таинства привозилось из
Византии. Хмельными напитками были
бродивший мёд и пиво. С этих далеких времен
сохранился назаменитый рефрен многих
народных сказок: “И я там был. Мед, пиво пил.
По усам текло, а в рот не попало”.
9.
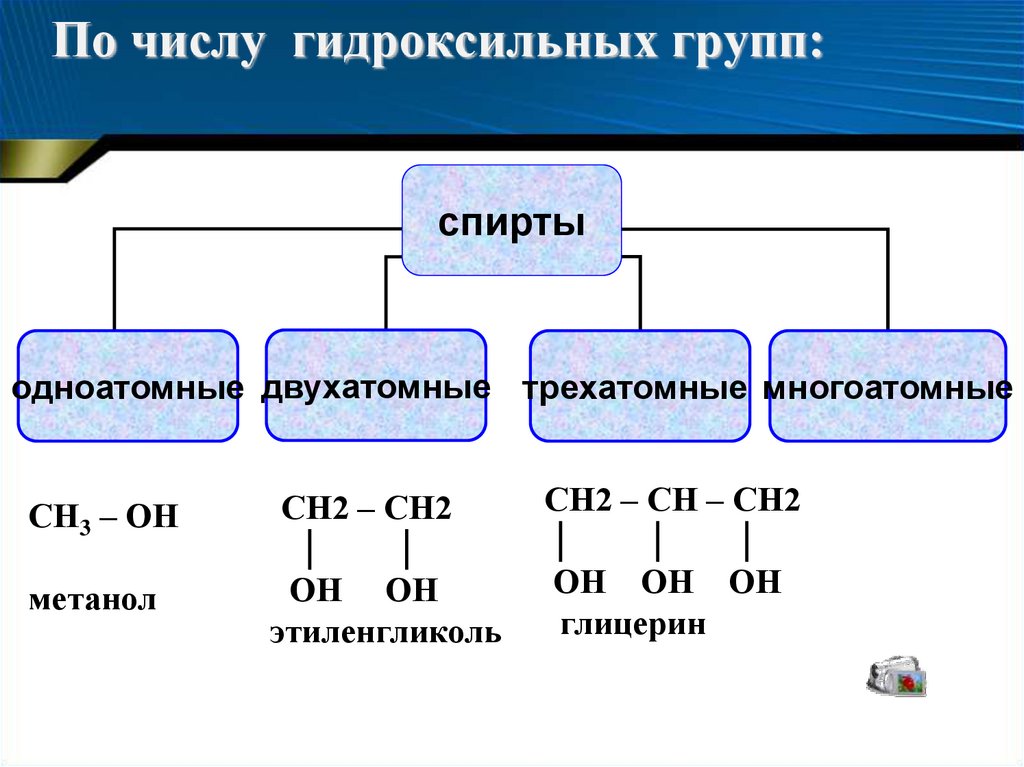
По числу гидроксильных групп:спирты
одноатомные двухатомные трехатомные многоатомные
СН3 – ОН
метанол
СН2 – СН2
ОН ОН
этиленгликоль
СН2 – СН – СН2
ОН ОН ОН
глицерин
10.
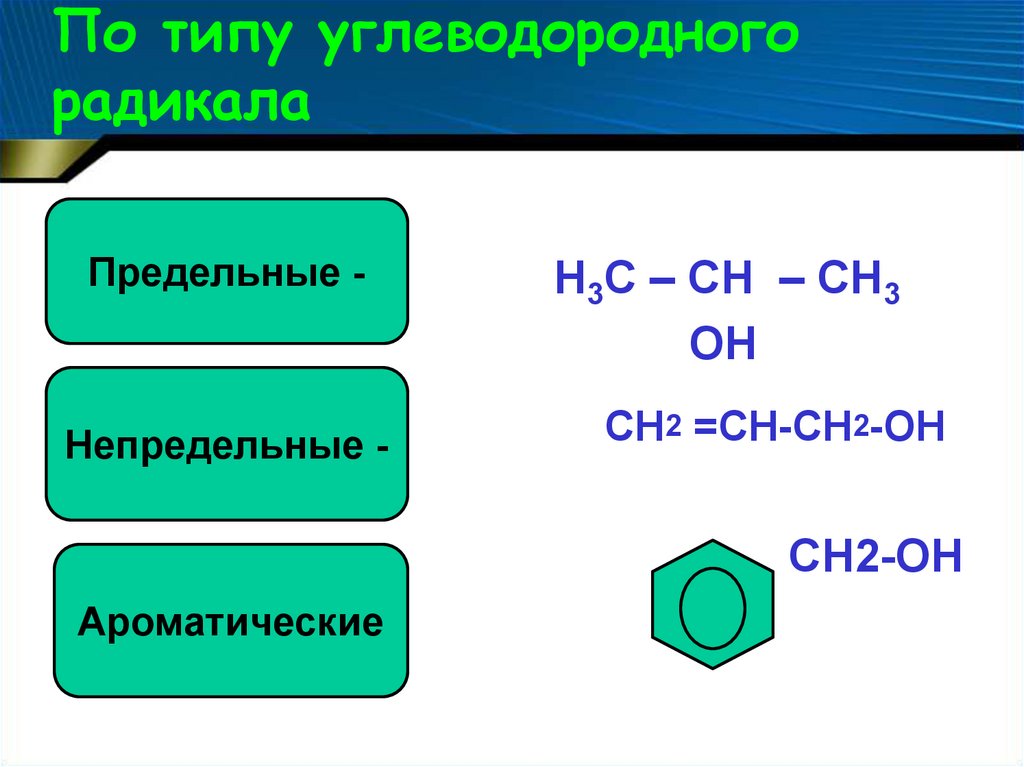
По типу углеводородногорадикала
Предельные -
Непредельные -
Н3С – СН – СН3
ОН
СН2 =СН-СН2-ОН
СН2-ОН
Ароматические
11.
По положению гидроксильнойгруппы:
Одноатомные спирты
Первичный
Вторичный
Третичный
12.
Этанол, пентанол-213.
14.
Вывод• Названия одноатомных спиртов
образуются из названия углеводорода с
самой длинной углеродной цепью,
содержащей гидроксильную группу, путём
добавления суффикса -ол.
• Для многоатомных спиртов перед
суффиксом -ол по-гречески (-ди-, -три-, ...)
указывается количество гидроксильных
групп.
• Например: CH3-CH2-OH этанол
15.
Номенклатура и изомерияЦифрами после суффикса указывают положение
гидроксильной группы в главной цепи:
H
|
H- C – O H
|
H
метанол
H H H
3 |2 |1
H- C – C – C -OH
|
| |
H H H
пропанол-1
H H H
1 | 2 |3
H - C – C – C -H
|
| |
H OH H
пропанол -2
16.
17.
Физические свойства.• Температура кипения спиртов выше
температуры кипения соответствующих
углеводородов.
• Среди спиртов нет газов.
• С увеличением относительной молекулярной
массы спиртов повышаются их температуры
кипения, уменьшается растворимость в воде.
18.
Это объясняется наличием межмолекулярнойводородной связи, которая может
образовываться как между молекулами
спиртов, так и между молекулами спиртов и
воды.
19.
20.
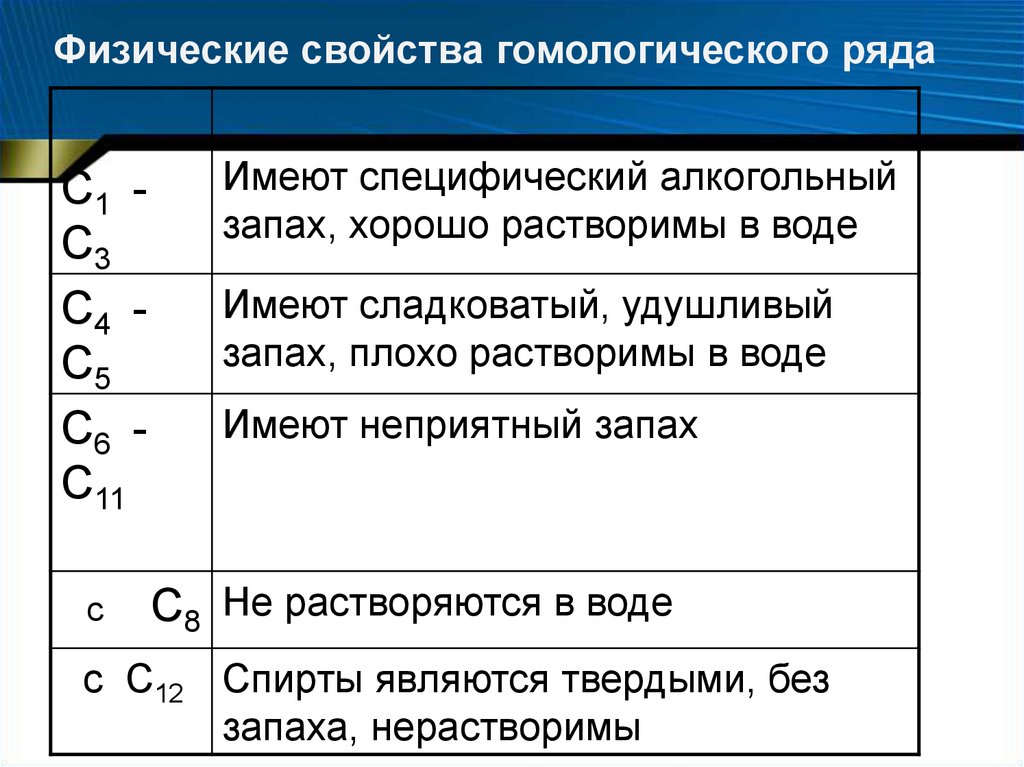
Физические свойства гомологического рядаC1 C3
C4 C5
C6 C11
c
Имеют специфический алкогольный
запах, хорошо растворимы в воде
Имеют сладковатый, удушливый
запах, плохо растворимы в воде
Имеют неприятный запах
C8 Не растворяются в воде
c C12 Спирты являются твердыми, без
запаха, нерастворимы
21.
Физические свойства• Низшие и средние спирты (С -C )1
11
летучие, бесцветные жидкости с
резким, характерным алкогольным
запахом, жгучим вкусом.
Растворимы в воде до актонола.
• Высшие спирты (C - и выше)12
твердые вещества с приятным
запахом. Нерастворимы в воде.
22.
• Домашнее задание:• П.15, упр.1, 3
23.
Химические свойстваСпирты являются cлабыми амфотерными
соединениями.
I По связи O – H.
Взаимодействие со щелочными и щелочноземельными металлами (кислотные свойства)
2 R – OH + 2 Na
2 R – O-Na + H2
алкоголятNa
1)
Алкоголяты легко гидролизуются:
R – ONa + HOH
ROH + NaOH
24.
Реакция этерификации(от лат. ester –эфир) – образование сложных эфиров.
O
t,H2SO4
R - OH + HO - C – R|
О
H2O + R - O - C – R|
сложный эфир
25.
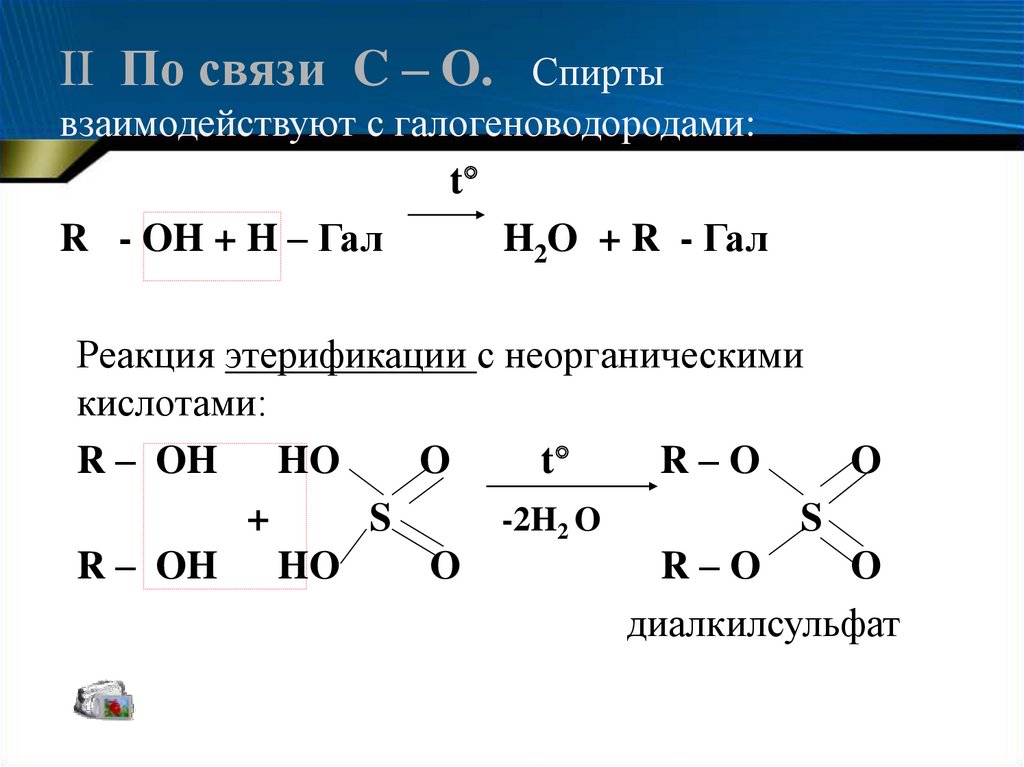
II По связи C – O.Спирты
взаимодействуют с галогеноводородами:
t
R - OH + H – Гал
H2O + R - Гал
Реакция этерификации с неорганическими
кислотами:
R – OH
HO
O
t
R–O
O
+
S
-2H2 O
S
R – OH
HO
O
R–O
O
диалкилсульфат
26.
27.
Реакции, идущие по нескольким связямодновременно
Реакция межмолекулярной дегидратации:
H2SO4 (к), t<140
R-OH + HO-R
H2O + R- O- R
Простой эфир
Реакция внутримолекулярной дегидратации:
H2SO4 (к), t<140
R - CH - CH - R
OH H
R - CH = CH - R
-H2O
Алкен
28.
Взаимодействие спирта с оксидом меди(II)O
t
C2H5OH + CuO
Этанол
CH3 – C
+ Cu + H2O
H
Уксусный альдегид
Горение спирта
C2H5OH + 3O2
2CO2 +3 H2O
29.
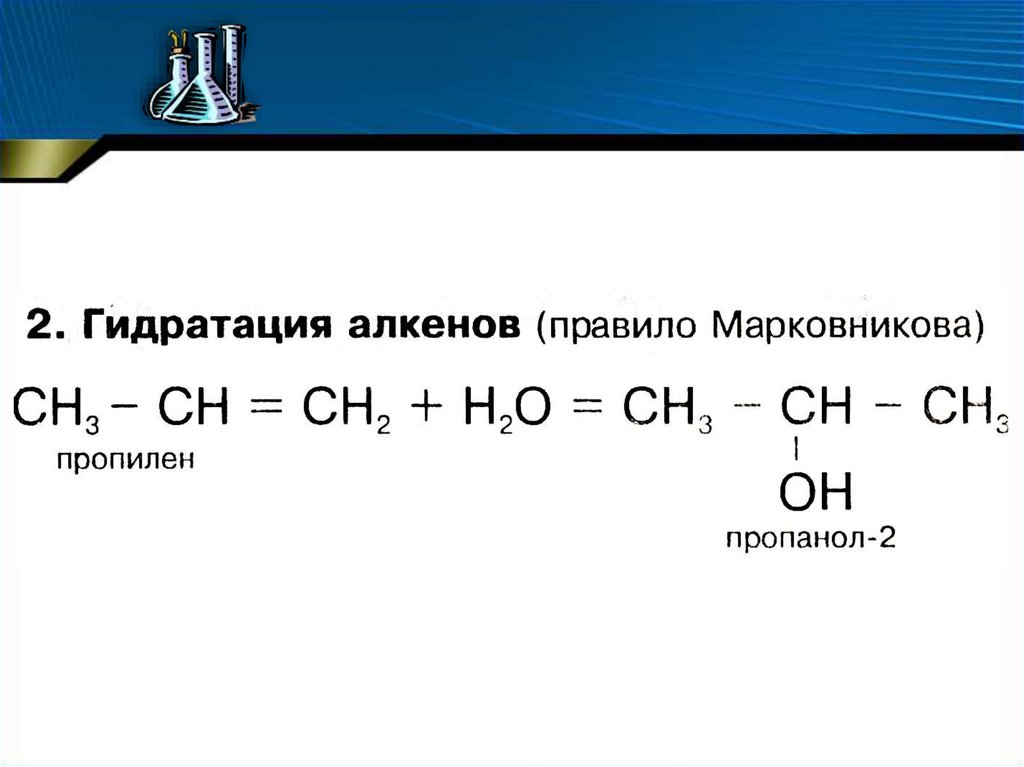
Способы получения спиртов30.
31.
32.
33.
34.
Применение предельныходноатомных спиртов
35.
36.
37.
38.
39.
ПрименениеCH3OH
C2H5OH
Производство формальдегида,
медикаментов.
Получение уксусной кислоты,
медикаментов, красителей,
растворителей, горючего для
двигателей и т.д.
C5H11OH
В парфюмерии ; как реагент для
определения жирности молочных
продуктов.
C16 – C20
Антикоррозийные смазки
40.
Дружить или не дружить соспиртом.
Спирт относится к ксенобиотикам – веществам, не
содержащимся в человеческом организме, но влияющим на
его жизнедеятельность. Все зависит от дозы.
1. Спирт – это питательное вещество, которое
обеспечивает организм энергией. В средние века за счет
потребления алкоголя организм получал около 25%
энергии.
2. Спирт – это лекарственное средство, имеющее
дезинфицирующее и антибактериальное действие.
3. Спирт – это яд, нарушающий естественные
биологические процессы, разрушающий внутренние
органы и психику и при чрезмерном употреблении
влекущий смерть.
41.
В организме алкогольоказывает четыре основных
эффекта:
-обеспечивает организм энергией;
-замедляет работу центральной
нервной системы, снижает ее
эффективность;
-стимулирует производство мочи
(вследствие этого клетки
обезвоживаются);
-выводит из строя печень
42.
43.
ВОПРОСЫ ДЛЯ ЗАКРЕПЛЕНИЯ1. В одном сосуде без подписи находится
вода, а в другом – спирт. Можно ли
воспользоваться индикатором, чтобы
их распознать?
2. Кому принадлежит честь получения
чистого спирта?
3. Может ли спирт быть твердым
веществом?
4. Молекулярная масса метанола 32, а
углекислого газа 44. Сделайте вывод об
агрегатном состоянии спирта.
44.
Дополнительное заданиеСпирту, название которого 3 –
метилпентанол -1 соответствует
структурная формула:
45.
Домашнее задание:• П. 16, упр.1-2
• П.17







































 Химия
Химия