Похожие презентации:
Предельные одноатомные спирты
1.
2.
Определение спиртов
Классификация спиртов
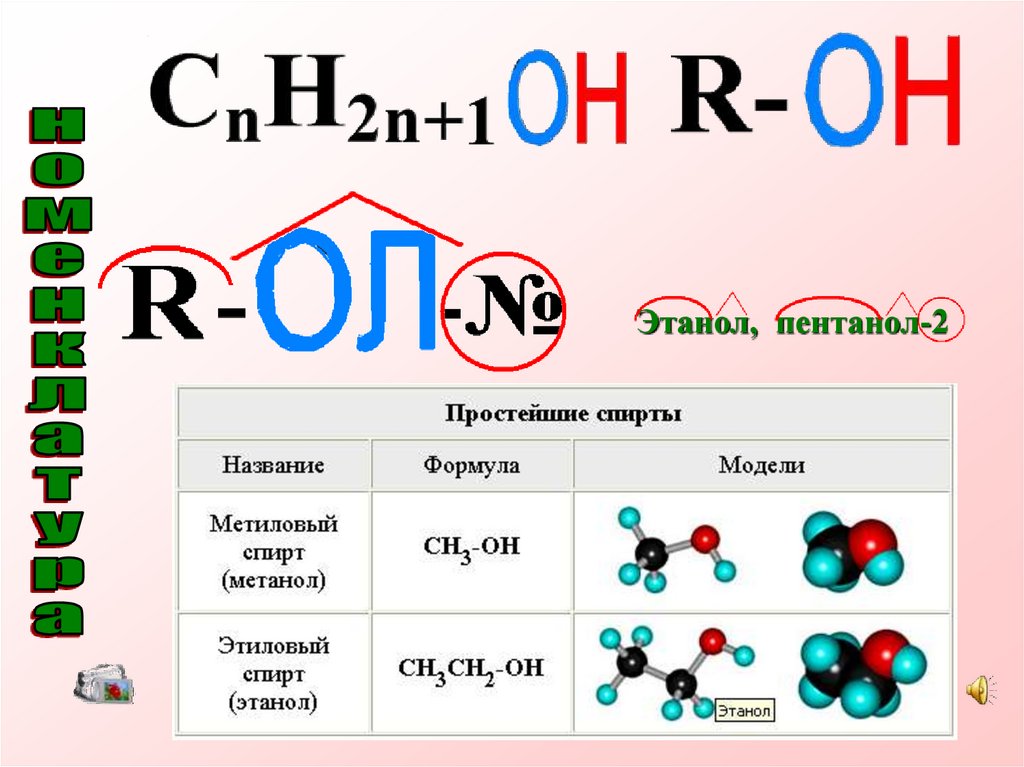
Номенклатура
Изомерия
Физические свойства
Химические свойства
Физиологическое действие спиртов
Применение спиртов
Получение спиртов
3.
Спиртами называются органическиевещества, молекулы которых
содержат одну или несколько
функциональных гидроксильных
групп, соединенных с
углеводородным радикалом.
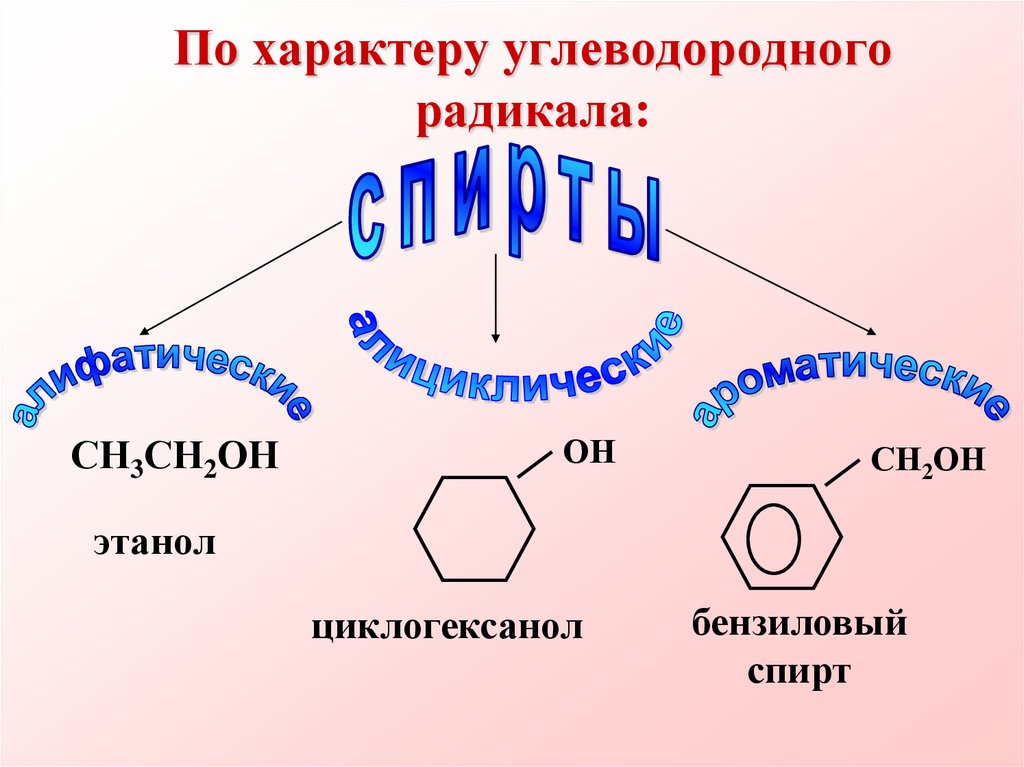
4. По характеру углеводородного радикала:
СН3СН2ОНОН
СН2ОН
этанол
циклогексанол
бензиловый
спирт
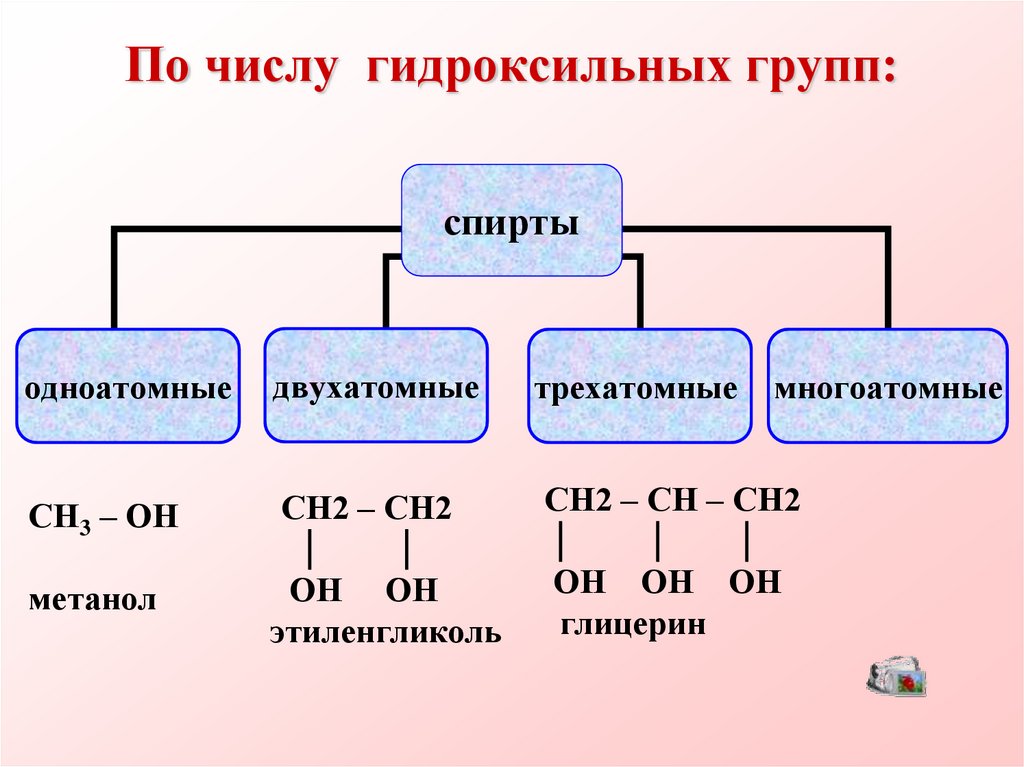
5. По числу гидроксильных групп:
спиртыодноатомные
двухатомные
СН3 – ОН
СН2 – СН2
метанол
ОН ОН
этиленгликоль
трехатомные
многоатомные
СН2 – СН – СН2
ОН ОН ОН
глицерин
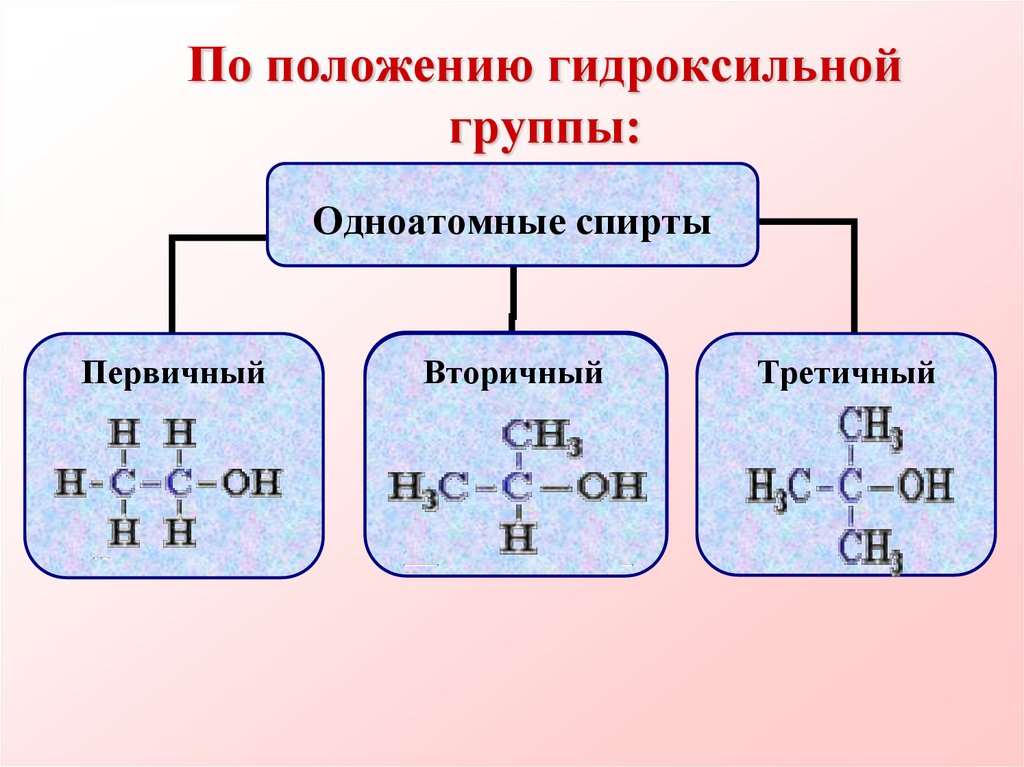
6. По положению гидроксильной группы:
Одноатомные спиртыПервичный
Вторичный
Третичный
7.
Этанол, пентанол-28.
Вывод• Названия одноатомных спиртов
образуются из названия углеводорода с
самой длинной углеродной цепью,
содержащей гидроксильную группу, путём
добавления суффикса -ол.
• Для многоатомных спиртов перед
суффиксом -ол по-гречески (-ди-, -три-, ...)
указывается количество гидроксильных
групп.
• Например: CH3-CH2-OH этанол
9. Виды изомерии спиртов
Структурная1. Углеродной
цепи
2. Положения
функционально
й группы
10. Физические свойства.
• Температура кипения спиртов вышетемпературы кипения соответствующих
углеводородов.
• Среди спиртов нет газов.
• С увеличением относительной молекулярной
массы спиртов повышаются их температуры
кипения, уменьшается растворимость в воде.
11.
Это объясняется наличием межмолекулярнойводородной связи, которая может
образовываться как между молекулами
спиртов, так и между молекулами спиртов и
воды.
R-O
R
Hδ+--- Oδ- H
R–O
H
Hδ+--- Oδ-
H
12.
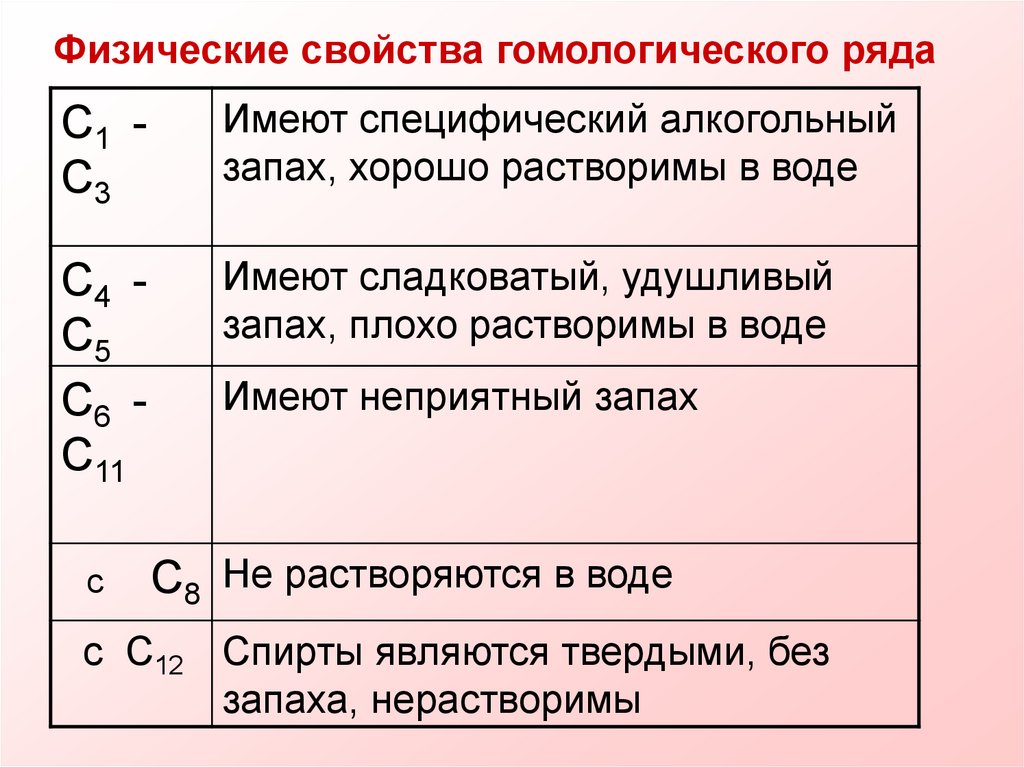
Физические свойства гомологического рядаC1 C3
Имеют специфический алкогольный
запах, хорошо растворимы в воде
C4 C5
C6 C11
Имеют сладковатый, удушливый
запах, плохо растворимы в воде
c
Имеют неприятный запах
C8 Не растворяются в воде
c C12 Спирты являются твердыми, без
запаха, нерастворимы
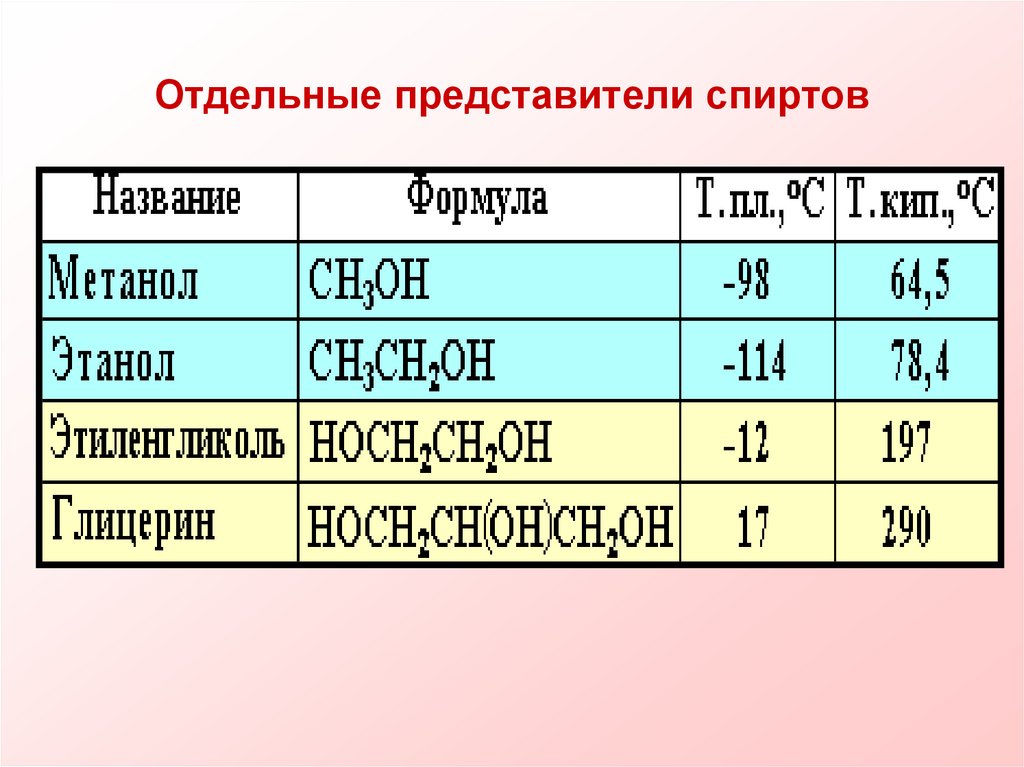
13. Отдельные представители спиртов
14. Химические свойства
Спирты являются амфотерными соединениями.I По связи O – H.
1) Взаимодействие со щелочными и щелочно-
земельными металлами
2 R – OH + 2 Na
2 R – O-Na + H2
алкоголятNa
Алкоголяты легко гидролизуются:
R – ONa + HOH
ROH + NaOH
15.
Реакция этерификации(от лат. ester –эфир) – образование сложных эфиров.
O
t,H2SO4
R - OH + HO - C – R|
О
H2O + R - O - C – R|
сложный эфир
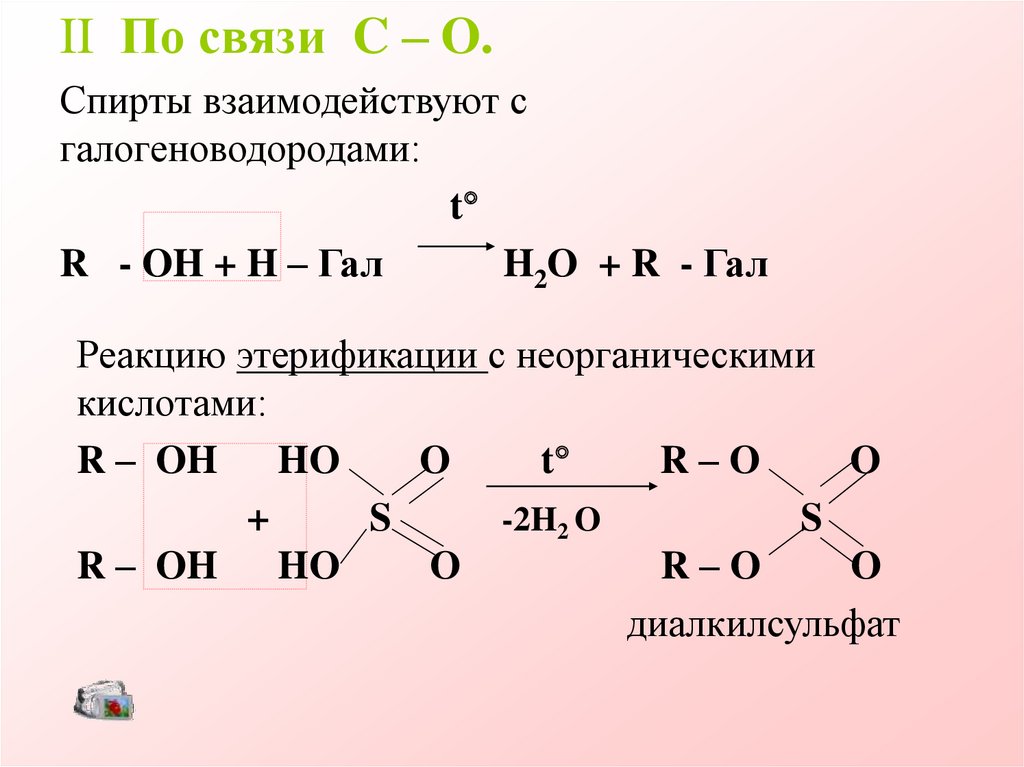
16.
II По связи C – O.Спирты взаимодействуют с
галогеноводородами:
t
R - OH + H – Гал
H2O + R - Гал
Реакцию этерификации с неорганическими
кислотами:
R – OH
HO
O
t
R–O
O
+
S
-2H2 O
S
R – OH
HO
O
R–O
O
диалкилсульфат
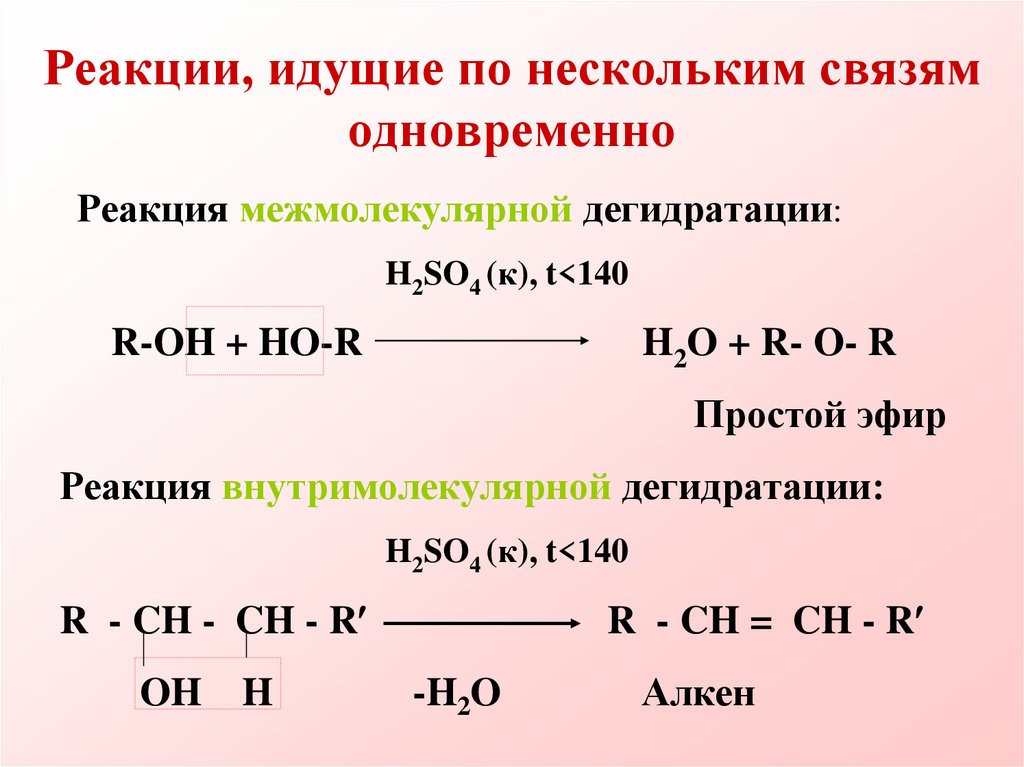
17. Реакции, идущие по нескольким связям одновременно
Реакция межмолекулярной дегидратации:H2SO4 (к), t<140
R-OH + HO-R
H2O + R- O- R
Простой эфир
Реакция внутримолекулярной дегидратации:
H2SO4 (к), t<140
R - CH - CH - R
OH H
R - CH = CH - R
-H2O
Алкен
18.
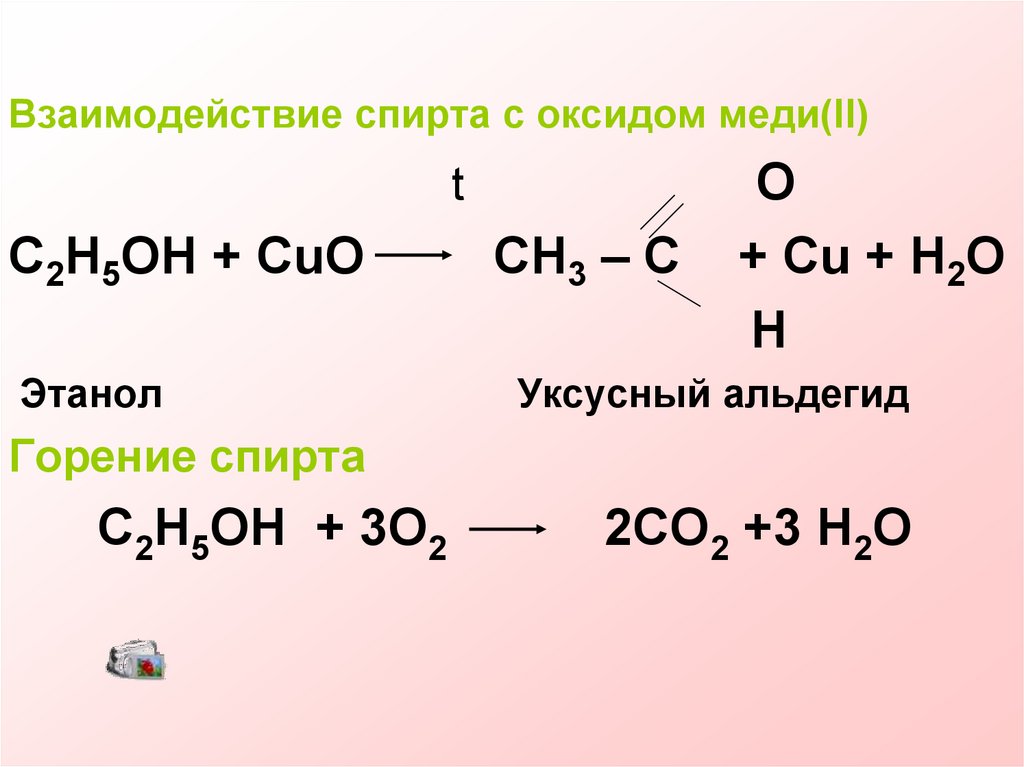
Взаимодействие спирта с оксидом меди(II)t
C2H5OH + CuO
Этанол
CH3 – C
O
+ Cu + H2O
H
Уксусный альдегид
Горение спирта
C2H5OH + 3O2
2CO2 +3 H2O
19. Вредное воздействие этанола
• Изменения структуры мозга, вызванныемноголетней алкогольной
интоксикацией, почти необратимы, и
даже после длительного воздержания от
употребления спиртных напитков они
сохраняются. Если же человек не может
остановиться, то органические и,
следовательно, психические отклонения
от нормы идут по нарастающей.
20. Вредное воздействие этанола
• Алкоголь крайне неблагоприятно влияетна сосуды головного мозга. В начале
опьянения они расширяются, кровоток в
них замедляется, что приводит к
застойным явлениям в головном мозге.
Затем, когда в крови помимо алкоголя
начинают накапливаться вредные
продукты его неполного распада,
наступает резкий спазм, сужение сосудов,
развиваются такие опасные осложнения,
как мозговые инсульты, приводящие к
тяжелой инвалидности и даже смерти.
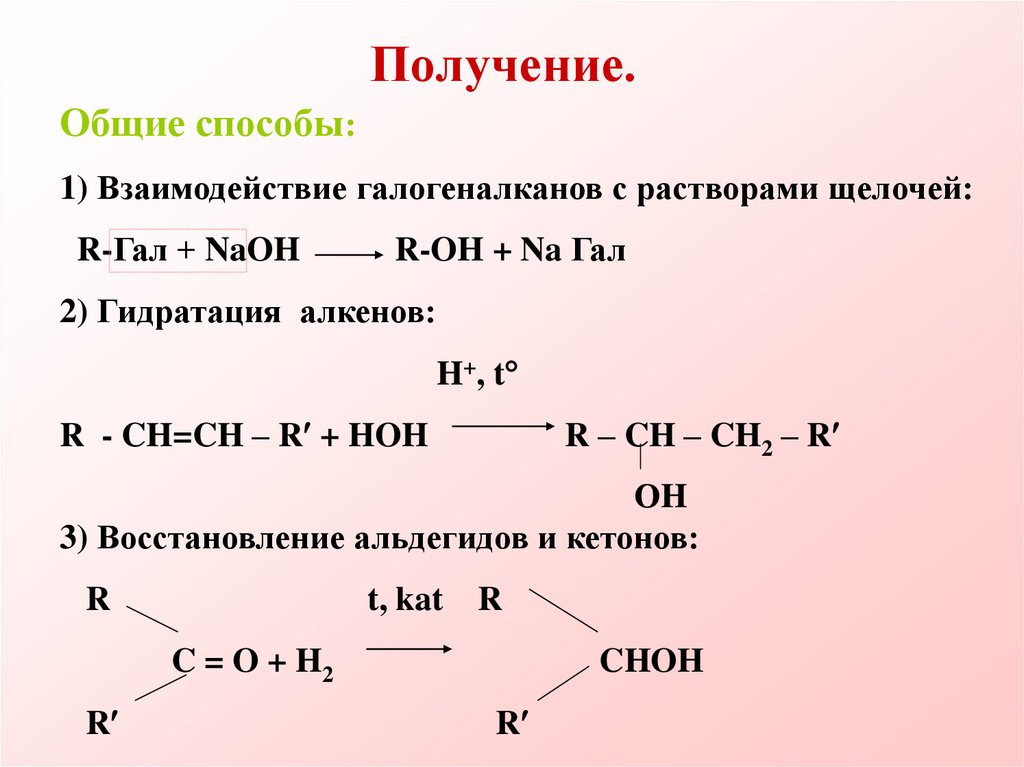
21. Получение.
Общие способы:1) Взаимодействие галогеналканов с растворами щелочей:
R-Гал + NaOH
R-OH + Na Гал
2) Гидратация алкенов:
H+, t
R - CH=CH – R + HOH
R – CH – CH2 – R
ОH
3) Восстановление альдегидов и кетонов:
R
t, kat
R
C = O + H2
R
CHOH
R
22. Получение
Частные способы.Метанол получают из синтез – газа.
t, P, ZnO
CO + 2H2
CH3OH
Этанол получают брожением глюкозы.
дрожжи
C6H12O6
2CO2 + 2C2H5OH
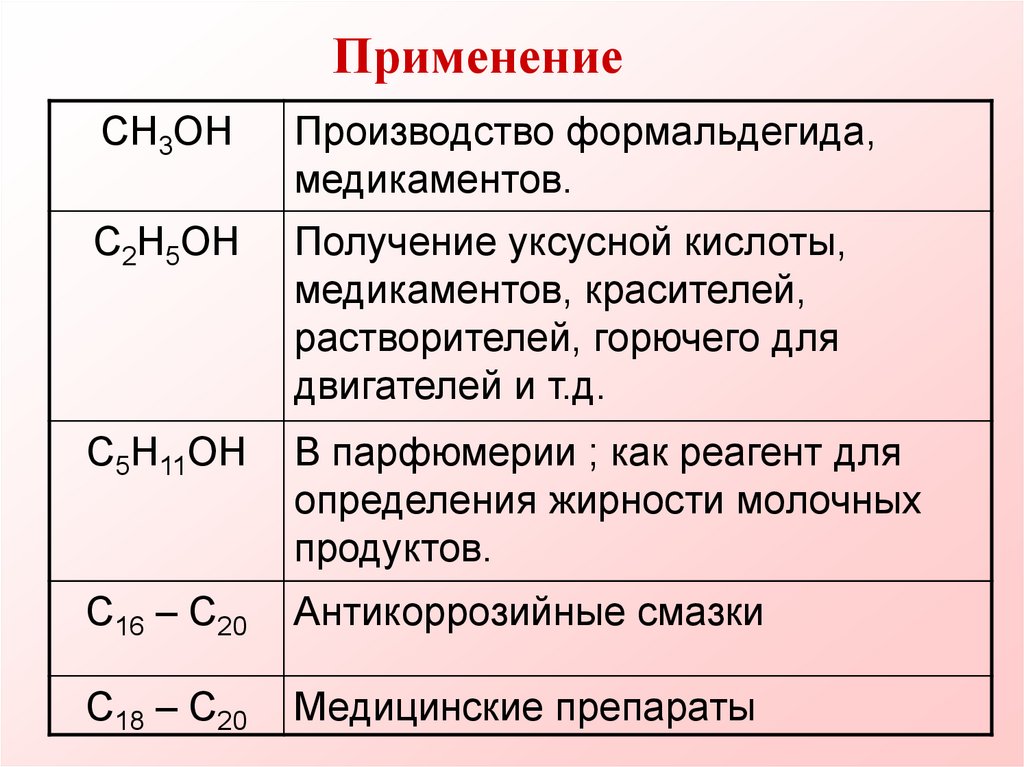
23. Применение
CH3OHПроизводство формальдегида,
медикаментов.
C2H5OH
Получение уксусной кислоты,
медикаментов, красителей,
растворителей, горючего для
двигателей и т.д.
C5H11OH
В парфюмерии ; как реагент для
определения жирности молочных
продуктов.
C16 – C20
Антикоррозийные смазки
C18 – C20
Медицинские препараты












 Химия
Химия