Похожие презентации:
Молекулярная физика. Основное уравнение МКТ
1. Молекулярная физика
2. Основы мкт
Создать ссылки на слайды
с соответствующими
заголовками
Молекулярно-кинетическая теория
Масса и размеры молекул
Количество вещества
Строение газов, жидкостей и твердых тел
Идеальный газ
Среднее значение квадрата скорости молекул
Основное уравнение мкт
3. Молекулярно-кинетическая теория
• МКТ объясняет свойства макроскопических тели тепловых процессов, на основе представлений о
том, что все тела состоят из отдельных,
беспорядочно движущихся частиц.
• Макроскопические тела – тела, состоящие из
большого количества частиц.
• Микроскопические тела – тела, состоящие из
малого количества частиц.
4. Основные положения мкт
• Вещество состоит из частиц• Частицы непрерывно и хаотически
движутся
• Частицы взаимодействуют друг с другом
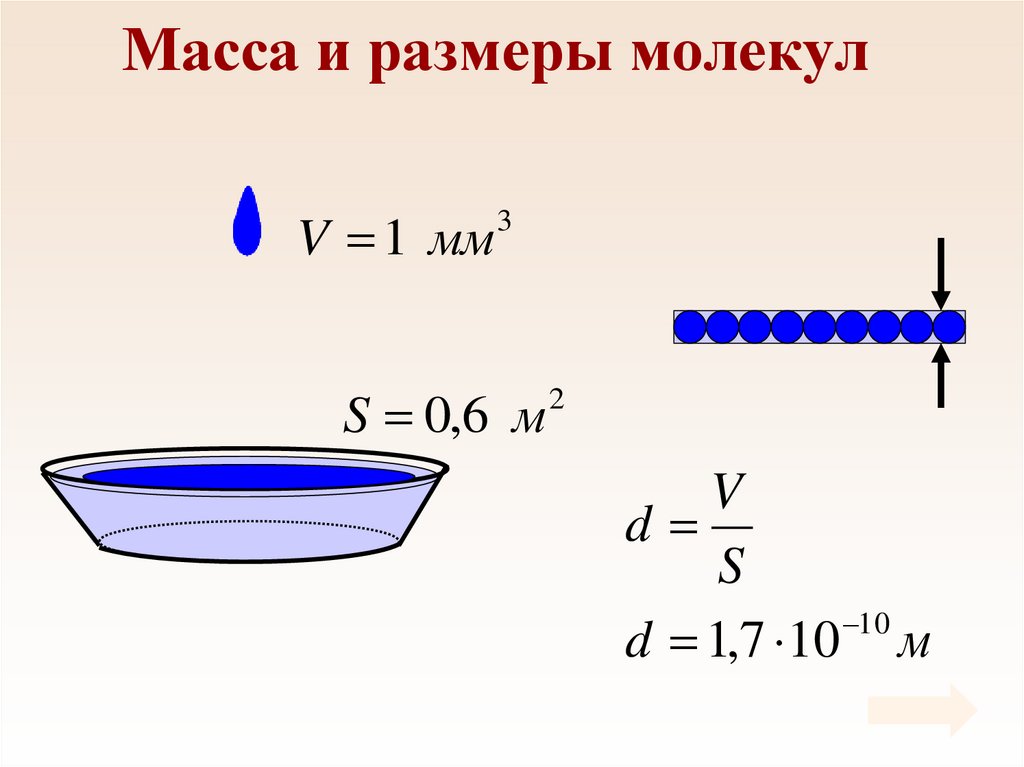
5. Масса и размеры молекул
V 1 мм3
S 0,6 м
2
V
d
S
10
d 1,7 10 м
6. Масса и размеры молекул
22В 1 г воды содержится 3,7 * 10 молекул.
m0 воды
1г
3,7 10
22
2,7 10
23
г
Массы молекул в макроскопических масштабах
чрезвычайно малы.
7. Количество вещества
В 1 моле любого вещества содержится одно и то жечисло атомов или молекул.
1
- постоянная
N A 6,022 10
моль Авогадро
23
Количество вещества равно отношению числа
молекул в данном теле к постоянной Авогадро.
N
NA
8. Количество вещества
Молярной массой вещества называют массувещества, взятого в количестве
1 моль.
m0 N A
кг
моль
m0 - масса одной молекулы или атома
m0
NA
9. Количество вещества
m m0 Nm – масса вещества
m
N
N N A N A
m
- формула для расчета
числа частиц в теле
10. Таблица
Свойства газов, жидкостей итвердых тел
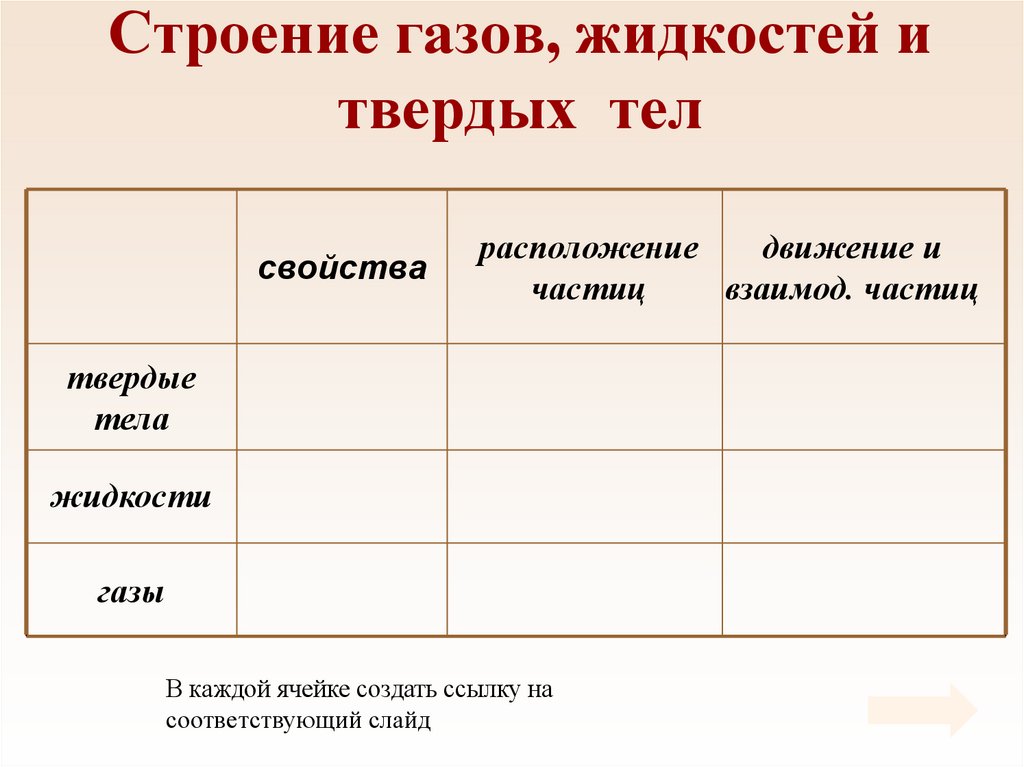
11. Строение газов, жидкостей и твердых тел
свойстварасположение
движение и
частиц
взаимод. частиц
твердые
тела
жидкости
газы
В каждой ячейке создать ссылку на
соответствующий слайд
12. Свойства
• Твердые тела сохраняют объем и форму.13. Свойства
• Жидкости сохраняют объем и принимают формусосуда.
• Обладают текучестью.
14. Свойства
• Газы не имеют формы, занимают весьпредоставленный объем.
15. Расположение частиц
• Частицы расположены в строгом порядкевплотную друг к другу.
• Кристаллическая решетка.
16. Расположение частиц
• Частицы расположены вплотную друг к другу,образуют только ближний порядок.
17. Расположение частиц
• Частицы расположены на значительныхрасстояниях (расстояния между частицами
во много раз больше размеров самих
частиц).
18. Движение и взаимодействие частиц
• Частицы совершают колебательные движенияоколо положения равновесия
• Силы притяжения и отталкивания
значительны
19. Движение и взаимодействие частиц
• Частицы совершают колебательные движенияоколо положения равновесия, изредка совершая
скачки на новое место. Время оседлой жизни
молекулы воды при комнатной температуре 1012с. С ростом температуры время оседлой жизни
уменьшается.
• Силы притяжения и отталкивания значительны
20. Движение и взаимодействие частиц
• Частицы свободно перемещаются по всемуобъему, двигаясь поступательно
• Силы притяжения почти отсутствуют, силы
отталкивания проявляются при соударениях
21. Идеальный газ
Идеальный газ – это газ, в котором• Частицы – материальные точки
• Частицы взаимодействуют только при
соударениях
• Удары абсолютно упругие
22. Среднее значение квадрата скорости молекул
• Скорость – величина векторная, поэтому средняяскорость движения частиц в газе равна нулю.
ср
1 2 3 ...
N
0
23. Среднее значение квадрата скорости молекул
22 3 ...
2
1
2
2
N
x y z
2
2
2
x y z
2
x
2
2
1 2
3
2
2
0
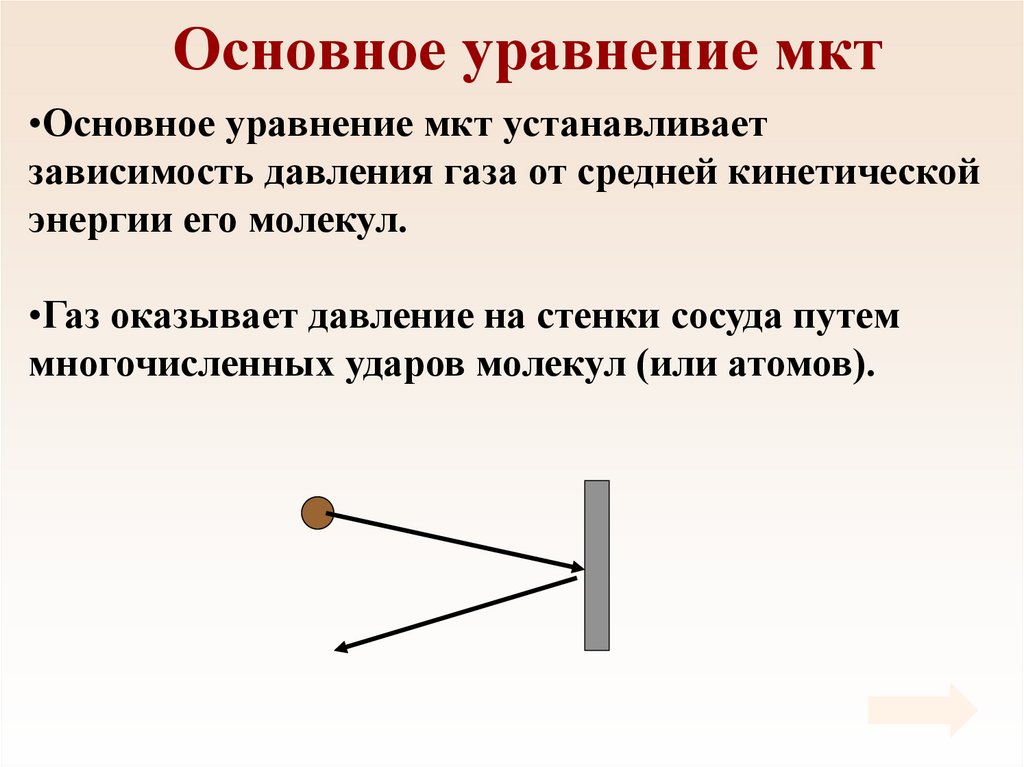
24. Основное уравнение мкт
•Основное уравнение мкт устанавливаетзависимость давления газа от средней кинетической
энергии его молекул.
•Газ оказывает давление на стенки сосуда путем
многочисленных ударов молекул (или атомов).
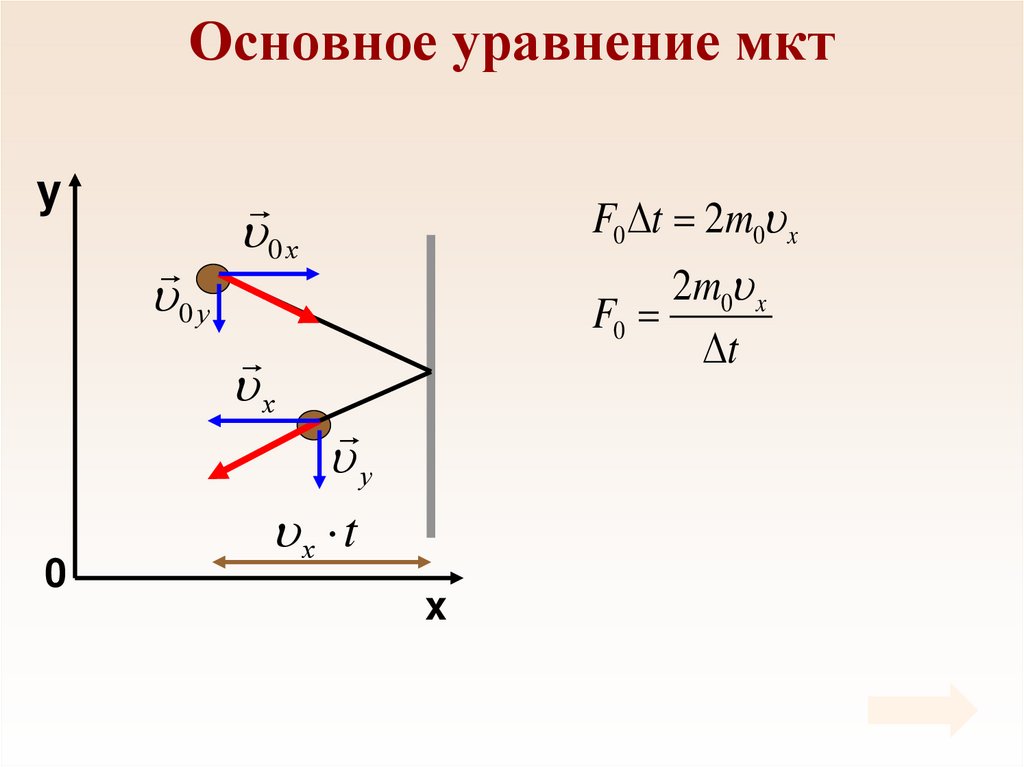
25. Основное уравнение мкт
y0 у
F0 t 2m0 x
0 х
2m0 x
F0
t
х
0
у
х t
x
26. Число ударов и общая сила
Fx N F0L
S
1
2
N nV ,
Fx m0 n x S
2
V SL S x t 2 1 2
1
N nS x t
2
x
3
27. Основное уравнение мкт
12
F nm0 S
3
F
p
S
2
m0
Ek 0
2
1
2
p m0 n
3
2
p nEk 0
3
N m
m0 n m0
V V
1
2
p
3


































 Физика
Физика








