Похожие презентации:
Ароматические углеводороды (арены)
1.
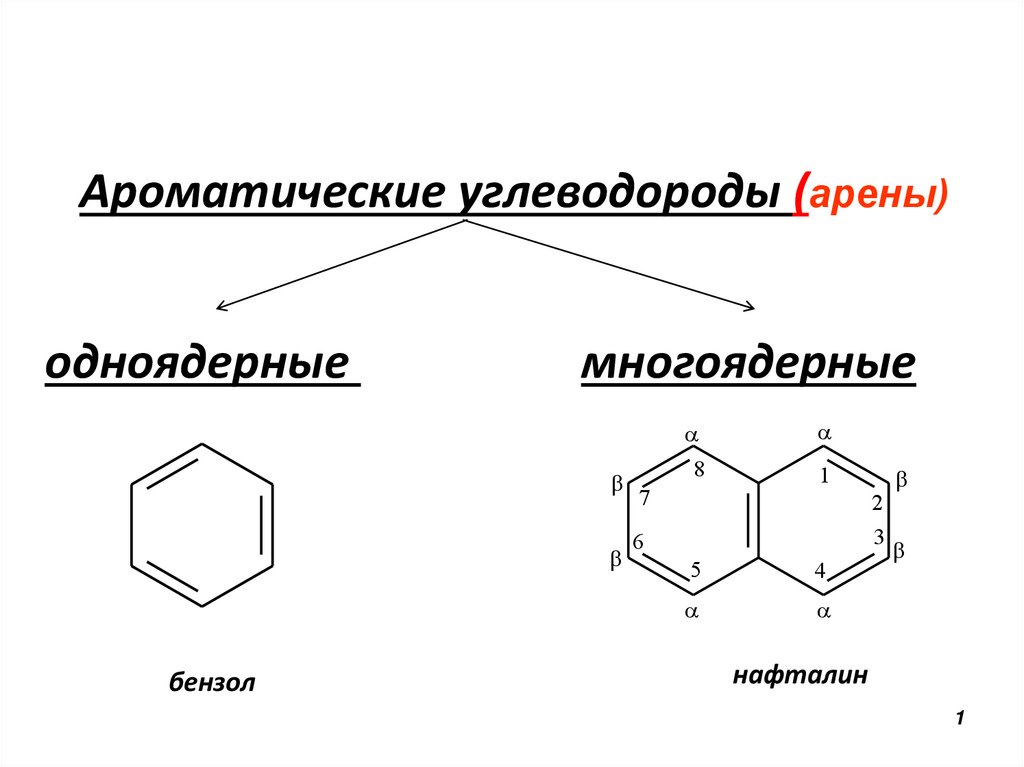
Ароматические углеводороды (арены)одноядерные
многоядерные
бензол
8
1
7
2
3
6
5
4
нафталин
1
2.
Ароматические углеводородыкарбоциклические
гетероциклические
небензоидные
бензоидные
СnH2n-6
π-избыточные
толуол
Пиррол
π-недостаточные
2
Пиридин
3.
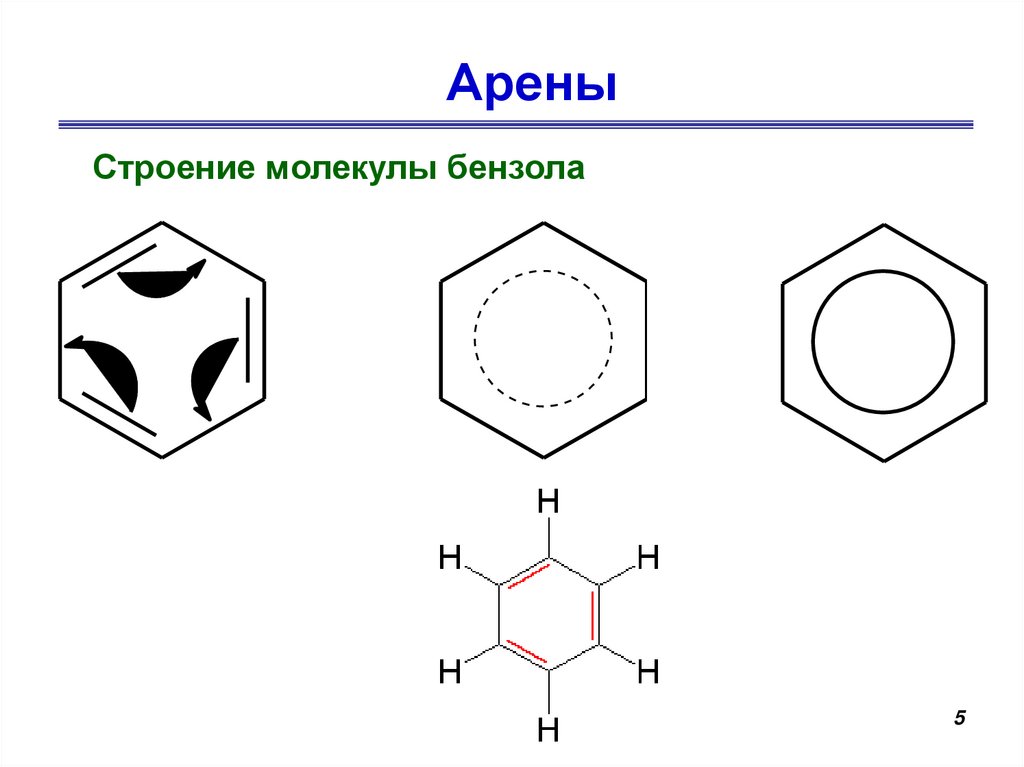
Одноядерные ареныСтроение молекулы бензола
А. Кекуле
(1865)
H
H
H
C
H
C
C
C
C
C
H
H
Бензол (бензен) С6Н6
3
4.
АреныСтроение молекулы бензола
0,109 нм
4
5.
АреныСтроение молекулы бензола
5
6.
АреныНоменклатура и изомерия
CH3
CH
стирол
(винилбензол
CH2
толуол
(метилбензол)
CH3
CH3
о-ксилол
(1,2-диметилбензол)
6
7.
АреныНоменклатура и изомерия
CH3
CH3
CH3
CH
кумол
(изопропилбензол)
OCH3
CH3
анизол
(метоксибензол)
CH3
мезителен
(1,3,5-триметилбензол)
7
8.
АреныНоменклатура и изомерия
CH2
фенил
бензил
CH
бензилиден
8
9.
Строение и номенклатурааренов
X
о ("около")
м
п
("против")
("мeжду")
9
10.
Реакции электрофильногозамещения, SЕ
1. Алкилирование
+
AlCl3
CH3Cl
2. Ацилирование
+ CH3 C Сl +
O
CH3
+ HCl;
AlCl3
O
C
CH3
+ HCl;
10
11.
3. Галогенирование+ Br2 + FeBr3
4. Нитрование
+ HNO3 + H2SO4
5. Сульфирование
+ H2SO4 + SO3
Br
+
HBr;
NO2
+ H2O;
SO3 H
.
11
12.
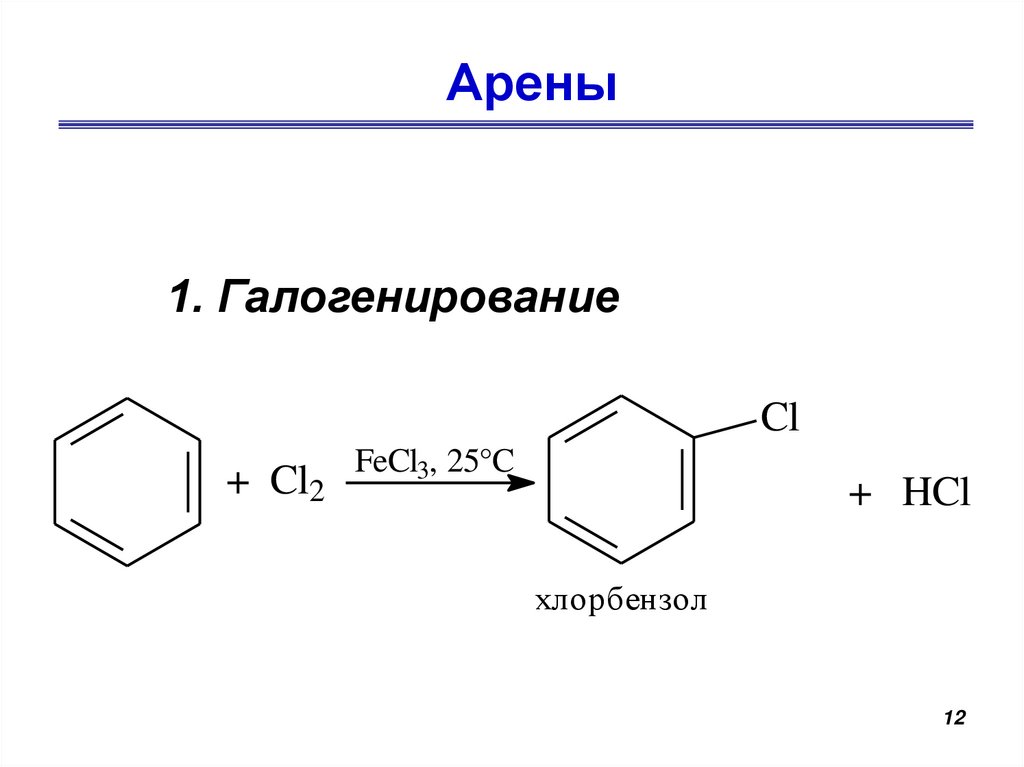
Арены1. Галогенирование
Cl
+ Cl2
FeCl3, 25°C
+ HCl
хлорбензол
12
13.
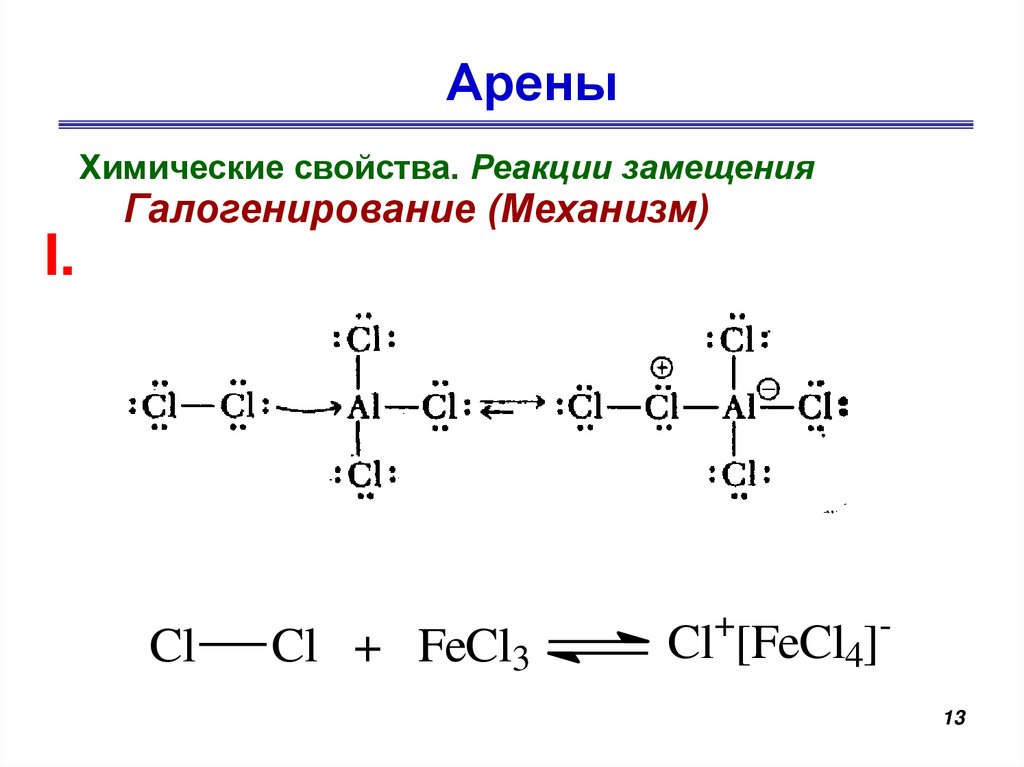
АреныХимические свойства. Реакции замещения
Галогенирование (Механизм)
I.
Cl
Cl + FeCl3
+
-
Cl [FeCl4]
13
14.
II. π-комплекс+
Cl
Cl
Cl2
A.V.Vasilyev, S.V.Lindeman, J.Kochi //
Chemical Communications, 2001, p. 909
14
14
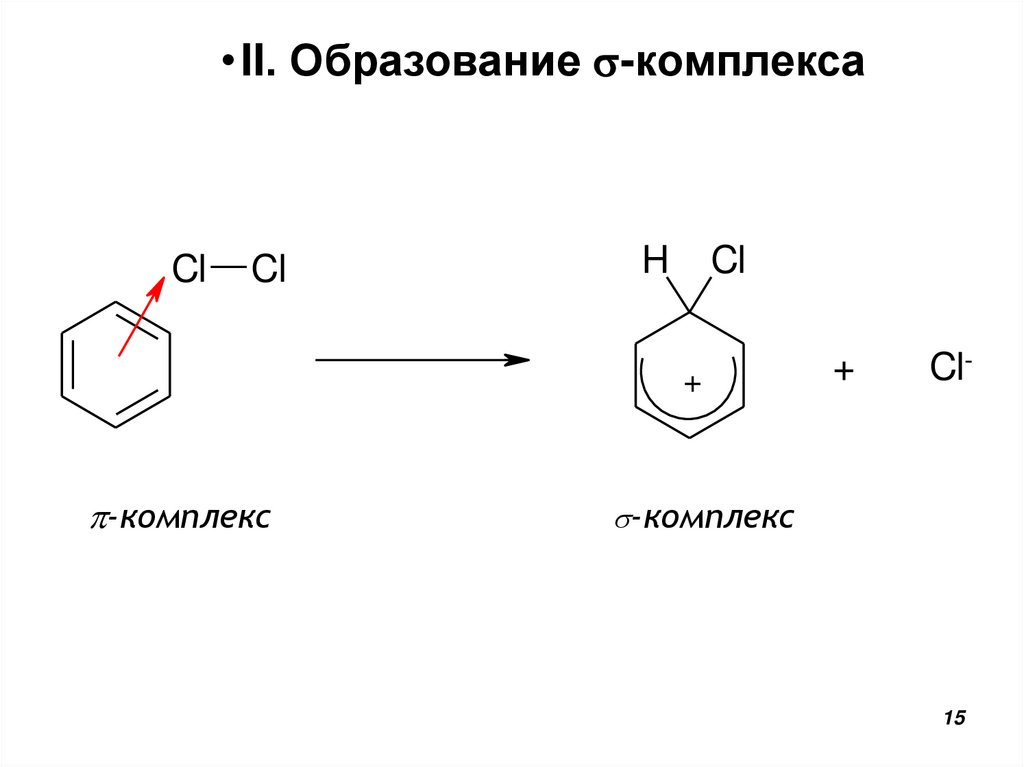
15.
• II. Образование s-комплексаCl
Cl
H
Cl
+
p-комплекс
+
Cl-
s-комплекс
15
16.
III. Выброс протонаCl
Cl
H
Cl
+
H
+
- H+
s-комплекс
p-комплекс
IV. Регенерация катализатора
H+ + AlCl4- → HAlCl4 → HCl + AlCl3
16
16
17.
Йодсодержащие гормоны щитовидной железы17
18.
АреныГалогенирование (Радикальное замещение)
CH3
+ Cl2
CH2Cl
hv
+ HCl
18
19.
2. Нитрование+ HNO3
H2SO4 (конц.)
NO2
+
H2O
нитробензол
19
20.
I. Генерирование электрофильной частицы.20
21.
II.III.
H
NO2
NO2
+
+
s-комплекс
+
H
нитробензол
21
21
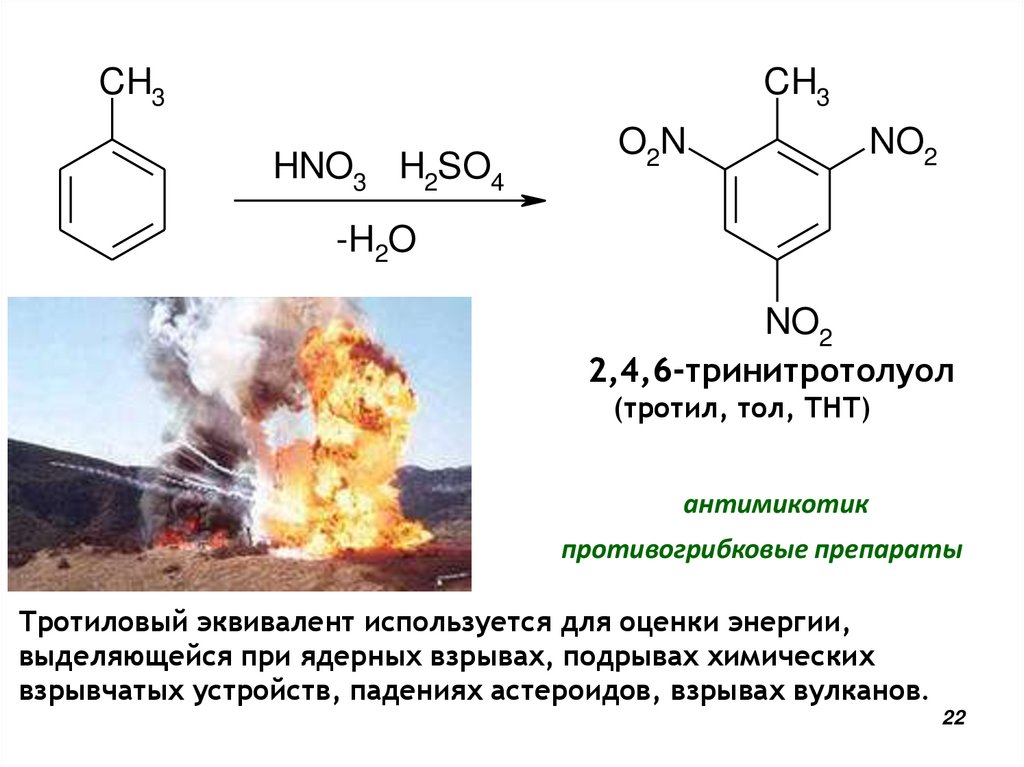
22.
CH3CH3
HNO3 H2SO4
NO2
O2N
-H2O
NO2
2,4,6-тринитротолуол
(тротил, тол, ТНТ)
антимикотик
противогрибковые препараты
Тротиловый эквивалент используется для оценки энергии,
выделяющейся при ядерных взрывах, подрывах химических
взрывчатых устройств, падениях астероидов, взрывах вулканов.
22
23.
3. Алкилирование по Фриделю - Крафтсу1877-1878 гг.
Алкилирование ароматических углеводородов) и
их производных в присутствии безводного AlCl3
и др. кислотных катализаторов- получение
алкилбензолов.
+
23
24.
АреныХимические свойства. Реакции замещения
Алкилирование (механизм)
CH3
Cl + AlCl3
+
CH3[AlCl4]H
CH3
s-комплекс
толуол
CH3
+
+
+
CH3
CH3
p-комплекс
H+ + AlCl4-
AlCl3 + HCl
+
24
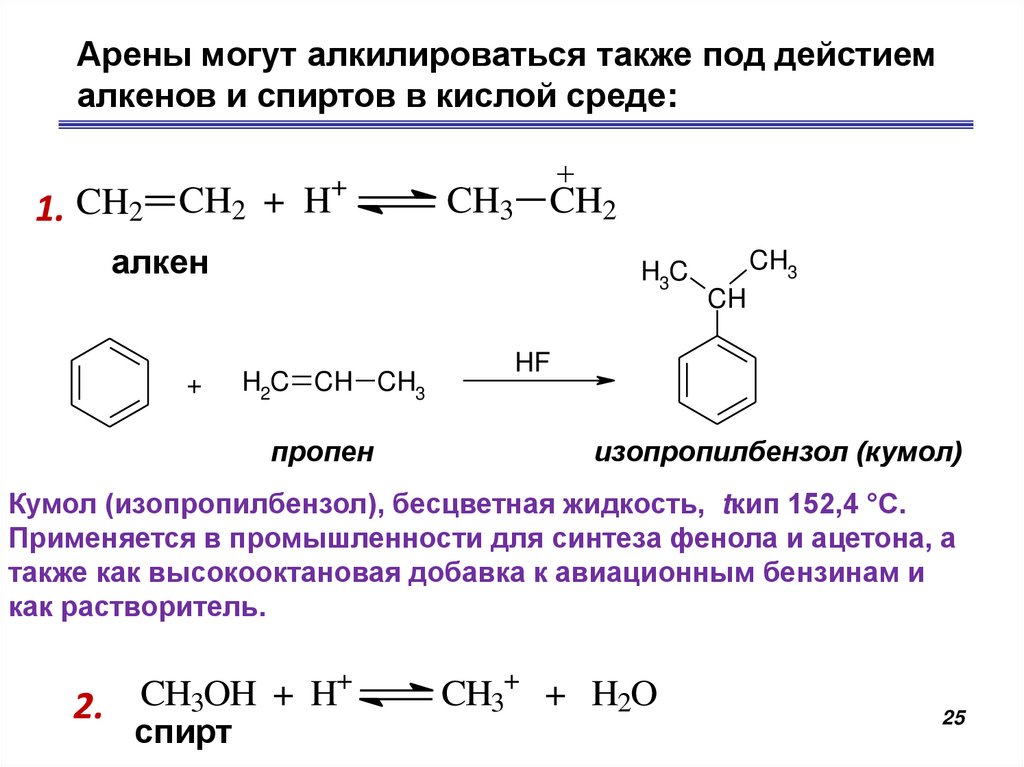
25.
Арены могут алкилироваться также под дейстиемалкенов и спиртов в кислой среде:
+
1. CH2 CH2 + H
+
CH3 CH2
алкен
+
H3C
H2C CH CH3
пропен
CH3
CH
HF
изопропилбензол (кумол)
Кумол (изопропилбензол), бесцветная жидкость, tкип 152,4 °С.
Применяется в промышленности для синтеза фенола и ацетона, а
также как высокооктановая добавка к авиационным бензинам и
как растворитель.
+
CH
OH
+
H
3
2.
спирт
CH3+ + H2O
25
26.
4. Ацилирование по Фриделю-КрафтсуАцилирование — введение в молекулу
органического соединения ацильной группы –
получение кетонов ароматического ряда.
O
O
+
CH3 C
AlCl3
C CH3
+ HCl
Cl
ацетилхлорид
метилфенилкетон
26
27.
Ацилирование (Механизм)Реакции замещения
O
CH3
+
C
Cl
AlCl3
[CH3CO]+[AlCl4]-
ацетилхлорид
27
28.
Ацилирование (Механизм)O
CH3OC
+
+ [CH3CO]
[CH3CO]+
C
H
+
CH3
-H+
s-комплекс
ацетофенон
Ацетофенон (метилфенилкетон, ацетилбензол) – используется в
производстве лекарственных препаратов и в качестве отдушки
(запах черёмухи) в производстве мыла.
28
29.
• 5. СульфированиеSO3H
SO3
H2SO4 дым.
бензолсульфокислота
29
29
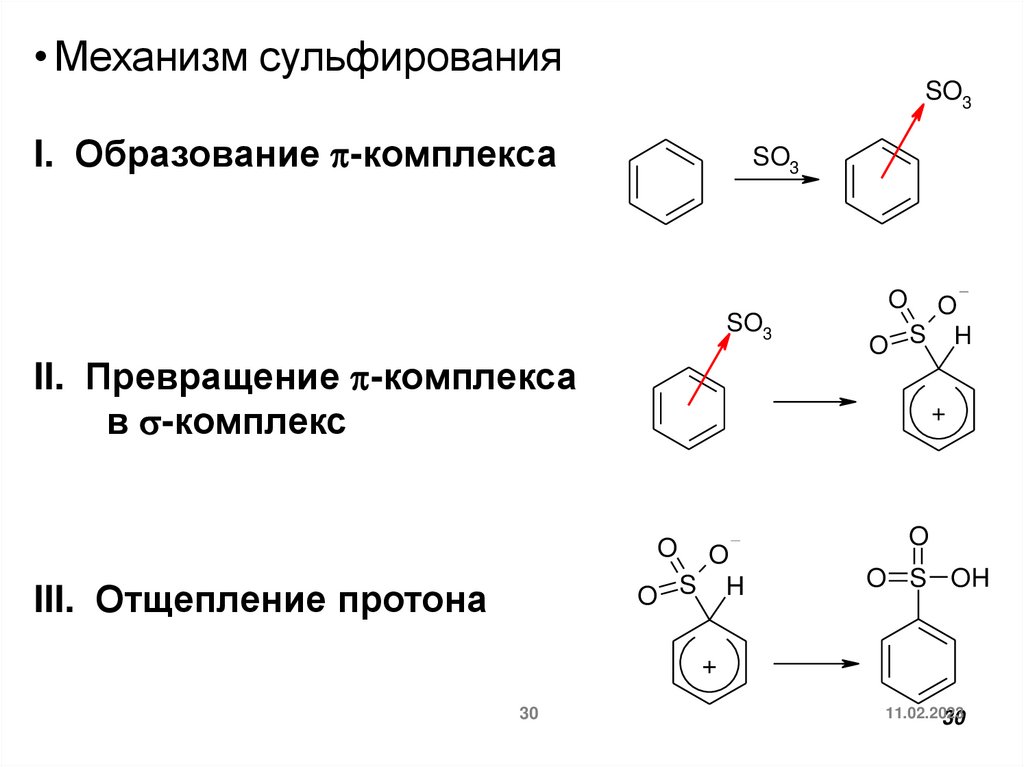
30.
• Механизм сульфированияSO3
I. Образование p-комплекса
SO3
O
SO3
II. Превращение p-комплекса
в s-комплекс
+
O
O
O S H
III. Отщепление протона
O
O S H
O
O S OH
+
30
11.02.2023
30
31.
Влияние заместителей.
Электронодонорные
заместители
+I- Эффект (алкильные радикалы)
R
R
R
H
X
+X
R
H
X
H
X
Дополнительное смещение
электронного облака по s-связи
в сторону вакантной орбитали.
31
32.
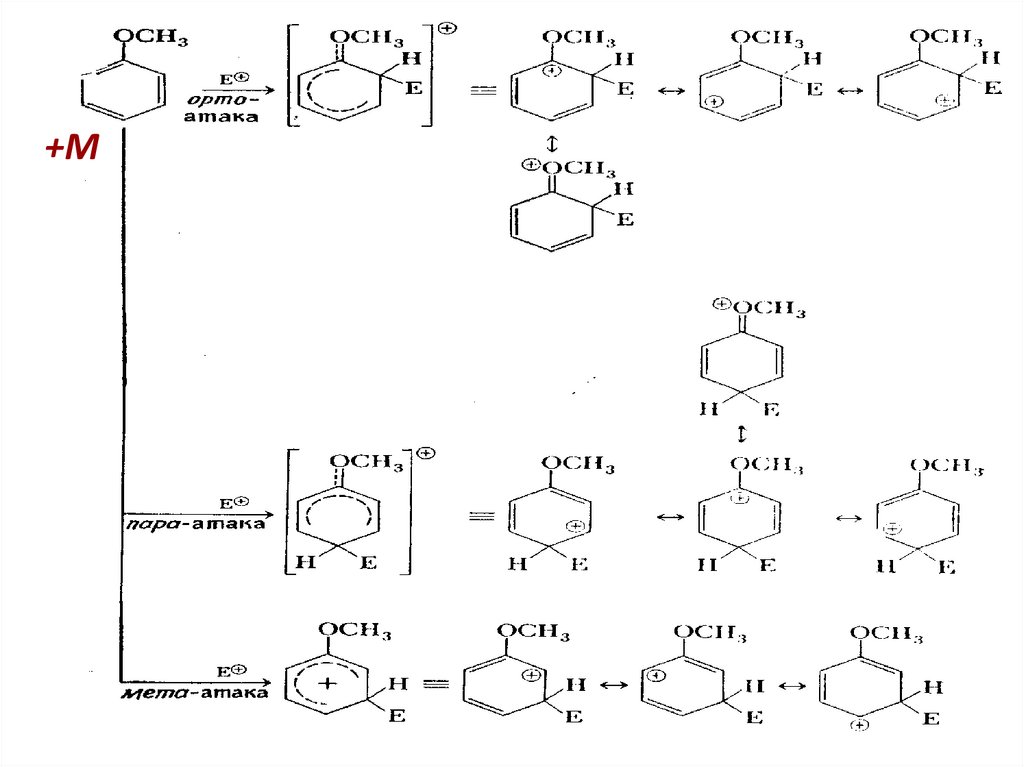
+М32
33.
Эффекты заместителей приэлектрофильном замещении
1. Заместители (ориентанты) первого рода (доноры):
—ОН, —OR, —OCOR, —SH,- SR, —NH2, —NHR, -NR2 ,
-NHCOCH3 , -Alk, –C6H5,
Они активируют бензольное кольцо и
ориентируют новый заместитель в орто- и параположения ( орто- и пара-ориентанты).
.
33
34.
Эффекты заместителейпри электрофильном замещении
2. Заместители (ориентанты) второго рода (акцепторы):
—CN, —СООН, —SO3H, —СНО, —COR, —COOR, —NO2
дезактивируют бензольное кольцо и вновь входящий
заместитель ориентируют в мета-положение
(мета-ориентанты).
34
35.
АреныХимические свойства. Реакции замещения
Влияние заместителей на реакционную способность
NH2
NH3
-I
M=0
акцептор
HNO3
H2SO4
NO2
35
36.
Ориентанты III родаГалогены (F, Cl, Br, I)- направляют
электрофильное замещение в орто и параположения и дезактивируют реакцию SE
+М
Cl
-I
-
-
-
36
37.
Стерические факторыCH3
CH3
CH3
NO2
+
CH3
CH3
C
CH3
58%
HNO3 (H2SO4)
-H2O
NO2
37%
CH3
CH3
C
CH3
CH3
CH3
C
CH3
NO2
+
16%
NO2
73%
37
38.
Окисление боковой цепи38
39.
АреныХимические свойства. Окисление
CH3
COOH
[O]
t
CH3
CH
CH3
COOH
п-метилизопропилбензол (цимол)
терефталевая
кислота
39
40.
Реакции SE в ароматическом кольцемогут протекать и при участии ферментов:
CH2
CH
COO
O2
Фермент
НO
CH2
CH
Фенилаланин NH3
Тирозин
NH3
Недостаточность фермента вызывает фенилкетонурию.
OCH3 + Cl2
Хлориназа
OCH3 +
Cl
COO
.
OCH3 ;
Анизол
60 %
40 %
Cl
Такое же соотношение изомеров, как в реакции с Cl2/FeCl.3
40
41.
Многоядерные ароматическиесоединения
Соединения с конденсированными
бензольными ядрами
41
42.
Многоядерные ароматическиесоединения
Соединения с конденсированными бензольными
ядрами
8
1
7
2
3
6
5
4
нафталин
42
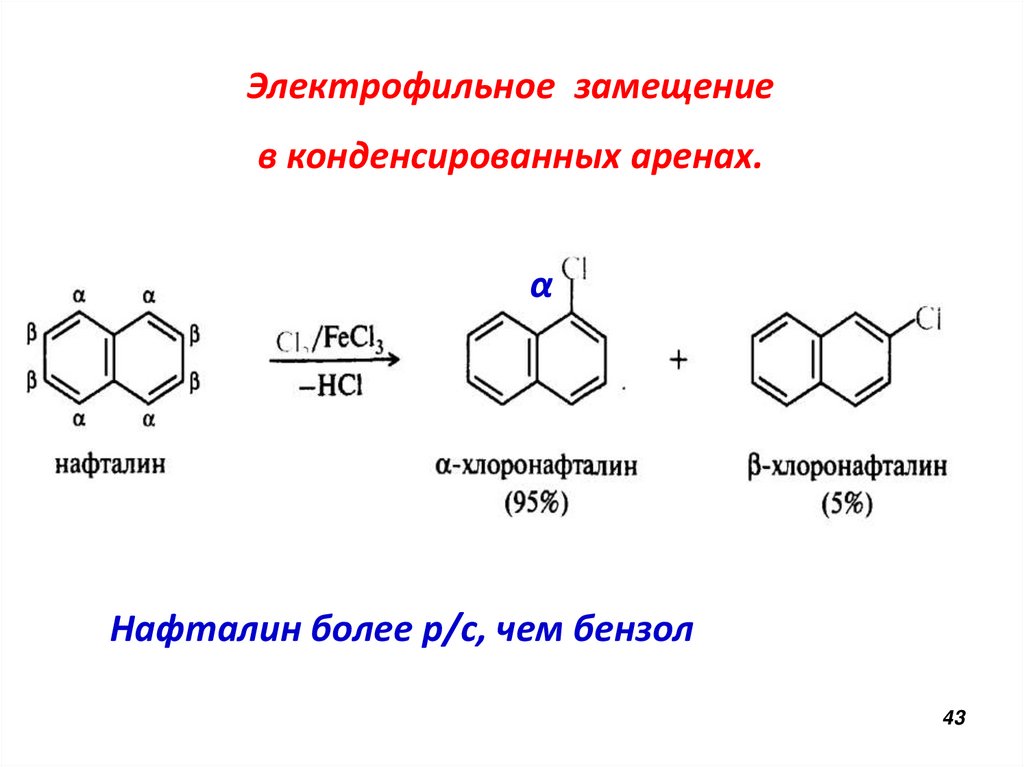
43.
Электрофильное замещениев конденсированных аренах.
α
Нафталин более р/с, чем бензол
43
44.
Сульфирование нафталинажесткие условия,
длительно
термодинамический контроль
Более ТД стаб.
мягкие условия
Кинетический контроль
V образования наиб.
44


































 Химия
Химия








